Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
CRISPR / Cas9 система
Содержание
- 1. CRISPR / Cas9 система
- 2. CRISPR — Clustered Regularly Interspaced Short Palindromic
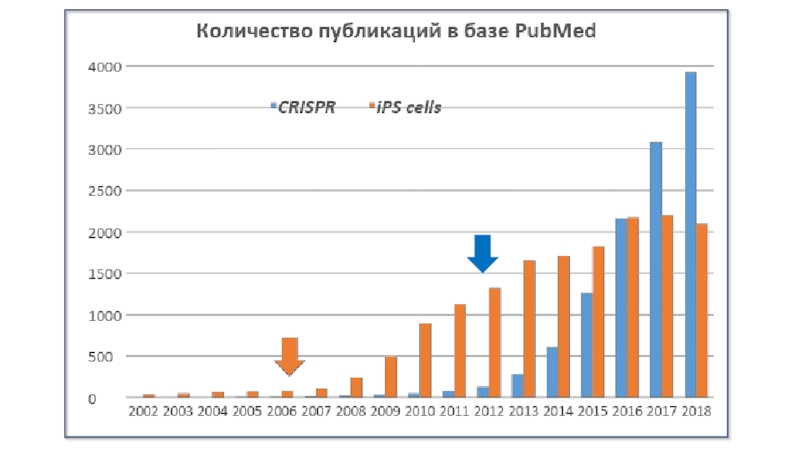
- 3. 2002 – введено название CRISPR, идентифицированы сцепленные
- 4. Слайд 4
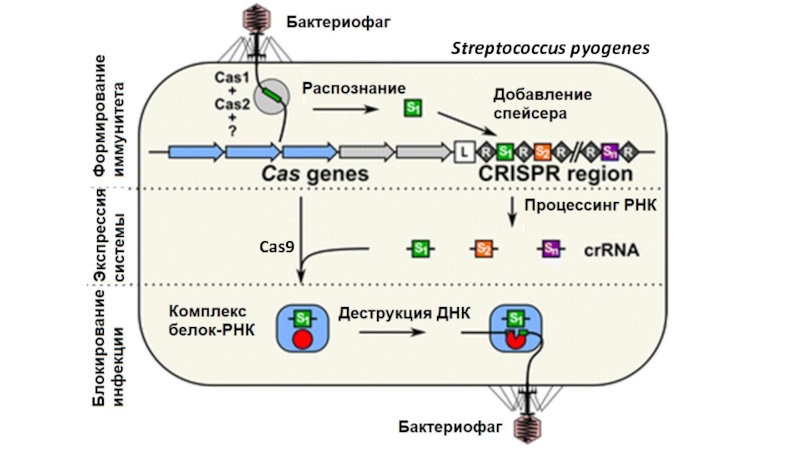
- 5. Cas9Streptococcus pyogenes
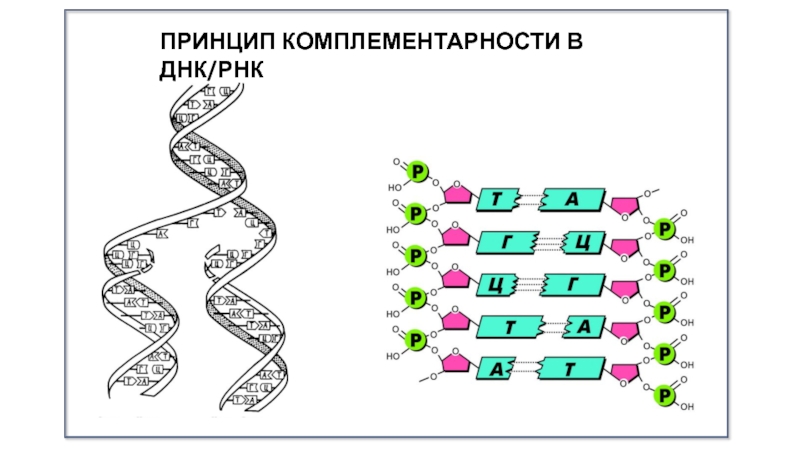
- 6. ПРИНЦИП КОМПЛЕМЕНТАРНОСТИ В ДНК/РНК
- 7. Как система адаптирована под задачи генной инженерии?Сконструирована
- 8. Слайд 8
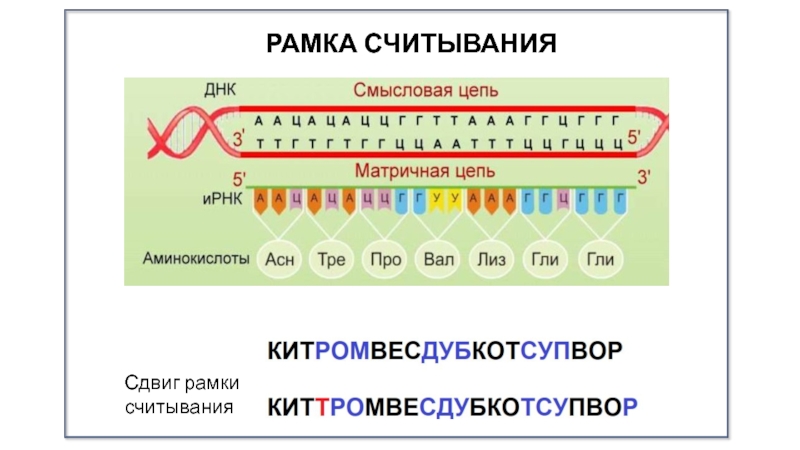
- 9. РАМКА СЧИТЫВАНИЯСдвиг рамки считывания
- 10. Какие организмы уже удалось изменить при помощи
- 11. Группы вопросов и примененийМедицинские исследования: поиск значимых
- 12. Создание модельных животных Цели: 1) Отработка технологии
- 13. Danio rerioПолучены наследуемые мутации по 162 локусамМыши
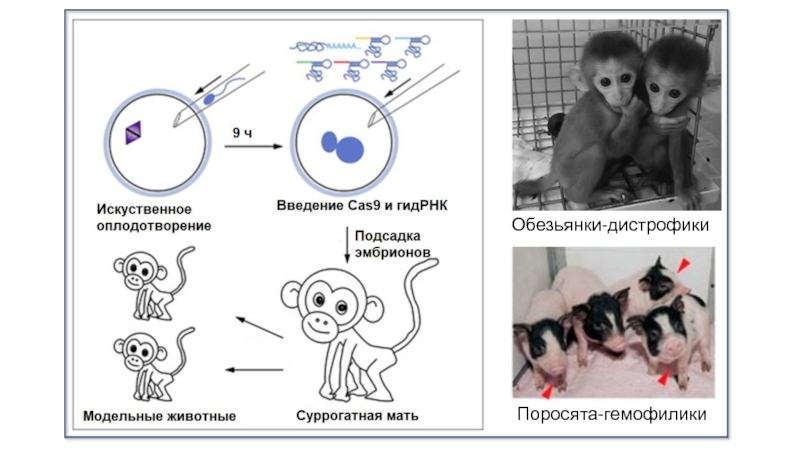
- 14. Обезьянки-дистрофикиПоросята-гемофилики
- 15. Испытания возможностей использования CRISPR для лечения генетических заболеваний 2014-2018
- 16. Болезни, вылеченные или облегченные при помощи редактирования
- 17. Мышей вылечили от гемофилии, восстановив поломанный ген
- 18. CRISPR в клинических испытанияхС 2016 г –
- 19. Проблемы в контексте медицинского примененияОбеспечить достаточно высокую
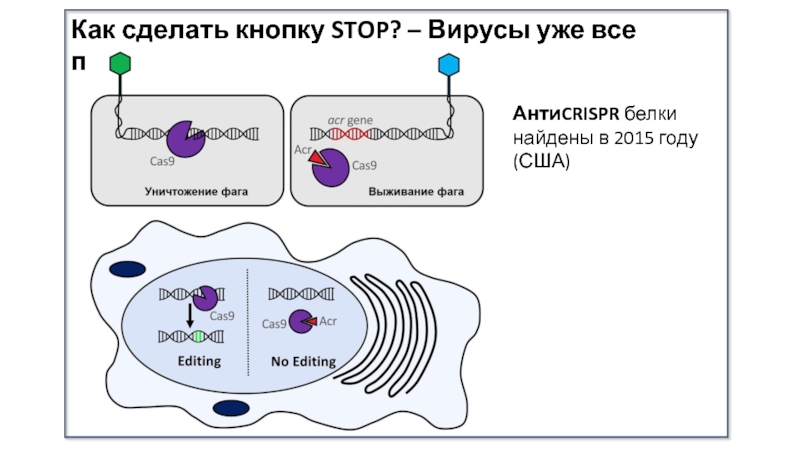
- 20. Как сделать кнопку STOP? – Вирусы уже все придумалиАнтиCRISPR белки найдены в 2015 году (США)
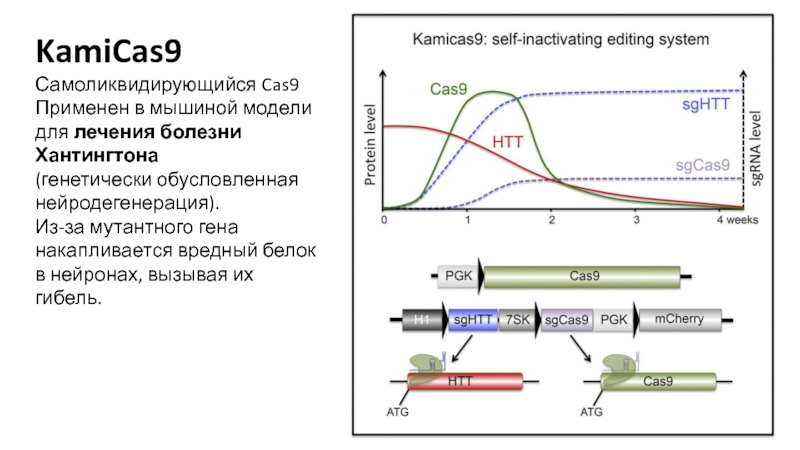
- 21. KamiCas9Самоликвидирующийся Cas9 Применен в мышиной модели для
- 22. Решение проблемы повышения точности действияПолучены телята с
- 23. Можно точечно редактировать ДНК и без внесения
- 24. Горячие новости (21 февраля): открыт новый вариант
- 25. Редактирование эмбрионов человека В Великобритании официально разрешено
- 26. CRISPR/Cas9-mediated gene editing in human tripronuclear zygotes
- 27. CRISPR/Cas9-mediated gene editing in human zygotes using
- 28. Зиготы получали оплодотворением яйцеклеток с нормальным вариантом
- 29. Возможности совмещения технологий CRISPR/Cas и стволовых клеток
- 30. Аналогичные исследования начаты с органоидами мозга, сосудов
- 31. Получены универсальные стволовые клетки, невидимые для иммунной
- 32. https://www.karger.com/Article/FullText/480370Идея получения химерных «гуманизированных» животных для выращивания органов для трансплантации
- 33. Ген SALL1 – контролер формирования зачатка почек.Если
- 34. ДиагностикаНа основе Cas13a создан сверхчувствительный высокоспецифичный тест
- 35. Даешь вкусные помидоры! (18 февр. 2019)Искусственная селекция
- 36. EvolvR: система для «прицельной эволюции» (2018)Результат: в
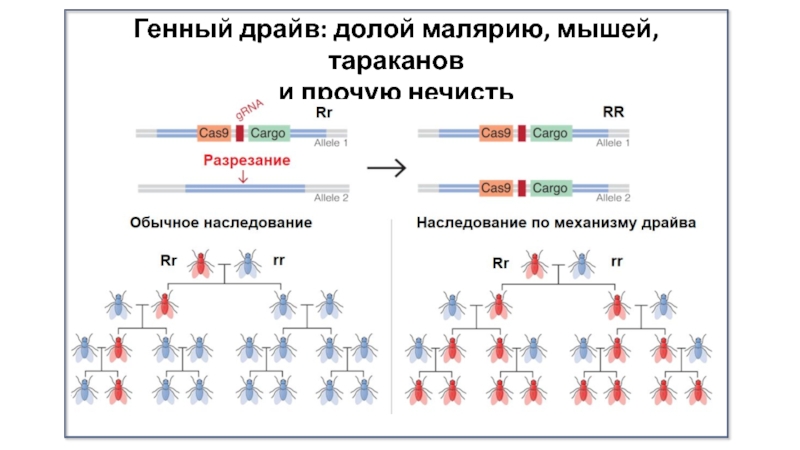
- 37. Генный драйв: долой малярию, мышей, тараканов и прочую нечисть
- 38. Эволюционные исследованияСтарые гены ⟹ новые геныНовые гены ⟹ старые гены
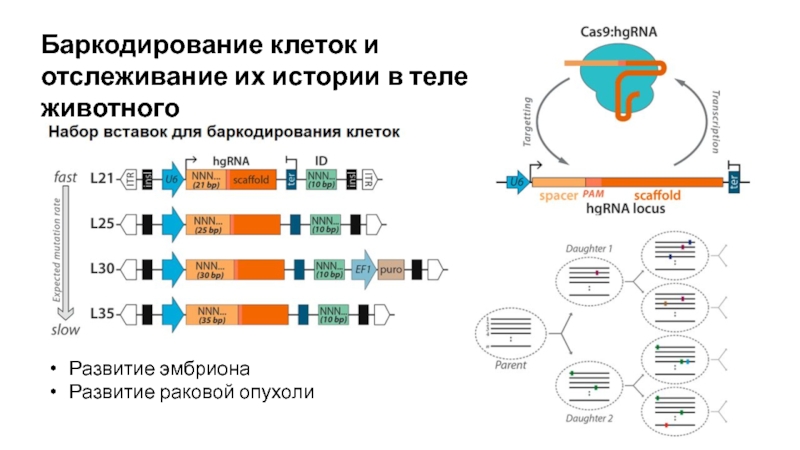
- 39. Баркодирование клеток и отслеживание их истории в теле животногоРазвитие эмбрионаРазвитие раковой опухоли
- 40. Использование CRISPR/Cas для мечения внутриклеточных белков
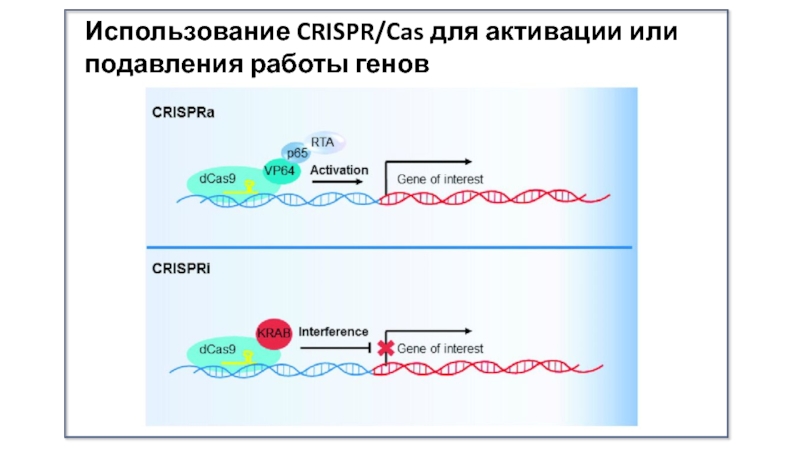
- 41. Использование CRISPR/Cas для активации или подавления работы генов
- 42. Итак, чем же так хороша система CRISPR/Cas?Простота
- 43. CRISPOR (http://crispor.tefor.net/) – простой бесплатный онлайн ресурс для подбора подходящих гидРНК
- 44. Слайд 44
- 45. РискиСлишком простая система. Можно сделать все без
- 46. Спасибо за внимание
- 47. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2CRISPR — Clustered Regularly Interspaced Short Palindromic Repeats Кластеры регулярно
прерывающихся коротких палиндромных повторов
1987 – открытие странных участков в геноме
E. coli, состоящих из чередований повторов и уникальных спейсерных последователь-ностей (Японцы). Случайно, статья вообще не про это.1995-2002 – обнаружение широкой распространенности CRISPR у бактерий и архей. Использовали в качестве «штрих-кода» для опознания видов и штаммов микроорганизмов.
21-35 п.о.
21-35 п.о.
Слайд 32002 – введено название CRISPR, идентифицированы сцепленные белки, названные Cas,
установлено их родство с хеликазами.
2003 – (быстрое расширение баз данных
по секвенированным геномам) обнаружено соответствие спейсерных последовательностей фрагментам геномов фагов (вирусов) и некоторых плазмид.2006 – показано, что CRISPR вместе с группой белков Cas обеспечивают противофаговую защиту у микроорганизмов.
2008-2010 – расшифрован механизм работы системы CRISPR/Cas противофагового иммунитета.
2011 – в экспериментах на E.coli установили минимальный необходимый набор компонентов системы (группа из Литвы, рук. Шикшнис): CRISPR + Cas9
2012 – Дженифер Дудна с коллегами (Калифорния) разработали технологию модификации генома на основе системы CRISPR/Cas. Одновременно аналогичную технологию предложила и группа из Литвы, но Калифорнийская система оказалась компактнее.
С 2013 – быстрое появление все новых модификаций этой технологии и ее адаптация под решение широкого круга экспериментальных задач в области молекулярной биологии клеток, биологии онтогенеза, генетических заболеваний и др.
Слайд 7Как система адаптирована под задачи генной инженерии?
Сконструирована цельная гидРНК (gRNA),
которая совмещает в себе функции crRNA (комплементарное спаривание с целевой
последовательностью) и tracrRNA (привлечение эндонуклеазы Cas). Эта гидРНК кодируется одним геном длиной около 100 п.о. и экспрессируется с промоторов для РНК полимеразы III.Созданы искусственные варианты гена эндонуклеазы Cas9 c нуклеотидной последовательностью, адаптированной под систему трансляции целевого организма (оптимизированные наборы кодонов) + пришит сигнал ядерной локализации.
Создаются разнообразные варианты гена с измененными функциями и характеристиками.
Дженнифер Дудна (статья за 2012 год)
Слайд 10Какие организмы уже удалось изменить при помощи CRISPR/Cas?
Позвоночные:
Беспозвоночные: Растения:
Лягушка Дрозофила Кукуруза
Аксолотль Водяная блоха Рис
Рыбы
Аскарида СоргоМышь Шелкопряд Апельсин
Крыса Табак
Обезьяна Пшеница
Кролик Свинья Человек Арабидопсис
Томат
Слайд 11Группы вопросов и применений
Медицинские исследования: поиск значимых (вредных) мутаций, создание
моделей для изучения генетических заболеваний.
Медицинское применение: диагностика, лечение инфекционных, генетических,
онкологических заболеваний.Биотехнологическое применение: создание новых белков, животных и растений с новыми полезными для человека свойствами.
Борьба с вредителями (генный драйв).
Функциональные исследования: расшифровка функции генов, изучение поведения клеток в организме.
Эволюционные исследования: поиск значимых (полезных) мутаций, благодаря которым адаптировались разные виды.
Слайд 12Создание модельных животных Цели: 1) Отработка технологии 2) Проверка гипотез о патогенности определенных
мутаций. 3) Отработка возможных подходов к лечению (лекарства, стволовые клетки, реверсия
к норме при помощи редактирования CRISPR/Cas и пр.) В настоящее время ряд фирм делает мышей и крыс с нужными мутациями под заказ.Слайд 13Danio rerio
Получены наследуемые мутации по 162 локусам
Мыши с внесенной поломкой
в ген тирозиназы.
Тирозиназа – фермент, необходимый для синтеза меланина.
Починив ген
обратно, из альбиносов получили темных мышей.Слайд 16Болезни, вылеченные или облегченные при помощи редактирования на модельных животных:
Гипертрофическая
кардиомиопатия
Гиперхолестеринемия (Ген PCSK9)
Гемофилия
Мышечная дистрофия
Прогерия (преждевременное старение)
Атрофия сетчатки глаз
Тирозинемия (нарушение
синтеза белка, истощение)Болезнь Хантигтона (атрофия нейронов мозга)
Аутизм
Муковисцидоз
Серповидно-клеточная анемия, талассемия
Катаракта
Онкологии
Слайд 17Мышей вылечили от гемофилии, восстановив поломанный ген фактора свертывания крови
(2016)
Обнаружили новую мутацию, связанную с тяжелой формой семейной гемофилии B
– в факторе 9 системы свертывания крови.Получили мутантную больную мышь, при помощи модификации одноклеточного эмбриона с использованием CRISPR/Cas.
Молодым и взрослым мышам вводили внутривенно плазмиды или аденовирусные векторы для экспрессии гидРНК, белка Cas9 под специфичным для печени промотором и нормальный вариант последовательности F9. Ген встраивался в заданную область генома.
Редактирование прошло примерно в 1% клеток печени (при введении голых плазмид).
Получили устойчивую нормализацию свертываемости крови.
Слайд 18CRISPR в клинических испытаниях
С 2016 г – в Китае. Терапия
опухолей. Отключение гена-подавителя иммунитета в лимфоцитах (ex vivo). 86 пациентов
(большинство уже умерли от диагностированного рака).C 2017 – аналогичные испытания в США.
С октября 2018 – в Европе. Терапия серповидно-клеточной анемии – патологии эритроцитов из-за мутации в гене гемоглобина. 12 пациентов.
С 2019 – планируется в США. Терапия врожденных дефектов сетчатки (потеря зрения) из-за мутации в генах LCA10, USH2A, RPE65 или CEP290. Рассчитывают привлечь по 10-20 пациентов. Особенность – проведение in vivo (введение компонентов системы CRISPR/Cas напрямую в сетчатку). Система названа EDIT-101.
Слайд 19Проблемы в контексте медицинского применения
Обеспечить достаточно высокую специфичность редактирования.
Обеспечить достаточно
высокую эффективность.
Не навредить по недостатку знаний.
Варианты применения:
Лечение взрослых редактированными
клетками (ex vivo).Лечение взрослых введением системы для редактирования в определенные участки организма (in vivo).
Раннее лечение введением системы в эмбрион внутри матки.
Редактирование генома на стадии одноклеточного зародыша.
Слайд 20Как сделать кнопку STOP? – Вирусы уже все придумали
АнтиCRISPR белки
найдены в 2015 году (США)
Слайд 21KamiCas9
Самоликвидирующийся Cas9
Применен в мышиной модели для лечения болезни Хантингтона
(генетически обусловленная нейродегенерация).
Из-за мутантного гена накапливается вредный белок в нейронах,
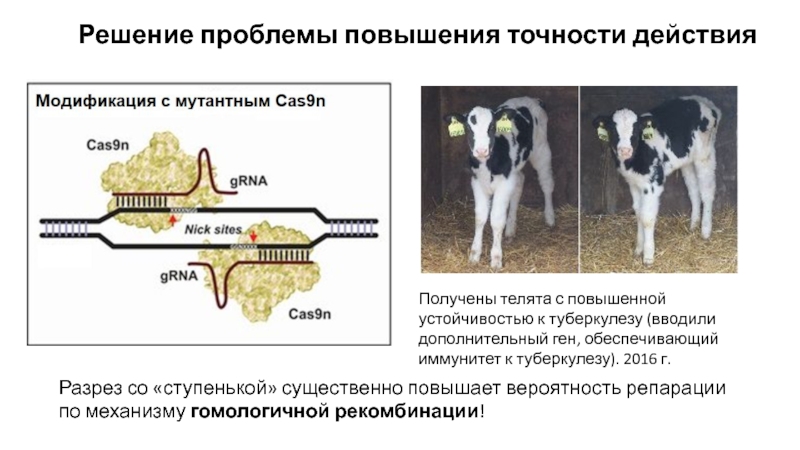
вызывая их гибель.Слайд 22Решение проблемы повышения точности действия
Получены телята с повышенной устойчивостью к
туберкулезу (вводили дополнительный ген, обеспечивающий иммунитет к туберкулезу). 2016 г.
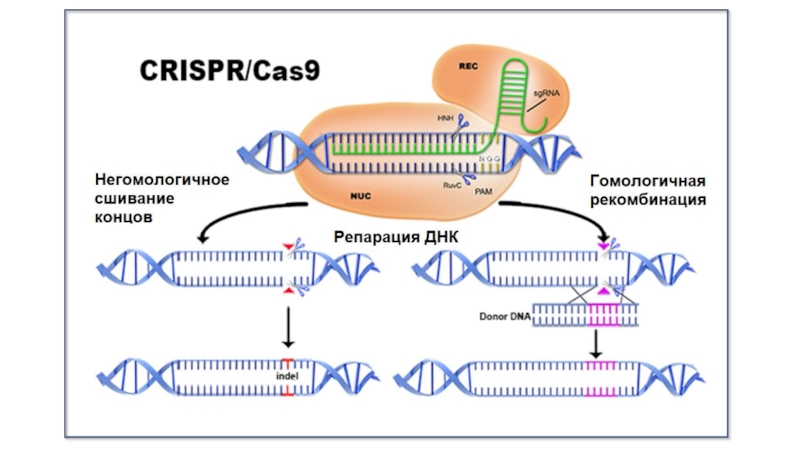
Разрез со «ступенькой» существенно повышает вероятность репарации по механизму гомологичной рекомбинации!
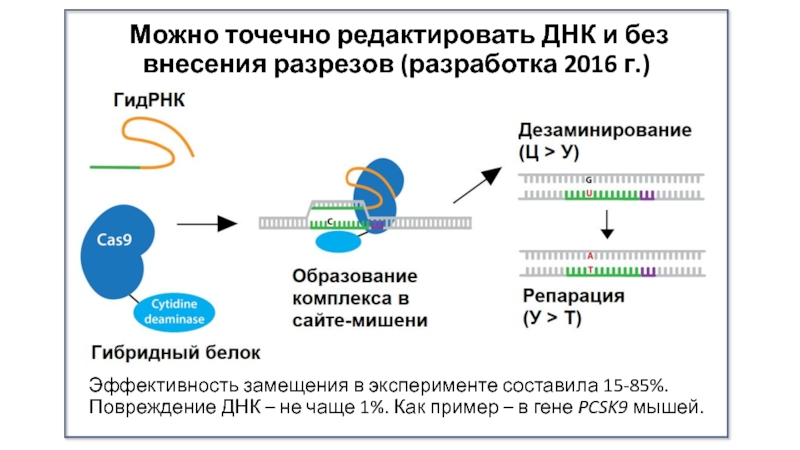
Слайд 23Можно точечно редактировать ДНК и без внесения разрезов (разработка 2016
г.)
Эффективность замещения в эксперименте составила 15-85%. Повреждение ДНК – не
чаще 1%. Как пример – в гене PCSK9 мышей.Слайд 24Горячие новости (21 февраля): открыт новый вариант Cas9 – короче,
точнее и с большим выбором сайтов
3 варианта фермента из менингококка
Neisseria meningitidisНоворожденных мышат: 5
Альбиносы – 2
Мозаики (серо-белые) – 3
Токсичность – 0
Редактированной ДНК 84-100%
Слайд 25Редактирование эмбрионов человека В Великобритании официально разрешено в исследовательских целях с
2015 г. В настоящее время проводится также в Китае, США,
России. Максимальная продолжительность разрешенных экспериментов – 14 дней. Цели: 1) отработка технологии (с перспективой на применение в будущем); 2) изучение роли генов и их мутаций в ранних событиях эмбрионального развития человека. Поиск причин женского бесплодия (выкидыши).Слайд 26CRISPR/Cas9-mediated gene editing in human tripronuclear zygotes Protein and Cell,
April 2015
Оплодотворение
In vitro
Материал на
выброс (2-5 %)
Развивается до
стадии
бластоцистыМикрошприцем вводили в оплодотворенную яйцеклетку:
мРНК Cas9
мРНК Gfp
gRNA, нацеленную на ген бета-гемоглобина (HBB)
ssDNA с областями гомологии и некоторыми заменами
Результаты:
Эффективность введения – 71 из 86 (83%)
Внесение надреза в гене HBB – 28 из 54 (52%)
Внесение ожидаемых замен – 4 из 28 (14%)
6 из 6 проверенных эмбрионов были мозаиками, содержали мутации HBB типа indel, и имели дополнительные мутации в неспецифичных участках генома.
Слайд 27CRISPR/Cas9-mediated gene editing in human zygotes using Cas9 protein Molecular
genetics and genomics, март 2017
(статья представлена в июле 2016) Китай
Эксперименты
проводили на здоровых 2N зиготах; гены HBB и G6PD, исправляли мутации, связанные с талассемией и фавизмом. Зиготы получали оплодотворением яйцеклеток с нормальным вариантом спермой от гетерозиготного мужчины.
Микрошприцем вводили в оплодотворенную яйцеклетку в G2 фазе:
белок Cas9; gRNA, нацеленную на ген-мишень
ssDNA с нужным участком гена (нормальный аллель)
Результаты:
Эффективность введения – 6 из 6 (100%)
Разрез и редактирование – 6 из 6 (100%)
Редактирование по пути HDR – 1 из 4 для гена HBB; 2 из 2 для GAPDH
Полное секвенирование проведено для 1 эмбриона, при этом неспецифических изменений генома в нем не обнаружено.
Слайд 28Зиготы получали оплодотворением яйцеклеток с нормальным вариантом спермой от больного
мужчины.
Мутация в гене MYBPC3 вызывает в гетерозиготном состоянии гипертрофическую кардиомиопатию.
Всего
использовали 22 зиготы (и 10 контрольных).Ожидаемое число нормальных зигот – 50%
По результатам эксперимента – 72%.
Гомологичная рекомбинация прошла с материнской хромосомой.
Эффективность редактирования около 50%.
Мозаицизма и неспецифических мутаций не выявлено.
Октябрь 2018 – российская статья о редактировании CCR5 у эмбрионов
Ноябрь 2018 – заявление Хе о рождении детей с редактированным CCR5.
Correction of a pathogenic gene mutation in human embryos (2017, Миталипов, США)
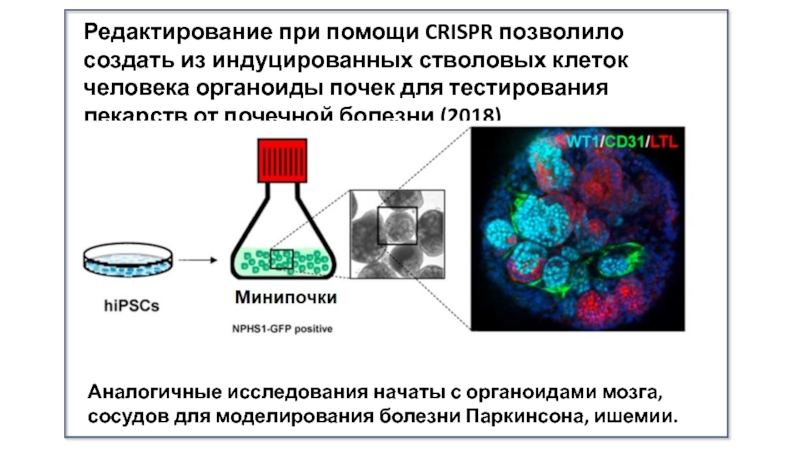
Слайд 30Аналогичные исследования начаты с органоидами мозга, сосудов для моделирования болезни
Паркинсона, ишемии.
Редактирование при помощи CRISPR позволило создать из индуцированных стволовых
клеток человека органоиды почек для тестирования лекарств от почечной болезни (2018)Слайд 31Получены универсальные стволовые клетки, невидимые для иммунной системы (18 февр.
2019)
Каждая клетка предъявляет иммунной системе «паспорт» (молекулы MHC I и
MHC II) по которым иммунная система может отличить свои клетки от чужих.Чужие клетки уничтожаются Т лимфоцитами;
«Беспаспортные клетки» - естественными киллерами (NK).
В результате привитые чужие клетки отторгаются. Приходится подавлять иммунную систему и пациент становится уязвимым для инфекции.
При помощи CRISPR были сломаны два гена, необходимые для предъявления MHC I и MHC I, а обычной модификацией добавлен ген, отменяющий срабатывание клеток NK.
Результат: у мышей приживались стволовые клетки от других мышей! Без подавления иммунной системы!
А что, если так получать клетки, вырабатывающие инсулин для пациентов с аутоиммунным диабетом???
НО: берегитесь рака!!!
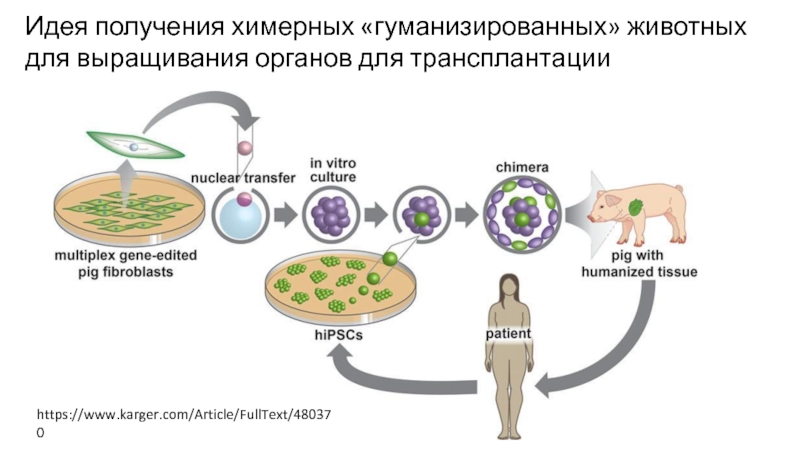
Слайд 32https://www.karger.com/Article/FullText/480370
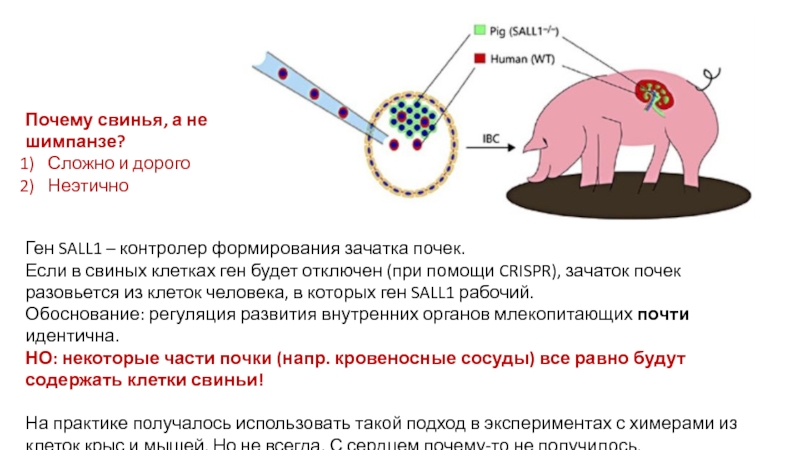
Идея получения химерных «гуманизированных» животных для выращивания органов для трансплантации
Слайд 33Ген SALL1 – контролер формирования зачатка почек.
Если в свиных клетках
ген будет отключен (при помощи CRISPR), зачаток почек разовьется из
клеток человека, в которых ген SALL1 рабочий.Обоснование: регуляция развития внутренних органов млекопитающих почти идентична.
НО: некоторые части почки (напр. кровеносные сосуды) все равно будут содержать клетки свиньи!
На практике получалось использовать такой подход в экспериментах с химерами из клеток крыс и мышей. Но не всегда. С сердцем почему-то не получилось.
Почему свинья, а не шимпанзе?
Сложно и дорого
Неэтично
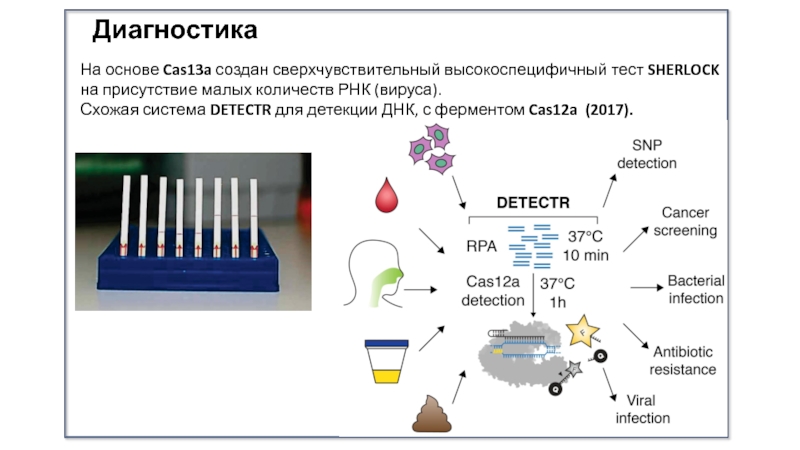
Слайд 34Диагностика
На основе Cas13a создан сверхчувствительный высокоспецифичный тест SHERLOCK на присутствие
малых количеств РНК (вируса).
Схожая система DETECTR для детекции ДНК, с
ферментом Cas12a (2017).Слайд 35Даешь вкусные помидоры! (18 февр. 2019)
Искусственная селекция помогла создать культуры
с массой замечательных свойств. Но попутно появились и не такие
приятные свойства, от которых сложно избавиться.Выход: зная, какие гены ответственны за нужные признаки, заново начать с диких растений и изменить гены только там, где требуется.
20 продуктов готовят к выпуску на рынки США в ближайшие годы.
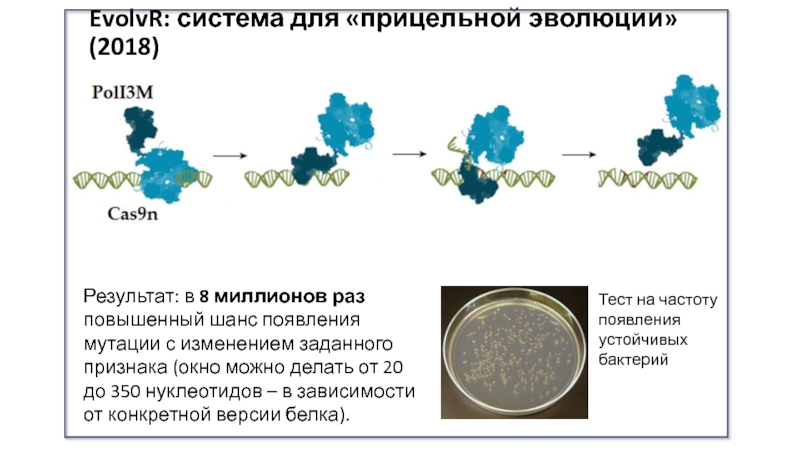
Слайд 36EvolvR: система для «прицельной эволюции» (2018)
Результат: в 8 миллионов раз
повышенный шанс появления мутации с изменением заданного признака (окно можно
делать от 20 до 350 нуклеотидов – в зависимости от конкретной версии белка).Тест на частоту появления устойчивых бактерий
Слайд 39Баркодирование клеток и отслеживание их истории в теле животного
Развитие эмбриона
Развитие
раковой опухоли
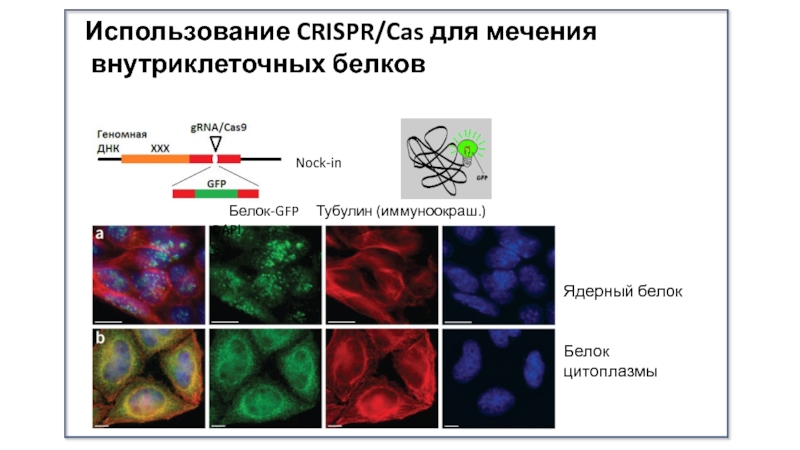
Слайд 40Использование CRISPR/Cas для мечения
внутриклеточных белков
Белок-GFP
Тубулин (иммуноокраш.) DAPI
Nock-in
Ядерный белок
Белок цитоплазмы
Слайд 42Итак, чем же так хороша система CRISPR/Cas?
Простота дизайна, высокая эффективность
и специфичность генной модификации клеток и организмов, а следовательно, экономия
денег и времени.Возможность работы с множеством различных биологических объектов, в том числе тех, которые не являются классическими модельными объектами.
Возможность ориентации одновременно на большое число геномных локусов.
Гибкая адаптация системы под решение широкого круга научных и практических задач: модификация генома, регуляция активности генов, прижизненное наблюдение за компонентами клетки и др.
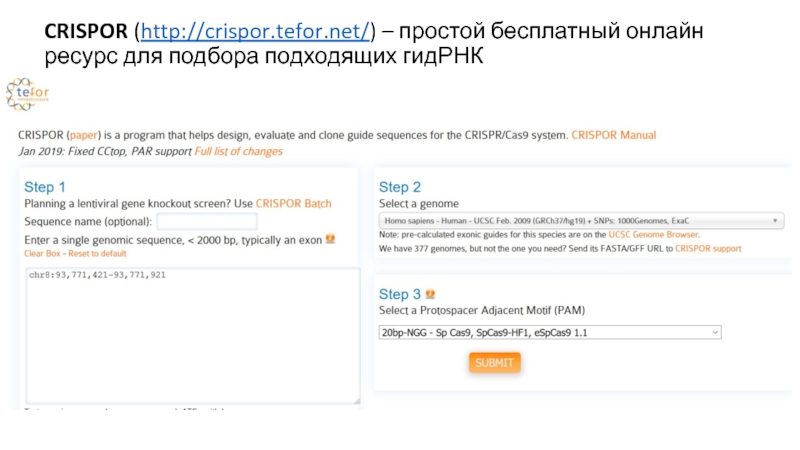
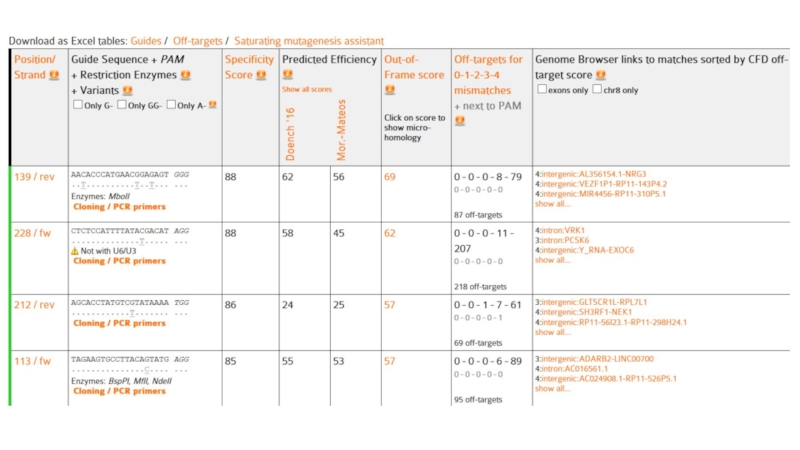
Слайд 43CRISPOR (http://crispor.tefor.net/) – простой бесплатный онлайн ресурс для подбора подходящих
гидРНК
Слайд 45Риски
Слишком простая система. Можно сделать все без шума достаточно дешево
и незаметно. А соблазн поиграться в Бога велик.
Риск грубых ошибок
или злонамеренного вредительства действительно есть, и вопрос о механизмах контроля действительно серьезный.Здоровье
Сельское хозяйство
Биоразнообразие