Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Амины
Содержание
- 1. Амины
- 2. Азотсодержащие соединения
- 3. Амины – это производные аммиака, в молекуле
- 4. Модель молекулы метиламина
- 5. Слайд 5
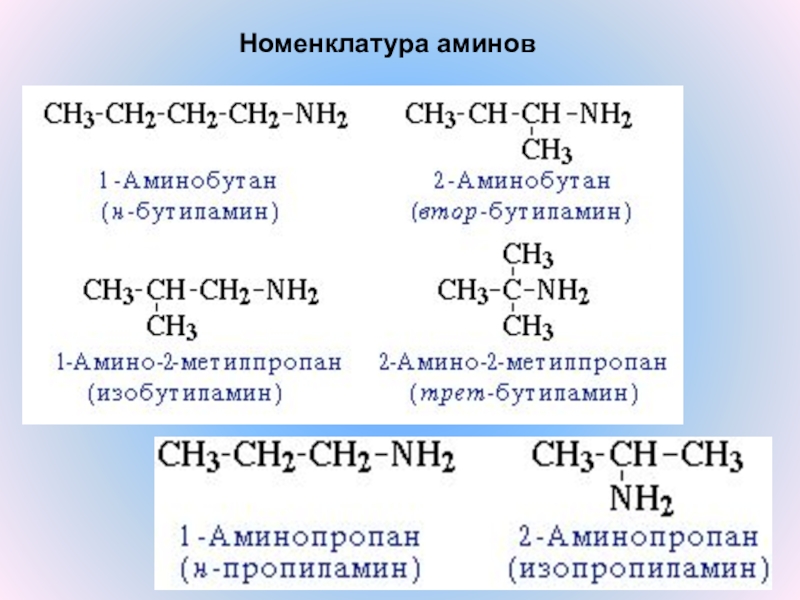
- 6. Номенклатура аминов
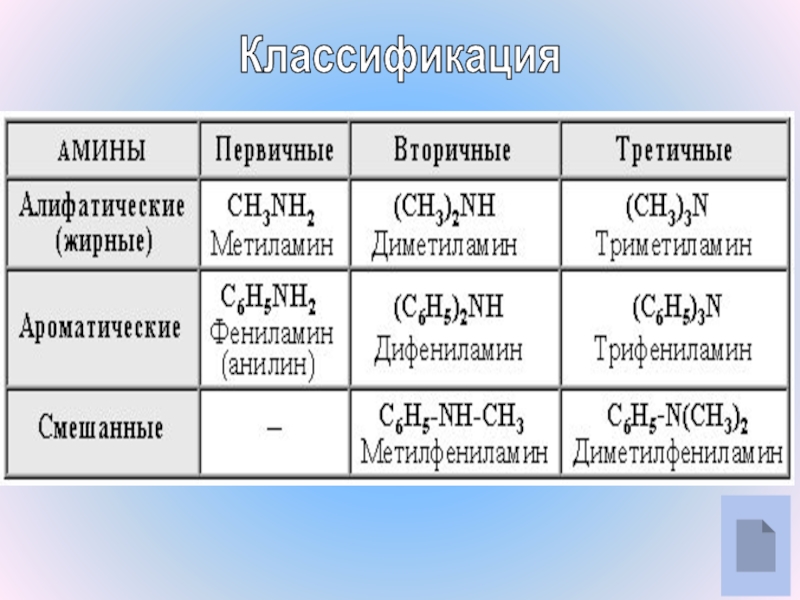
- 7. Классификация
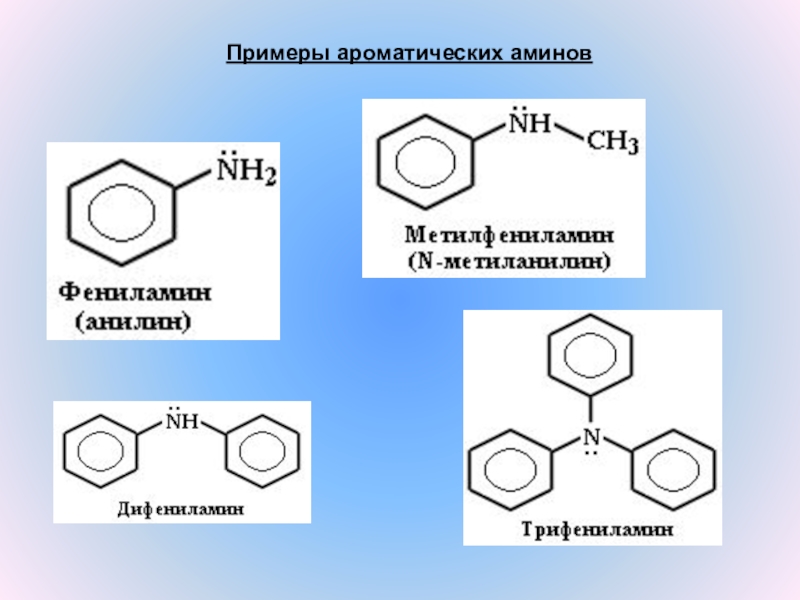
- 8. Примеры ароматических аминов
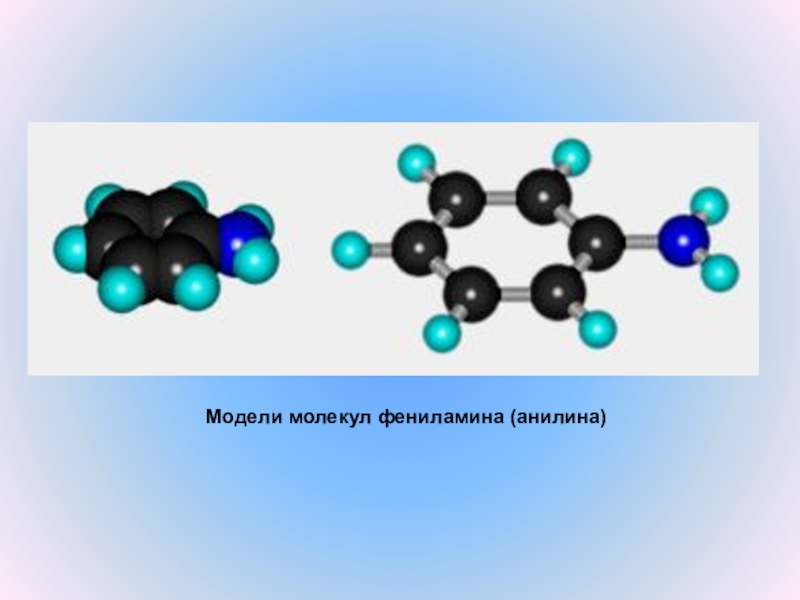
- 9. Модели молекул фениламина (анилина)
- 10. Структурная изомерия- углеродного скелета, начиная с С4H9NH2
- 11. Физические свойства аминовПри обычной температуре только низшие
- 12. Химические свойства аминов:Взаимодействие с кислотамиВзаимодействие с водойРеакции окисления
- 13. Основные свойства аминов:CH3-NH2 + HCl
- 14. Бромирование анилинаДля ароматических аминов характерны также реакции замещения в бензольном ядре
- 15. Амины способны окисляться с образованием различных продуктов,
- 16. Получение аминовАмины получают из галогеноалканов и аммиака.Анилин
- 17. Этим способом получают из первичных аминов вторичные
- 18. Скачать презентанцию
Азотсодержащие соединения
Слайды и текст этой презентации
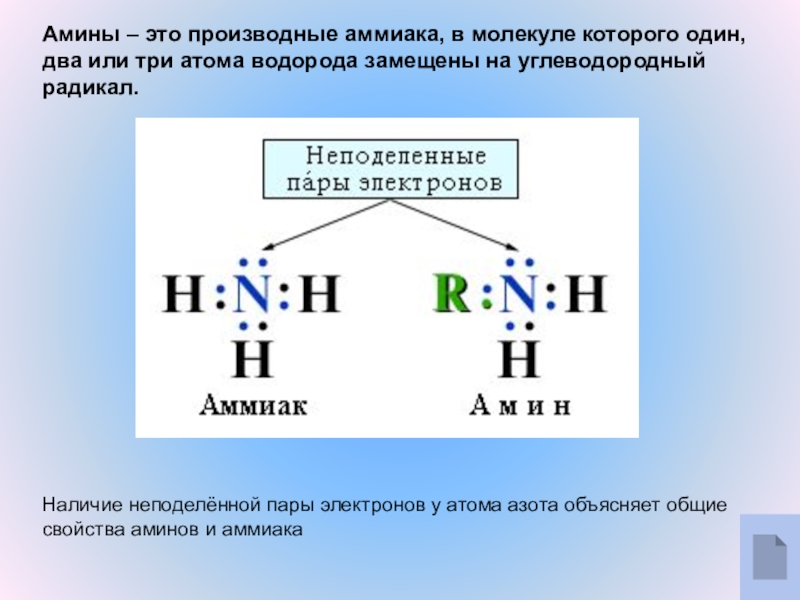
Слайд 3Амины – это производные аммиака, в молекуле которого один, два
или три атома водорода замещены на углеводородный радикал.
электронов у атома азота объясняет общие свойства аминов и аммиакаСлайд 10Структурная изомерия
- углеродного скелета, начиная с С4H9NH2
- положения
аминогруппы, начиная с С3H7NH2
- изомерия аминогруппы, связанная с изменением
степени замещенности атомов водорода при азоте Пространственная изомерия
Возможна оптическая изомерия, начиная с С4H9NH2
Изомерия
Слайд 11Физические свойства аминов
При обычной температуре только низшие жирные амины CH3NH2,
(CH3)2NH, (CH3)3N – газы (с запахом аммиака), средние амины –
жидкости с резким запахом гниющей рыбы, высшие – твердые вещества без запаха.Амины способны к образованию водородных связей с водой.
Поэтому низшие амины хорошо растворимы в воде. С увеличением числа и размеров углеводородных радикалов растворимость аминов в воде уменьшается, т.к. увеличиваются пространственные препятствия к
образованию водородных связей.
Ароматические амины – бесцветные жидкости и твердые вещества с неприятным запахом, в воде практически не растворяются.
Слайд 12Химические свойства аминов:
Взаимодействие с кислотами
Взаимодействие с водой
Реакции окисления
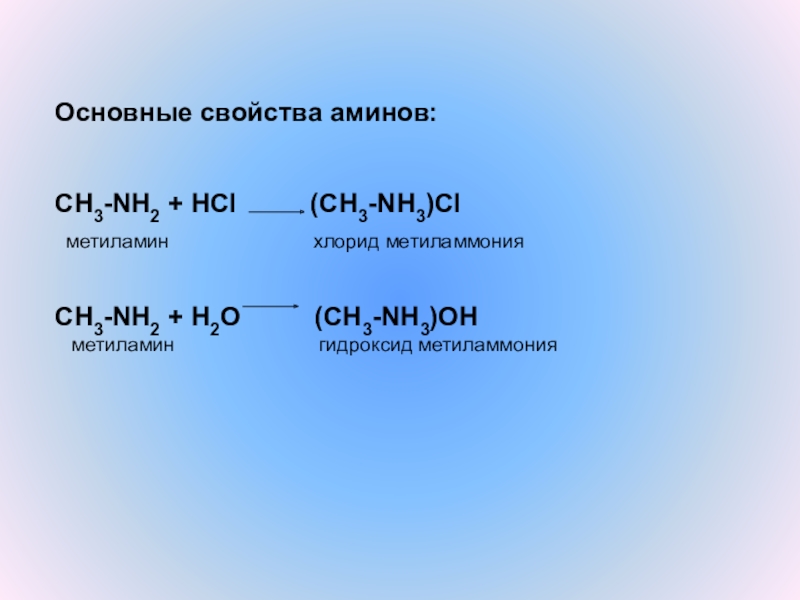
Слайд 13Основные свойства аминов:
CH3-NH2 + HCl (CH3-NH3)Cl
метиламин
хлорид метиламмонияCH3-NH2 + H2O (CH3-NH3)OH
метиламин гидроксид метиламмония
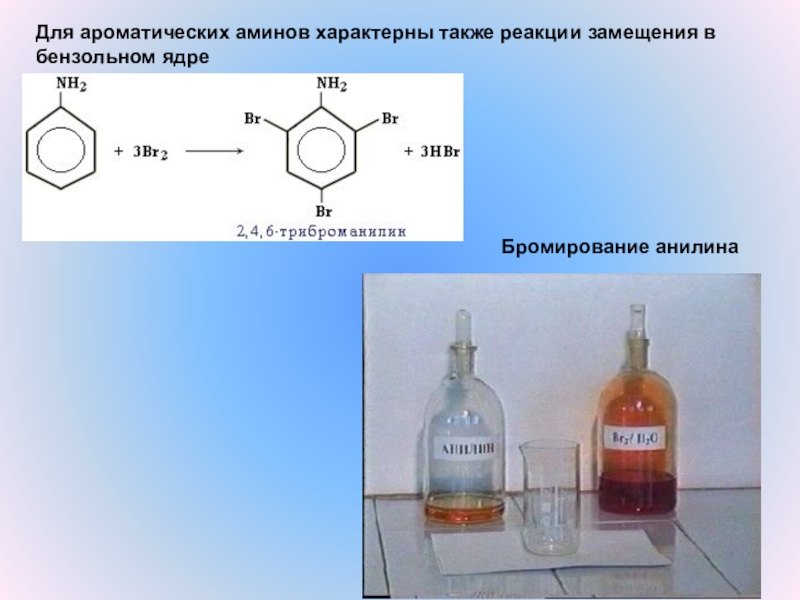
Слайд 14Бромирование анилина
Для ароматических аминов характерны также реакции замещения в бензольном
ядре
Слайд 15Амины способны окисляться с образованием различных продуктов, строение которых зависит
от типа амина и условий реакции.
Например, при действии перманганата калия
на первичные ароматические амины образуются нитропроизводные аренов:KMnO4
С6H5NH2 + 3[O] С6H5NO2 + H2O
анилин нитробензол
Ароматические амины легко окисляются на воздухе, приобретая при этом темную окраску.
Полное окисление аминов происходит при их горении:
4СH3NH2 + 9O2 4CO2 + 10H2O + 2N2
В отличие от аммиака, амины способны воспламеняться от открытого пламени.
Слайд 16Получение аминов
Амины получают из галогеноалканов и аммиака.
Анилин в промышленности получают
по реакции Зинина:
C6H5NO2 + 6H
C6H5NH2 + H2Oнитробензол анилин
Атомарный водород образуется при действии соляной кислоты на чугунную стружку
Слайд 17Этим способом получают из первичных аминов вторичные и третичные, а
из вторичных – третичные. Процесс идет через образование солей алкиламмония,
которые при нагревании превращаются амины.Например:
tC
CH3NH2 + C2H5Cl [(CH3)2NH2]+Cl– (CH3)2NH + HCl
метиламин хлорид диметил- диметиламин
аммония
В избытке алкилгалогенида образуется третичные амины:
tC
CH3NH2 + 2C2H5Br CH3N(C2H5)2 + 2HBr
метиламин метилдиэтиламин
Реакции алкилирования аминов