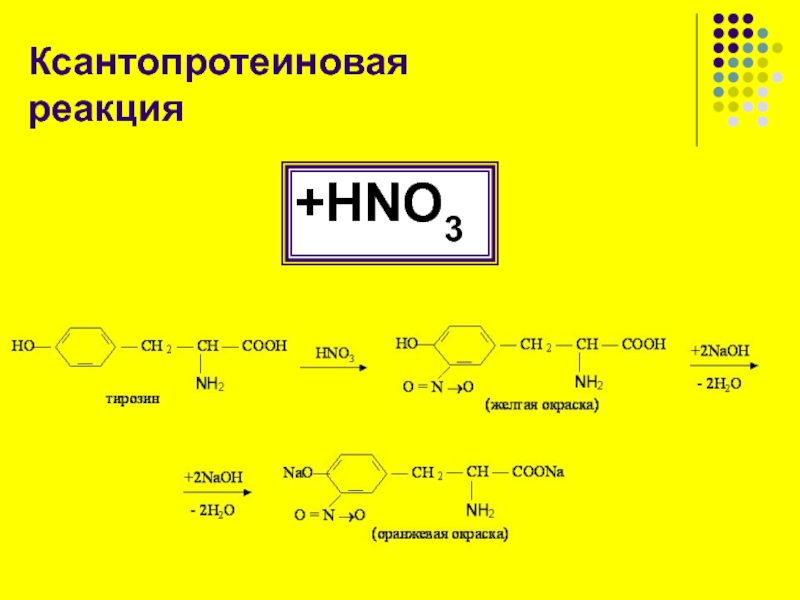
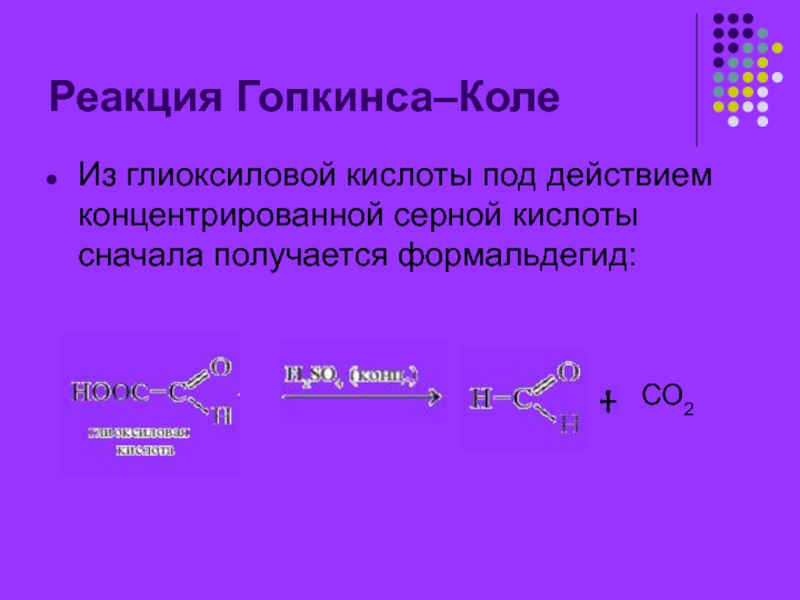
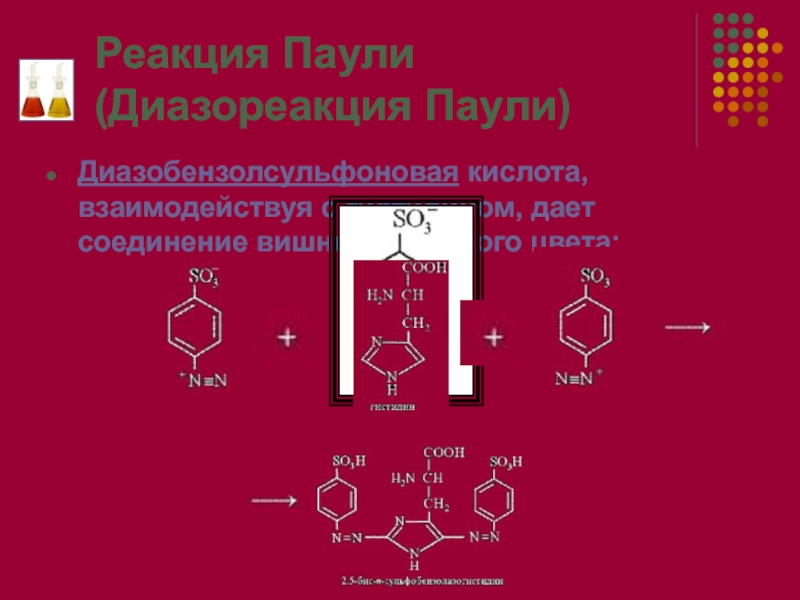
множество цветных (в том числе именных) реакций. Многие из них
высокоспецифичны, что позволяет определять ничтожные количества той или иной аминокислоты.Надо помнить, что все качественные реакции – это реакции не собственно на белки, а на определенные аминокислоты, входящие в их состав.