Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Экологический цикл производства и применения биоэтанола
Содержание
- 1. Экологический цикл производства и применения биоэтанола
- 2. Слайд 2
- 3. Получение этанола из растительного сырьяэнергию можно получить,
- 4. Выход этанола из тонны сырья, 90%ая конверсия
- 5. Выход продуктов с тонны сырья (сухой помол):
- 6. Размер завода в Европе - средний биозавод
- 7. СХЕМА ГЛИКОЛИЗА Ф1 гексокиназа; Ф2 глюкозофосфатизомераза; Ф3
- 8. Получение глицеринаЕсли к дрожжам, сбраживающим глюкозу, добавить
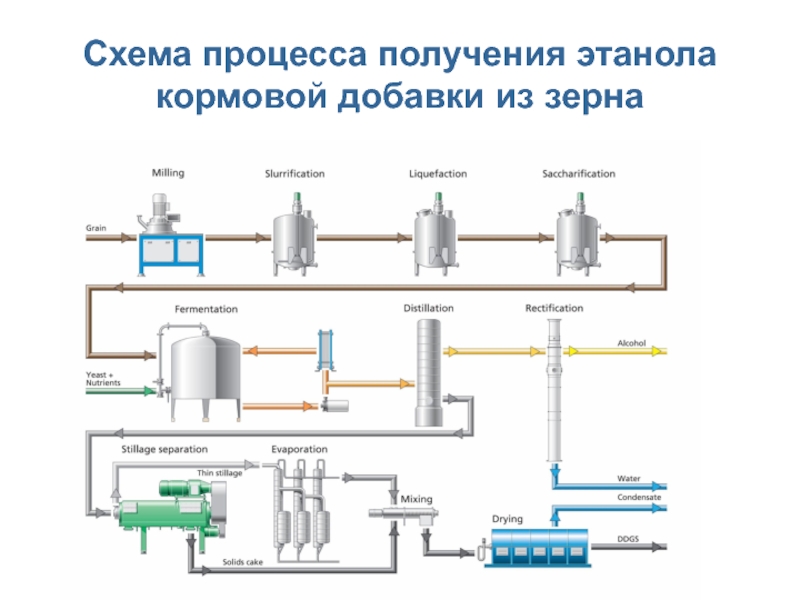
- 9. Схема процесса получения этанола кормовой добавки из зерна
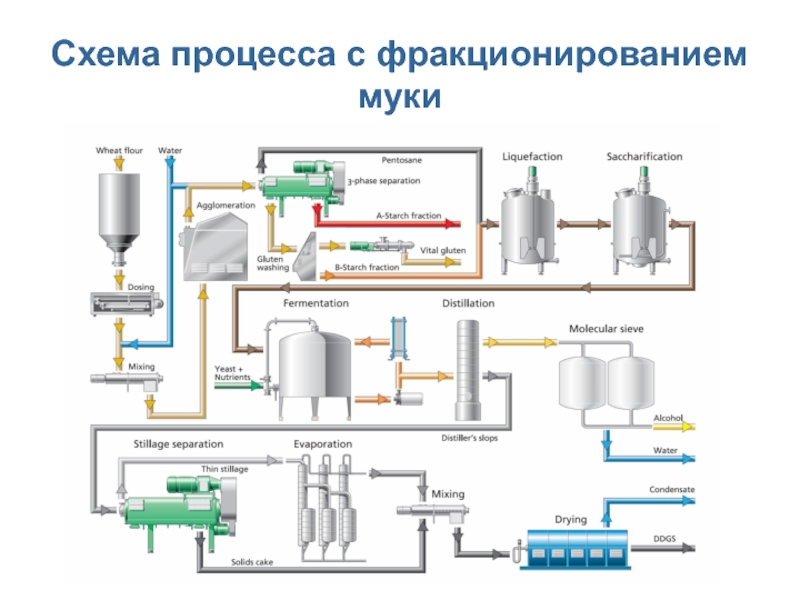
- 10. Схема процесса с фракционированием муки
- 11. Промышленная или "белая" биотехнология - использование микроорганизмов
- 12. Слайд 12
- 13. Ацетонбутанольное брожениеClostridium histolyticum или С. septicum -
- 14. Образование нейтральных продуктов при броженииПри ацетонобутиловом брожении
- 15. Слайд 15
- 16. Спорообразование у анаэробных бактерий: 1 — Clostridium
- 17. Созревание спор у Cl. sporopenitum
- 18. Преимущества бутанола в качесстве биотоплива перед этанолом:
- 19. Основные продукты брожения некоторых сахаролитических клостридиев
- 20. 11 г/л н-бутанола и 3,4 г/л ацетона
- 21. Молочнокислое брожениеЛактат-дегидрогеназаХарактеристика таксономических групп гомоферментативных молочнокислых бактерийСООН
- 22. Использование полилактатовСредства личной гигиены, защитная одежда, фильтры,
- 23. Технологическая схема получения молочной кислотыНа сегодняшний день
- 24. Пропионовокислое брожениеВ род Propionibacterium входят грамположительные, неподвижные,
- 25. Уксуснокислые бактерииУксуснокислые бактерии, выделенные в роды Gluconobacter
- 26. Производство уксуса Продуцент Acetobacter acetiКомпоненты питательной среды Этиловый
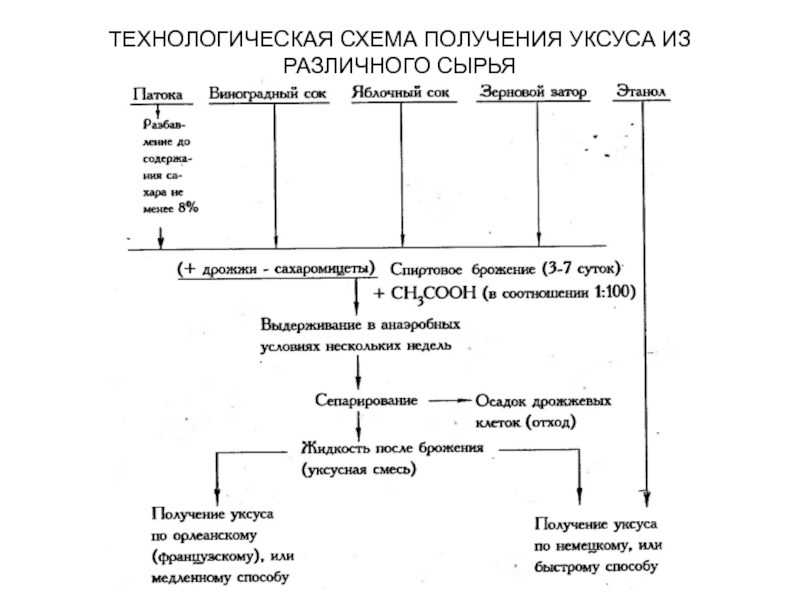
- 27. ТЕХНОЛОГИЧЕСКАЯ СХЕМА ПОЛУЧЕНИЯ УКСУСА ИЗ РАЗЛИЧНОГО СЫРЬЯ
- 28. Получение L-аскорбиновой кислоты Ферментацию G.oxydans проводят на
- 29. ПОЛУЧЕНИЕ ДИОКСИАЦЕТОНА Бактерии Gluconobacter oxydans 8% глицерина, 0,2%
- 30. Ориентировочные дозы внесения моногидрата лимонной кислоты в
- 31. ПОЛУЧЕНИЕ ЛИМОННОЙ КИСЛОТЫAspergillus niger. 1 – гифы;
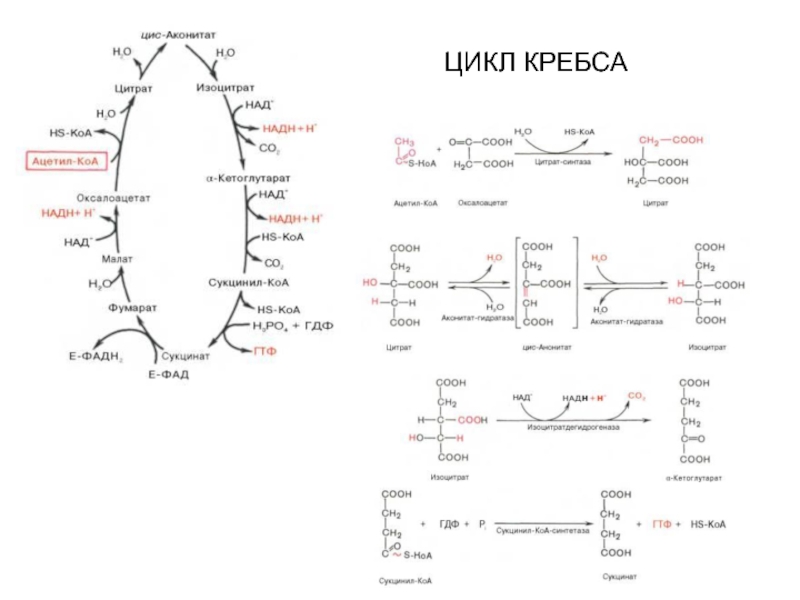
- 32. ЦИКЛ КРЕБСА
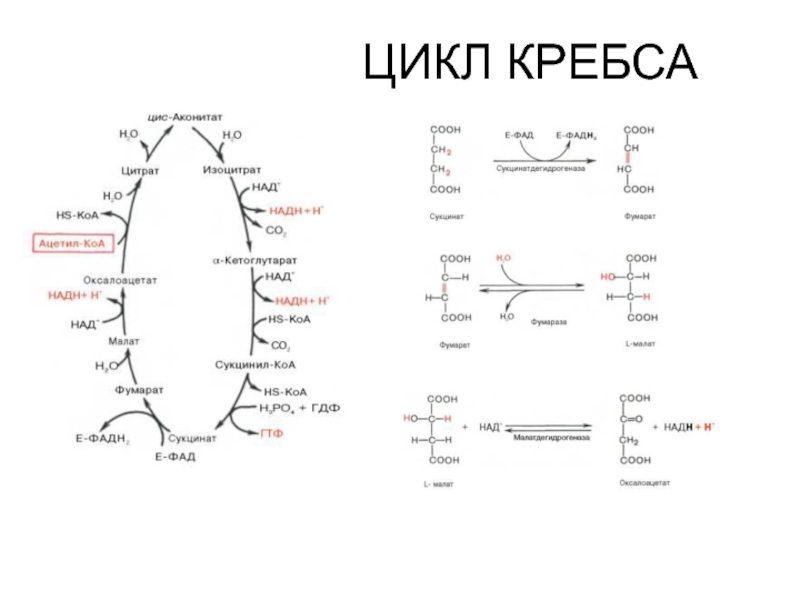
- 33. ЦИКЛ КРЕБСА
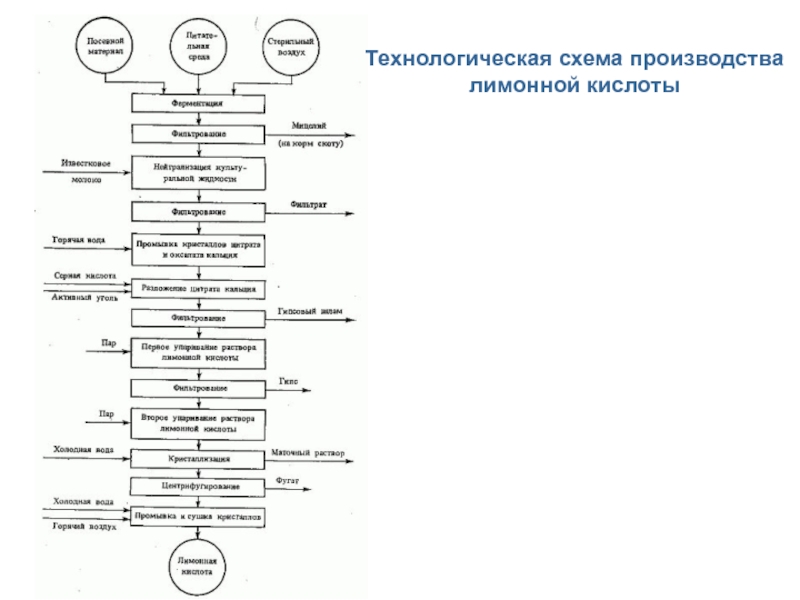
- 34. Технологическая схема производства лимонной кислоты
- 35. Слайд 35
- 36. Рост Aspergillus niger и образование
- 37. Слайд 37
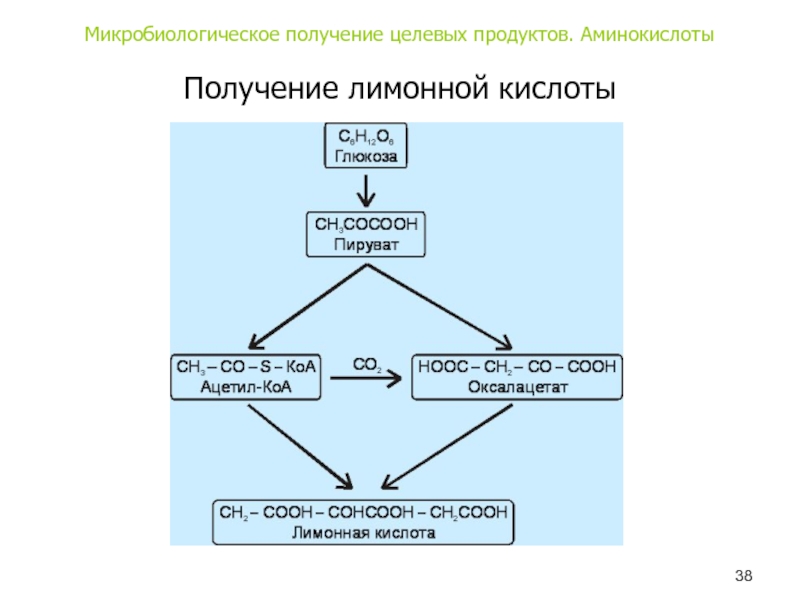
- 38. Получение лимонной кислотыМикробиологическое получение целевых продуктов. Аминокислоты
- 39. Скачать презентанцию
Слайды и текст этой презентации
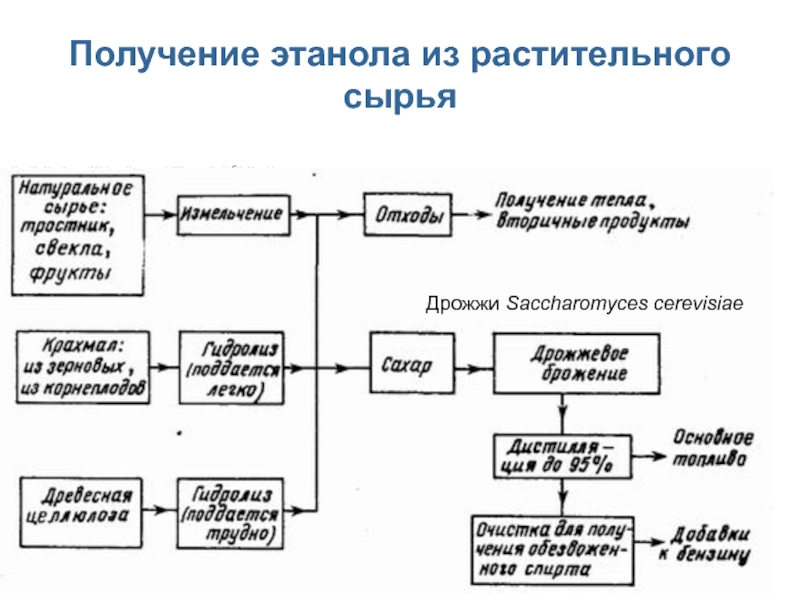
Слайд 3Получение этанола из растительного сырья
энергию можно получить, сжигая остающиеся отходы
биомассы.
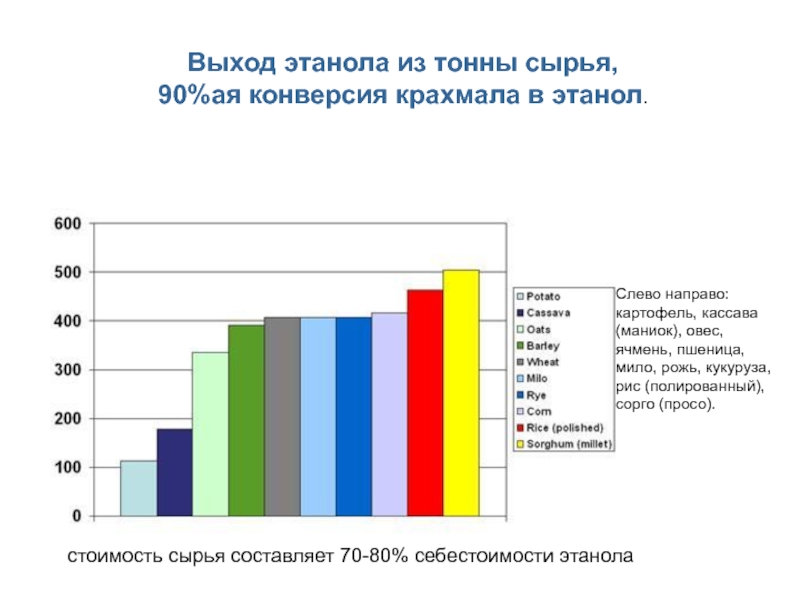
Слайд 4Выход этанола из тонны сырья,
90%ая конверсия крахмала в этанол.
Слево
направо: картофель, кассава (маниок), овес, ячмень, пшеница, мило, рожь, кукуруза,
рис (полированный), сорго (просо).стоимость сырья составляет 70-80% себестоимости этанола
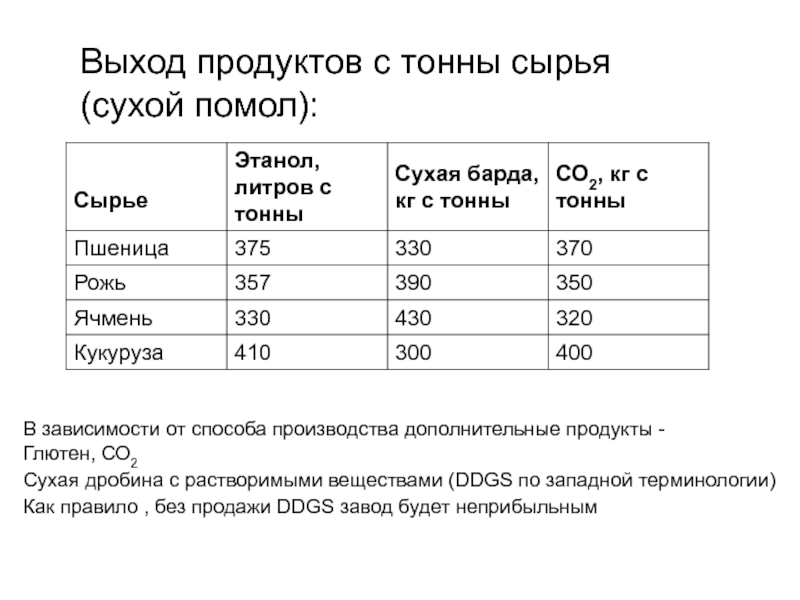
Слайд 5Выход продуктов с тонны сырья (сухой помол):
В зависимости от
способа производства дополнительные продукты -
Глютен, СО2
Сухая дробина с растворимыми
веществами (DDGS по западной терминологии) Как правило , без продажи DDGS завод будет неприбыльным
Слайд 6
Размер завода в Европе - средний биозавод производит от 150
до 200 млн литров этанола год. Некоторые заводы имеют мощность
1 млрд литров этанола год. Строить завод мощностью менее 75 млн литров нецелесообразно.Степень очистки - биозавод по производству этанола имеет две ректификационные колонны в отличие от завода пищевого спирта, где таких колон пять
Содержание воды - топливный биоэтанол почти не содержит воды его концентрация 99.8%. Поэтому в технологии используется дополнительное обезвоживание при помощи молекулярных сит
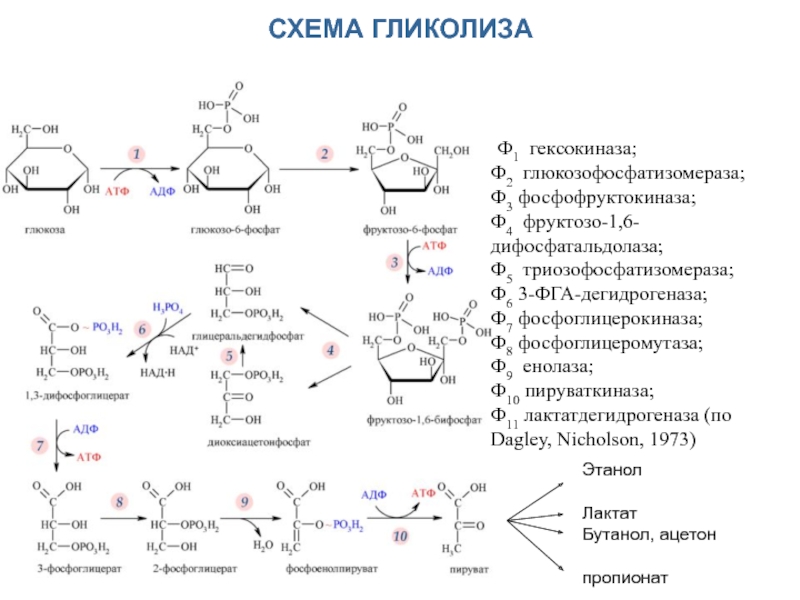
Слайд 7СХЕМА ГЛИКОЛИЗА
Ф1 гексокиназа;
Ф2 глюкозофосфатизомераза;
Ф3 фосфофруктокиназа;
Ф4 фруктозо-1,6-дифосфатальдолаза;
Ф5 триозофосфатизомераза;
Ф6 3-ФГА-дегидрогеназа;
Ф7 фосфоглицерокиназа;
Ф8 фосфоглицеромутаза;
Ф9 енолаза;
Ф10 пируваткиназа;
Ф11 лактатдегидрогеназа (по Dagley, Nicholson, 1973)
Этанол
Лактат
Бутанол, ацетон
пропионат
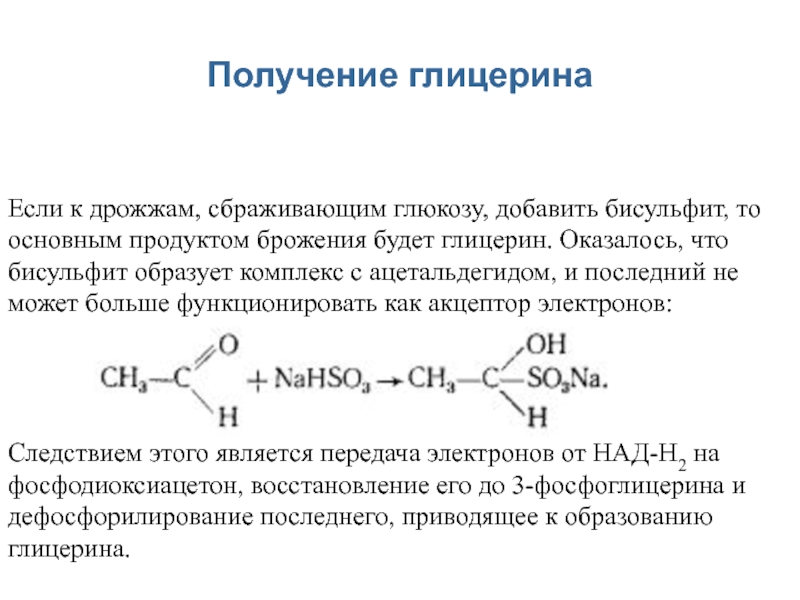
Слайд 8Получение глицерина
Если к дрожжам, сбраживающим глюкозу, добавить бисульфит, то основным
продуктом брожения будет глицерин. Оказалось, что бисульфит образует комплекс с
ацетальдегидом, и последний не может больше функционировать как акцептор электронов:Следствием этого является передача электронов от НАД-H2 на фосфодиоксиацетон, восстановление его до 3-фосфоглицерина и дефосфорилирование последнего, приводящее к образованию глицерина.
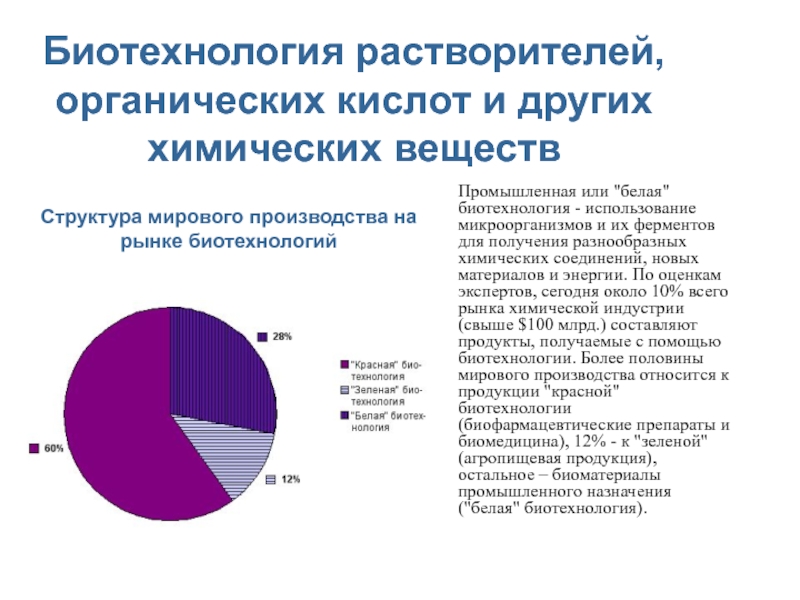
Слайд 11Промышленная или "белая" биотехнология - использование микроорганизмов и их ферментов
для получения разнообразных химических соединений, новых материалов и энергии. По
оценкам экспертов, сегодня около 10% всего рынка химической индустрии (свыше $100 млрд.) составляют продукты, получаемые с помощью биотехнологии. Более половины мирового производства относится к продукции "красной" биотехнологии (биофармацевтические препараты и биомедицина), 12% - к "зеленой" (агропищевая продукция), остальное – биоматериалы промышленного назначения ("белая" биотехнология).Биотехнология растворителей, органических кислот и других химических веществ
Структура мирового производства на рынке биотехнологий
Слайд 13Ацетонбутанольное брожение
Clostridium histolyticum или С. septicum - газовая гангрена.
Clostridium
tetani - столбняк. Эта бактерия при своем росте выделяет очень
сильный нейротоксин, вызывающий тонические судороги мышц.Clostridium botulinum – ботулизм (лат. botulus - колбаса). Образуемый ею токсин может вызвать смерть вследствие нервного паралича, в частности паралича дыхания. Токсин этот термолабилен и быстро (за 15 мин) инактивируется при кипячении.
Клостридии - возбудители болезней и продуценты токсинов
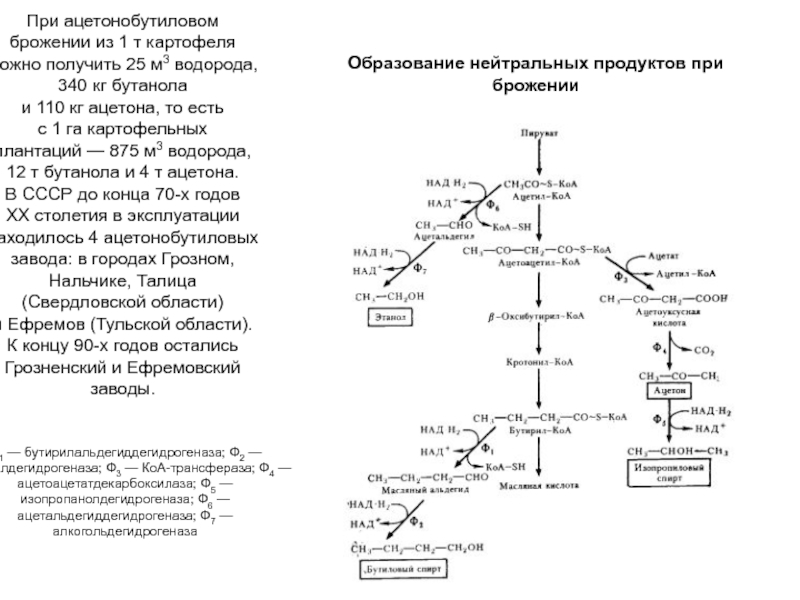
Слайд 14Образование нейтральных продуктов при брожении
При ацетонобутиловом брожении из 1 т картофеля можно получить
25 м3 водорода, 340 кг бутанола и 110 кг ацетона, то есть с 1 га картофельных плантаций — 875 м3 водорода, 12 т бутанола и 4 т ацетона.
В СССР
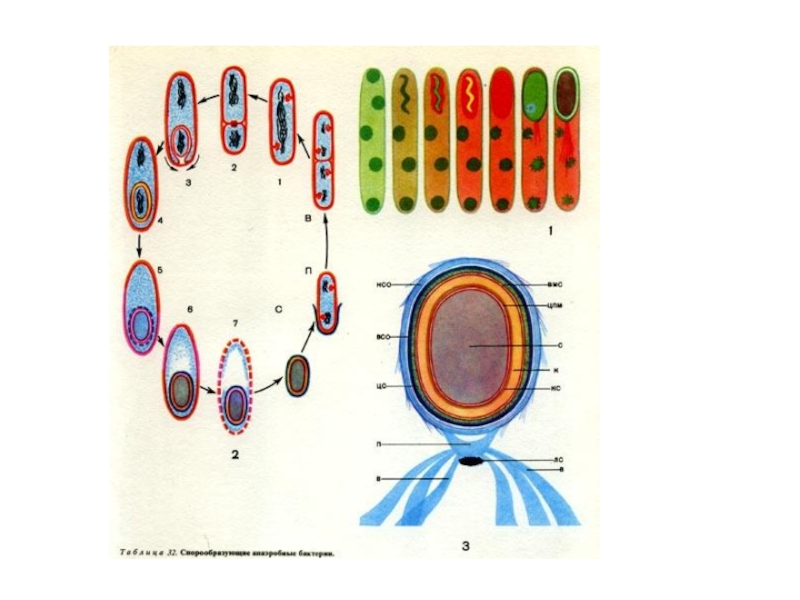
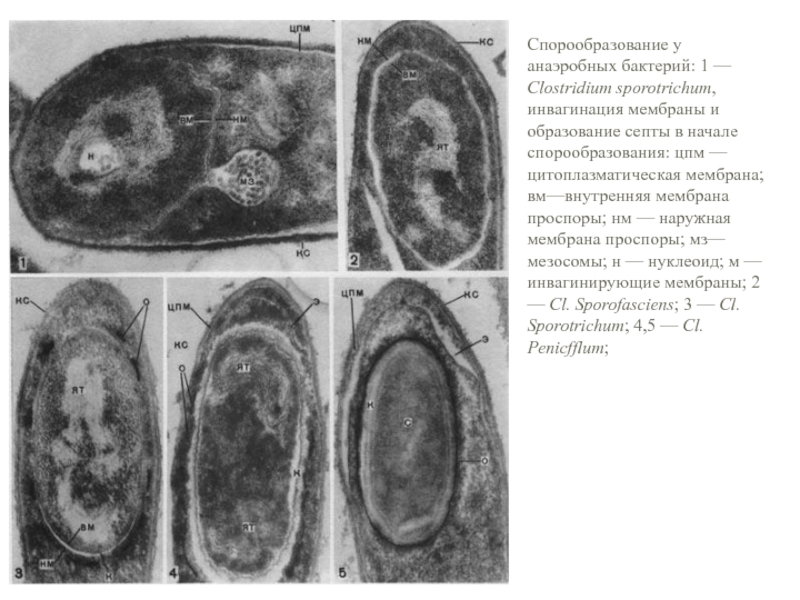
до конца 70-х годов XX столетия в эксплуатации находилось 4 ацетонобутиловых завода: в городах Грозном, Нальчике, Талица (Свердловской области) и Ефремов (Тульской области). К концу 90-х годов остались Грозненский и Ефремовский заводы. Слайд 16Спорообразование у анаэробных бактерий: 1 — Clostridium sporotrichum, инвагинация мембраны
и образование септы в начале спорообразования: цпм — цитоплазматическая мембрана;
вм—внутренняя мембрана проспоры; нм — наружная мембрана проспоры; мз—мезосомы; н — нуклеоид; м — инвагинирующие мембраны; 2 — Cl. Sporofasciens; 3 — Cl. Sporotrichum; 4,5 — Cl. Penicfflum;Слайд 18Преимущества бутанола в качесстве биотоплива перед этанолом:
1. Бутанол при сгорании
дает на 25% больше энергии, чем этанол: 25 529 кДж на 1 литр бутанола
против 19 494 кДж на 1 литр этанола. Бензин - около 26 688 кДж на 1 литр;2. Бутанол безопаснее в использовании, поскольку он в шесть раз менее летуч, чем этанол и в 13,5 раз менее летуч, чем бензин. Не требует особых изменений пропорций смеси при использовании зимой и летом.
3. Бутанол — гораздо менее агрессивное вещество, чем этанол, поэтому может транспортироваться по существующим топливным трубопроводам;
4. Бутанол можно смешивать с бензином;
5. Бутанол может полностью заменять бензин, тогда как этанол может использоваться только как добавка к бензину с максимальным содержанием в смеси не более 85% и только после существенных переделок двигателя. В настоящее время в мире преобладают смеси с 10%-ным содержанием этанола;
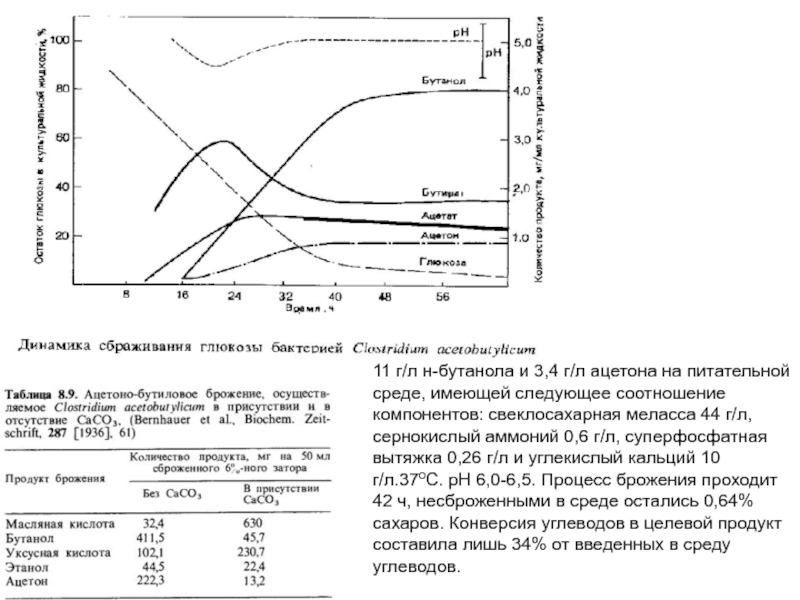
Слайд 2011 г/л н-бутанола и 3,4 г/л ацетона на питательной среде,
имеющей следующее соотношение компонентов: свеклосахарная меласса 44 г/л, сернокислый аммоний
0,6 г/л, суперфосфатная вытяжка 0,26 г/л и углекислый кальций 10 г/л.37оС. pH 6,0-6,5. Процесс брожения проходит 42 ч, несброженными в среде остались 0,64% сахаров. Конверсия углеводов в целевой продукт составила лишь 34% от введенных в среду углеводов.Слайд 21Молочнокислое брожение
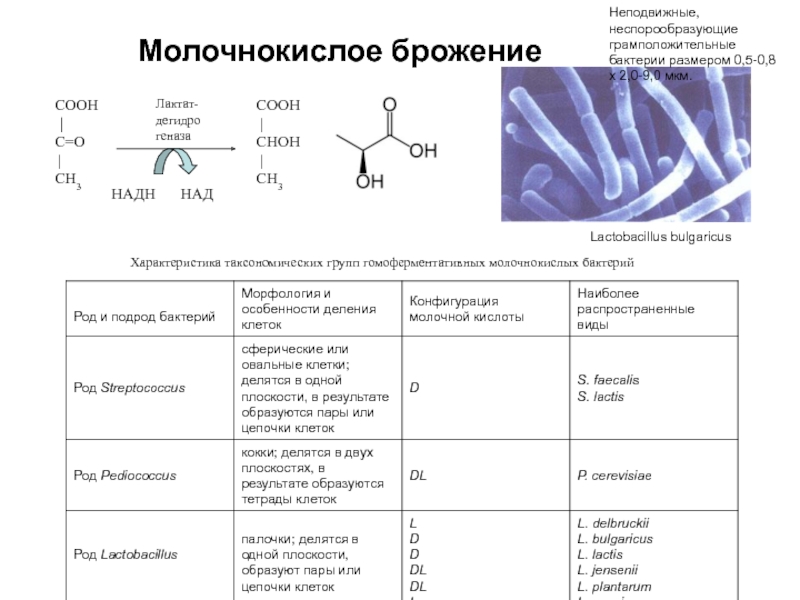
Лактат-дегидрогеназа
Характеристика таксономических групп гомоферментативных молочнокислых бактерий
СООН
|
С=О
|
СН3
НАДН
НАД
СООН
|
СНОН
|
СН3
Неподвижные, неспорообразующие грамположительные бактерии размером 0,5-0,8 x 2,0-9,0 мкм.
Lactobacillus
bulgaricusСлайд 22Использование полилактатов
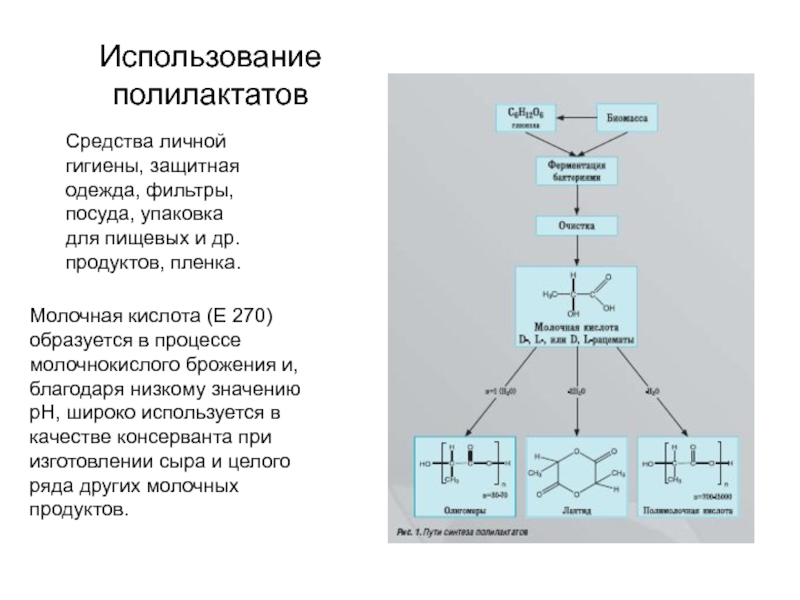
Средства личной гигиены, защитная одежда, фильтры, посуда, упаковка для
пищевых и др. продуктов, пленка.
Молочная кислота (Е 270) образуется в
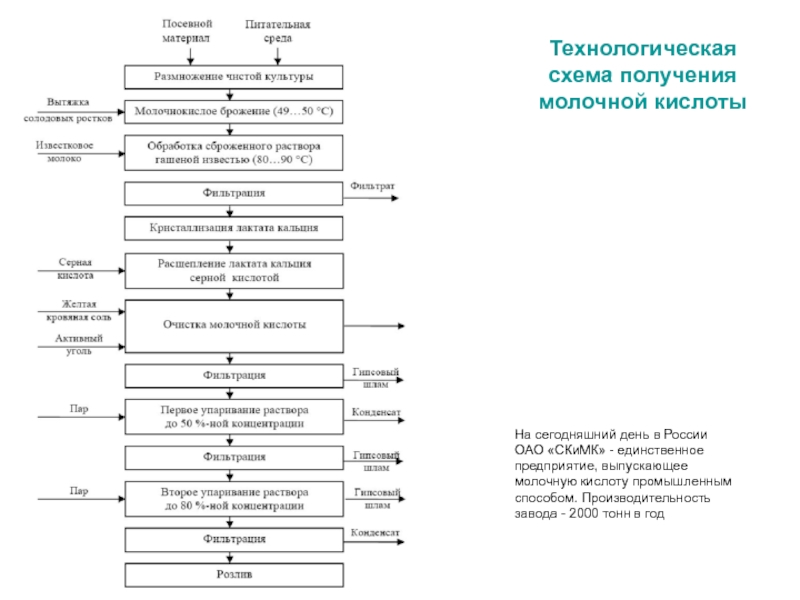
процессе молочнокислого брожения и, благодаря низкому значению рН, широко используется в качестве консерванта при изготовлении сыра и целого ряда других молочных продуктов. Слайд 23Технологическая схема получения молочной кислоты
На сегодняшний день в Росcии ОАО
«СКиМК» - единственное предприятие, выпускающее молочную кислоту промышленным способом. Производительность
завода - 2000 тонн в годСлайд 24Пропионовокислое брожение
В род Propionibacterium входят грамположительные, неподвижные, не образующие спор
палочковидные бактерии, размножающиеся бинарным делением. В зависимости от условий культивирования
и цикла развития форма клетки может меняться до кокковидной, изогнутой или булавовидной. Типовой вид — P. freudenreichii.Е280 пропионовая кислота, Е281 пропионат натрия, Е282 пропионат кальция, Е283 пропионат калия,
Пропионовая кислота и ее соли (Е 280-283) рекомендуются в качестве основного консерванта (или в комбинации с сорбиновой кислотой и ее солями) для сыроварения. Пропионаты также используются при производстве других молочных продуктов и в хлебопечении.
Слайд 25Уксуснокислые бактерии
Уксуснокислые бактерии, выделенные в роды Gluconobacter и Acetobacter, могут
получать энергию, осуществляя неполное окисление ряда органических соединений. Это грамотрицательные
бесспоровые палочки, слабоподвижные за счет перитрихиально или полярно расположенных жгутиков, или неподвижные. Облигатные аэробы.К числу окисляемых соединений относятся одноатомные спирты, содержащие от 2 до 5 углеродных атомов, а также многоатомные спирты — производные сахаров. Окисление первичных спиртов приводит к образованию кислот. Например, этанол с помощью соответствующих дегидрогеназ окисляется до ацетата:
С2Н5ОН CH3-CHO
CH3-CHO CH3-CОOН
Вторичные спирты окисляются до кетонов:
CH3-CHOH-CH3 CH3-CO-CH3.
Многоатомные спирты окисляются этими бактериями в альдозы и кетозы, например: сорбит ® сорбоза; глицерин ® диоксиацетон. Альдозы и кетозы могут далее окисляться в соответствующие кислоты.
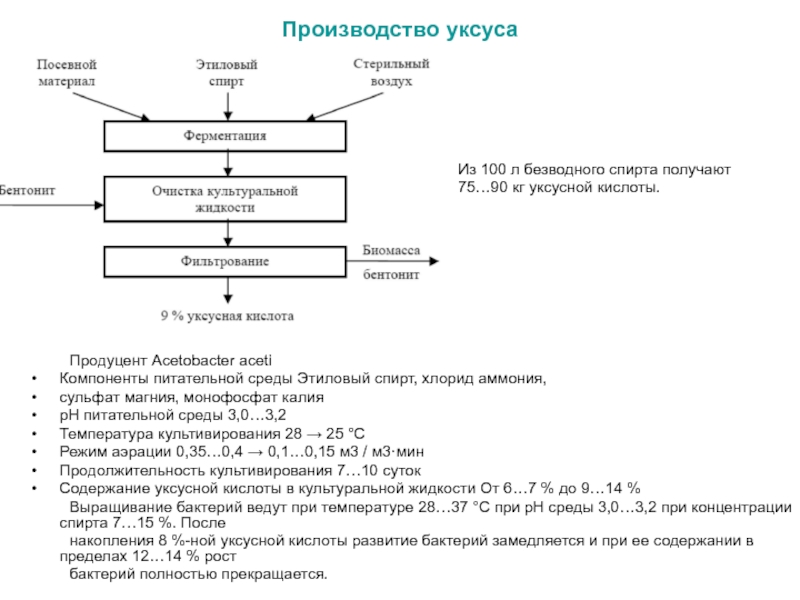
Слайд 26Производство уксуса
Продуцент Acetobacter aceti
Компоненты питательной среды Этиловый спирт, хлорид аммония,
сульфат
магния, монофосфат калия
рН питательной среды 3,0…3,2
Температура культивирования 28 → 25
°СРежим аэрации 0,35…0,4 → 0,1…0,15 м3 / м3·мин
Продолжительность культивирования 7…10 суток
Содержание уксусной кислоты в культуральной жидкости От 6…7 % до 9…14 %
Выращивание бактерий ведут при температуре 28…37 °С при рН среды 3,0…3,2 при концентрации спирта 7…15 %. После
накопления 8 %-ной уксусной кислоты развитие бактерий замедляется и при ее содержании в пределах 12…14 % рост
бактерий полностью прекращается.
Из 100 л безводного спирта получают 75…90 кг уксусной кислоты.
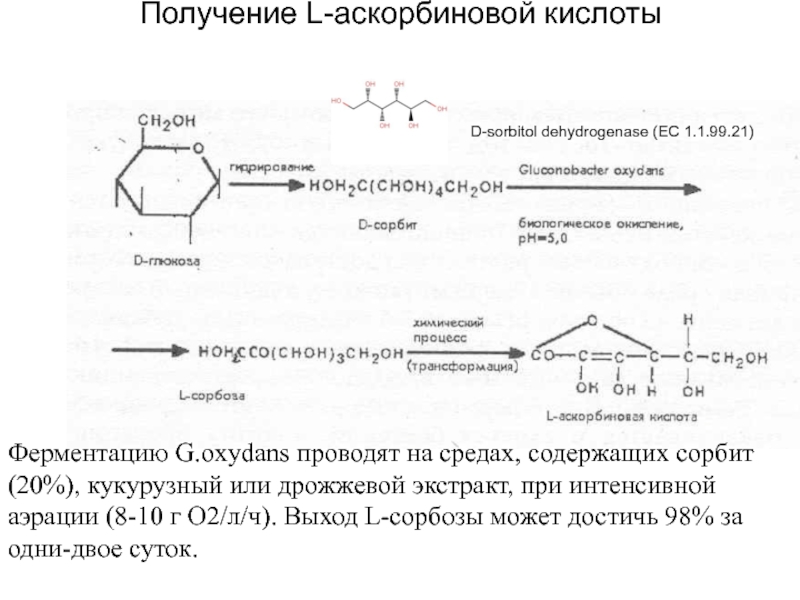
Слайд 28Получение L-аскорбиновой кислоты
Ферментацию G.oxydans проводят на средах, содержащих сорбит (20%),
кукурузный или дрожжевой экстракт, при интенсивной аэрации (8-10 г О2/л/ч).
Выход L-сорбозы может достичь 98% за одни-двое суток.D-sorbitol dehydrogenase (EC 1.1.99.21)
Слайд 29ПОЛУЧЕНИЕ ДИОКСИАЦЕТОНА
Бактерии Gluconobacter oxydans
8% глицерина, 0,2% монокалийфосфата, 1% (по
сухой массе) дрожжевого экстракта.
Выращивание биомассы 36 ч при 28оС.
Клетки бактерий отделяют от питательной среды центрифугированием и отмывают водопроводной водой от посторонних примесей.
Подготовленную таким образом биомассу помещают в биореактор и заливают двумя литрами раствора состава: глицерин 10%, монокалийфосфат 0,2% и водопроводная вода. Процесс биотрансформации ведут в аэробных условиях при интенсивном перемешивании, поддерживая температуру 28оС и рН 5,0 48 ч. Диоксиацетон 9,6% (96%).Слайд 30Ориентировочные дозы внесения моногидрата лимонной кислоты в различные продукты
Е330
ОАО
«Белгородский завод лимонной кислоты (Цитробел)»
по объему производства лимонная кислота является
одним из главных продуктов микробного синтеза, мировой объем ее производства достигает 400 тыс. тонн в год (около 325 млн евро)Слайд 31ПОЛУЧЕНИЕ ЛИМОННОЙ КИСЛОТЫ
Aspergillus niger. 1 – гифы; 2 – конидиеносец;
3 – пузырек; 4 – стеригмы первого ряда; 5 –
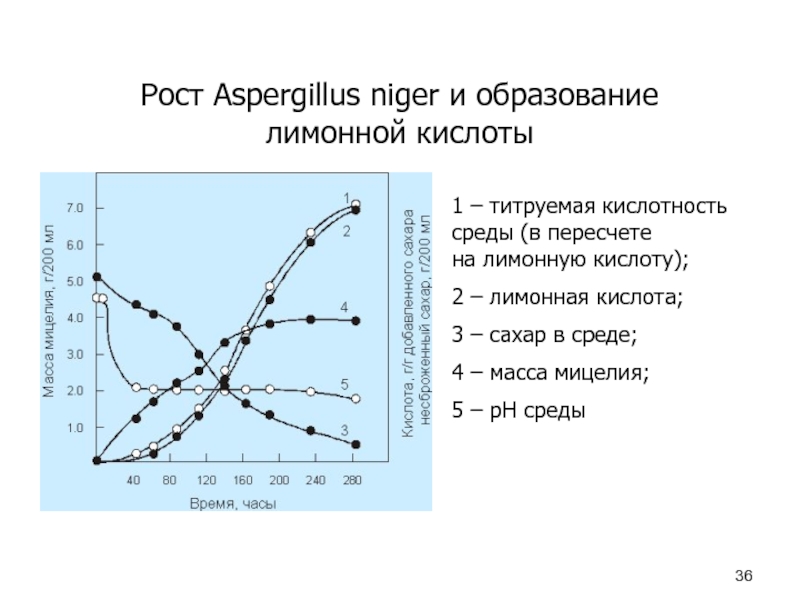
стеригмы второго ряда; 6 – конидии; 7 – опорные клетки.Слайд 36Рост Aspergillus niger и образование
лимонной кислоты
1 – титруемая кислотность
среды (в пересчете на лимонную кислоту); 2 – лимонная кислота;
3 – сахар в среде;
4 – масса мицелия;
5 – рН среды