Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Электрокинетические свойства коллоидно?дисперсных систем. Строение мицелл
Содержание
- 1. Электрокинетические свойства коллоидно?дисперсных систем. Строение мицелл
- 2. Электрокинетические свойства коллоидно‒дисперсных систем. Строение мицеллЛекция №23
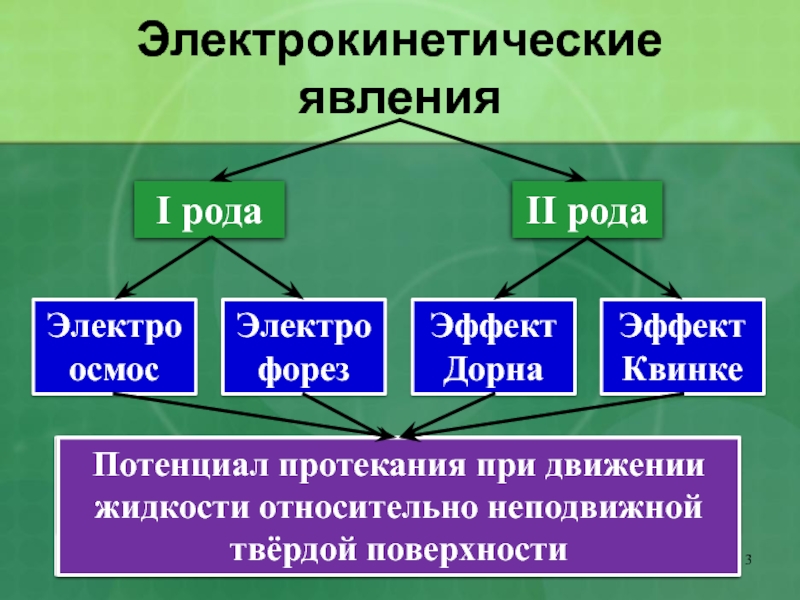
- 3. Электрокинетические явленияI родаII родаЭлектрофорезЭлектроосмосЭффект ДорнаЭффект КвинкеДвижение частиц
- 4. Мицеллярная теория лиофобных золейМицелла ‒ гетерогенная микросистема,
- 5. Мицеллярная теория лиофобных золей – агрегат с
- 6. Мицеллярная теория лиофобных золей– ядро с адсорбционным
- 7. Получение золя конденсационным методом по реакции обменаBaCl2 + H2SO4 ? BaSO4↓ + 2HClизбытокагрегатBa2+2Cl–ПОИпротивоионстабилизаторm[BaSO4]·nBa2+·(2n – x)Cl–{}x+·xCl–
- 8. Мицелла{m[BaSO4] • nBa2+ (2n – x)Cl–}x+ • xCl–агрегатадсорбционный слойядрогрануладиффузионный слойМИЦЕЛЛА
- 9. Факторы агрегативной устойчивости золяОдноимённый заряд коллоидных частиц;Гидратная (сольватная) оболочка, окружающая ионы диффузионного слоя.BaSO4
- 10. Возникновение ДЭС и потенциалов в мицелле{m[BaSO4] •
- 11. Возникновение ДЭС и потенциалов в мицеллеПо величине
- 12. Факторы, влияющие на ζКонцентрация стабилизатора.Состояние ИЭТ золя,
- 13. {m[BaSO4] • nBa2+ (2n – x)Cl–}x+ •xCl–Электрофорез и электроосмоскатоданодЭлектрофорезЭлектроосмос
- 14. Расчёт ζПоскольку ζ обнаруживает себя при попадании
- 15. СПАСИБО ЗА ВНИМАНИЕ!
- 16. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Электрокинетические свойства коллоидно‒дисперсных систем. Строение мицелл
Лекция №23 курса
«Общая химия»
Лектор: проф.
Иванова Надежда Семёновна
Слайд 3Электрокинетические явления
I рода
II рода
Электрофорез
Электроосмос
Эффект Дорна
Эффект Квинке
Движение частиц ДФ в неподвижной
ДС
Движение жидкости относительно неподвижной твёрдой поверхности пористых мембран
Потенциал оседания при
движении частиц ДФ в неподвижной жидкостиПотенциал протекания при движении жидкости относительно неподвижной твёрдой поверхности
Слайд 4Мицеллярная теория лиофобных золей
Мицелла ‒ гетерогенная микросистема, состоящая из микрокристалла
ДФ, окружённого сольватированными ионами стабилизатора.
В мицелле выделяют следующие части:
‒ микрокристаллы
ДФ; их число определяют «m».АГРЕГАТ
Слайд 5Мицеллярная теория лиофобных золей
– агрегат с адсорбированными на нём
потенциалопределяющими ионами (ПОИ).
– ионы, сообщающие заряд коллоидной частице; находят по
правилу Панета – Фаянса – Гана. Их число определяют «n».– ионы, заряд которых противоположен заряду ПОИ.
ЯДРО
ПОИ
ПРОТИВОИОНЫ
Входят в адсорбционный слой противоионов, прочно связанных электростатическим притяжением с ядром; «n – x».
Входят в диффузионный слой противоионов, число которых равно «х»
Слайд 6Мицеллярная теория лиофобных золей
– ядро с адсорбционным слоем противоионов, являющаяся
гигантским многозарядным ионом.
Источником ПОИ и противоионов являются стабилизаторы – электролиты
(один из реагентов, продукт реакции, постороннее вещество).ГРАНУЛА / КОЛЛОИДНАЯ ЧАСТИЦА
Слайд 7Получение золя конденсационным методом по реакции обмена
BaCl2 + H2SO4 ?
BaSO4↓ + 2HCl
избыток
агрегат
Ba2+
2Cl–
ПОИ
противоион
стабилизатор
m[BaSO4]
·nBa2+
·(2n – x)Cl–
{
}
x+
·xCl–
Слайд 8Мицелла
{m[BaSO4] • nBa2+ (2n – x)Cl–}x+ • xCl–
агрегат
адсорбционный слой
ядро
гранула
диффузионный слой
МИЦЕЛЛА
Слайд 9
Факторы агрегативной устойчивости золя
Одноимённый заряд коллоидных частиц;
Гидратная (сольватная) оболочка, окружающая
ионы диффузионного слоя.
BaSO4
Слайд 10Возникновение ДЭС и потенциалов в мицелле
{m[BaSO4] • nBa2+ (2n –
x)Cl–}x+ • xCl–
На границе между ядром и всеми противоионами возникает
ДЭС и потенциал, который называется электротермодинамическим (φ,ε)На границе между гранулой и противоионами диффузионного слоя возникает ДЭС и электрокинетический потенциал (ζ)
Слайд 11Возникновение ДЭС и потенциалов в мицелле
По величине 0 ≤ ζ
< φ. При ζ = 0 имеет место изоэлектрическая точка
золя (ИЭТ), в которой происходит полное разрушение золя.ζкрит. = ±30 мВ. При этом значении золь начинает разрушаться.
Т.о., по величине ζ можно судить об устойчивости золя: чем больше ζ, тем устойчивее золь.
Слайд 12Факторы, влияющие на ζ
Концентрация стабилизатора.
Состояние ИЭТ золя, ζ = 0.
Золь разрушается.
Концентрация посторонних электролитов.
При введении посторонних электролитов, ионы которых обладают
более высокой адсорбционной способностью, чем ионы стабилизатора, возможна перезарядка частиц золя.{m[BaSO4] • nBa2+
xCl–
x+
0
• 2nCl–}
(2n – x)Cl–}
Слайд 13{m[BaSO4] • nBa2+ (2n – x)Cl–}x+ •xCl–
Электрофорез и электроосмос
катод
анод
Электрофорез
Электроосмос
Слайд 14
Расчёт ζ
Поскольку ζ обнаруживает себя при попадании мицеллы в электрическое
поле, для его расчёта используются данные электрофореза и электроосмоса.
Uэ.ф. –
электрофоретическая подвижностьU0 – скорость движения частиц при электрофорезе
η – вязкость ДС
ε0/ε – диэлектрическая постоянная ДС и ДФ





![Электрокинетические свойства коллоидно?дисперсных систем. Строение мицелл Получение золя конденсационным методом по реакции обменаBaCl2 + H2SO4 ? BaSO4↓ + 2HClизбытокагрегатBa2+2Cl–ПОИпротивоионстабилизаторm[BaSO4]·nBa2+·(2n – x)Cl–{}x+·xCl– Получение золя конденсационным методом по реакции обменаBaCl2 + H2SO4 ? BaSO4↓ + 2HClизбытокагрегатBa2+2Cl–ПОИпротивоионстабилизаторm[BaSO4]·nBa2+·(2n – x)Cl–{}x+·xCl–](/img/thumbs/c0a35932d82759ea2781ac2ea6b8b156-800x.jpg)
![Электрокинетические свойства коллоидно?дисперсных систем. Строение мицелл Мицелла{m[BaSO4] • nBa2+ (2n – x)Cl–}x+ • xCl–агрегатадсорбционный слойядрогрануладиффузионный слойМИЦЕЛЛА Мицелла{m[BaSO4] • nBa2+ (2n – x)Cl–}x+ • xCl–агрегатадсорбционный слойядрогрануладиффузионный слойМИЦЕЛЛА](/img/thumbs/9c5d0e0f0521e67ca174f895701e18e2-800x.jpg)

![Электрокинетические свойства коллоидно?дисперсных систем. Строение мицелл Возникновение ДЭС и потенциалов в мицелле{m[BaSO4] • nBa2+ (2n – x)Cl–}x+ Возникновение ДЭС и потенциалов в мицелле{m[BaSO4] • nBa2+ (2n – x)Cl–}x+ • xCl–На границе между ядром и](/img/thumbs/e1615249e5132c95a93c8bdb573e5c7e-800x.jpg)


![Электрокинетические свойства коллоидно?дисперсных систем. Строение мицелл {m[BaSO4] • nBa2+ (2n – x)Cl–}x+ •xCl–Электрофорез и электроосмоскатоданодЭлектрофорезЭлектроосмос {m[BaSO4] • nBa2+ (2n – x)Cl–}x+ •xCl–Электрофорез и электроосмоскатоданодЭлектрофорезЭлектроосмос](/img/thumbs/34cd9afe1cf9f90b0332dfc20a74751f-800x.jpg)