Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Фенолы
Содержание
- 1. Фенолы
- 2. Производные ароматических углеводородов, в молекулах которых гидроксильные группы связаны с бензольным кольцом, называются фенолами.
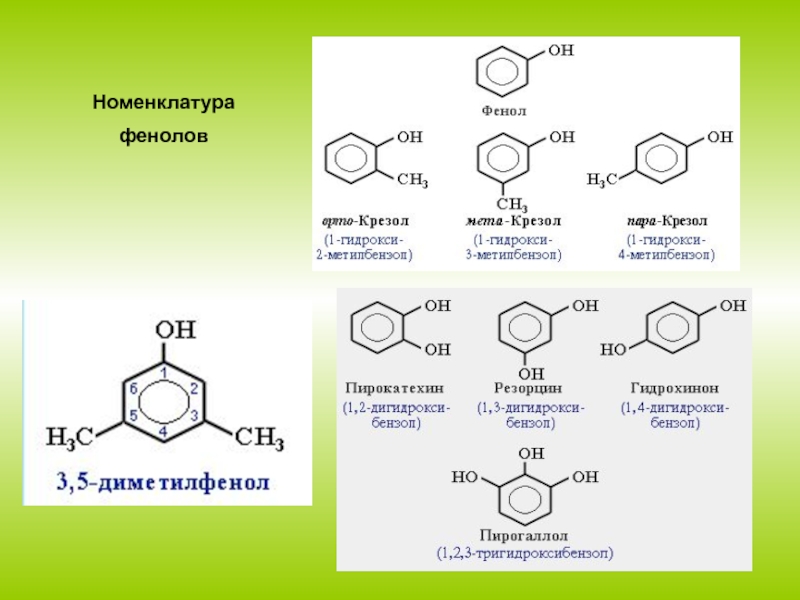
- 3. Номенклатурафенолов
- 4. Строение
- 5. Мезомерный эффект в молекуле фенола – причина усиления кислотных свойств
- 6. Химические свойства фенола
- 7. Фенолы – более сильные кислоты, чем спирты
- 8. Качественная реакция на фенолы
- 9. Слайд 9
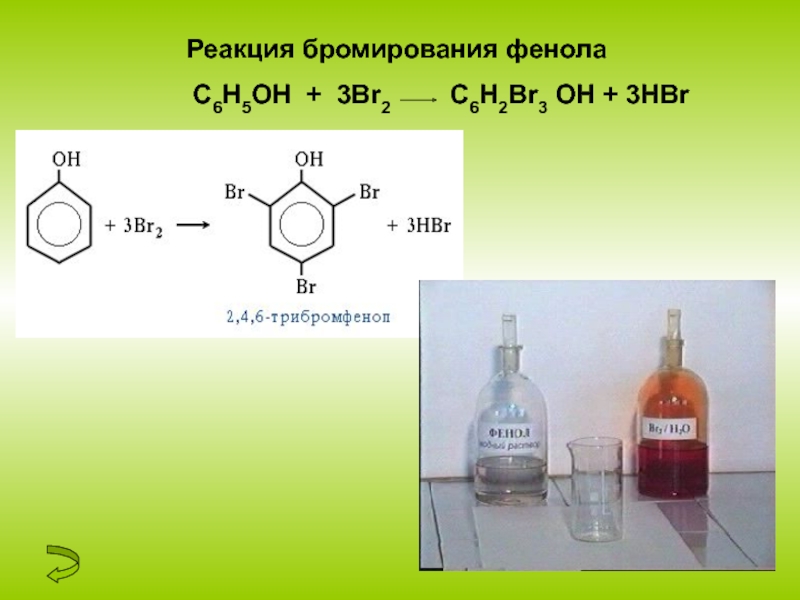
- 10. Реакция бромирования фенола
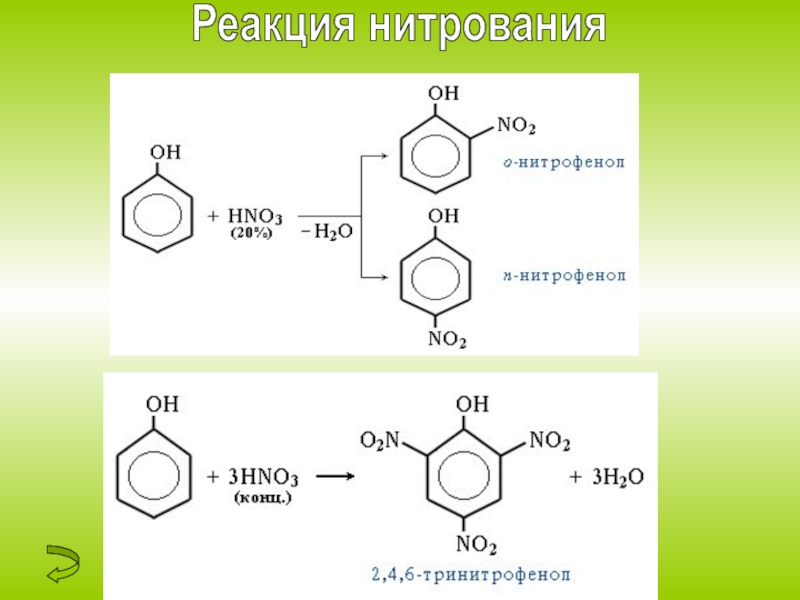
- 11. Реакция нитрования
- 12. Слайд 12
- 13. Получение1- Получают фенол по схеме:C6H6 C6H5Cl C6H5OH2- кумольный способ(из изопропилбензола)
- 14. - производство фенолформальдегидных смол;- полупродукт в органическом синтезепроизводство красителейпроизводство лекарств (резорцин)в составе фотоматериалов (гидрохинон)в составе антиоксидантовПрименение
- 15. Вопросы для контроля:1.Какие вещества относят к фенолам?2.
- 16. Скачать презентанцию
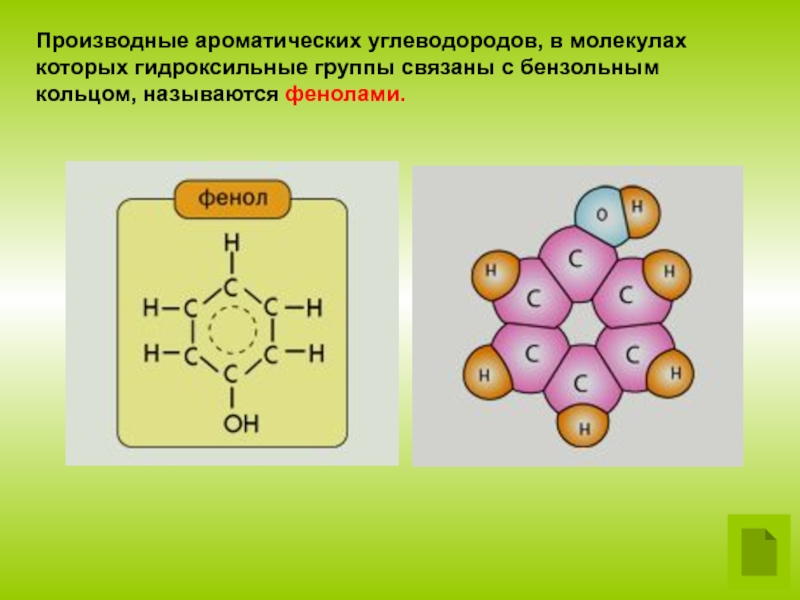
Производные ароматических углеводородов, в молекулах которых гидроксильные группы связаны с бензольным кольцом, называются фенолами.
Слайды и текст этой презентации
Слайд 2Производные ароматических углеводородов, в молекулах которых гидроксильные группы связаны с
бензольным кольцом, называются фенолами.
Слайд 7Фенолы – более сильные кислоты, чем спирты и вода, т.к.
за счет участия неподеленной электронной пары кислорода в сопряжении с
-электронной системой бензольного кольца полярность связи О–Н увеличивается.Фенолы реагируют с гидроксидами щелочных и щелочноземельных металлов, образуя соли – феноляты:
C6H5OH + NaOH C6H5ONa + H2O
фенолят натрия
Образование фенолята железа под действием раствора хлорида железа (III) является качественной реакцией на фенолы (раствор приобретает коричнево-фиолетовую окраску).
Слайд 9 Реакции фенола
по бензольному кольцу
Гидроксильная группа фенола повышает электронную плотность
в бензольном кольце,
особенно, в орто- и пара-положениях (+М-эффект ОН-группы).
Поэтому фенол значительно активнее бензола вступает в реакции
электрофильного замещения (SE) в ароматическом кольце.
1. Нитрование. Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара-нитрофенолов .
При использовании концентрированной HNO3 образуется 2,4,6-
тринитрофенол (пикриновая кислота)
2. Галогенирование. Фенол легко при комнатной температуре
взаимодействует с бромной водой с образованием белого осадка
2,4,6-трибромфенола (качественная реакция на фенол)
3. Конденсация с альдегидами . Данная реакция имеет
большое практическое значение и используется при получении
фенолформальдегидных смол.
Получение
Слайд 13Получение
1- Получают фенол по схеме:
C6H6 C6H5Cl
C6H5OH
2- кумольный способ
(из изопропилбензола)
Слайд 14
- производство фенолформальдегидных смол;
- полупродукт в органическом синтезе
производство красителей
производство лекарств
(резорцин)
в составе фотоматериалов (гидрохинон)
в составе антиоксидантов
Применение
Слайд 15Вопросы для контроля:
1.Какие вещества относят к фенолам?
2. Почему фенол проявляет
кислотные свойства сильнее, чем одноатомные спирты?
3.Какие химические свойства характерны для
фенола?4. Какие реакции можно использовать для идентификации фенола?
5. Как получают фенол?
6. Назовите области применения фенола и его производных.