Слайд 1Ферменты используемые в молекулярном клонировании
Лекция №1
Лектор:
Давыдова Ольга Константиновна, к.б.н., доцент
Слайд 2Рекомендуемая литература:
Жимулев, И.Ф. Общая и молекулярная генетика: учеб. пособие для вузов - Новосибирск : Сибирское ун-ое
изд-во, 2006. - 479 с.
Коничев А.С., Севастьянова Г.А. Молекулярная биология. – М., Изд.
Центр «Академия», 2005.
Генетика: учеб. для вузов / В. И. Иванов [и др.]; под ред. В. И. Иванова. - М. : Академкнига, 2006. - 638 с.
Щелкунов С.Н. Генетическая инженерия: Учеб.-справ. пособие. – Новосибирск: Сиб. унив. изд-во, 2004. – 496с.
Давыдова О. К. Методы генетических исследований микроорганизмов: учебн. пособие. - Оренбург. – 2013. – 132 с.
Слайд 3План лекции:
Рестриктазы. Классификация, номенклатура и характеристика рестриктаз.
ДНК-полимераза.
Обратная транскриптаза.
ДНК-лигаза.
Терминальная трансфераза.
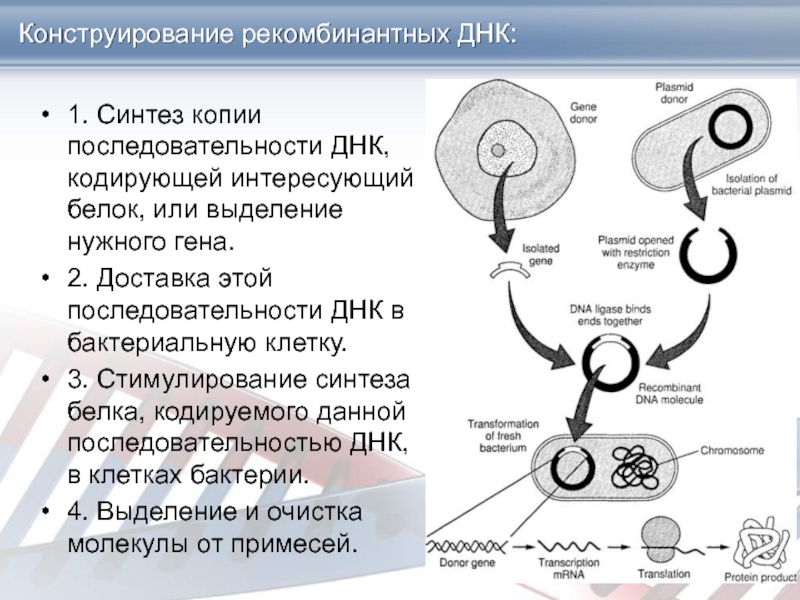
Слайд 4Конструирование рекомбинантных ДНК:
1. Синтез копии последовательности ДНК, кодирующей интересующий белок,
или выделение нужного гена.
2. Доставка этой последовательности ДНК в бактериальную
клетку.
3. Стимулирование синтеза белка, кодируемого данной последовательностью ДНК, в клетках бактерии.
4. Выделение и очистка молекулы от примесей.
Слайд 5Генные инженеры используют элементы генетических систем, функционирующие в природе
Ферменты, применяемые
при конструировании рекомбинантных ДНК, можно разделить на несколько групп:
ферменты,
с помощью которых получают фрагменты ДНК (рестриктазы);
ферменты, синтезирующие ДНК на матрице ДНК (полимеразы) или РНК (обратные транскриптазы);
ферменты, соединяющие фрагменты ДНК (лигазы);
ферменты, позволяющие осуществить изменение структуры концов фрагментов ДНК (терминальная трансфереза).
Слайд 6Рестриктазы
(рестрицирующие эндонуклеазы, эндонуклеазы рестрикции, сайт специфические эндодезоксирибонуклеазы)
- это ферменты,
узнающие и атакующие определенные последовательности нуклеотидов в молекуле ДНК (сайты
рестрикции), разрезая их фосфодиэфирные связи (эндо- означает, что они разрезают молекулу изнутри, а не по краям) - это основной инструмент генной инженерии.
Фрагменты ДНК, в том числе и фрагменты, содержащие гены, получают с использованием ферментов рестриктаз.
Слайд 7Рестриктазы
Первую рестриктазу выделили из бактерии и охарактеризовали Г.О. Смит, К.
Уилкокс и Дж.Дж. Келли в 1968 году.
Поскольку разные бактерии
по-разному метят свою ДНК, то и рестриктазы должны узнавать разные последовательности.
Каждая из сотен известных сегодня рестриктаз распознает специфическую короткую (обычно длиной 4 и 6 нуклеотидов) последовательность в двухцепочечной ДНК и расщепляет ДНК только в этом участке.
Слайд 8Молекулярные палиндромы
«Ты сыт»
Молекулярный палиндром — это последовательность оснований, которая
также читается одинаково в любом направлении, например: 3'-GAATTC-5' или
5'-CTTAAG-3'.
Слайд 9Рестриктазы
При попытке вставить человеческий ген в бактериальную ДНК могут возникнуть
следующие проблемы:
- сложно внедрить ДНК в клетку. Нужен вектор, который
будет транспортировать ДНК в клетку;
- попав в клетку, человеческая ДНК будет опознаваться бактерией как чужеродная, основываясь на том факте, что бактериальная ДНК кольцевая, а человеческая — линейная. Бактерия будет уничтожать чужеродную ДНК. Поэтому необходимо вставить человеческую ДНК в кольцевой форме.
Слайд 10Рестриктаза EcoR1
Расщепляет фосфодиэфирные связи обеих цепей ДНК между G и
А в последовательности 5'-GAATTC-3‘, что приводит к образованию комплементарных «липких»
концов (ААТТ), которые удерживаются вместе за счет спаривания оснований.
Отделить друг от друга их можно путем небольшого нагревания. При охлаждении липкие концы гибридизуются вновь в правильной ориентации. Места расщепления можно соединить с помощью ДНК-лигазы.
Слайд 11Метилазы
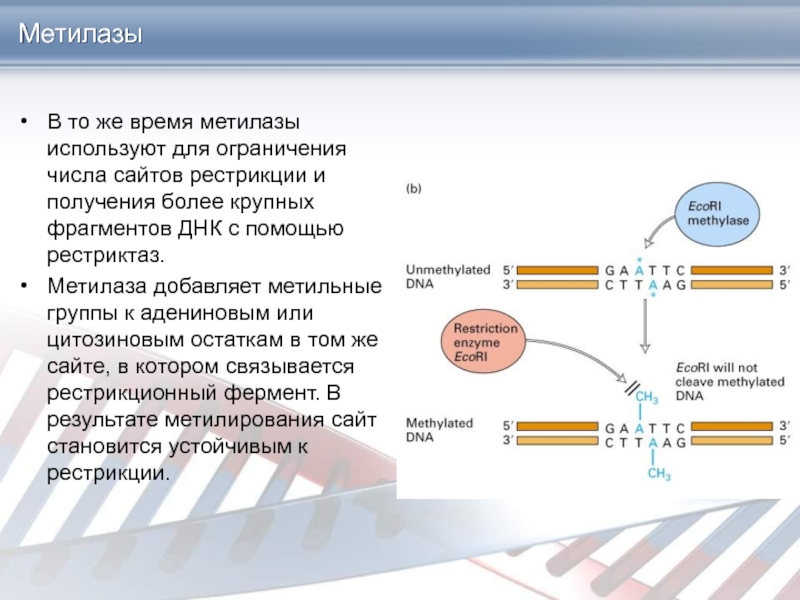
В то же время метилазы используют для ограничения числа
сайтов рестрикции и получения более крупных фрагментов ДНК с помощью
рестриктаз.
Метилаза добавляет метильные группы к адениновым или цитозиновым остаткам в том же сайте, в котором связывается рестрикционный фермент. В результате метилирования сайт становится устойчивым к рестрикции.
Слайд 12Классификация рестриктаз
К мелкощепящим относятся рестриктазы Hpa II и Alu, к
крупнощепящим - Eco R I и Hind III.
Если предположить,
что участки узнавания рестриктаз распределены вдоль цепи ДНК случайно, то мишень для ферментов, узнающих последовательность (сайт) из четырех нуклеотидов, должна встречаться в среднем 1 раз через каждые 256 пар оснований, а для ферментов, узнающих шесть нуклеотидов, - через 4096 пар оснований.
Если сайт рестрикции окажется внутри гена, то обработка ДНК-рестриктазой приведет к его инактивации. Вероятность такого события очень велика при обработке мелкощепящими рестриктазами и незначительна при применении крупнощепящих эндонуклеаз. Поэтому с целью получения неповрежденного гена расщепление проводят поочередно несколькими крупнощепящими рестриктазами, либо применяют прием "недорестрикции", т.е. рестрикцию проводят в таких условиях, когда происходит расщепление лишь в одном сайте.
Слайд 13Классификация рестриктаз
Различают 3 основных класса рестриктаз: 1, 2 и 3.
Все рестриктазы узнают на двуспиральной ДНК строго определенные последовательности, но
рестриктазы 1-го класса осуществляют разрывы в произвольных точках молекулы ДНК, а рестриктазы 2-го и 3-го классов узнают и расщепляют ДНК в строго определенных точках внутри сайтов узнавания или на фиксированном от них расстоянии.
Ферменты типов 1 и 3 имеют сложную субъединичную структуру и обладают двумя типами активностей - модифицирующей (метилирующей) и АТФ-зависимой эндонуклеазной.
Ферменты второго класса состоят из 2 отдельных белков: рестрицирующей эндонуклеазы и модифицирующей метилазы, поэтому в генной инженерии используются исключительно ферменты 2-го класса. Они нуждаются в ионах магния в качестве кофакторов.
В настоящее время выделено более 500 рестриктаз класса 2.
Слайд 14Изошизомерия
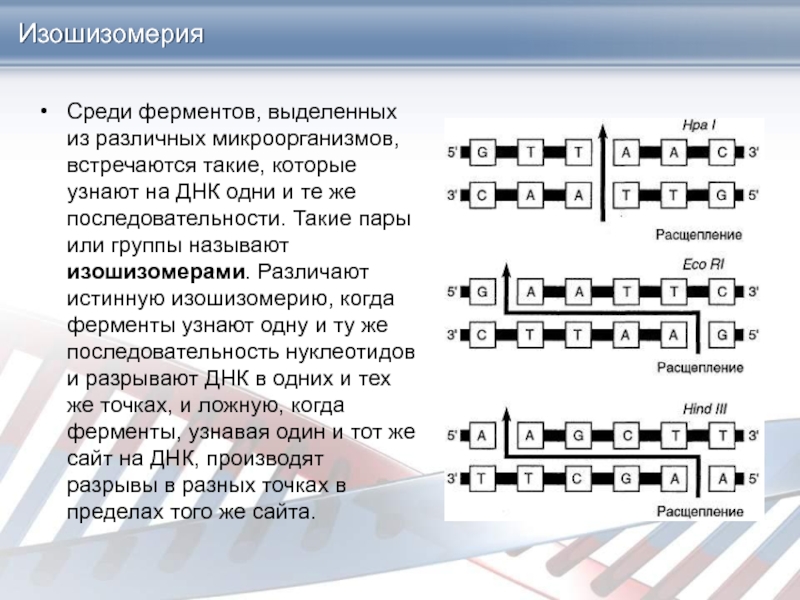
Среди ферментов, выделенных из различных микроорганизмов, встречаются такие, которые узнают
на ДНК одни и те же последовательности. Такие пары или
группы называют изошизомерами. Различают истинную изошизомерию, когда ферменты узнают одну и ту же последовательность нуклеотидов и разрывают ДНК в одних и тех же точках, и ложную, когда ферменты, узнавая один и тот же сайт на ДНК, производят разрывы в разных точках в пределах того же сайта.
Слайд 15Номенклатура рестриктаз
В 1973 году Смит и Натанс предложили номенклатуру рестриктаз,
включающую следующие пункты:
1. Аббревиатура названия каждого фермента является производной от
бинарного названия микроорганизма, содержащего данную метилазно-рестриктазную систему. Составляют по правилу: к первой прописной букве названия рода добавляют две первые строчные буквы вида.
Streptomyces albus - Sal, Escherichia coli - Eco
2. В случае необходимости добавляют обозначение серотипа или штамма, например, Есо B, Haemophilus influenzae d-Hind или Haemophilus influenzae с-Hinc .
3. Различные системы рестрикции - модификации, кодируемые одной бактериальной клеткой, обозначают римскими цифрами: Hind I, Hind II, Hind III (Haemophilus influenzae) – открыты в указанной последовательности.
4. Рестриктазы обозначают буквой R (R Hind III), метилазы - М (М Hind III).
Если система генетически локализована в геноме фага или на плазмиде, то после родо- видового названия указывается символ внехромосомного элемента: EcoP1.
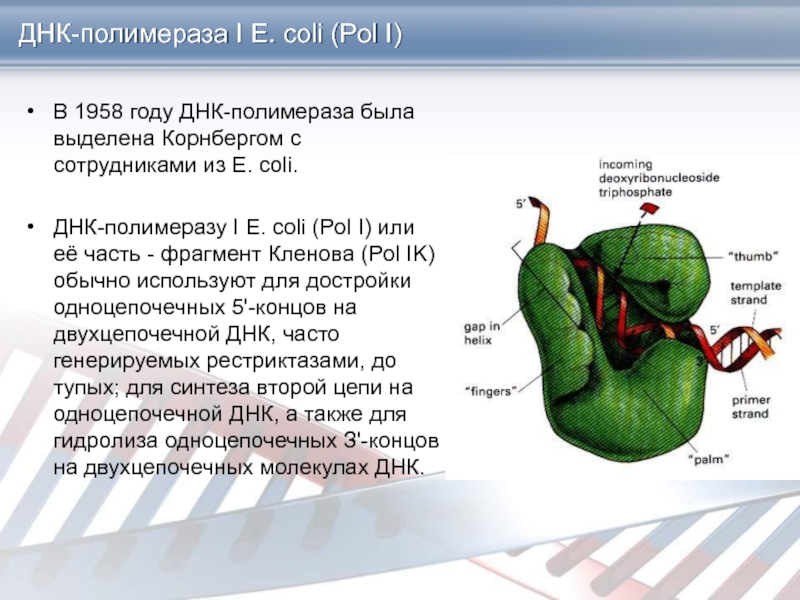
Слайд 16ДНК-полимераза I E. coli (Pol I)
В 1958 году ДНК-полимераза была
выделена Корнбергом с сотрудниками из E. coli.
ДНК-полимеразу I E. coli
(Pol I) или её часть - фрагмент Кленова (Pol IK) обычно используют для достройки одноцепочечных 5'-концов на двухцепочечной ДНК, часто генерируемых рестриктазами, до тупых; для синтеза второй цепи на одноцепочечной ДНК, а также для гидролиза одноцепочечных З'-концов на двухцепочечных молекулах ДНК.
Слайд 17ДНК-полимераза I E. coli (Pol I)
ДНК-полимераза I E. coli (Pol
I) не связывается с молекулами двухцепочечной кольцевой ДНК. Однако, если
такие молекулы денатурировать и получить одноцепочечные формы, то с последними полимераза связывается в количествах, пропорциональных длине этих участков — примерно одна молекула на 300 нуклеотидных остатков.
N - концевой домен соединен с соседним петлей из аминокислотных остатков и легко отделяется с помощью протеолитических ферментов. Оставшаяся часть бифункциональна, так как состоит из полимеразы и 3’ - 5’ экзонуклезы. Она названа фрагментом Кленова.
Слайд 18ДНК-полимераза I E. coli (Pol I)
Фермент состоит из мономерной полипептидной
цепи с молекулярной массой 103 кДа и имеет 3-х доменную
структуру.
1. 5‘- 3' полимеразная активность. Для реакции необходимо наличие одноцепочечной ДНК-матрицы и комплементарного участку этой цепи фрагмента — праймера (затравки) с З'-ОН концом.
2. 3'- 5' экзонуклеазная активность. Гидролизует одноцепочечную или двухцепочечную ДНК с З'-ОН конца. 3‘-5' нуклеаза расщепляет диэфирную связь только в неспаренных участках ДНК. Известно, что при полимеразной реакции с определенной частотой возможно включение в растущую цепь некомплементарного нуклеотида. 3'—5' экзонуклеаза, убирает ошибочный нуклеотид, на место которого затем присоединяется правильный нуклеотид-предшественник.
3. 5‘- 3' экзонуклеазная активность. Деградирует одну цепь двухцепочечной ДНК, начиная со свободного 5'-конца. В отличие от 3‘-5' экзонуклеазы 5‘-3' экзонуклеаза расщепляет диэфирную связь только в спаренных участках двухцепочечной молекулы ДНК. Более того, в то время как 3'—5' нуклеаза отщепляет одномоментно только один нуклеотид, 5‘-3' нуклеаза может вы¬резать с 5'- конца олигонуклеотиды длиной до десяти остатков.
Такое сочетание ферментативных активностей позволяет ДНК-полимеразе I E. coli играть активную роль в репарации повреждений ДНК in vivo.

Слайд 19Обратная транскриптаза или ревертаза
В 1964 г. Темин выдвинул гипотезу о
существовании вирусспецифичного фермента, способного синтезировать на РНК-матрице комплементарную ДНК.
В
1970 г. Темин с Мизутани, а также независимо от них Балтимор открыли искомый фермент в препарате внеклеточных вирионов вируса саркомы Рауса.
В генетической инженерии обратную транскриптазу используют для получения кДНК — копии эукариотического гена, не содержащей интронов. Для этого из организма выделяют зрелую мРНК (кодирующую соответствующий генный продукт: белок, РНК) и проводят с ней в качестве матрицы обратную транскрипцию. Полученную кДНК можно трансформировать в клетки бактерий для получения трансгенного продукта
Слайд 20Обратная транскриптаза или ревертаза
Обратная транскриптаза состоит из двух субъединиц —
a (65 кДа) и b (95 кДа), присутствующих в эквимолярном
количестве. Обратная транскриптаза обладает, по крайней мере, тремя ферментативными активностями:
1) ДНК-полимеразной, использующей в качестве матрицы как РНК, так и ДНК;
2) активностью РНКазы Н, гидролизующей РНК в составе гибрида РНК—ДНК, но не одно- или двухцепочечную РНК;
3) ДНК-эндонуклеазной активностью.
Первые две активности необходимы для синтеза вирусной ДНК, а эндонуклеаза, по-видимому, важна для интеграции вирусной ДНК в геном клетки-хозяина.
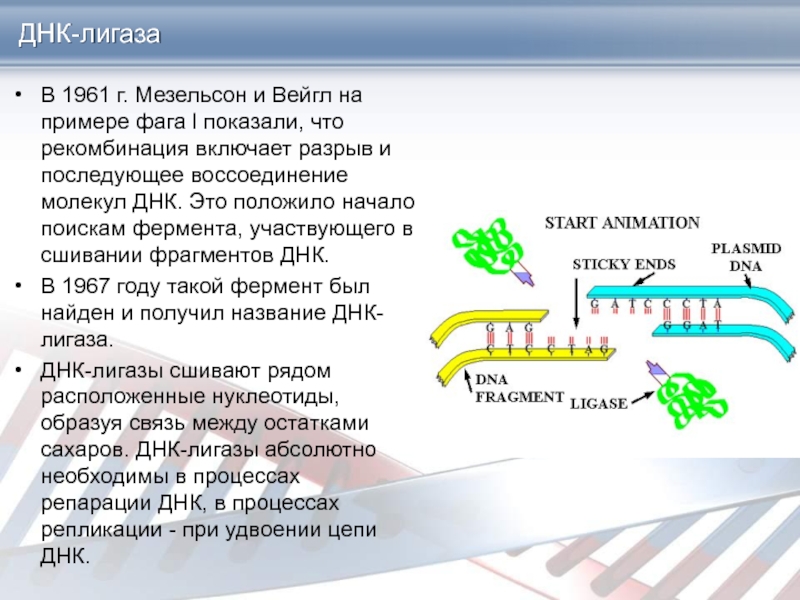
Слайд 21ДНК-лигаза
В 1961 г. Мезельсон и Вейгл на примере фага l
показали, что рекомбинация включает разрыв и последующее воссоединение молекул ДНК.
Это положило начало поискам фермента, участвующего в сшивании фрагментов ДНК.
В 1967 году такой фермент был найден и получил название ДНК-лигаза.
ДНК-лигазы сшивают рядом расположенные нуклеотиды, образуя связь между остатками сахаров. ДНК-лигазы абсолютно необходимы в процессах репарации ДНК, в процессах репликации - при удвоении цепи ДНК.
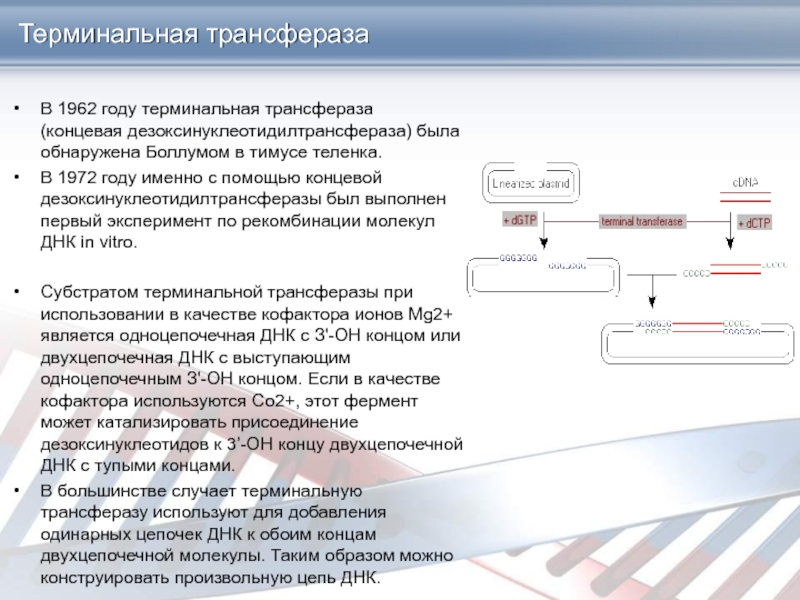
Слайд 22Терминальная трансфераза
В 1962 году терминальная трансфераза
(концевая дезоксинуклеотидилтрансфераза) была обнаружена
Боллумом в тимусе теленка.
В 1972 году именно с помощью
концевой дезоксинуклеотидилтрансферазы был выполнен первый эксперимент по рекомбинации молекул ДНК in vitro.
Субстратом терминальной трансферазы при использовании в качестве кофактора ионов Mg2+ является одноцепочечная ДНК с З'-ОН концом или двухцепочечная ДНК с выступающим одноцепочечным З'-ОН концом. Если в качестве кофактора используются Co2+, этот фермент может катализировать присоединение дезоксинуклеотидов к 3’-ОН концу двухцепочечной ДНК с тупыми концами.
В большинстве случает терминальную трансферазу используют для добавления одинарных цепочек ДНК к обоим концам двухцепочечной молекулы. Таким образом можно конструировать произвольную цепь ДНК.