Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Гемопоез та його регуляція на різних стадіях диференціюваня гемопоетичних
Содержание
- 1. Гемопоез та його регуляція на різних стадіях диференціюваня гемопоетичних
- 2. Система крові являє собою похідне мезенхіми і
- 3. Як відомо, кістковий мозок є гетерогенною структурою,
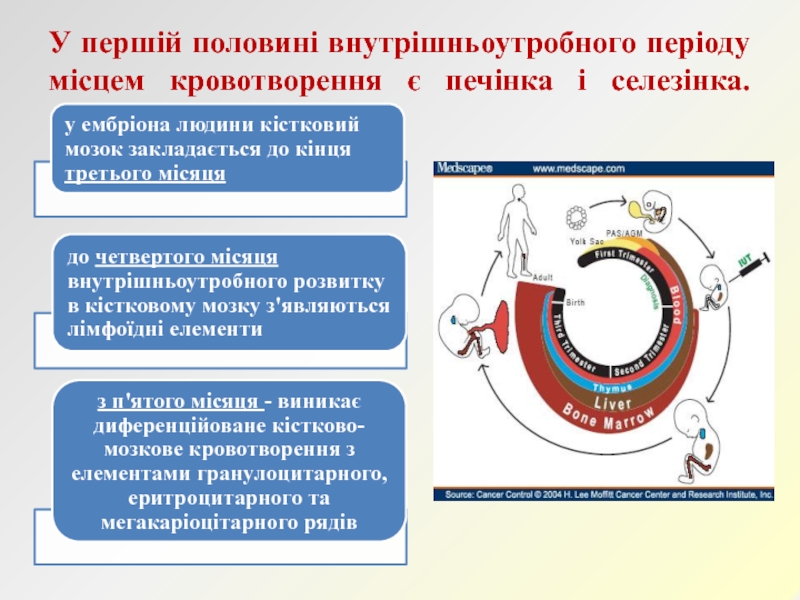
- 4. У першій половині внутрішньоутробного періоду місцем кровотворення є печінка і селезінка.
- 5. У кістковому мозку існують області так званого
- 6. В даний час очевидно наявність шести класів
- 7. плюрипотентні стовбурові клітини (ППСК) - морфологічно розпізнавана
- 8. Стовбурові клітини в стані спокою виконують дві
- 9. Починаючі з комітованих клітин кісткового мозку,
- 10. Слідом за класом ППСК виникає мультипотентна стовбурова
- 11. Третім класом недиференційованих клітин
- 12. Торкаючись кінетики гемопоезу, слід зазначити, що
- 13. Конститутивний гемопоез регулюється цитокінами і міжклітинними взаємодіями
- 14. Згідно з даними літератури, найважливішими стимуляторами
- 15. Посилення лейкопоезу виникає під впливом прозапальних цитокінів:
- 16. Стимуляторами еритропоезу є еритропоетин, гормони
- 17. Цитокіни володіють характеристиками: плейотропність і взаємозамінність біологічного
- 18. Мітогенна дія, пов'язана з активацією синтезу ДНК
- 19. До теперішнього часу немає єдиного принципу класифікації
- 20. За характером участі в гемопоезі цитокіни умовно
- 21. Залежно від структури клітин - мішеней цитокінів
- 22. Цитокіни, що беруть участь у гемопоезі,
- 23. Рецептор ФСК, c-kit,
- 24. Fit-3-ліганд. Іншим стимулятором гемопоезу
- 25. Гранулоцитарний колонієстимулюючий фактор (КСФ-Г). Синтез КСФ-Г
- 26. Макрофагальний колонієстимулюючий фактор (КСФ-М). Макрофагальний колонієстимулюючий фактор
- 27. Рецептори M-CSF відносяться до
- 28. Гранулоцитарно-макрофагальний колонієстимулюючий фактор (КСФ-ГМ). КСФ-ГМ-ростовий фактор,
- 29. Рецептори КСФ-ГМ володіють високою афінністю зв'язування ліганду.
- 30. Еритропоетин (ЕП ) . Ген ЕП
- 31. Пригнічують продукцію ЕП та еритропоез ФНО,
- 32. Тромбопоетин (ТРП). ТРП-це ростовий фактор мегакаріоцитів і
- 33. Важлива роль в процесі диференціювання і проліферації
- 34. Інтерлейкін-4 (ІЛ -4). Одним з важливих
- 35. ІЛ- 4 є типовим плейотропним цитокіном
- 36. Інтерлейкін-6 (ІЛ -6). ІЛ- 6 відкритий як
- 37. Інтерлейкін-7 (ІЛ -7). ІЛ- 7 синтезується
- 38. Рецептор ІЛ- 7 складається з двох субодиниць:
- 39. Перші дані, що свідчать про здатність ІЛ-
- 40. Слайд 40
- 41. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Гемопоез та його регуляція на різних стадіях диференціюваня
гемопоетичних клітин кісткового мозку
Слайд 2Система крові являє собою похідне мезенхіми і включає наступні основні
компоненти: кров і лімфу , органи кровотворення та імунопоезу ,
а також клітини крові ,які емігрують в сполучну тканину, і епітеліальні тканини.В останні роки досягнуто певних успіхів в уніфікації уявлень про характер і механізмах процесів гемопоезу в кістковому мозку, ролі цитокінів в гістогенезі елементів крові. З моменту народження людини розвиток первинниих поліпотентних стовбурових клітин і мієлопоез відбуваються в кістковому мозку, в той час як лімфопоез - в тимусі, селезінці і лімфатичних вузлах. В умовах патології мієлопоез у дорослої людини може поновитися в селезінці і печінці, повторюючи гемопоез плода.
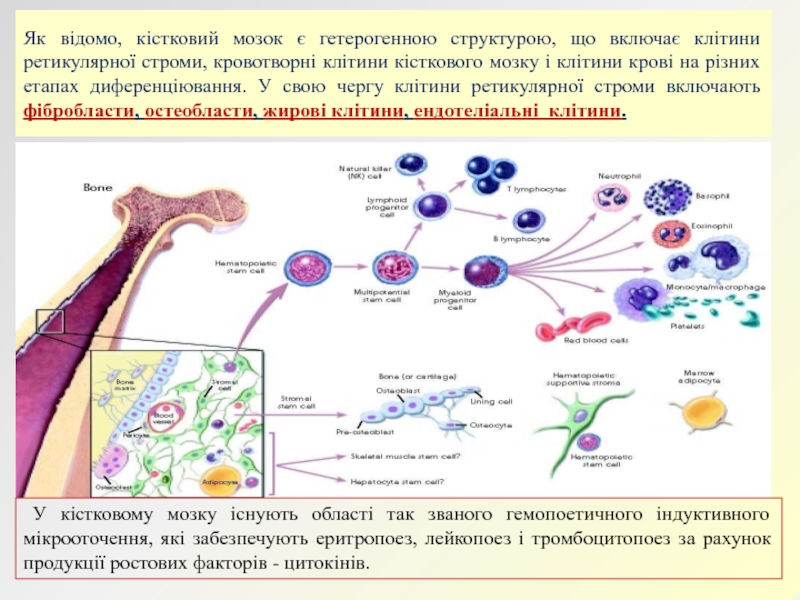
Слайд 3Як відомо, кістковий мозок є гетерогенною структурою, що включає клітини
ретикулярної строми, кровотворні клітини кісткового мозку і клітини крові на
різних етапах диференціювання. У свою чергу клітини ретикулярної строми включають фібробласти, остеобласти, жирові клітини, ендотеліальні клітини. У кістковому мозку існують області так званого гемопоетичного індуктивного мікрооточення, які забезпечують еритропоез, лейкопоез і тромбоцитопоез за рахунок продукції ростових факторів - цитокінів.
Слайд 5У кістковому мозку існують області так званого гемопоетичного індуктивного мікрооточення,
які забезпечують еритропоез, лейкопоез і тромбоцитопоез за рахунок продукції ростових
факторів - цитокінів.Щодня у людини оновлюється близько 100 млрд формених елементів периферичної крові. У гемопоетичній тканині кісткового мозку гранулоцити і їх попередники становлять близько 60%, еритроїдні попередники - 20%, лімфо- і моноцити - близько 10%, а недиференційовані та клітини які руйнуються - також близько 10%.
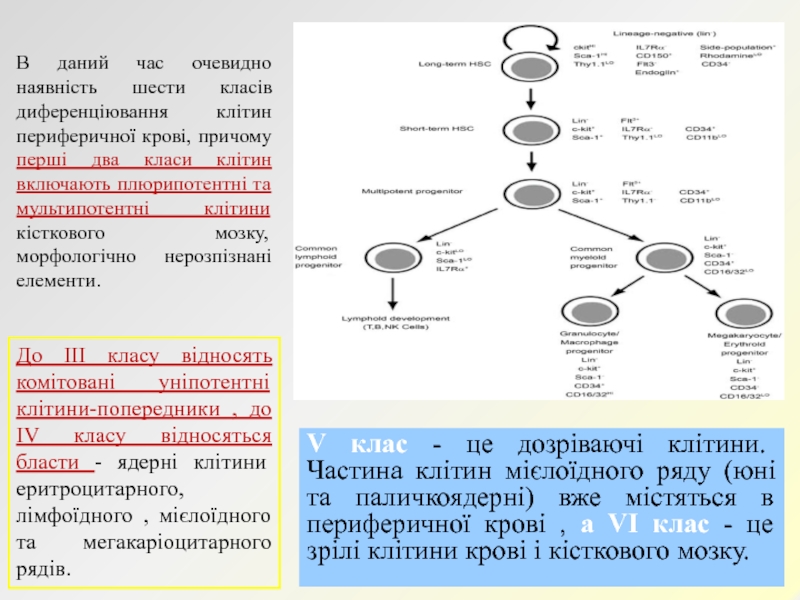
Слайд 6В даний час очевидно наявність шести класів диференціювання клітин периферичної
крові, причому перші два класи клітин включають плюрипотентні та мультипотентні
клітини кісткового мозку, морфологічно нерозпізнані елементи.V клас - це дозріваючі клітини. Частина клітин мієлоїдного ряду (юні та паличкоядерні) вже містяться в периферичної крові , а VI клас - це зрілі клітини крові і кісткового мозку.
До III класу відносять комітовані уніпотентні клітини-попередники , до IV класу відносяться бласти - ядерні клітини еритроцитарного, лімфоїдного , мієлоїдного та мегакаріоцитарного рядів.
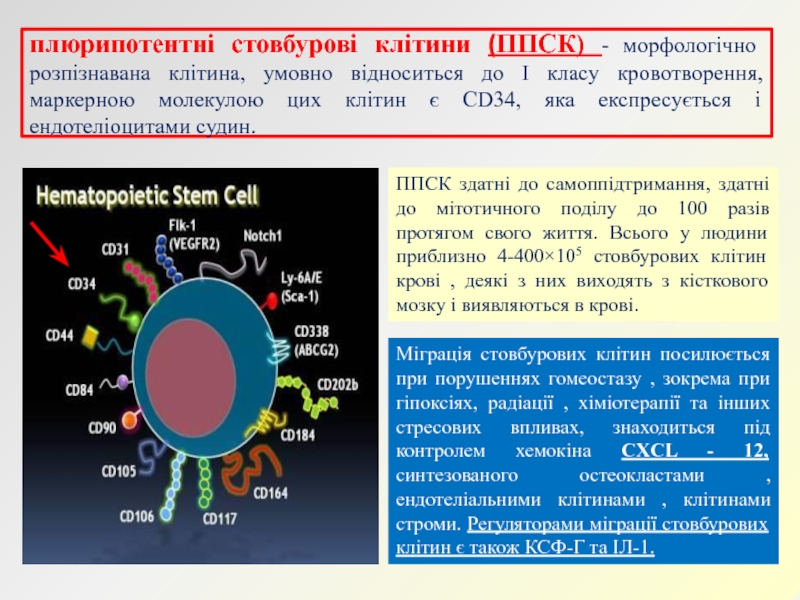
Слайд 7плюрипотентні стовбурові клітини (ППСК) - морфологічно розпізнавана клітина, умовно відноситься
до I класу кровотворення, маркерною молекулою цих клітин є CD34,
яка експресується і ендотеліоцитами судин.ППСК здатні до самоппідтримання, здатні до мітотичного поділу до 100 разів протягом свого життя. Всього у людини приблизно 4-400×105 стовбурових клітин крові , деякі з них виходять з кісткового мозку і виявляються в крові.
Міграція стовбурових клітин посилюється при порушеннях гомеостазу , зокрема при гіпоксіях, радіації , хіміотерапії та інших стресових впливах, знаходиться під контролем хемокіна CXCL - 12, синтезованого остеокластами , ендотеліальними клітинами , клітинами строми. Регуляторами міграції стовбурових клітин є також КСФ-Г та ІЛ-1.
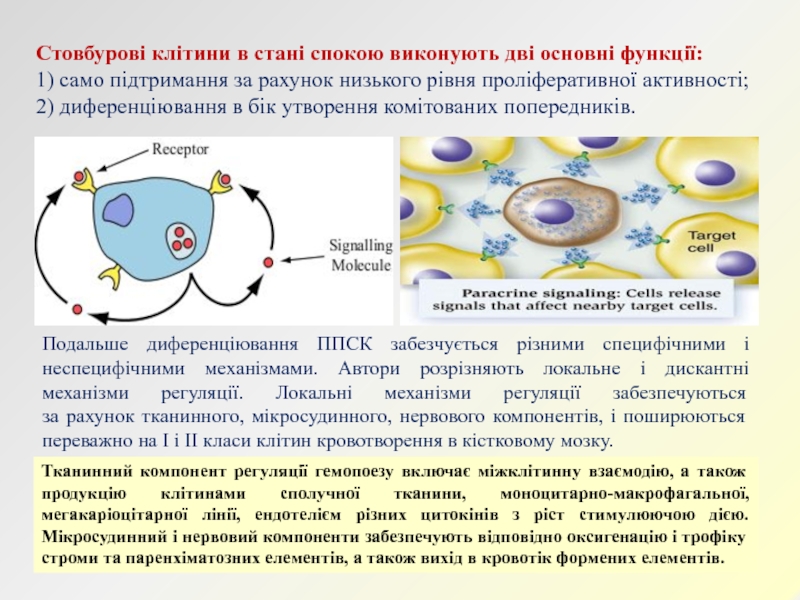
Слайд 8Стовбурові клітини в стані спокою виконують дві основні функції: 1)
само підтримання за рахунок низького рівня проліферативної активності; 2) диференціювання
в бік утворення комітованих попередників.Подальше диференціювання ППСК забезчується різними специфічними і неспецифічними механізмами. Автори розрізняють локальне і дискантні механізми регуляції. Локальні механізми регуляції забезпечуються
за рахунок тканинного, мікросудинного, нервового компонентів, і поширюються переважно на I і II класи клітин кровотворення в кістковому мозку.
Тканинний компонент регуляції гемопоезу включає міжклітинну взаємодію, а також продукцію клітинами сполучної тканини, моноцитарно-макрофагальної, мегакаріоцітарної лінії, ендотелієм різних цитокінів з ріст стимулюючою дією. Мікросудинний і нервовий компоненти забезпечують відповідно оксигенацію і трофіку строми та паренхіматозних елементів, а також вихід в кровотік формених елементів.
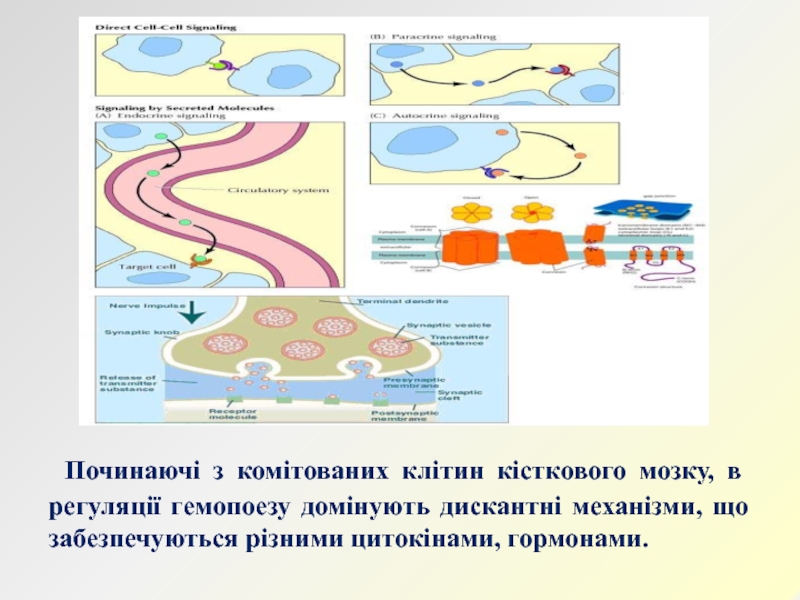
Слайд 9 Починаючі з комітованих клітин кісткового мозку, в регуляції гемопоезу
домінують дискантні механізми, що забезпечуються різними цитокінами, гормонами.
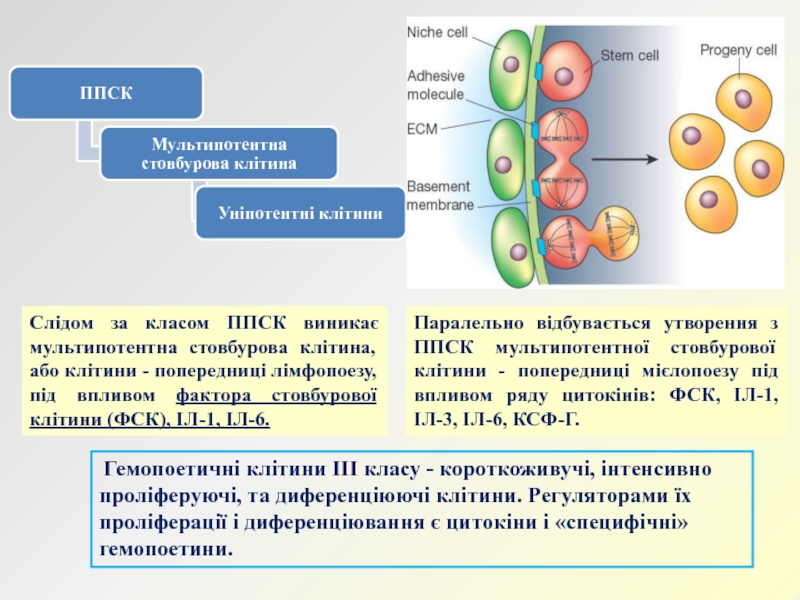
Слайд 10Слідом за класом ППСК виникає мультипотентна стовбурова клітина, або клітини
- попередниці лімфопоезу, під впливом фактора стовбурової клітини (ФСК), ІЛ-1,
ІЛ-6.Паралельно відбувається утворення з ППСК мультипотентної стовбурової клітини - попередниці мієлопоезу під впливом ряду цитокінів: ФСК, ІЛ-1, ІЛ-3, ІЛ-6, КСФ-Г.
Гемопоетичні клітини III класу - короткоживучі, інтенсивно проліферуючі, та диференціюючі клітини. Регуляторами їх проліферації і диференціювання є цитокіни і «специфічні» гемопоетини.
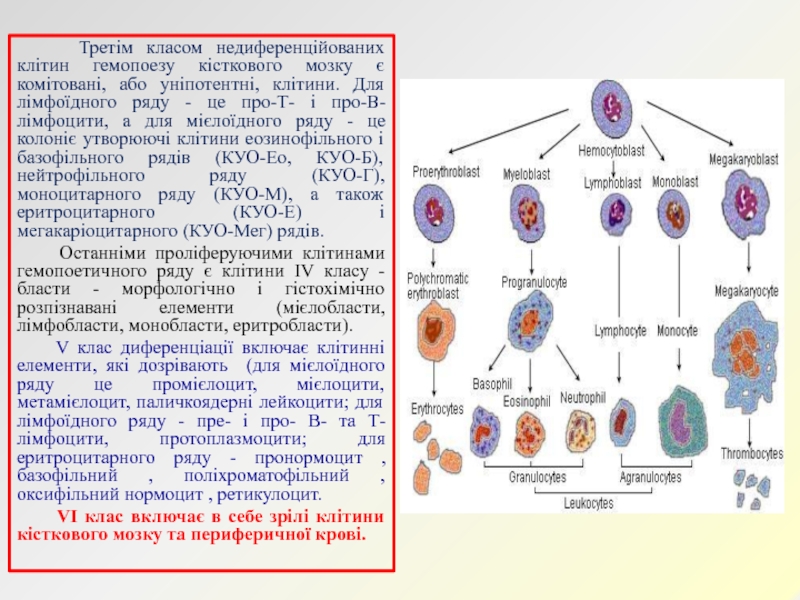
Слайд 11 Третім класом недиференційованих клітин гемопоезу кісткового мозку
є комітовані, або уніпотентні, клітини. Для лімфоїдного ряду - це
про-Т- і про-В-лімфоцити, а для мієлоїдного ряду - це колоніє утворюючі клітини еозинофільного і базофільного рядів (КУО-Ео, КУО-Б), нейтрофільного ряду (КУО-Г), моноцитарного ряду (КУО-М), а також еритроцитарного (КУО-Е) і мегакаріоцитарного (КУО-Мег) рядів.Останніми проліферуючими клітинами гемопоетичного ряду є клітини IV класу - бласти - морфологічно і гістохімічно розпізнавані елементи (мієлобласти, лімфобласти, монобласти, еритробласти).
V клас диференціації включає клітинні елементи, які дозрівають (для мієлоїдного ряду це промієлоцит, мієлоцити, метамієлоцит, паличкоядерні лейкоцити; для лімфоїдного ряду - пре- і про- В- та Т- лімфоцити, протоплазмоцити; для еритроцитарного ряду - пронормоцит , базофільний , поліхроматофільний , оксифільний нормоцит , ретикулоцит.
VI клас включає в себе зрілі клітини кісткового мозку та периферичної крові.
Слайд 12 Торкаючись кінетики гемопоезу, слід зазначити, що для клітин –
попередниць, які діляться, мітотичний цикл, крім мітозу, включає фазу G1.
Під час цієї фази відбувається підготовка гемо поетичних клітин до синтезу ДНК , а далі S-фазу, що характеризується подвоєнням кількості ДНК, і фазу G2, що включає період підготовки до мітотичного поділу.Тривалість мітотичного циклу для морфологічно нерозпізнаних клітин- попередниць становить у середньому близько 20 годин.
Слайд 13Конститутивний гемопоез регулюється цитокінами і міжклітинними взаємодіями і здійснюється в
особливих зонах скупчення стовбурових клітин. Частина стовбурових клітин, повільно розмножуючись,
мігрує в інші зони кісткового мозку , де і диференціюється.Індукований гемопоез можливий при порушеннях гомеостазу при різних стресових впливах (гіпоксія, інтоксикація, іонізуюча радіація) і регулюється в основному КСФ -Г , ІЛ- 1 , ФСК.
Слайд 14 Згідно з даними літератури, найважливішими стимуляторами проліферації і диференціювання
клітин гранулоцитарного і моноцитарного рядів є колонієстимулюючі фактори (КСФ).
Найбільш вивчені
мульти-КСФ (ІЛ-3), гранулоцитарно-макрофагальний КСФ (КСФ -ГМ), макрофагальний КСФ (КСФ-М), гранулоцитарний КСФ (КСФ-Г).
КСФ є пептидами, що продукуються у людини моноцитарно - макрофагальними клітинами крові різних тканин, зокрема клітинами кісткового мозку, а також лімфоцитами, ендотеліальними клітинами, фібробластами, тучними клітинами на тлі антигенної стимуляції.
Слайд 15Посилення лейкопоезу виникає під впливом прозапальних цитокінів: ІЛ-1, ІЛ-6, ІЛ-8,
а також під впливом ряду медіаторів запалення, зокрема лейкотрієнів В4
, С4, а також ФСК , що виробляється клітками мікрооточення стовбурових клітин. До числа стимуляторів лейкопоезу відносяться також вітамін В12, аскорбінова кислота, фолієва кислота, залізо.Універсальними стимуляторами гранулоцитарно-моноцитарного лейкопоезу являються гормони адаптації: катехоламіни, глюкокортикоїди, що реалізують свої ефекти на кістковий мозок через посилення утворення КСФ і інтерлейкінів.
Призупинення кістково-мозкового кровотворення можливо під впливом ряду медіаторів запалення, таких, як простагландини Е1, Е2, ІЛ-10, ІЛ-13, ФНП-α, трансформуючий фактор росту бета (ТФР-β), а також лактоферин і кислого ізоферитин.
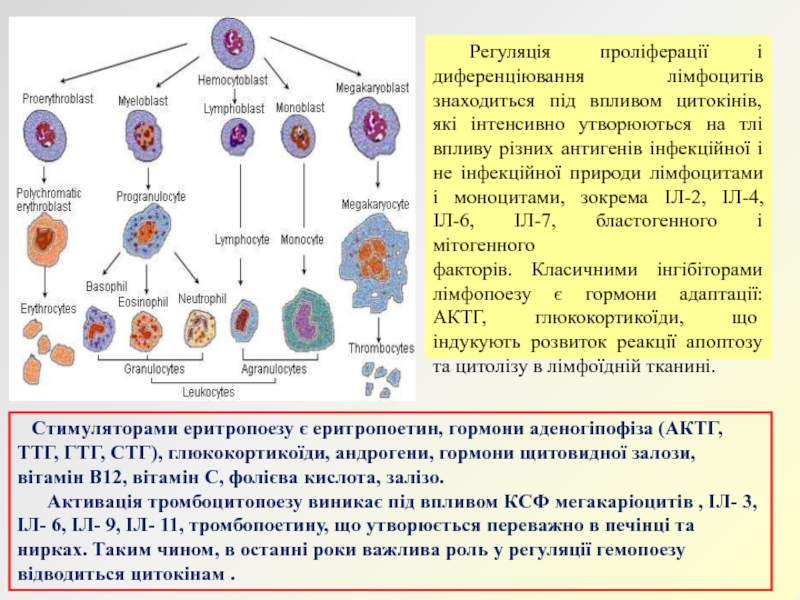
Слайд 16 Стимуляторами еритропоезу є еритропоетин, гормони аденогіпофіза (АКТГ, ТТГ,
ГТГ, СТГ), глюкокортикоїди, андрогени, гормони щитовидної залози, вітамін В12, вітамін
С, фолієва кислота, залізо.Активація тромбоцитопоезу виникає під впливом КСФ мегакаріоцитів , ІЛ- 3, ІЛ- 6, ІЛ- 9, ІЛ- 11, тромбопоетину, що утворюється переважно в печінці та нирках. Таким чином, в останні роки важлива роль у регуляції гемопоезу відводиться цитокінам .
Регуляція проліферації і диференціювання лімфоцитів знаходиться під впливом цитокінів, які інтенсивно утворюються на тлі впливу різних антигенів інфекційної і не інфекційної природи лімфоцитами і моноцитами, зокрема ІЛ-2, ІЛ-4, ІЛ-6, ІЛ-7, бластогенного і мітогенного
факторів. Класичними інгібіторами лімфопоезу є гормони адаптації: АКТГ, глюкокортикоїди, що індукують розвиток реакції апоптозу та цитолізу в лімфоїдній тканині.
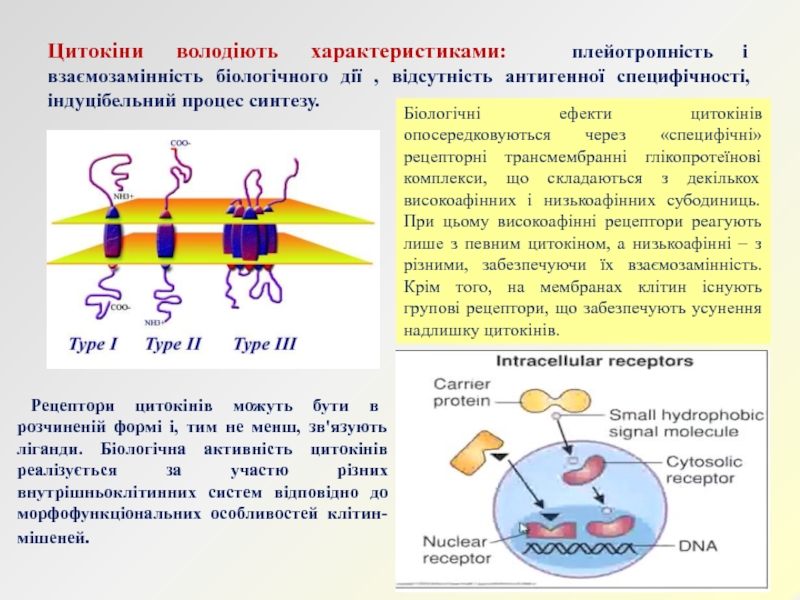
Слайд 17Цитокіни володіють характеристиками: плейотропність і взаємозамінність біологічного дії , відсутність
антигенної специфічності, індуцібельний процес синтезу.
Біологічні ефекти цитокінів опосередковуються через «специфічні»
рецепторні трансмембранні глікопротеїнові комплекси, що складаються з декількох високоафінних і низькоафінних субодиниць. При цьому високоафінні рецептори реагують лише з певним цитокіном, а низькоафінні – з різними, забезпечуючи їх взаємозамінність. Крім того, на мембранах клітин існують групові рецептори, що забезпечують усунення надлишку цитокінів. Рецептори цитокінів можуть бути в розчиненій формі і, тим не менш, зв'язують ліганди. Біологічна активність цитокінів реалізується за участю різних внутрішньоклітинних систем відповідно до морфофункціональних особливостей клітин-мішеней.
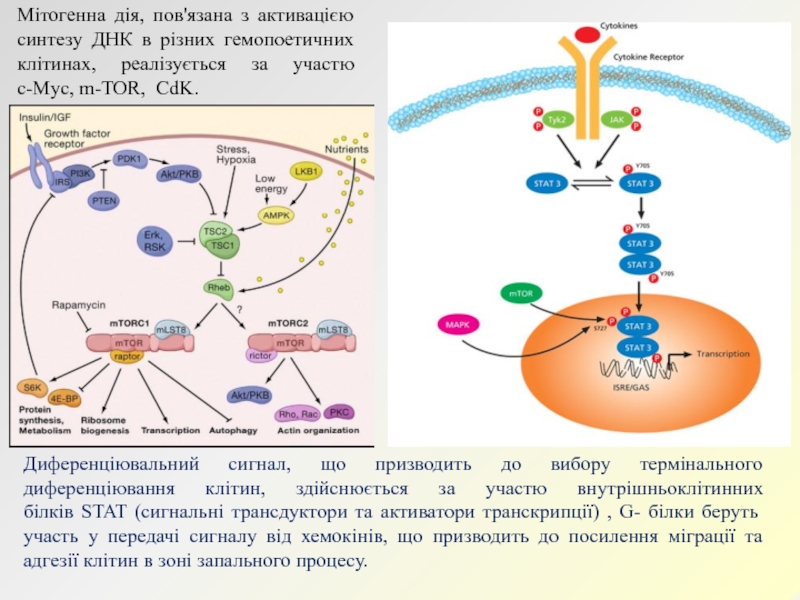
Слайд 18Мітогенна дія, пов'язана з активацією синтезу ДНК в різних гемопоетичних
клітинах, реалізується за участю с-Myc, m-TOR, CdK.
Диференціювальний сигнал, що призводить
до вибору термінального диференціювання клітин, здійснюється за участю внутрішньоклітинних
білків STAT (сигнальні трансдуктори та активатори транскрипції) , G- білки беруть участь у передачі сигналу від хемокінів, що призводить до посилення міграції та адгезії клітин в зоні запального процесу. Слайд 19До теперішнього часу немає єдиного принципу класифікації цитокінів. Згідно з
однією з класифікацій виділяють наступні групи цитокінів: - інтерлейкіни, що забезпечують
медіаторну міжклітинну взаємодію в імунній системі; - фактори некрозу пухлини , що володіють цитотоксичним і регуляторним дією; - колонієстимулюючі фактори–фактори росту і диференціювання гемопоетичних клітин; - хемокіни - хемоатрактанти для лейкоцитів; - фактори росту, що регулюють ріст, диференціювання і функціональну активність клітин різної тканинної приналежності (фактори росту фібробластів, ендотеліальних клітин, епідермісу,тромбоцитів, трансформують фактори росту).Слайд 20За характером участі в гемопоезі цитокіни умовно ділять на дві
групи:
1) цитокіни , регулюють -конститутивний та
індукований гемопоез. До них відносять ФСК , КСФ -Г , КСФ -М , КСФ - ГМ , ІЛ- 3, тромбопоетин ( ТРП) , ІЛ- 11 , еритропоетини (ЕП ) і прозапальні цитокіни : ІЛ - 1 , ІЛ- 6 , ФНП , ІЛ-3 , КСФ - ГМ . Останні стимулюють проліферацію і диференціювання всіх клітин-попередниць мієлоїдного ряду на ранніх етапах їх розвитку;
2) специфічні цитокіни, під контролем яких перебувають більш диференційовані клітини. Так, тип дозрівання еритроцитів контролюється ЕП, тромбоцитів - ТРП та ІЛ-11, дозрівання попередників лімфоцитів знаходиться під контролем ІЛ-4 та ІЛ-5. Дозрівання лімфоїдного ростка кровотворення контролює також ІЛ-7 – ростовий фактор для Т- і В- лімфоцитів.Слайд 21Залежно від структури клітин - мішеней цитокінів ділять на 3
групи: 1) цитокіни, що впливають в основному на
стовбурові клітини, - ФСКkit -ligand), fit-Зліганд; 2) цитокіни, що володіють широким спектром біологічної активності , спрямованої на стовбурові клітини, коммітовані попередники та зрілі клітини декількох паростків кровотворення - КСФ-ГМ, ІЛ-3; 3) місцево - специфічні цитокіни, діючі головним чином на клітини певного ростка: КСФ-Г (гранулоцитарного паростка), КСФ-М (моноцитарного ростка), ІЛ- 3 ( мульти -КСФ ), ТРП (тромбоцитарного ростка), ЕП (еритроцитарного ростка), ІЛ-5 стимулює кінцеві стадії утворення еозинофілів .
Слайд 22 Цитокіни, що беруть участь у гемопоезі, можуть бути розділені
за будовою їх рецепторів на 3 групи:
1) гемопоетичні рецептори I
класу: ТРП, ЕП, КСФ-Г, КСФ-ГМ та інші;
2) імуноглобуліноподібні рецептори з внутрішньоклітинною тирозин-кіназною активністю: ФСК (kit-ligand), fit-3-ligand, КСФ-М;3) рецептори із загальною β-субодиницею: КСФ-ГМ, ІЛ-3,ІЛ-5; 4) рецептори із загальною γ-субодиницею: ІЛ-2, ІЛ-4, ІЛ-15, ІЛ-21 та інші.
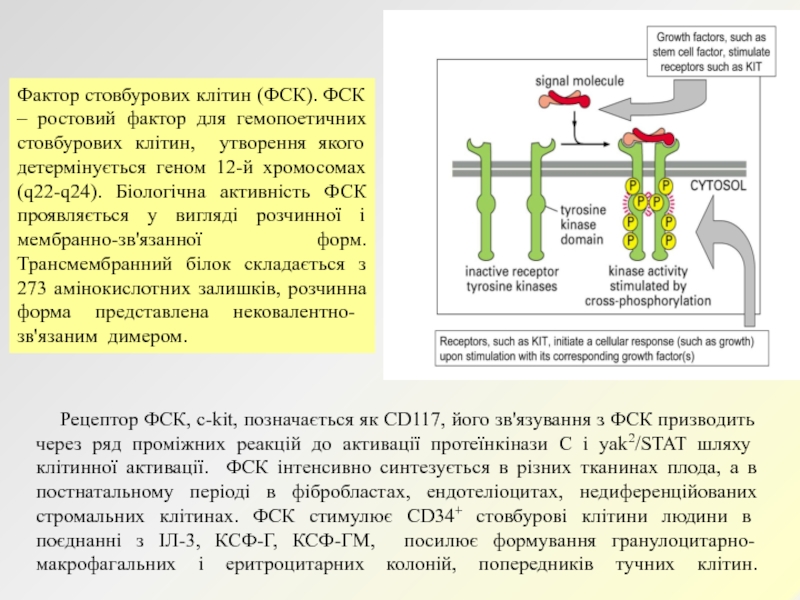
Слайд 23 Рецептор ФСК, c-kit, позначається як CD117, його
зв'язування з ФСК призводить через ряд проміжних реакцій до активації
протеїнкінази С і yak2/STAT шляху клітинної активації. ФСК інтенсивно синтезується в різних тканинах плода, а в постнатальному періоді в фібробластах, ендотеліоцитах, недиференційованих стромальних клітинах. ФСК стимулює CD34+ стовбурові клітини людини в поєднанні з ІЛ-3, КСФ-Г, КСФ-ГМ, посилює формування гранулоцитарно-макрофагальних і еритроцитарних колоній, попередників тучних клітин.Фактор стовбурових клітин (ФСК). ФСК – ростовий фактор для гемопоетичних стовбурових клітин, утворення якого детермінується геном 12-й хромосомах (q22-q24). Біологічна активність ФСК
проявляється у вигляді розчинної і мембранно-зв'язанної форм. Трансмембранний білок складається з 273 амінокислотних залишків, розчинна форма представлена нековалентно-зв'язаним димером.
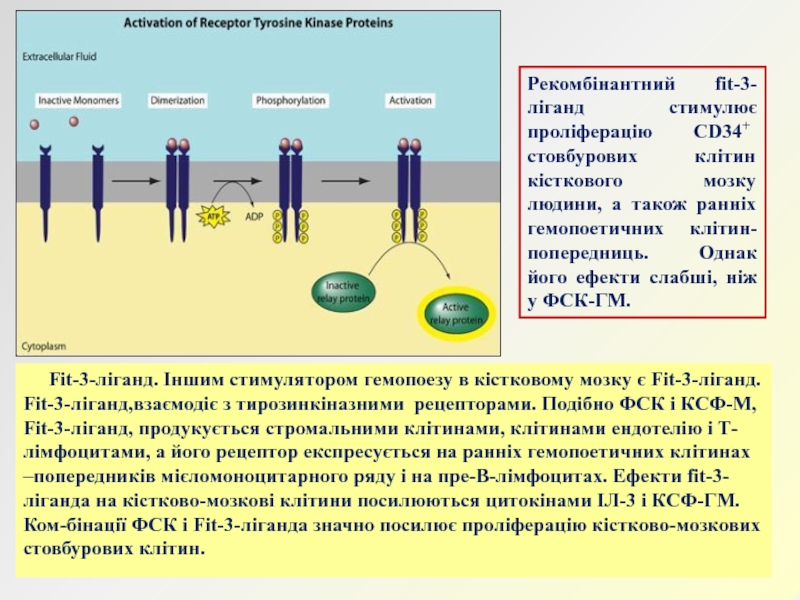
Слайд 24 Fit-3-ліганд. Іншим стимулятором гемопоезу в кістковому мозку
є Fit-3-ліганд. Fit-3-ліганд,взаємодіє з тирозинкіназними рецепторами. Подібно ФСК і КСФ-М,
Fit-3-ліганд, продукується стромальними клітинами, клітинами ендотелію і Т-лімфоцитами, а його рецептор експресується на ранніх гемопоетичних клітинах –попередників мієломоноцитарного ряду і на пре-В-лімфоцитах. Ефекти fit-3-ліганда на кістково-мозкові клітини посилюються цитокінами ІЛ-3 і КСФ-ГМ. Ком-бінації ФСК і Fit-3-ліганда значно посилює проліферацію кістково-мозкових стовбурових клітин.Рекомбінантний fit-3-ліганд стимулює проліферацію CD34+ стовбурових клітин кісткового мозку людини, а також ранніх гемопоетичних клітин-попередниць. Однак його ефекти слабші, ніж у ФСК-ГМ.
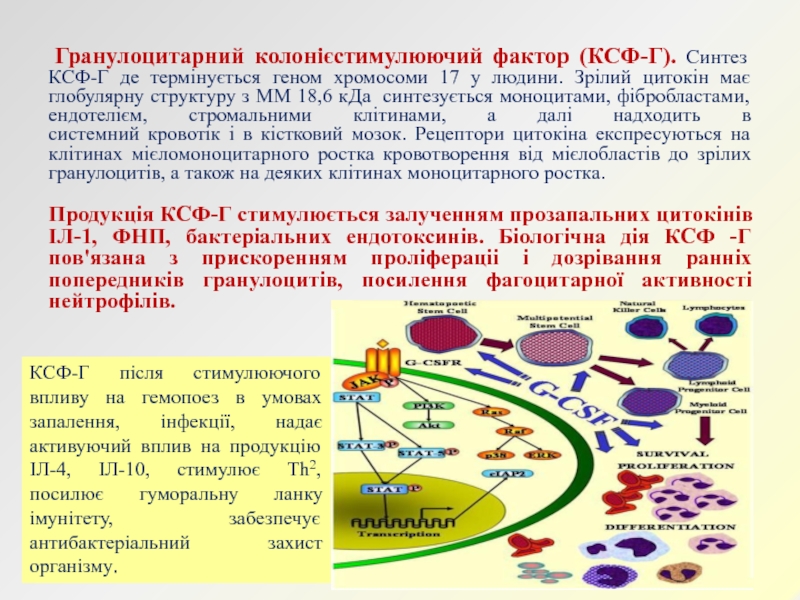
Слайд 25 Гранулоцитарний колонієстимулюючий фактор (КСФ-Г). Синтез КСФ-Г де термінується геном
хромосоми 17 у людини. Зрілий цитокін має глобулярну структуру з
ММ 18,6 кДа синтезується моноцитами, фібробластами, ендотелієм, стромальними клітинами, а далі надходить в системний кровотік і в кістковий мозок. Рецептори цитокіна експресуються на клітинах мієломоноцитарного ростка кровотворення від мієлобластів до зрілих гранулоцитів, а також на деяких клітинах моноцитарного ростка.Продукція КСФ-Г стимулюється залученням прозапальних цитокінів ІЛ-1, ФНП, бактеріальних ендотоксинів. Біологічна дія КСФ -Г пов'язана з прискоренням проліфераціі і дозрівання ранніх попередників гранулоцитів, посилення фагоцитарної активності нейтрофілів.
КСФ-Г після стимулюючого впливу на гемопоез в умовах запалення, інфекції, надає активуючий вплив на продукцію ІЛ-4, ІЛ-10, стимулює Th2, посилює гуморальну ланку імунітету, забезпечує антибактеріальний захист організму.
Слайд 26Макрофагальний колонієстимулюючий фактор (КСФ-М). Макрофагальний колонієстимулюючий фактор КСФ -М продукується
стромальними клітинами кісткового мозку, фібробластами, моноцитами, макрофагами, гепатоцитами, ендотелієм, гладком'язовими
клітинами. КСФ -М кодується геном, розташованим на короткому плечі першої хромосоми в зоні р13-р21. Мономер КСФ -М складається з 256 амінокислот, існує у вигляді розчинної і мембранно-зв'язаної форми.КСФ -М стимулює проліферацію, диференціювання клітин-попередниць моноцитарного ряду, викликає розвиток моноцитозу, тромбоцитопенії, інколи нейтропенії, підвищує протипухлинну антитілозалежну цитотоксичність моноцитів і антибактеріальну активність клітин моноцитарно-макрофагального ряду.
Слайд 27 Рецептори M-CSF відносяться до сімейства рецепторів ростових
факторів, кодуються протоонкогенах c-fmg, експресуються на всіх клітинах моноцитарного ряду,
гладком'язових клітинах і на трофобласті.Ген КСФ -М в багатьох клітинах експресується конститутивно, посилення синтезу цитокіну виникає під впливом ІЛ- 10, ФНП- α, КСФ-ГМ, прогестероном, ІЛ- 4.
Слайд 28 Гранулоцитарно-макрофагальний колонієстимулюючий фактор (КСФ-ГМ). КСФ-ГМ-ростовий фактор, в нормі він
синтезується в незначних кількостях, а при запаленні різного генезу інтенсивність
синтезу зростає під впливом бактеріальних ендотоксинів, прозапальних цитокінів. Зрілий КСФ-ГМ має ММ 14,5 кДа, складається з 127 амінокислотних залишків. Інтенсивне глікозилювання КСФ-ГМ в процесі синтезу призводить до збільшення його ММ і синтетичної біологічної активності. Біологічна активність КСФ-ГМ спрямована на стимуляцію і диференціювання мієломоноцитарних попередників гемопоезу, колоній мегакаріоцитів, а також на посилення функціональної активності нейтрофілів, еозинофілів, моноцитів за рахунок стимуляції хемотаксису, адгезії, продукції активних форм кисню.
КСФ-ГМ викликає посилення антигенпрезентуючої функції моноцитів, цитотоксичності моноцитів відносно пухлинних клітин.
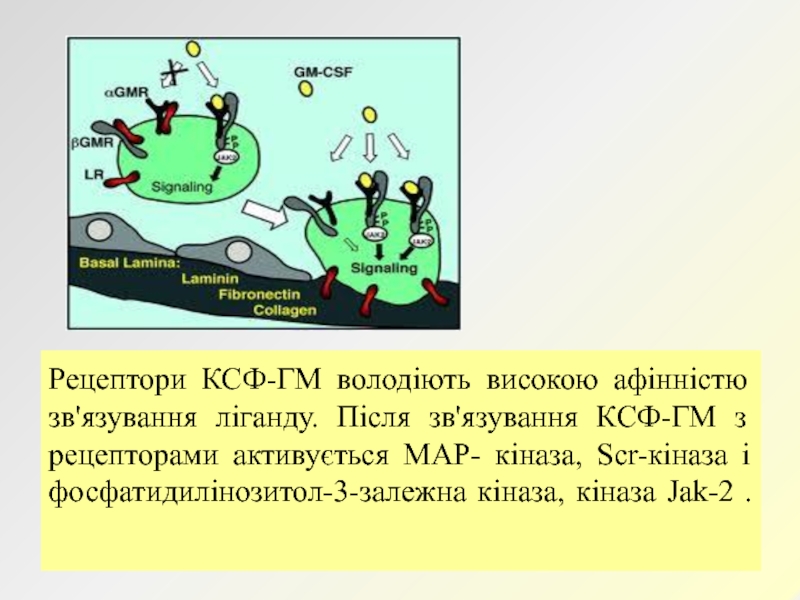
Слайд 29Рецептори КСФ-ГМ володіють високою афінністю зв'язування ліганду. Після зв'язування КСФ-ГМ
з рецепторами активується МАР- кіназа, Scr-кіназа і фосфатидилінозитол-3-залежна кіназа, кіназа
Jak-2 .Слайд 30 Еритропоетин (ЕП ) . Ген ЕП знаходиться на хромосомі
7 ( llq-22q ) . Зрілий ЕП складається з 165
амінокислотних залишків, має ММ 18000 кДа, глікозилювання може призводити до утворення декількох біологічно активних форм ЕП з ММ до 30000 кДа. Основним місцем синтезу ЕП у дорослої людини є інтерстиціальні фібробластоподібні клітини нирок в області перитубулярних капілярів, 10-15 % ЕП синтезуються гепатоцитами і епітелієм, оточуючим центральні вени печінки. У мозку, плаценті, селезінці та легенях синтезується лише незначна кількість ЕП.
До числа біологічних ефектів ЕП відноситься стимуляція утворення фактора росту судинного ендотелію і відповідно ангіогенезу, а також гальмування апоптозу клітин за рахунок активації bcl-2 та інактивації киназ. У зв'язку з цим слід зазначити, що рецептори ЕП експресуються не тільки на клітинах еритроїдного ряду кісткового мозку, але і на ендотелії, гладких м'язах, клітинах нирок, слизової шлунково -кишкового тракту.
Слайд 31
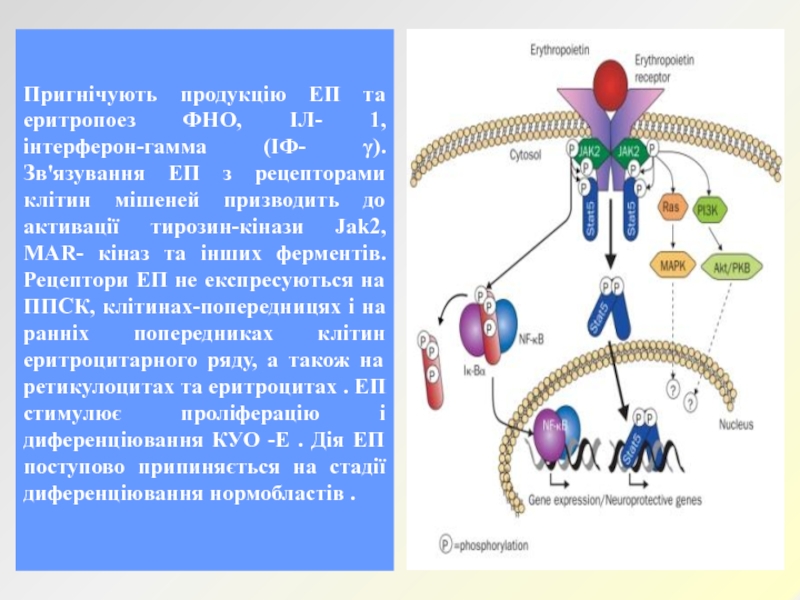
Пригнічують продукцію ЕП та еритропоез ФНО, ІЛ- 1, інтерферон-гамма
(ІФ- γ). Зв'язування ЕП з рецепторами клітин мішеней призводить до
активації тирозин-кінази Jak2, MAR- кіназ та інших ферментів. Рецептори ЕП не експресуються на ППСК, клітинах-попередницях і на ранніх попередниках клітин еритроцитарного ряду, а також на ретикулоцитах та еритроцитах . ЕП стимулює проліферацію і диференціювання КУО -Е . Дія ЕП поступово припиняється на стадії диференціювання нормобластів .Слайд 32Тромбопоетин (ТРП). ТРП-це ростовий фактор мегакаріоцитів і дозрівання тромбоцитів, у
зв'язку з чим синонімом ТРП є мегакаріоцітарний ростовой і диференціювальний
фактор. Ген ТРП людини кодує поліпептид з ММ 35,5 кДа, що піддається активному глікозилюванні в області С- кінця, втрати амінокислотних залишків і зниження ММ . Однак при цьому активність ТРП може зростати, що виявлено у 14-членного пептидного антагоніста ТРП.Основними місцями продукції ТРП є печінка, нирки, селезінка. Рецептори ТРП експресуються на стовбурових клітинах (CD34+), комітованих попередниках, мегакаріоцити і зрілих тромбоцитах, але відсутні на гранулоцитах, моноцитах, лімфоцитах .
Ефекти ТРП полягають у прискоренні дозрівання попередників тромбоцитопоезу, посилюються гемопоетичними ростовими факторами ФСК, Fit-3-лігандом та ІЛ-3. ТРП не впливає на агрегаційну здатність тромбоцитів і вивільнення біологічно активних речовин.
Слайд 33Важлива роль в процесі диференціювання і проліферації лімфоцитів відводиться системі
цитокінів, зокрема ІЛ- 4, ІЛ- 6, ІЛ- 7, ІЛ- 10,
ФНП- α.Інтерлейкін-3 (ІЛ -3). ІЛ- 3-мульти -КСФ стимулює розвиток гранулоцитарного, моноцитарного, мегакаріоцітарного і еритроїдного ростків кровотворення . Дія ІЛ- 3 зачіпає гемопоетичні клітини на ранніх етапах розвитку, починаючи зі стовбурної клітини, ІЛ- 3 стимулює проліферацію попередників В- лімфоцитів, функціональну активність зрілих лейкоцитів, моноцитів, посилює цитотоксичність макрофагів відносно пухлинних і бактеріальних клітин, стимулює диференціювання базофілів, еозинофілів, проліферацію ендотеліоцитів, експресію адгезивних молекул ELAM-1.
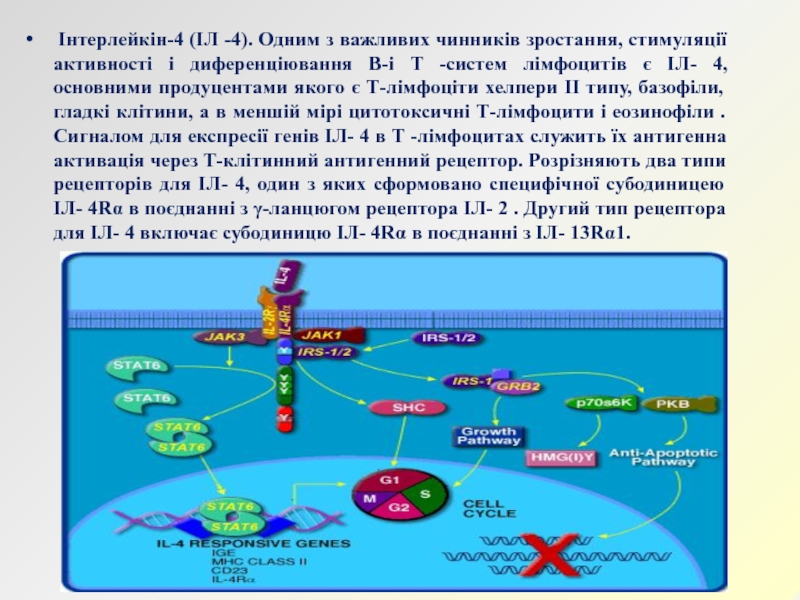
Слайд 34 Інтерлейкін-4 (ІЛ -4). Одним з важливих чинників зростання, стимуляції
активності і диференціювання В-і Т -систем лімфоцитів є ІЛ- 4,
основними продуцентами якого є Т-лімфоціти хелпери II типу, базофіли, гладкі клітини, а в меншій мірі цитотоксичні Т-лімфоцити і еозинофіли . Сигналом для експресії генів ІЛ- 4 в Т -лімфоцитах служить їх антигенна активація через Т-клітинний антигенний рецептор. Розрізняють два типи рецепторів для ІЛ- 4, один з яких сформовано специфічної субодиницею ІЛ- 4Rα в поєднанні з γ-ланцюгом рецептора ІЛ- 2 . Другий тип рецептора для ІЛ- 4 включає субодиницю ІЛ- 4Rα в поєднанні з ІЛ- 13Rα1.Слайд 35 ІЛ- 4 є типовим плейотропним цитокіном з широким спектром
біологічної активності, що охоплює багато типів лімфоїдних клітин, одним з
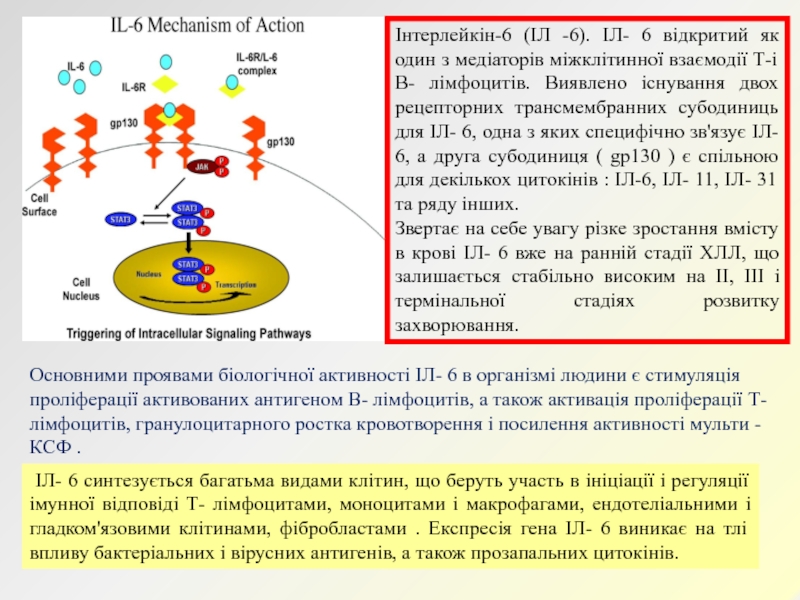
головних регуляторів розвитку алергічних реакцій, ростовим фактором для базофілів, еозинофілів, тучних клітин. Водночас біологічна активність ІЛ- 4 проявляється в ролі одного з основних негативних регуляторів розвитку реакцій клітинного імунітету. Вмісту зростає ІЛ -4 в крові хворих з ХЛЛ, що досягає максимуму на термінальній стадії розвитку патології.Слайд 36Інтерлейкін-6 (ІЛ -6). ІЛ- 6 відкритий як один з медіаторів
міжклітинної взаємодії Т-і В- лімфоцитів. Виявлено існування двох рецепторних трансмембранних
субодиниць для ІЛ- 6, одна з яких специфічно зв'язує ІЛ- 6, а друга субодиниця ( gp130 ) є спільною для декількох цитокінів : ІЛ-6, ІЛ- 11, ІЛ- 31 та ряду інших.Звертає на себе увагу різке зростання вмісту в крові ІЛ- 6 вже на ранній стадії ХЛЛ, що залишається стабільно високим на II, III і термінальної стадіях розвитку захворювання.
ІЛ- 6 синтезується багатьма видами клітин, що беруть участь в ініціації і регуляції імунної відповіді Т- лімфоцитами, моноцитами і макрофагами, ендотеліальними і гладком'язовими клітинами, фібробластами . Експресія гена ІЛ- 6 виникає на тлі впливу бактеріальних і вірусних антигенів, а також прозапальних цитокінів.
Основними проявами біологічної активності ІЛ- 6 в організмі людини є стимуляція проліферації активованих антигеном В- лімфоцитів, а також активація проліферації Т- лімфоцитів, гранулоцитарного ростка кровотворення і посилення активності мульти -КСФ .
Слайд 37 Інтерлейкін-7 (ІЛ -7). ІЛ- 7 синтезується клітинами строми кісткового
мозку, стимулює проліферацію попередників В- лімфоцитів і ранніх мієлоцитів .
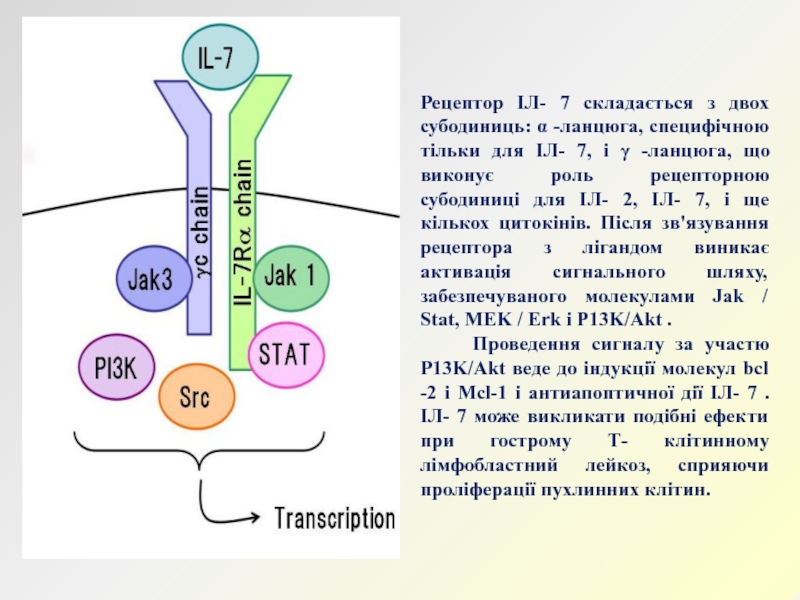
Ген ІЛ- 7 розташований на хромосомі 8q-12-13. Зрілий цитокин має ММ близько 17 кДа, складається з 152 амінокислотних залишків, в процесі N- глікозилювання та приєднання 34 вуглеводних залишків ММ активного ІЛ- 7 досягає 25 кДа . Конститутивним синтез ІЛ- 7 в невеликих кількостях забезпечується стромальними клітинами кісткового мозку епітелієм тимусу, селезінки, кератиноцитами і клітинами фетальної печінки.Слайд 38Рецептор ІЛ- 7 складається з двох субодиниць: α -ланцюга, специфічною
тільки для ІЛ- 7, і γ -ланцюга, що виконує роль
рецепторною субодиниці для ІЛ- 2, ІЛ- 7, і ще кількох цитокінів. Після зв'язування рецептора з лігандом виникає активація сигнального шляху, забезпечуваного молекулами Jak / Stat, MEK / Erk і P13K/Akt .Проведення сигналу за участю Р13K/Akt веде до індукції молекул bсl -2 і Мсl-1 і антиапоптичної дії ІЛ- 7 . ІЛ- 7 може викликати подібні ефекти при гострому Т- клітинному лімфобластний лейкоз, сприяючи проліферації пухлинних клітин.
Слайд 39Перші дані, що свідчать про здатність ІЛ- 7 посилювати проліферацію
про- В-і пре -В- лімфоцитів, опубліковані A. Namen et al
., 1988. Пізніше було показано, що ІЛ- 7 підсилює проліферацію пре -В- лімфоцитів синергічно з ФСК і fit-3-лігандом . ІЛ- 7 стимулює проліферацію В- лімфоцитів.ІЛ- 7-ростової фактор не тільки для ранніх попередників Т- лімфоцитів, які потім можуть диференціюватися в зрілі Th, Тс під впливом інших чинників диференціювання, а й для клітин пізніх стадій диференціювання Т- лімфоцитів. ІЛ- 7 не володіє прямою мітогенною ктивністю, а виступає в ролі костимулятора при антигенному впливі на Т -систему лімфоцитів. ІЛ- 7 підсилює продукцію ІФ- γ та ІЛ-4, діє синергічно з ІЛ- 12 .