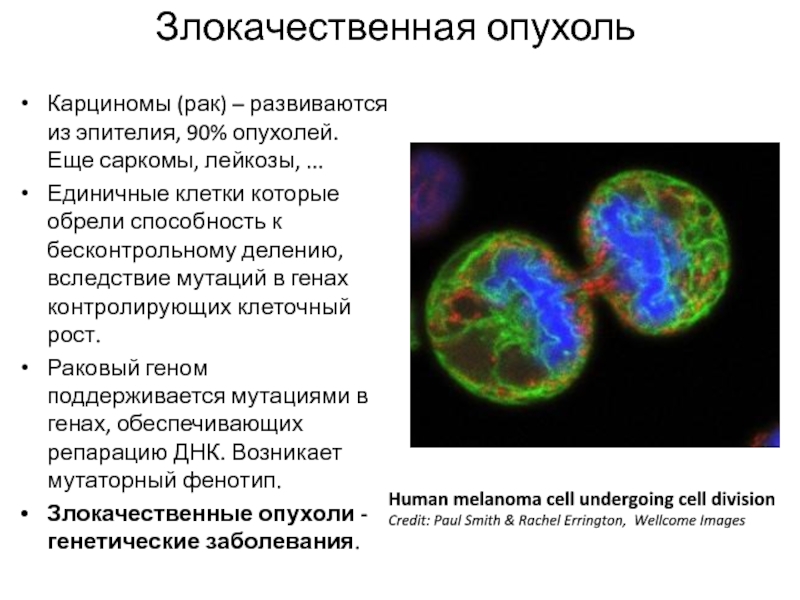
Слайд 2Злокачественная опухоль
Карциномы (рак) – развиваются из эпителия, 90% опухолей. Еще
саркомы, лейкозы, ...
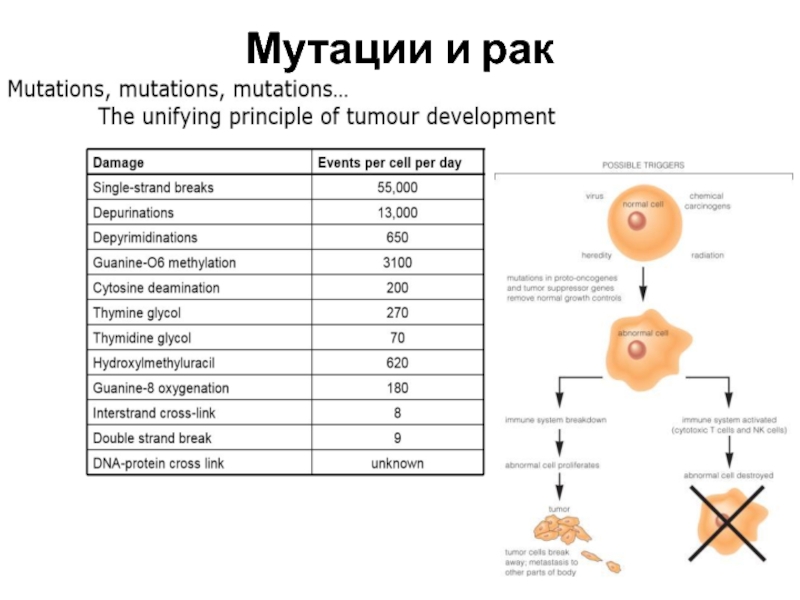
Единичные клетки которые обрели способность к бесконтрольному делению,
вследствие мутаций в генах контролирующих клеточный рост.
Раковый геном поддерживается мутациями в генах, обеспечивающих репарацию ДНК. Возникает мутаторный фенотип.
Злокачественные опухоли - генетические заболевания.
Human melanoma cell undergoing cell division
Credit: Paul Smith & Rachel Errington, Wellcome Images
Слайд 3Доброкачественные и злокачественные опухоли
Доброкачественные
медленный рост
нет инвазии или метастазирования
высокодифференцированы
Злокачественные
все наоборот
www.cancer.gov
Слайд 6Типы мутаций
Соматическая
Возникает de novo в ДНК клеток сомы
Не передается
потомкам
Генеративная (germline)
в ДНК половых клеток
Передается потомкам
Увеличивается риск, но соматические
мутации все равно нужны (cancer family syndrome)
синдром Ли-Фраумени, BRCA1/2 для РМЖ
CHALLENGE:
дифференцировать somatic/germline при секвенировании
Слайд 7Клональная эволюция раковых клеток
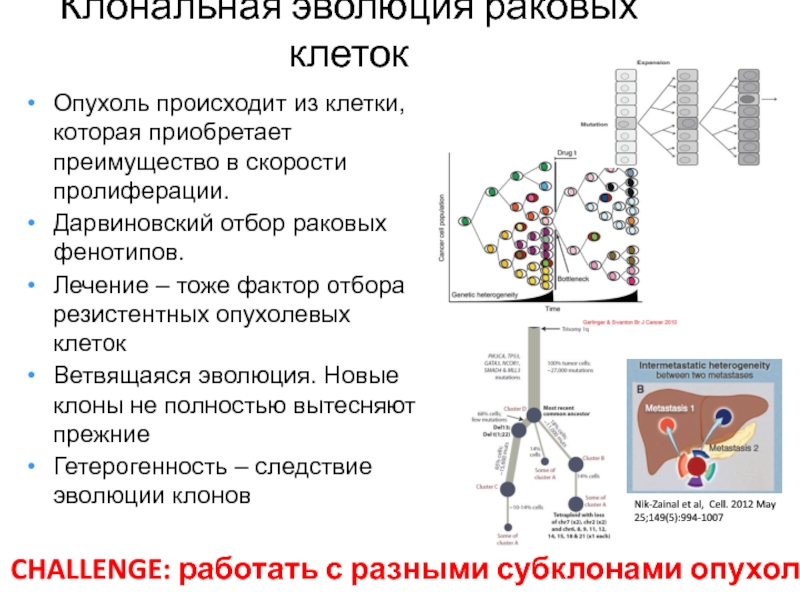
Опухоль происходит из клетки, которая приобретает преимущество
в скорости пролиферации.
Дарвиновский отбор раковых фенотипов.
Лечение – тоже фактор
отбора резистентных опухолевых клеток
Ветвящаяся эволюция. Новые клоны не полностью вытесняют прежние
Гетерогенность – следствие эволюции клонов
CHALLENGE: работать с разными субклонами опухоли
Nik-Zainal et al, Cell. 2012 May 25;149(5):994-1007
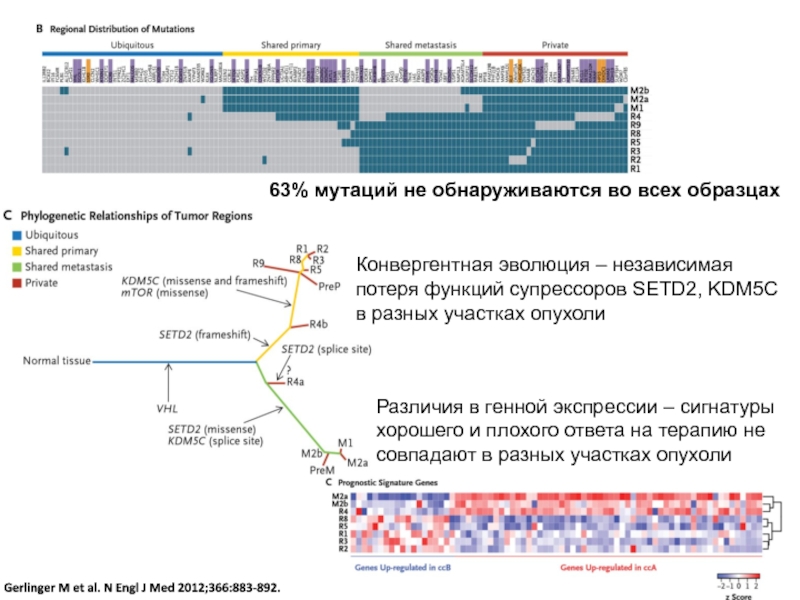
Слайд 8Gerlinger M et al. N Engl J Med 2012;366:883-892.
63% мутаций
не обнаруживаются во всех образцах
Конвергентная эволюция – независимая
потеря функций
супрессоров SETD2, KDM5C
в разных участках опухоли
Различия в генной экспрессии – сигнатуры хорошего и плохого ответа на терапию не совпадают в разных участках опухоли
Слайд 9Найти целевые события, которые произошли на ранней стадии туморогенеза и
поэтому есть у большинства клеток опухоли. Ultradeep sequencing 500-1000x
Определить доминантный
клон. Биопсии рецидивов и метастазов. Повторные биопсии во время прогрессии
Адаптивная терапия – поддерживать баланс между резистентными и чувствительными клонами. Сублетальные дозы.
Дальнейшее развитие single cell sequencing
Алгоритмы по деконволюции (TrAp)
Борьба с гетерогенностью
Слайд 10Drivers and passengers
CHALLENGE: как различать драйверов и пассажиров?
Зачем искать драйверы?
Чтобы на них воздействовать
Driver mutations:
Дают преимущество в росте
Находятся под положительным
отбором в процессе эволюции раковых клеток
Находятся в ‘cancer genes’. Таких генов ~300-500.
В одном образце в одном сигнальном пути скорее будет одна драйверная мутация
Происходят на ранних этапах онкогенеза
Cчитается, что в опухоли в среднем от 2 до 8 драйверных мутаций
Passenger mutations:
Возникают вследствие мутаторного фенотипа
Не дают преимущества в скорости роста, иногда мешая выживанию опухоли
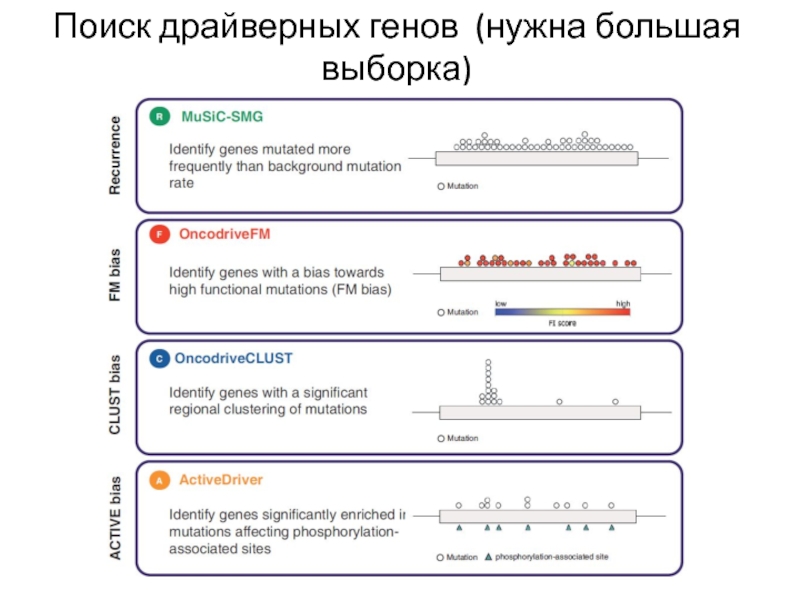
Слайд 11Поиск драйверных генов (нужна большая выборка)
Слайд 12Онкогены – стимулируют клеточный рост и дифференцировку. Мутации gain of
function, в специф. сайтах, достаточно одного аллеля.
Онкосупрессоры – ингибируют клеточный
рост и дифференцировку. Мутации loss of function, оба аллеля должны быть затронуты.
Gatekeepers (гены-привратники) – контролируют клеточный цикл, в том числе способствуют апоптозу
Caretakers (мутаторные гены)– защищают целостность генома, в том числе участвуют в репарации, расхождении хромосом при митозе.
Нет абсолютно четкого деления gatekeeper/caretaker
Онкогены и онкосупрессоры
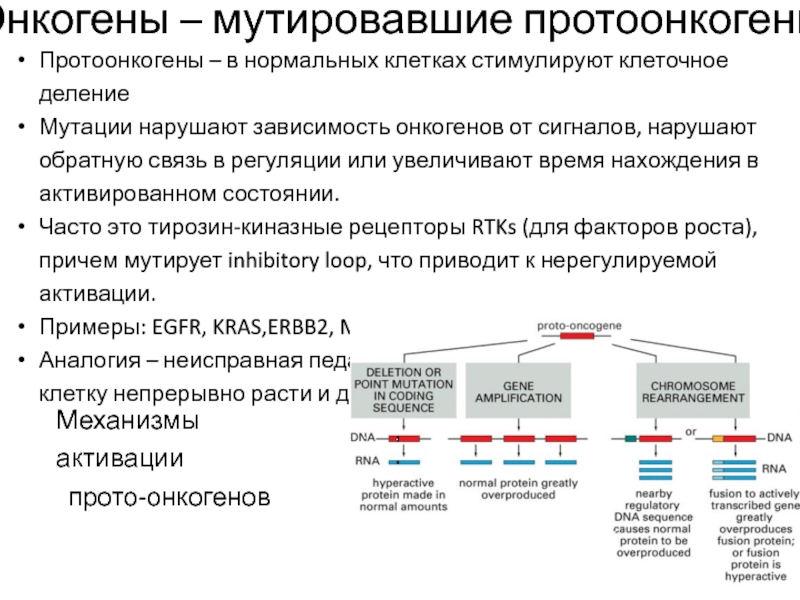
Слайд 13Онкогены – мутировавшие протоонкогены
Протоонкогены – в нормальных клетках стимулируют клеточное
деление
Мутации нарушают зависимость онкогенов от сигналов, нарушают обратную связь в
регуляции или увеличивают время нахождения в активированном состоянии.
Часто это тирозин-киназные рецепторы RTKs (для факторов роста), причем мутирует inhibitory loop, что приводит к нерегулируемой активации.
Примеры: EGFR, KRAS,ERBB2, MET, MYC
Аналогия – неисправная педаль газа в автомобиле. Заставляет клетку непрерывно расти и делиться.
Механизмы активации
прото-онкогенов
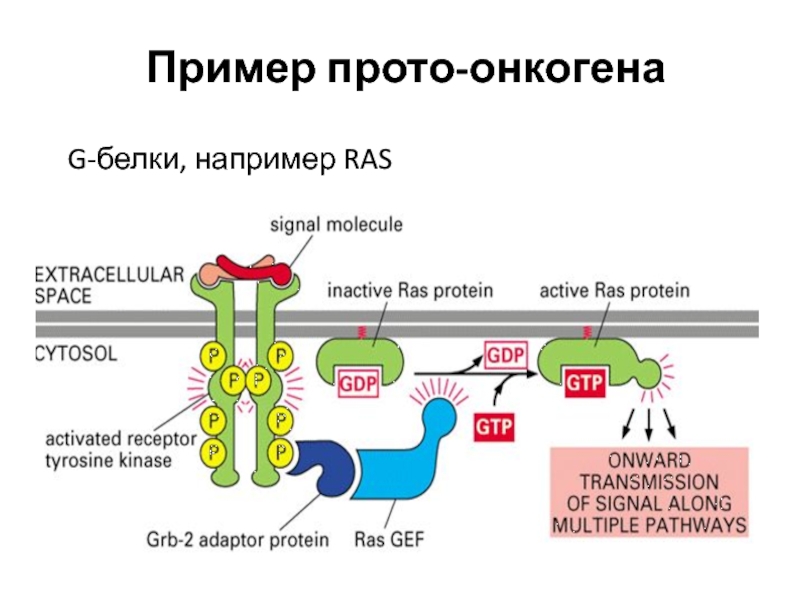
Слайд 14Пример прото-онкогена
G-белки, например RAS
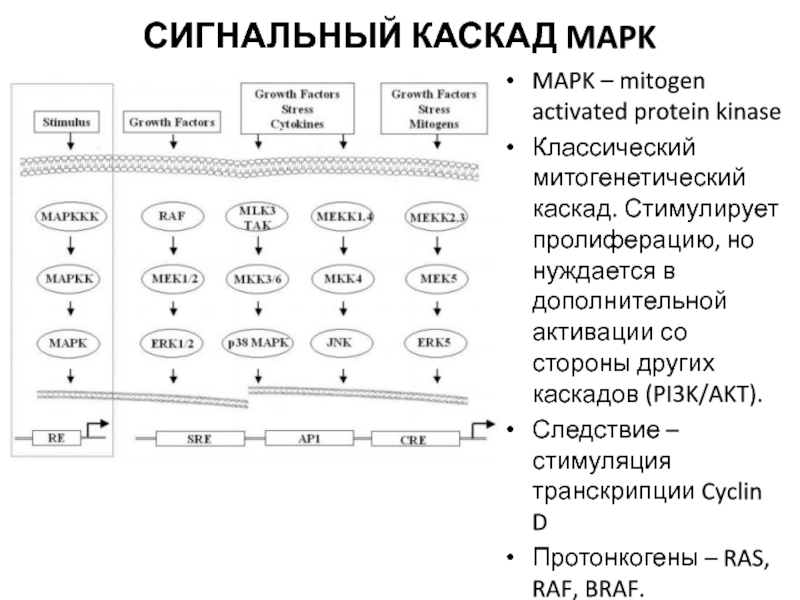
Слайд 15Сигнальный каскад MAPK
MAPK – mitogen activated protein kinase
Классический митогенетический каскад.
Стимулирует пролиферацию, но нуждается в дополнительной активации со стороны других
каскадов (PI3K/AKT).
Следствие – стимуляция транскрипции Cyclin D
Протонкогены – RAS, RAF, BRAF.
Слайд 16Супрессоры
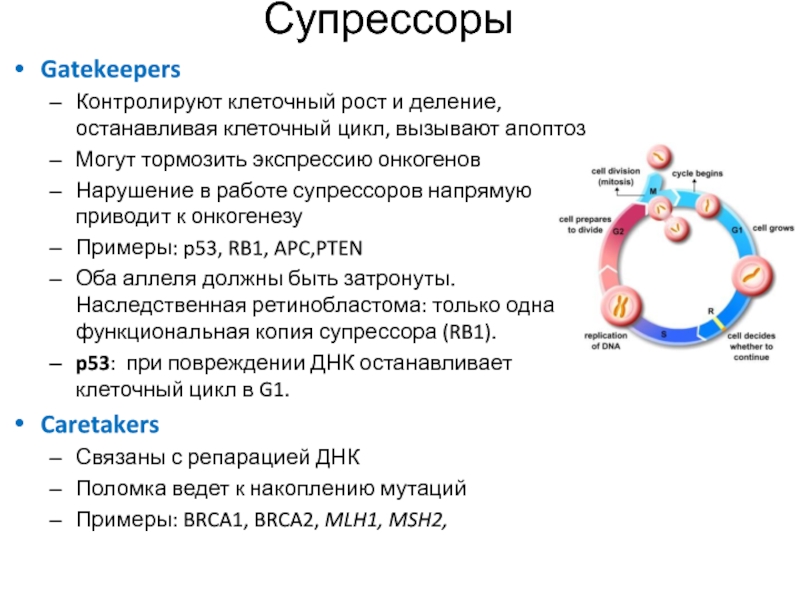
Gatekeepers
Контролируют клеточный рост и деление, останавливая клеточный цикл, вызывают апоптоз
Могут
тормозить экспрессию онкогенов
Нарушение в работе супрессоров напрямую приводит к онкогенезу
Примеры:
p53, RB1, APC,PTEN
Оба аллеля должны быть затронуты. Наследственная ретинобластома: только одна функциональная копия супрессора (RB1).
p53: при повреждении ДНК останавливает клеточный цикл в G1.
Caretakers
Связаны с репарацией ДНК
Поломка ведет к накоплению мутаций
Примеры: BRCA1, BRCA2, MLH1, MSH2,
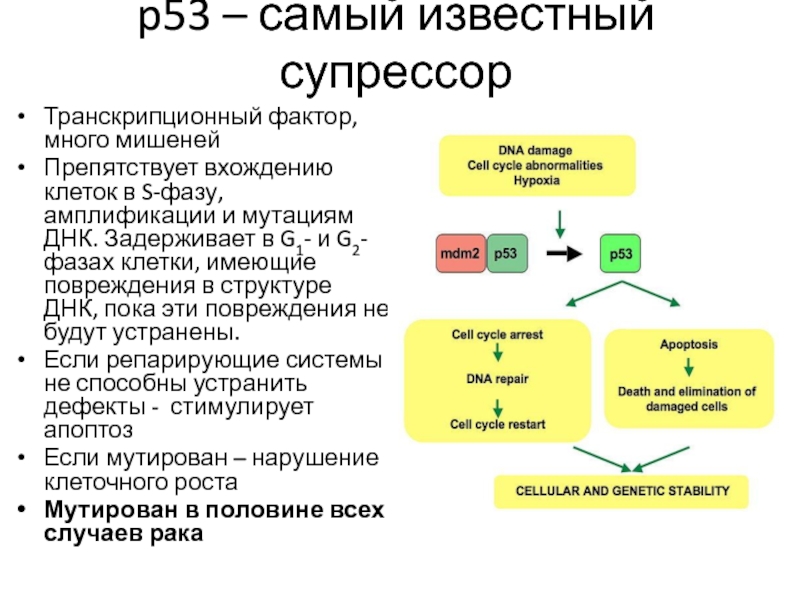
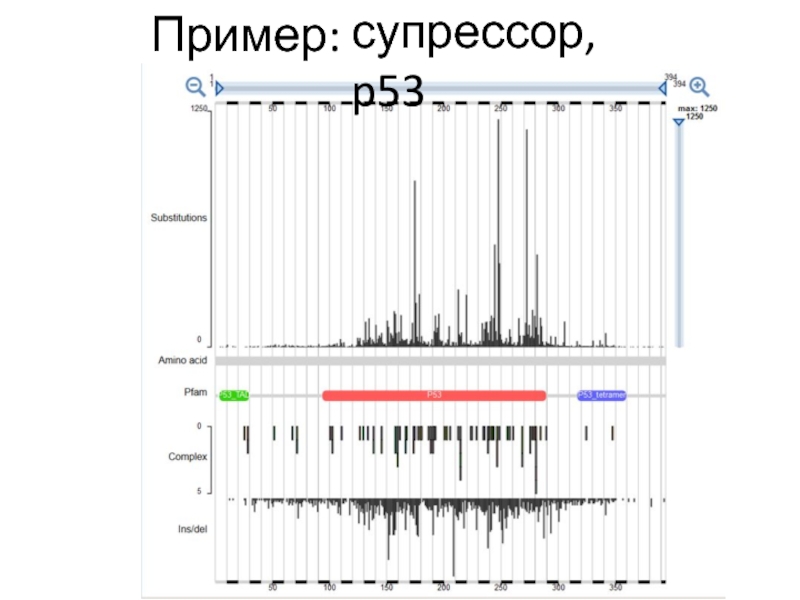
Слайд 17p53 – самый известный супрессор
Транскрипционный фактор, много мишеней
Препятствует вхождению клеток
в S-фазу, амплификации и мутациям ДНК. Задерживает в G1- и
G2-фазах клетки, имеющие повреждения в структуре ДНК, пока эти повреждения не будут устранены.
Если репарирующие системы не способны устранить дефекты - стимулирует апоптоз
Если мутирован – нарушение клеточного роста
Мутирован в половине всех случаев рака
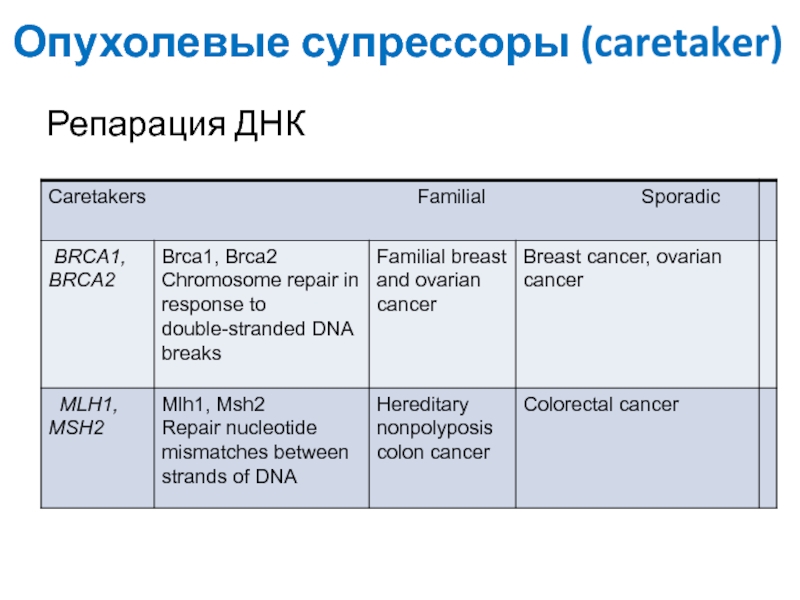
Слайд 18Репарация ДНК
Опухолевые супрессоры (caretaker)
Слайд 19
Одного онкогена недостаточно для развития заболевания, нужна кооперация с другими
генами (онкогенами или супрессорами)
Онкогены обычно группируются около одного сигнального пути,
а супрессоры чаще имеют более широкий набор функций.
Супрессоры и онкогены – часто антагонисты, но нет попарной комплементарности
Мутации, активирующие ген, встречаются гораздо … , чем подавляющие
Пример: активация онкогена RAS – только 3 кодона, а инактивация супрессора TP53 – по всему гену.
РЕЖЕ
Слайд 20Правило 20/20 (Vogelstein et al, 2013):
Онкоген: 20% мутаций должны встречаться
в одной и той же позиции, вызывая одинаковую аминокислотную замену.
Супрессор:
более 20% мутаций должны быть дезактивирующими
Truncating
Миссенс
Гиперметилирование промотора
Замены
Увеличение копийности
Замены
LoF-мутации (потеря функции, loss of function):
GoF (активирующие, gain)
Определение супрессоров и онкогенов: rule of thumb
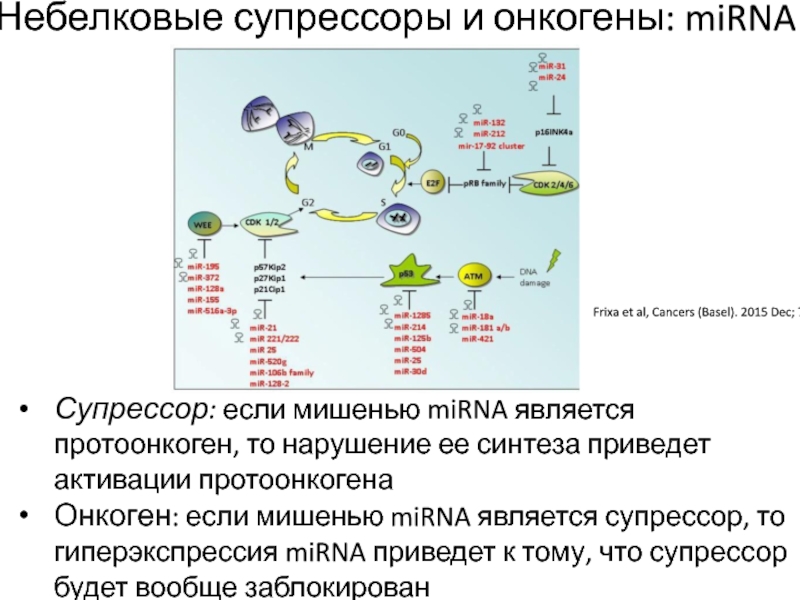
Слайд 21Frixa et al, Cancers (Basel). 2015 Dec; 7(4): 2466–2485.
Небелковые супрессоры
и онкогены: miRNA
Супрессор: если мишенью miRNA является протоонкоген, то нарушение
ее синтеза приведет активации протоонкогена
Онкоген: если мишенью miRNA является супрессор, то гиперэкспрессия miRNA приведет к тому, что супрессор будет вообще заблокирован
Слайд 22Какие типы раковых генов чаще являются мишенями лекарств – супрессоры
или онкогены?
Слайд 23Но как лечить супрессоры?
Мишенью будет не сам супрессор, а его
регулятор. Ex: MDM2 отрицательно регулирует p53, блокирование этого взаимодействия помогает.
Мишенью
будет downstream молекулы от супрессора. Например, мутантный p53 индуцирует экспрессию PDGFRb, который в свою очередь стимулирует инвазию и метастазирование.
Ингибировать каскады, которые активировались из-за мутантного супрессора. Ex: супрессор PTEN его инактивация ведет к повышению уровня PIP3, что в свою очередь активирует PI3K/AKT/mTOR pathway. Но инактивировать этот пасвей непросто, т.к. там куча обратных связей.
Synthetic lethality: если мутирован один из каскадов репарации, то надо заблокировать оставшиеся и раковая клетка умрет. Ex: targerting PARPs в BRCA1/2-мутантах.
Бороться с эпигенетикой (многие супрессоры гиперметилированы) – помогают ингибиторы DNMT (ДНК-метил-трансферазы)
Вакцины: давать мутантные пептиды из p53
Генная терапия: малоэффективно
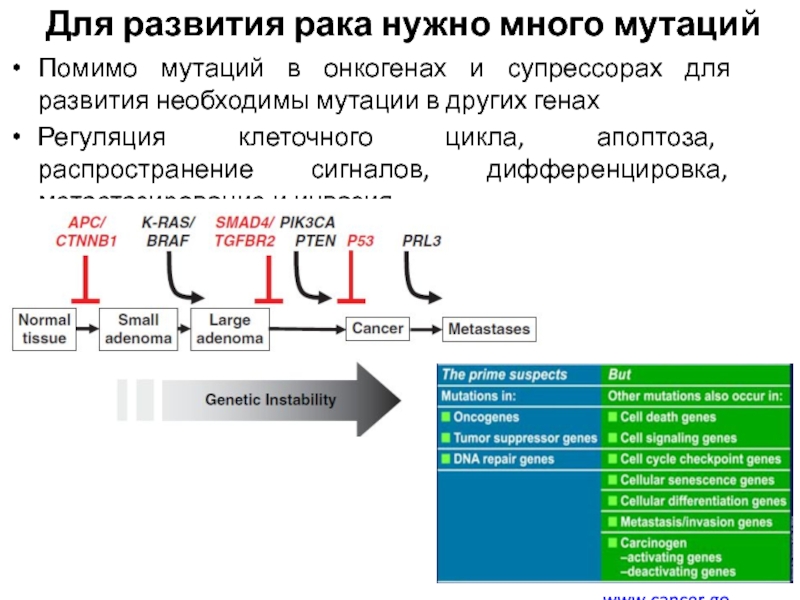
Слайд 24Для развития рака нужно много мутаций
Помимо мутаций в онкогенах и
супрессорах для развития необходимы мутации в других генах
Регуляция клеточного цикла,
апоптоза, распространение сигналов, дифференцировка, метастазирование и инвазия
www.cancer.gov
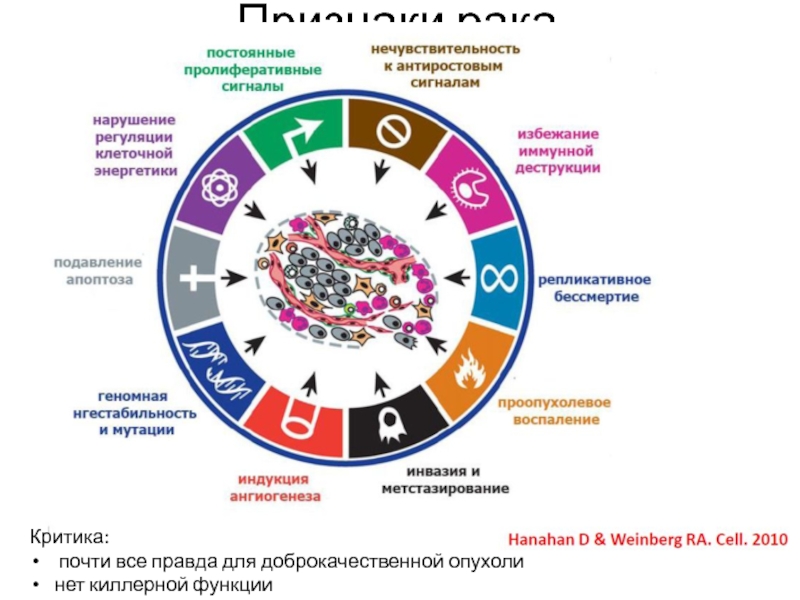
Слайд 25Признаки рака
Критика:
почти все правда для доброкачественной опухоли
нет киллерной функции
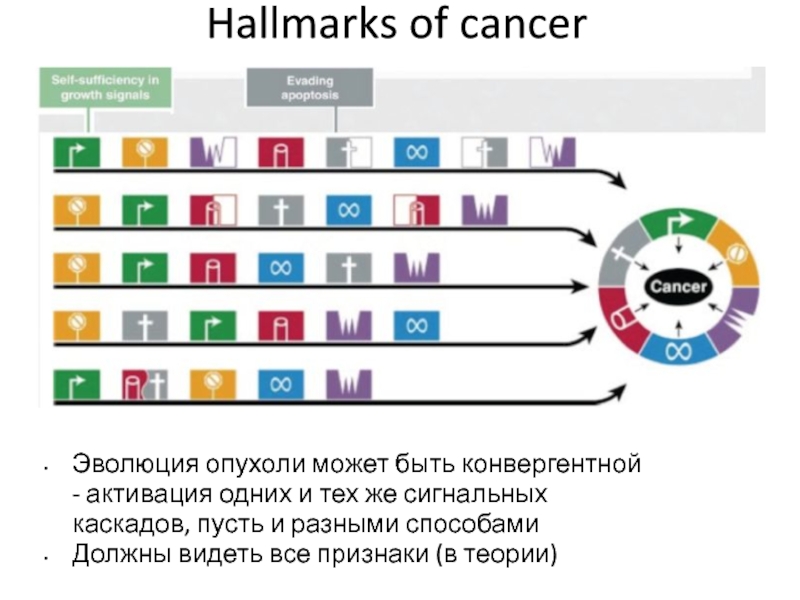
Слайд 26Эволюция опухоли может быть конвергентной - активация одних и тех
же сигнальных каскадов, пусть и разными способами
Должны видеть все признаки
(в теории)
Hallmarks of cancer
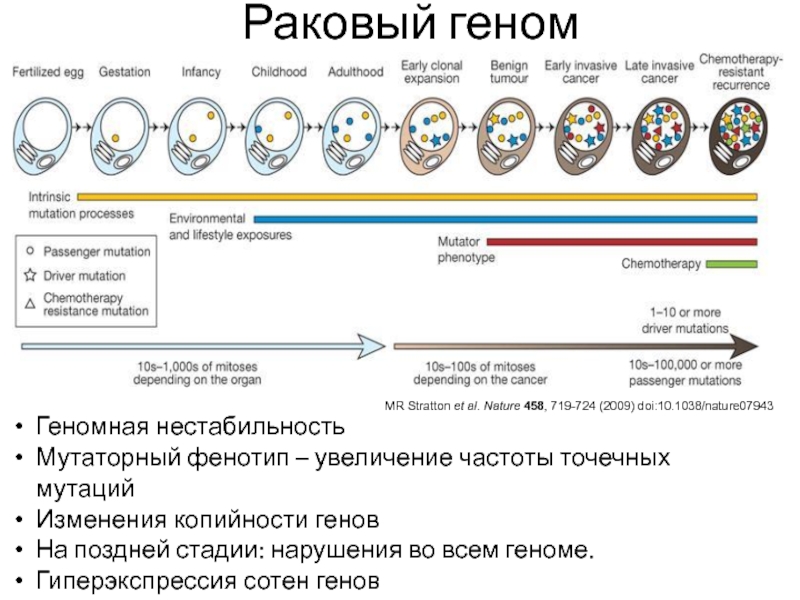
Слайд 27MR Stratton et al. Nature 458, 719-724 (2009) doi:10.1038/nature07943
Геномная нестабильность
Мутаторный
фенотип – увеличение частоты точечных мутаций
Изменения копийности генов
На поздней стадии:
нарушения во всем геноме.
Гиперэкспрессия сотен генов
Хромосомные перестройки, частичная полиплоидия
Раковый геном
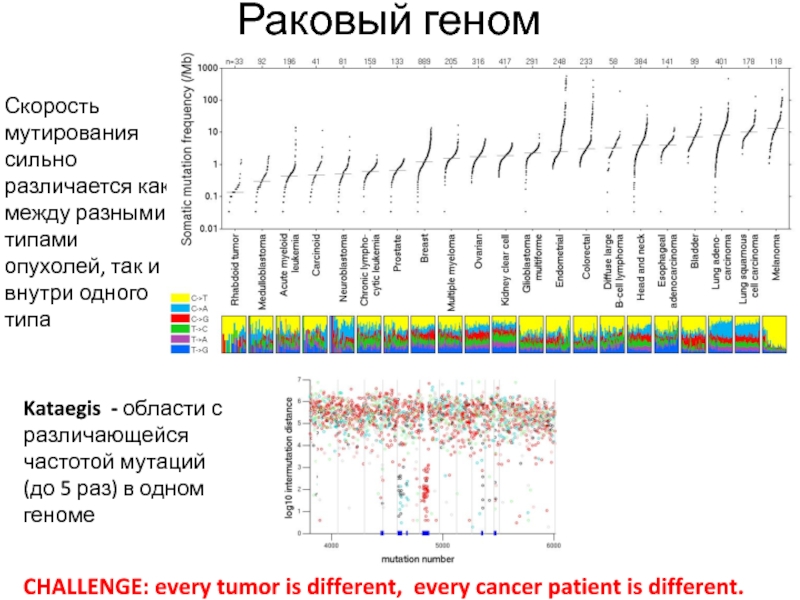
Слайд 28CHALLENGE: every tumor is different, every cancer patient is different.
Скорость
мутирования сильно различается как между разными типами опухолей, так и
внутри одного типа
Kataegis - области с различающейся частотой мутаций (до 5 раз) в одном геноме
Раковый геном
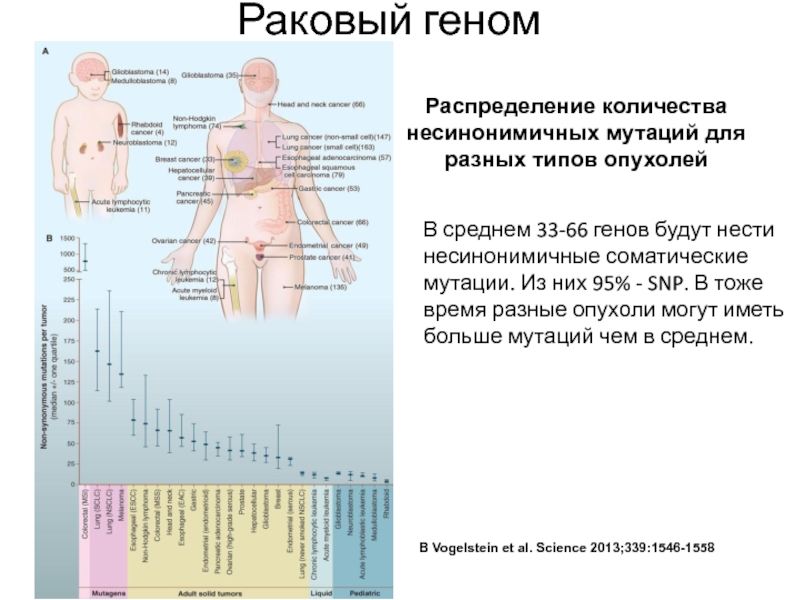
Слайд 29B Vogelstein et al. Science 2013;339:1546-1558
Распределение количества несинонимичных мутаций для
разных типов опухолей
В среднем 33-66 генов будут нести несинонимичные соматические
мутации. Из них 95% - SNP. В тоже время разные опухоли могут иметь больше мутаций чем в среднем.
Раковый геном
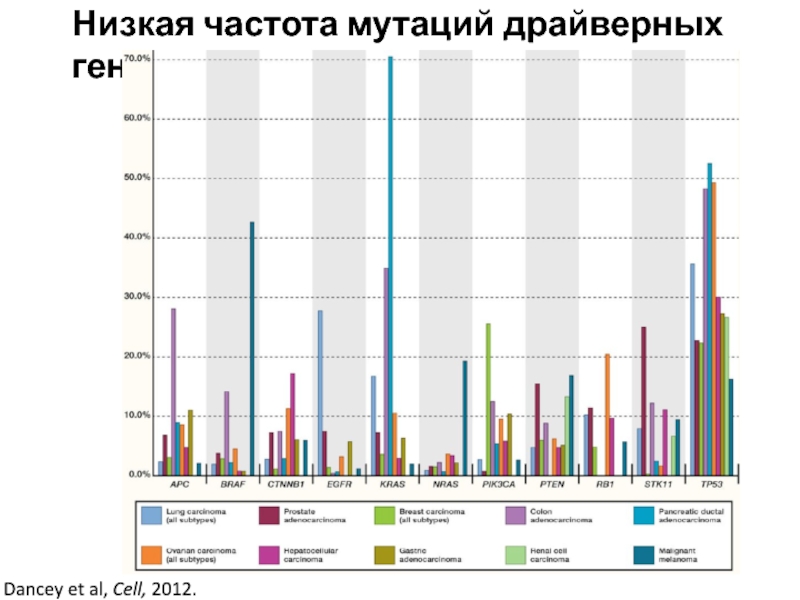
Слайд 30Низкая частота мутаций драйверных генов
Dancey et al, Cell, 2012.
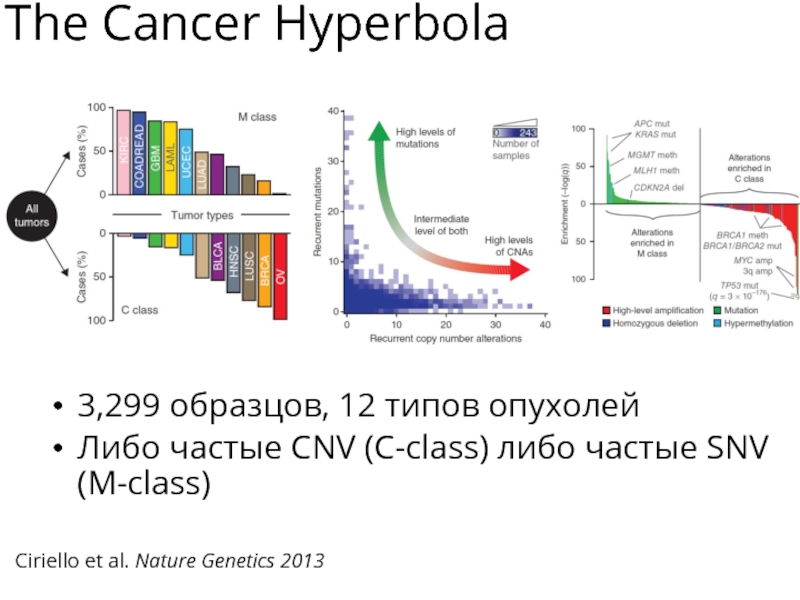
Слайд 31The Cancer Hyperbola
3,299 образцов, 12 типов опухолей
Либо частые CNV (C-class)
либо частые SNV (M-class)
Ciriello et al. Nature Genetics 2013
Слайд 32Пример: кариотип раковой клетки
Credit : Mira Grigorova and Paul Edwards,
Department of Pathology, University of Cambridge, unpublished
Source: www.path.cam.ac.uk/~pawefish/BreastCellLineDescriptions/HCC38.html
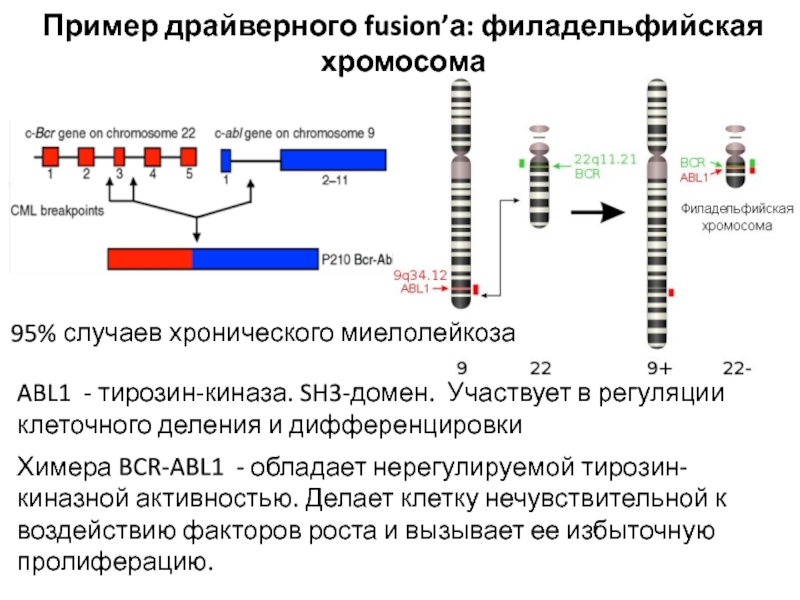
Слайд 33Пример драйверного fusion’а: филадельфийская хромосома
Химера BCR-ABL1 - обладает нерегулируемой тирозин-киназной
активностью. Делает клетку нечувствительной к воздействию факторов роста и вызывает
ее избыточную пролиферацию.
95% случаев хронического миелолейкоза
ABL1 - тирозин-киназа. SH3-домен. Участвует в регуляции клеточного деления и дифференцировки
Слайд 34Другие факторы
Вирусы
Папиломавирус человека – вызывает рак шейки матки; Есть вакцина!
HBV
и HCV: гепатоцеллюлярная карцинома
human immunodeficiency virus (HIV)—саркома Капоши и лимфомы
Карциногены
Асбест,
винил-хлорид, бензол
афлатоксин
Излучение
УФ, ретген, …
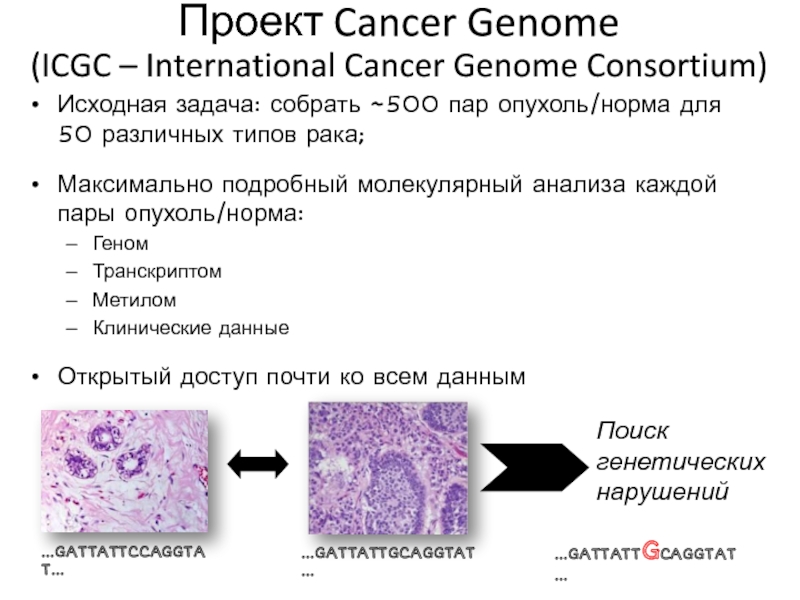
Слайд 35Исходная задача: собрать ~500 пар опухоль/норма для 50 различных типов
рака;
Максимально подробный молекулярный анализа каждой пары опухоль/норма:
Геном
Транскриптом
Метилом
Клинические данные
Открытый доступ
почти ко всем данным
Проект Cancer Genome
(ICGC – International Cancer Genome Consortium)
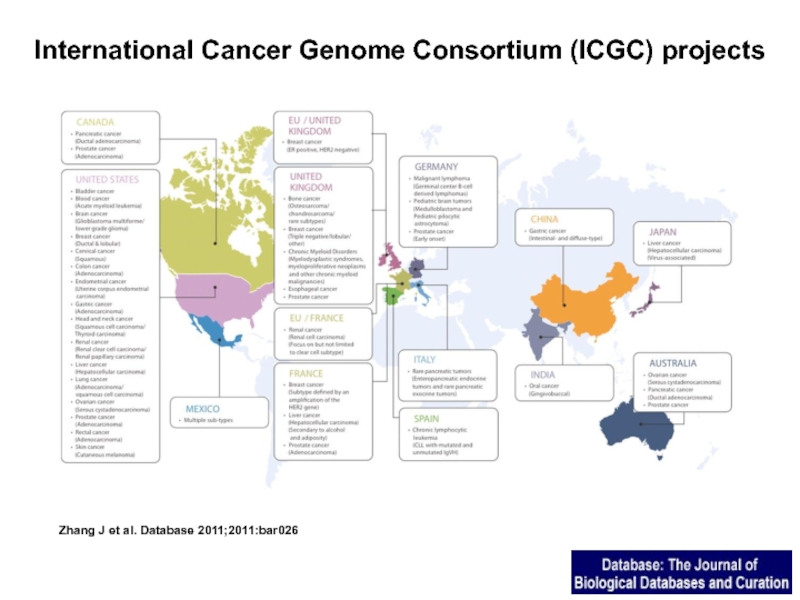
Слайд 36International Cancer Genome Consortium (ICGC) projects
Zhang J et al. Database
2011;2011:bar026
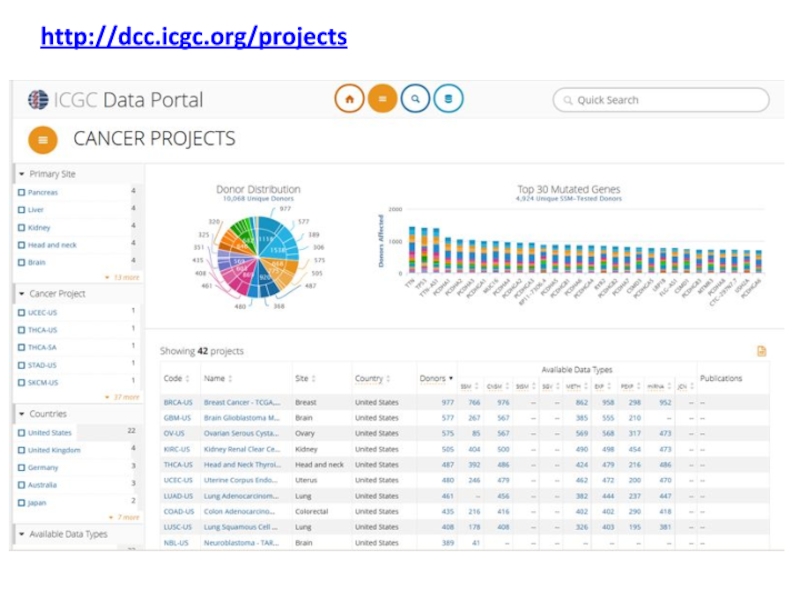
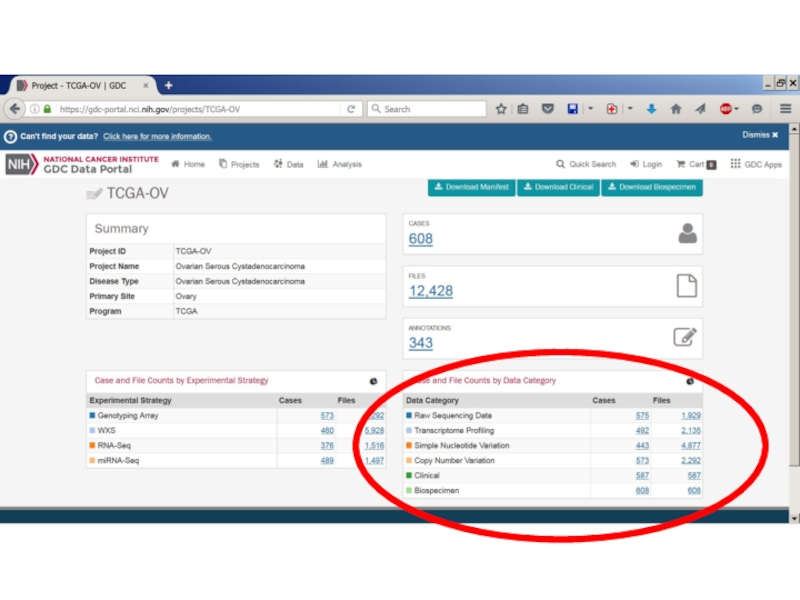
Слайд 38https://gdc.cancer.gov/
TCGA – The Cancer Genome Atlas
TARGET - Therapeutically Applicable Research
to Generate Effective Treatments
Слайд 41Молекулярные портреты опухолей
www.nature.com/tcga
Слайд 42Молекулярные портреты опухолей
http://cancergenome.nih.gov/publications
Слайд 43www.tumorportal.org - информационный портал опухолевых генов
Lawrence et al, Nature, 2014
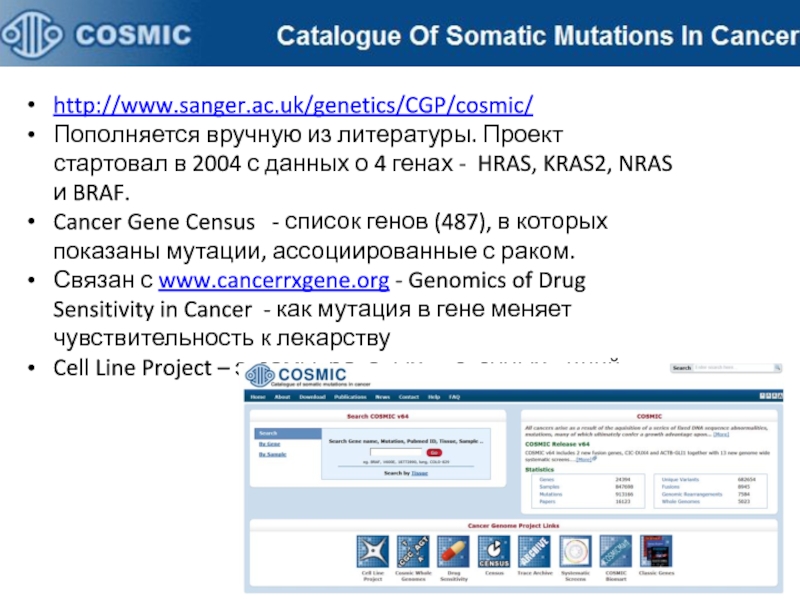
Слайд 45http://www.sanger.ac.uk/genetics/CGP/cosmic/
Пополняется вручную из литературы. Проект стартовал в 2004 с данных
о 4 генах - HRAS, KRAS2, NRAS и BRAF.
Cancer Gene
Census - список генов (487), в которых показаны мутации, ассоциированные с раком.
Связан с www.cancerrxgene.org - Genomics of Drug Sensitivity in Cancer - как мутация в гене меняет чувствительность к лекарству
Cell Line Project – экзомы раковых клеточных линий
Слайд 48Аннотация мутаций
Картирование на разметку генома
Сбор дополнительной информации
Предсказание функциональной значимости
Оценка драйверности
мутации
http://www.lifescisoft.com/ingenuity-variant-analysis.html
Цель – определить драйверные и actionable мутации
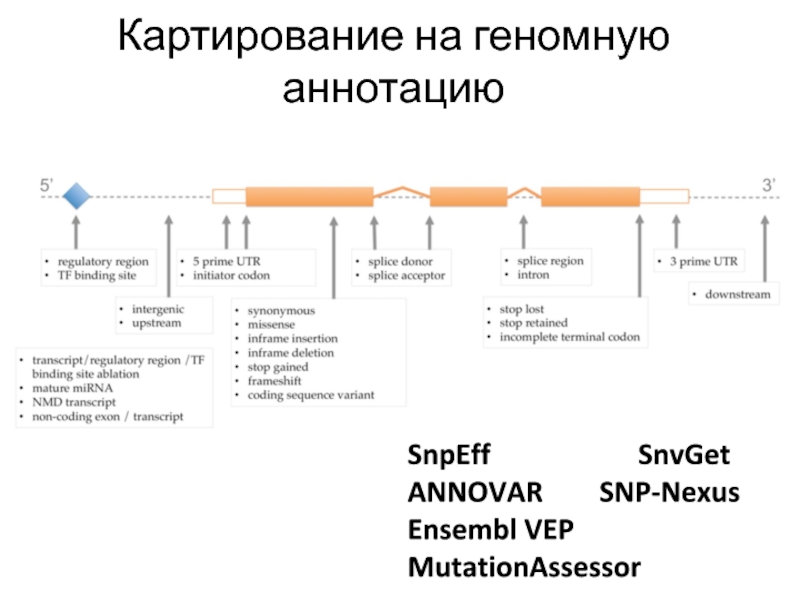
Слайд 49Картирование на геномную аннотацию
SnpEff
SnvGet
ANNOVAR SNP-Nexus
Ensembl VEP
MutationAssessor
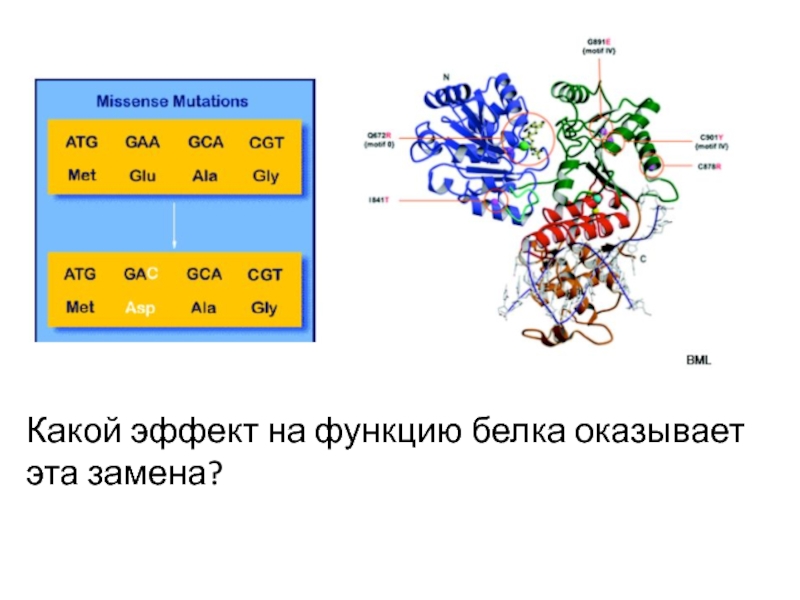
Слайд 50Какой эффект на функцию белка оказывает эта замена?
Слайд 51Предсказание функциональной значимости мутации
Не все аминокислотные замены одинаково вредны
Мутация
в консервативных участках вреднее
Признаки:
нуклеотидная/аминокислотная консервативность
Физико-химические свойства аминокислот
Методы:
Direct scoring
Machine learning
PolyPhen2, SIFT,
LRT, MutationAssessor, …
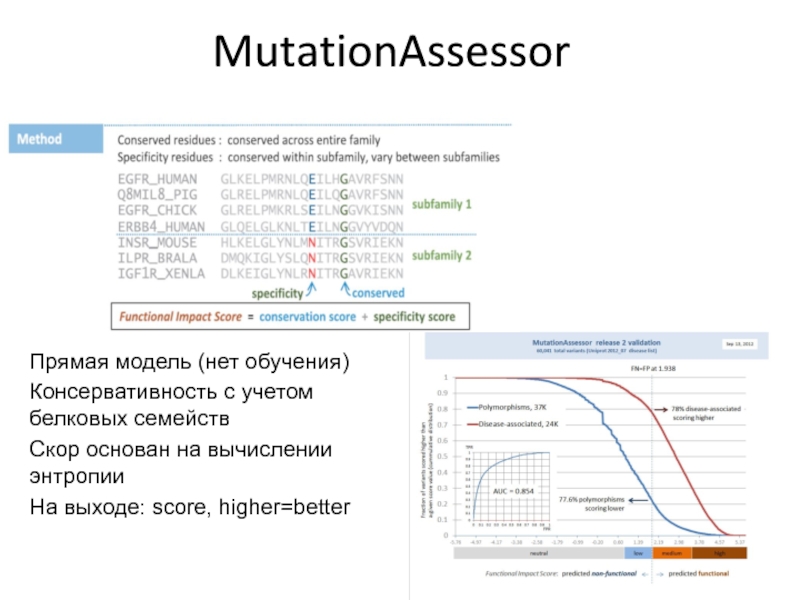
Слайд 52MutationAssessor
Прямая модель (нет обучения)
Консервативность с учетом белковых семейств
Скор основан на
вычислении энтропии
На выходe: score, higher=better
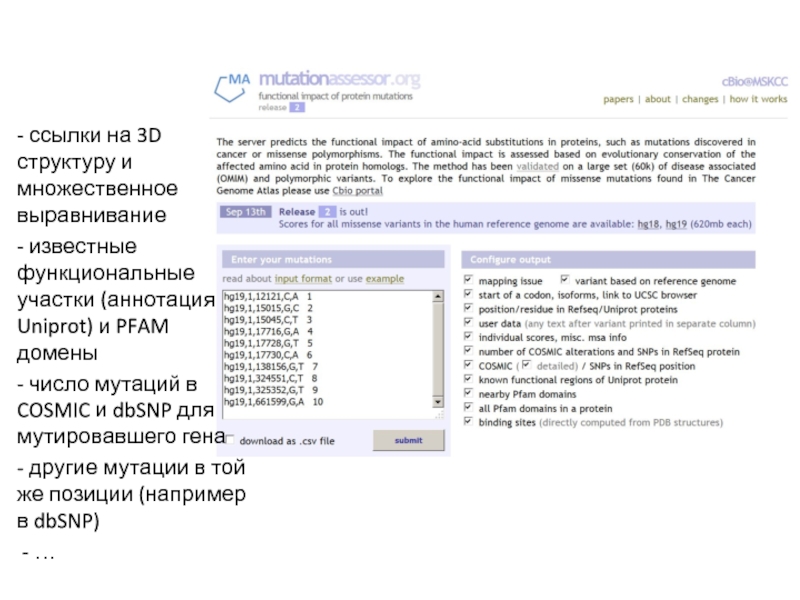
Слайд 53- ссылки на 3D структуру и множественное выравнивание
- известные функциональные
участки (аннотация Uniprot) и PFAM домены
- число мутаций в COSMIC
и dbSNP для мутировавшего гена
- другие мутации в той же позиции (например в dbSNP)
- …
Слайд 54Проблема
Методы часто дают противоречащие результаты
Что делать? Устраивать консилиум
dbNSFP, https://sites.google.com/site/jpopgen/dbNSFP
результаты 9 предсказалок + 2 интегрирующих скора
CONDEL, http://bg.upf.edu/condel/home
Интегрирует SIFT, Polyphen2, MAPP, LogR Pfam E-value и MutationAssessor.
Слайд 55Что делать с некодирующими полиморфизмами?
Составляют большинство замен при GWAS
Тоже могут
иметь функциональное значение: влияние на экспрессию
TFBS, промоторы, энхансеры, …
Сильный консерватизм
- подозрительно
Слайд 56вредность != драйверность
Некорректно использовать Polyphen2, MA, и т.д. для отбора
драйверных мутаций, но хотя бы можно удалить мутации которые вряд
ли повлияют на структуру белка
Проблема: нет хороших (больших) наборов данных для тестирования driver/passenger.
Слайд 57CHASM: предсказание драйверных мутаций
Классификация driver/passenger методом random forest
Обучающая выборка: драйверные
мутации – курированные из COSMIC, passenger – генерируются из фонового
распределения
~90 признаков (свойства аминокислотной замены, основанные на выравнивании оценки сохранения в мутированной позиции, предсказанная локальная структура в мутированной позиции и аннотации из таблицы характеристик UniProtKB).
http://www.cravat.us/
Слайд 58CRAVAT: Cancer-Related Analysis of Variants Toolkit
CHASM + SnvGet
На выходе скор
[0;1] – чем меньше, тем больше вероятность драйверности мутации
Слайд 59www.broadinstitute.org/oncotator/
Genomic Annotations
Аннотации генов, транскриптов и функциональных последствий с использованием наборов
ссылок UCSC KnownGenes hg19 и mirBase.
Общие аннотации SNP из dbSNP
(включает данные из 1, 2 и 3 исследований пилотного проекта 1000 геномов).
Protein Annotations
Сайт-специфичные аннотации белков
UniProt. Данные о лекарственных мишенях
из DrugBank. Gene Ontology.
Прогнозы воздействия на функцию
PolyPhen2.
Cancer Annotations
Аннотации наблюдаемых частот мутаций рака от COSMIC.
Аннотации опухолевых генов и мутаций из Cancer Gene Census.
Аннотации значительных областей амплификации/делеции от Tumorscape и TCGA Copy Number Portal.
Перекрывающиеся мутации Oncomap из Cancer Cell Line Encyclopedia.
Аннотации значительно мутированных генов, агрегированные из опубликованных анализов MutSig. Аннотации опухолевых генов из Familial Cancer Database.
Аннотации Human DNA Repair Gene из Wood et al.
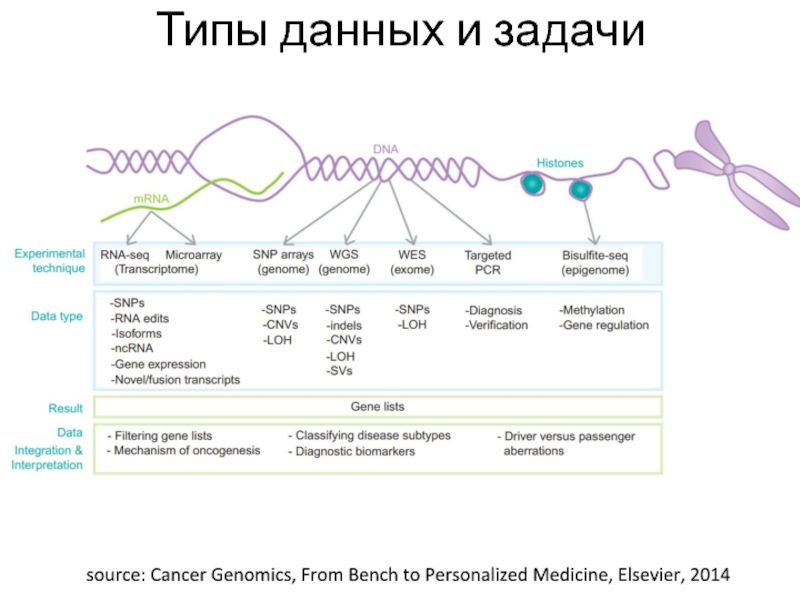
Слайд 60Типы данных и задачи
source: Cancer Genomics, From Bench to Personalized
Medicine, Elsevier, 2014
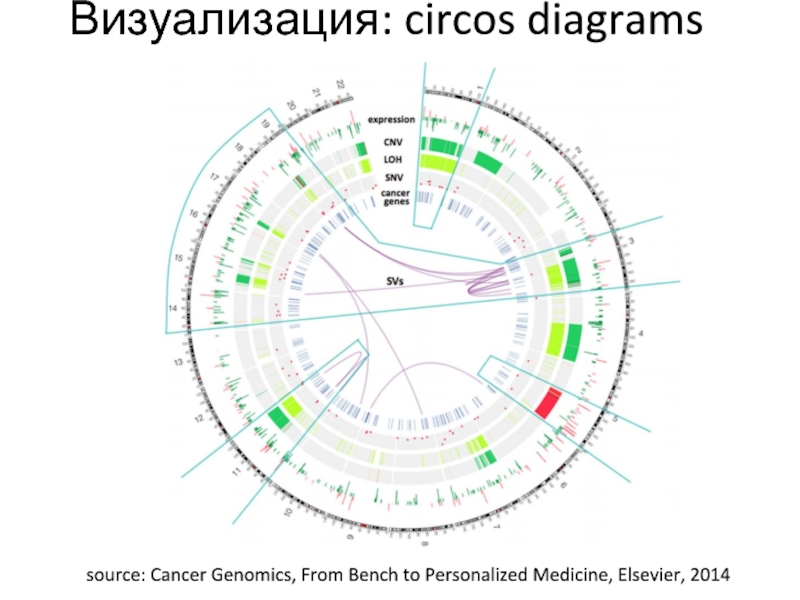
Слайд 61Визуализация: circos diagrams
source: Cancer Genomics, From Bench to Personalized Medicine,
Elsevier, 2014
Слайд 62Почему все это важно?
Потому что сможем лучше лечить!
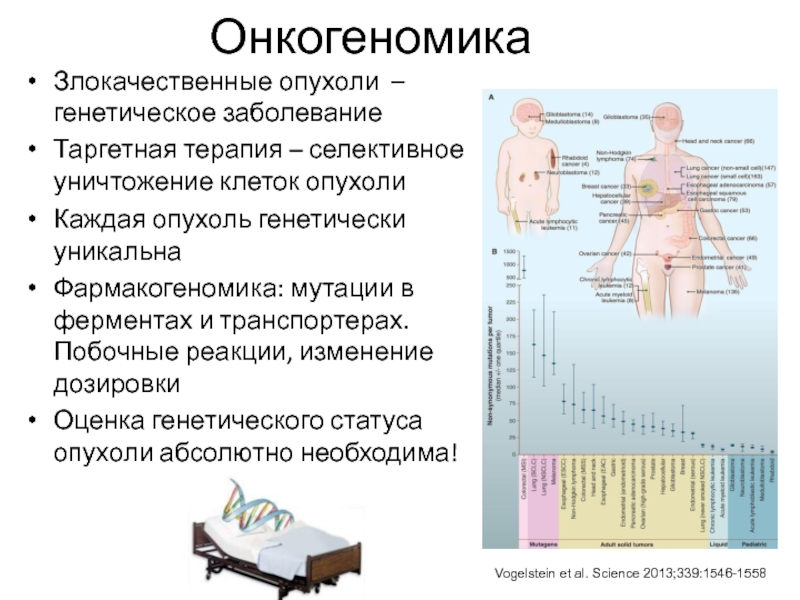
Слайд 63Онкогеномика
Злокачественные опухоли – генетическое заболевание
Таргетная терапия – селективное уничтожение клеток
опухоли
Каждая опухоль генетически уникальна
Фармакогеномика: мутации в ферментах и транспортерах. Побочные
реакции, изменение дозировки
Оценка генетического статуса опухоли абсолютно необходима!
Vogelstein et al. Science 2013;339:1546-1558
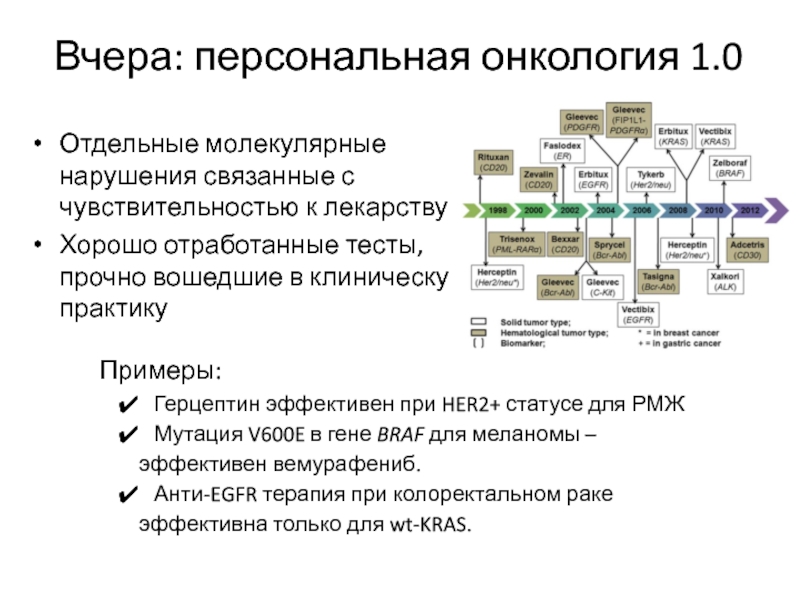
Слайд 64Вчера: персональная онкология 1.0
Отдельные молекулярные нарушения связанные с чувствительностью к
лекарству
Хорошо отработанные тесты, прочно вошедшие в клиническую практику
Примеры:
Герцептин
эффективен при HER2+ статусе для РМЖ
Мутация V600E в гене BRAF для меланомы – эффективен вемурафениб.
Анти-EGFR терапия при колоректальном раке эффективна только для wt-KRAS.
Слайд 65Клинически значимые мутации
Предсказывает чувствительность / резистентность к терапии
Влияет на
функцию ракового гена и является мишенью какого-либо лекарства.
Диагностическая или прогностическая
ценность
Влияет на особенности метаболизма или побочных эффектов лекарства (обычно генеративные мутации)
Базы данных:
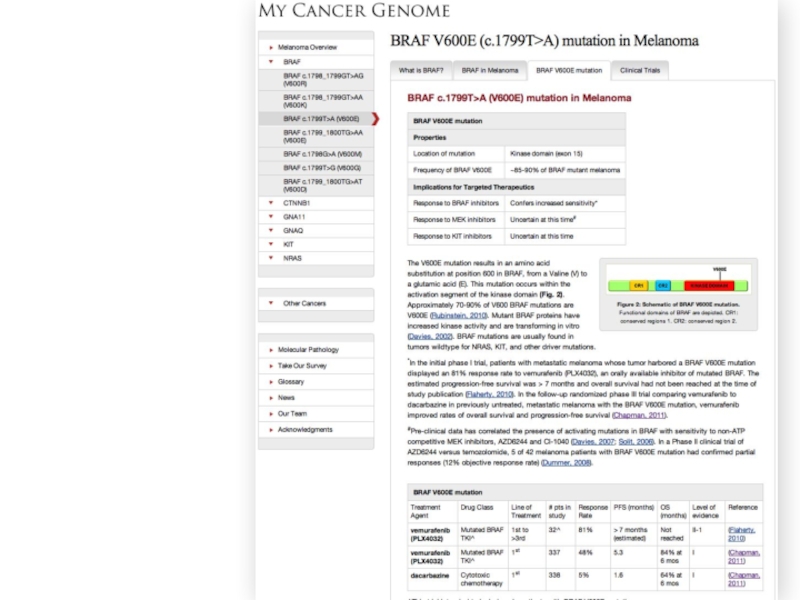
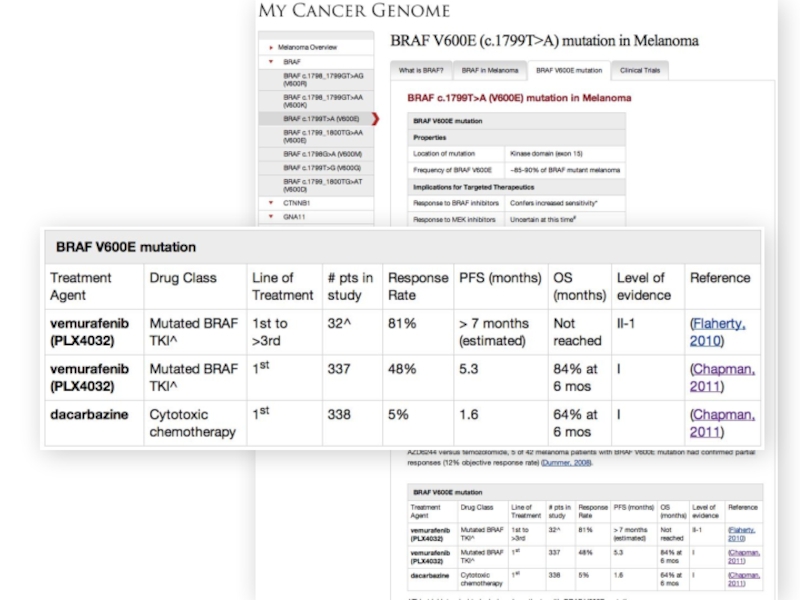
MyCancerGenome
Personalized Cancer Therapy
PGMD
PharmGKB
Критерии:
По разным оценкам: ~120 генов (разные уровни достоверности)
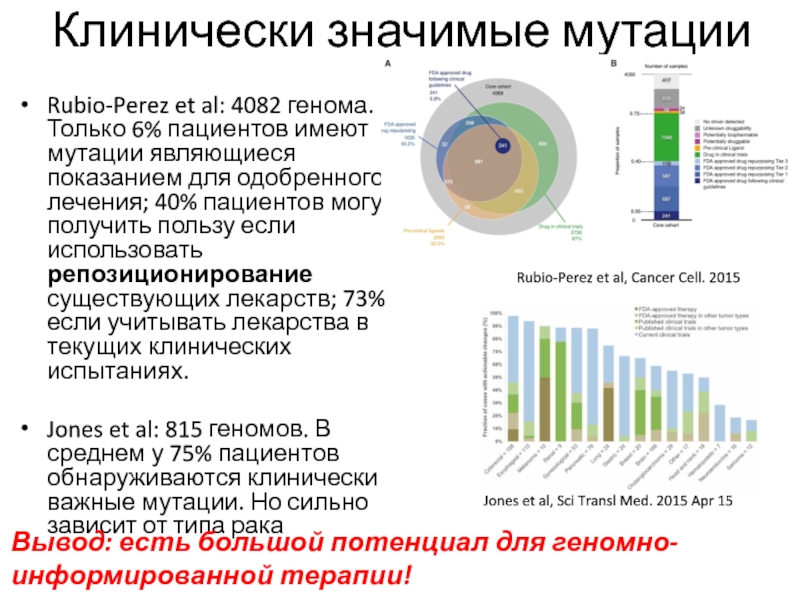
Слайд 66Rubio-Perez et al: 4082 генома. Только 6% пациентов имеют мутации
являющиеся показанием для одобренного лечения; 40% пациентов могут получить пользу
если использовать репозиционирование существующих лекарств; 73% если учитывать лекарства в текущих клинических испытаниях.
Jones et al: 815 геномов. В среднем у 75% пациентов обнаруживаются клинически важные мутации. Но сильно зависит от типа рака
Клинически значимые мутации
Jones et al, Sci Transl Med. 2015 Apr 15
Вывод: есть большой потенциал для геномно-информированной терапии!
Rubio-Perez et al, Cancer Cell. 2015
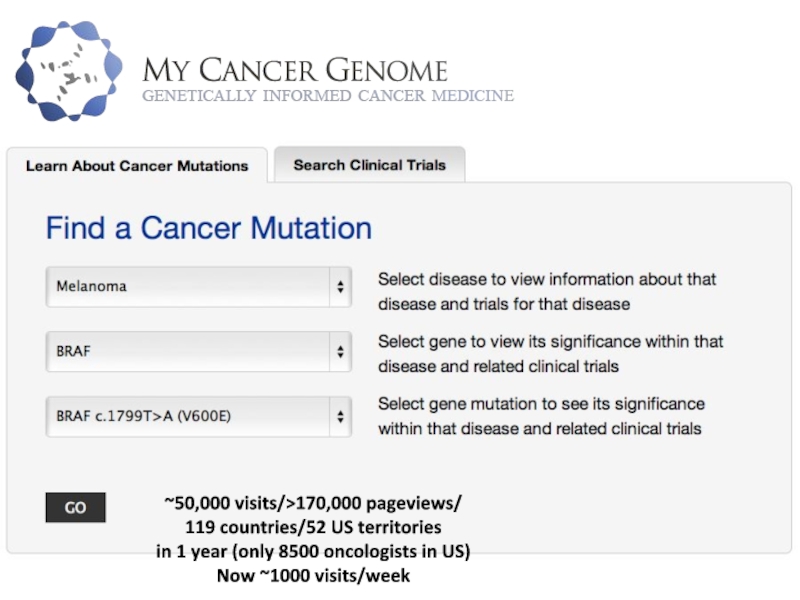
Слайд 67My cancer genome
~50,000 visits/>170,000 pageviews/
119 countries/52 US territories
in 1 year
(only 8500 oncologists in US)
Now ~1000 visits/week
Слайд 71Пример:
Секвенирование 315 ‘раковых’ генов
Отчет: список потенциально
эффективной / таргетной терапии. Включает текущие клинические испытания.
3000 тестов
за 2013 год
Сегодня: персональная онкология 2.0
Тестирование сотен генетических нарушений
Требуется спец. оборудование (часто методы NGS)
Увеличение требований к врачу (интерпретация данных)
Быстро становится стандартом
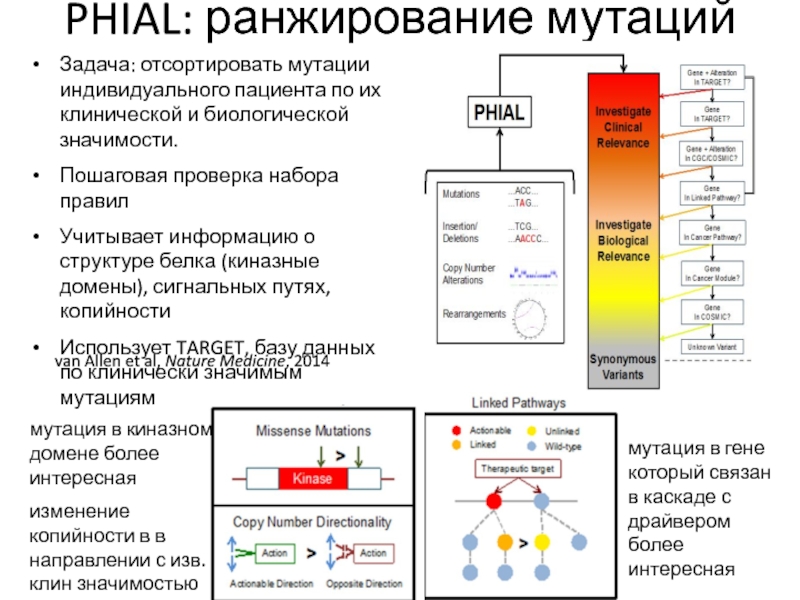
Слайд 72PHIAL: ранжирование мутаций
Задача: отсортировать мутации индивидуального пациента по их клинической
и биологической значимости.
Пошаговая проверка набора правил
Учитывает информацию о структуре белка
(киназные домены), сигнальных путях, копийности
Использует TARGET, базу данных по клинически значимым мутациям
van Allen et al, Nature Medicine, 2014
мутация в киназном домене более интересная
мутация в гене который связан в каскаде с драйвером более интересная
изменение копийности в в направлении с изв. клин значимостью
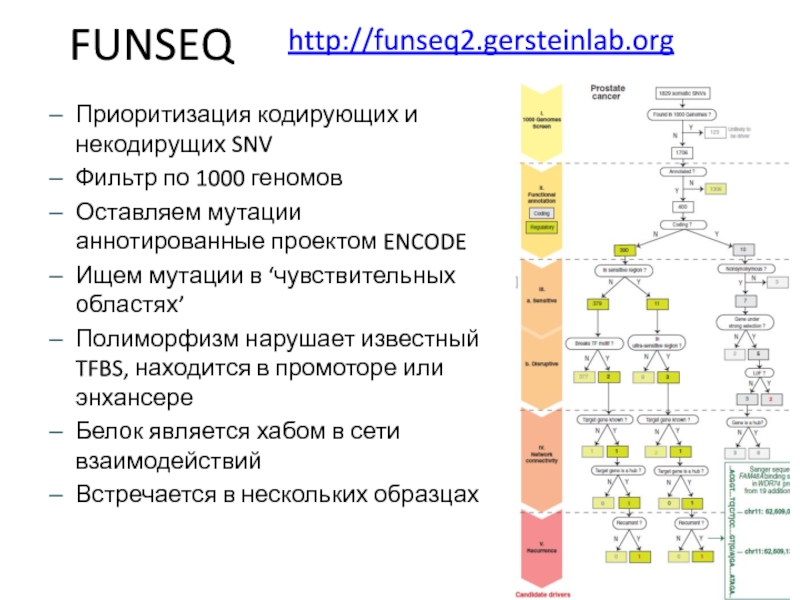
Слайд 73FUNSEQ
Приоритизация кодирующих и некодирущих SNV
Фильтр по 1000 геномов
Оставляем мутации аннотированные
проектом ENCODE
Ищем мутации в ‘чувствительных областях’
Полиморфизм нарушает известный TFBS, находится
в промоторе или энхансере
Белок является хабом в сети взаимодействий
Встречается в нескольких образцах
http://funseq2.gersteinlab.org
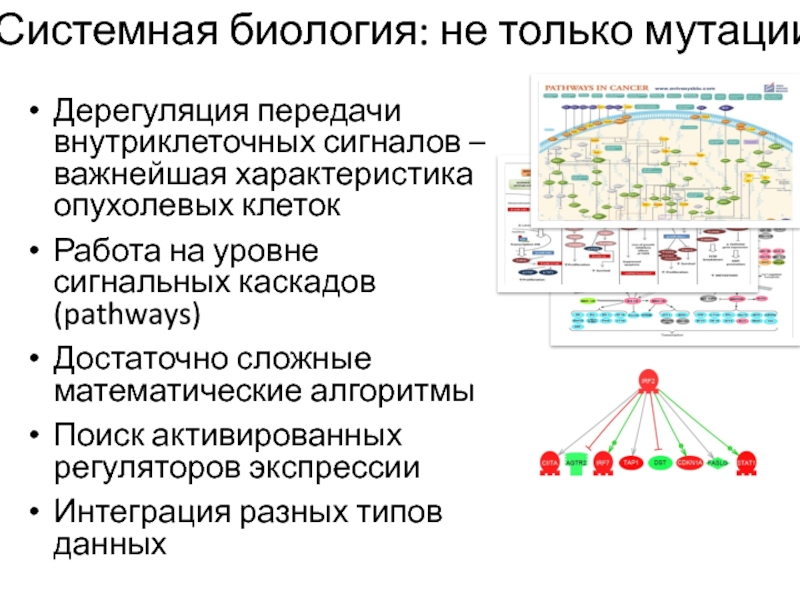
Слайд 74Системная биология: не только мутации
Дерегуляция передачи внутриклеточных сигналов –важнейшая характеристика опухолевых клеток
Работа на
уровне сигнальных каскадов (pathways)
Достаточно сложные математические алгоритмы
Поиск активированных регуляторов экспрессии
Интеграция
разных типов данных
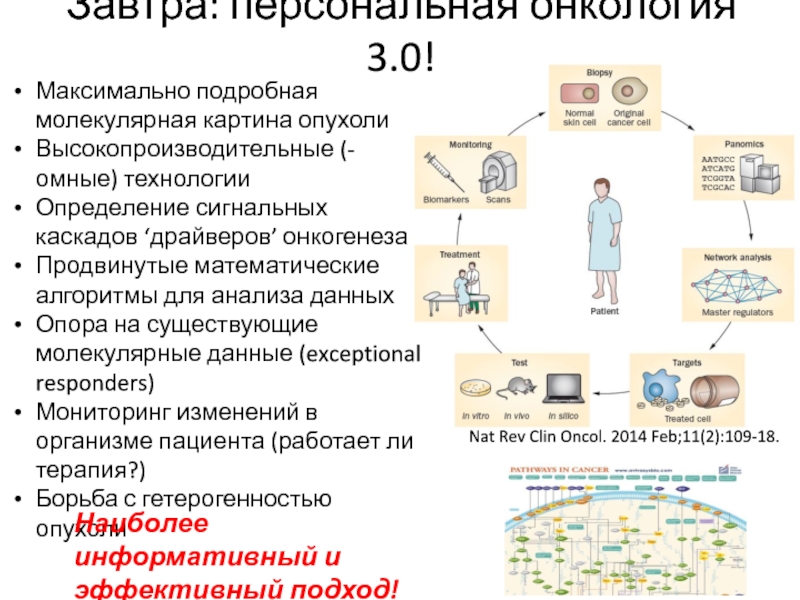
Слайд 75Nat Rev Clin Oncol. 2014 Feb;11(2):109-18.
Максимально подробная молекулярная картина опухоли
Высокопроизводительные
(-омные) технологии
Определение сигнальных каскадов ‘драйверов’ онкогенеза
Продвинутые математические алгоритмы для
анализа данных
Опора на существующие молекулярные данные (exceptional responders)
Мониторинг изменений в организме пациента (работает ли терапия?)
Борьба с гетерогенностью опухоли
Завтра: персональная онкология 3.0!
Наиболее информативный и эффективный подход!
Слайд 76Узкое место – анализ результатов
Good et al, Genome Biol. 2014;
15(8): 438.
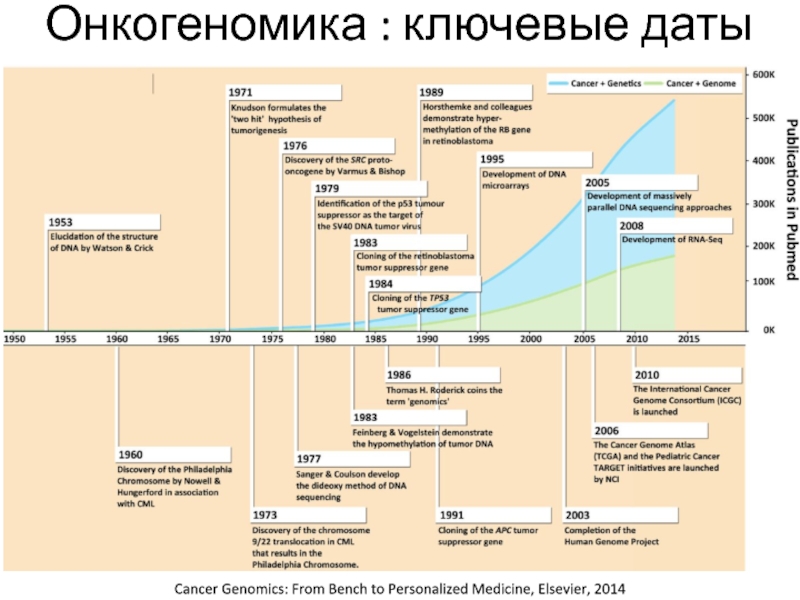
Слайд 77Cancer Genomics: From Bench to Personalized Medicine, Elsevier, 2014
Онкогеномика :
ключевые даты
Слайд 78Kotelnikova et al, Oncotarget, 2016
Более 30 компаний специализирующихся на онкогеномике
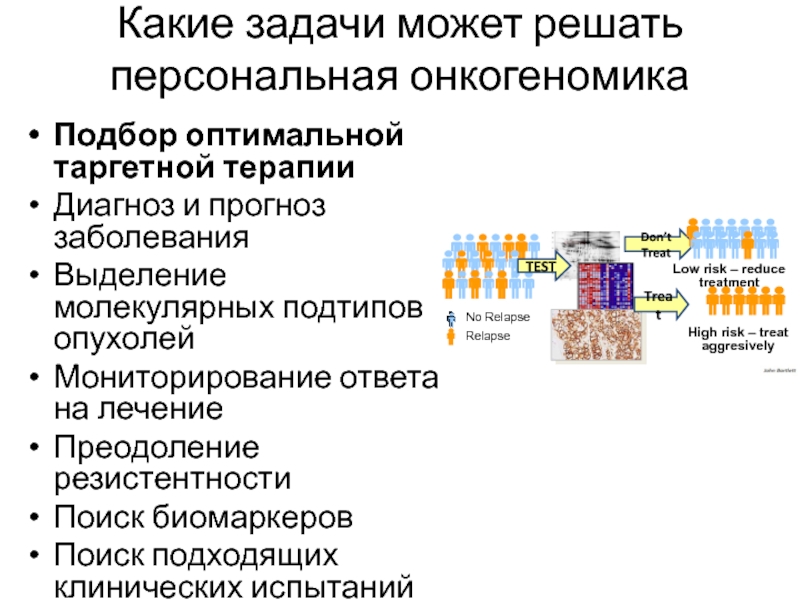
Слайд 79Какие задачи может решать персональная онкогеномика
Подбор оптимальной таргетной терапии
Диагноз и
прогноз заболевания
Выделение молекулярных подтипов опухолей
Мониторирование ответа на лечение
Преодоление резистентности
Поиск
биомаркеров
Поиск подходящих клинических испытаний
Слайд 80Некоторые проблемы и трудности
Гетерогенность опухолей, борьба с эволюцией
Малое количество лекарств
и мишеней
Стоимость
Разнообразие данных: мутации, экспрессия, CNV, fusions, сплайсинг.
Множество технологий, баз
данных, программного обеспечения. Ни на каком шаге нет общепризнанного стандарта.
Очень высокие требования к экспертам
…
Слайд 81Геном злокачественной опухоли: summary
Более 85% злокачественных опухолей являются вновь приобретенными
(не наследственными).
Мутации генома являются движущей силой канцерогенеза.
Геном каждой опухоли обладает
существенной индивидуальностью в плане локализации и количества мутаций.
Персональное исследование мутаций в будущем определит стратегию лечения: таргетные лекарственные средства против онкогенов. Ведущую роль будут играть методы NGS.
Слайд 82“There is no longer a question of whether cancer genome
sequencing should or can be done. It is a question
of who should do it, on whom, at what time points, on which specimens and with what tools.”
Вопроса “проводить ли секвенирование генома раковой опухоли” уже нет. Вопрос в том, кто должен это делать, в каких случаях, в какое время, на каких образцах и какими методами.
Laskin et al, Cold Spring Harb Mol Case Stud, 2015























![Геномика рака CRAVAT: Cancer-Related Analysis of Variants ToolkitCHASM + SnvGetНа выходе скор [0;1] CRAVAT: Cancer-Related Analysis of Variants ToolkitCHASM + SnvGetНа выходе скор [0;1] – чем меньше, тем больше вероятность](/img/thumbs/bb44a868289fe7c98c39d38291d53447-800x.jpg)