Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ГЛАВА II. МОЛЕКУЛЯРНАЯ ФИЗИКА И ТЕРМОДИНАМИКА § 2. Идеальный газ
Содержание
- 1. ГЛАВА II. МОЛЕКУЛЯРНАЯ ФИЗИКА И ТЕРМОДИНАМИКА § 2. Идеальный газ
- 2. I. Модель идеального газаИдеальный газ — коллектив
- 3. §2. Идеальный газII. Уравнение состояния идеального газа.
- 4. §2. Идеальный газ— постоянная БольцманаКонцентрация молекул —
- 5. III. Основное уравнение МКТРассмотрим равновесный идеальный газ,
- 6. 2. Число ударов о стенку за время
- 7. 4. Учёт давления всех скоростных групп молекулЗакон
- 8. IV. Молекулярно-кинетический смысл абсолютной температурыАбсолютная температура пропорциональна
- 9. Скачать презентанцию
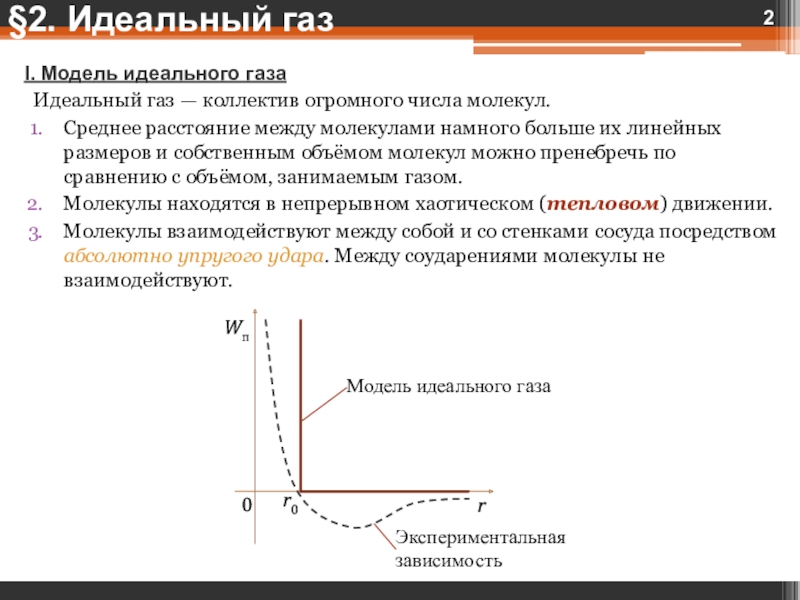
I. Модель идеального газаИдеальный газ — коллектив огромного числа молекул.Среднее расстояние между молекулами намного больше их линейных размеров и собственным объёмом молекул можно пренебречь по сравнению с объёмом, занимаемым газом.Молекулы находятся
Слайды и текст этой презентации
Слайд 2I. Модель идеального газа
Идеальный газ — коллектив огромного числа молекул.
Среднее
расстояние между молекулами намного больше их линейных размеров и собственным
объёмом молекул можно пренебречь по сравнению с объёмом, занимаемым газом.Молекулы находятся в непрерывном хаотическом (тепловом) движении.
Молекулы взаимодействуют между собой и со стенками сосуда посредством абсолютно упругого удара. Между соударениями молекулы не взаимодействуют.
§2. Идеальный газ
Слайд 3§2. Идеальный газ
II. Уравнение состояния идеального газа. Газовые законы
Уравнение состояния
идеального газа:
Частные случаи (газовые законы):
T = const: — закон Бойля-Мариотта
p = const: — закон Гей-Люссака
V = const: — закон
Шарля— уравнение Менделеева-Клапейрона
— универсальная газовая постоянная
Слайд 4§2. Идеальный газ
— постоянная Больцмана
Концентрация молекул — ФВ — характеристика
макросистемы, равная числу частиц в единичном объёме:
Закон Дальтона: давление смеси
газов равно сумме парциальных давлений компонент смеси:Доказательство
Нормальные условия: p0 = 1,01·105 Па; T0 = 273 К
Слайд 5III. Основное уравнение МКТ
Рассмотрим равновесный идеальный газ, состоящий из одинаковых
молекул массой m0. Все молекулы имеют разные по модулю и
направлению скорости. Давление газа обусловлено ударами молекул о стенку сосуда.1. Удар одной молекулы
Удар молекулы о стенку — абсолютно упругий.
II закон Ньютона:
— сила, с которой стенка действует на молекулу
τ — время удара
III закон Ньютона:
§2. Идеальный газ
Слайд 62. Число ударов о стенку за время Δt >> τ
i-я
скоростная группа молекул: v = (vi, vi ± Δv)
Число молекул внутри цилиндра, которые долетят
до стенки за время Δt:ni — концентрация молекул i-ой скоростной группы
Коэффициент 1/6 из всех молекул 1/3 движется вдоль оси x, из них ½ движется в направлении стенки.
3. Импульс, полученный стенкой от молекул i-ой скоростной группы за время Δt
Fi — модуль суммарной силы, с которой молекулы i-ой скоростной группы действуют на участок стенки площадью ΔS
Давление молекул i-ой скоростной группы
§2. Идеальный газ
Слайд 74. Учёт давления всех скоростных групп молекул
Закон Дальтона:
— средняя квадратичная
скорость молекулы идеального газа
— основное уравнение МКТ идеального газа
— основное
уравнение МКТ идеального газа для энергии— средняя кинетическая энергия поступательного движения молекулы идеального газа
§2. Идеальный газ
Слайд 8IV. Молекулярно-кинетический смысл абсолютной температуры
Абсолютная температура пропорциональна средней кинетической энергии
поступательного движения, приходящейся на 1 молекулу.
Энергетическая температура:
Численная оценка
При t = 27°C (T = 300 К)
для кислорода (µ = 3,2·10–2 кг/моль):θ = 4,2·10–21 Дж
§2. Идеальный газ