Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Государственное бюджетное образовательное учреждение высшего профессионального
Содержание
- 1. Государственное бюджетное образовательное учреждение высшего профессионального
- 2. « Первичный и вторичный гуморальный иммунный ответ.
- 3. Вопросы Фазы иммунного ответа.Типы иммунного ответа и
- 4. Структура и функции иммуноглобулинов
- 5. Рецепторы к антигенам на поверхности В клетки:Позволяют
- 6. Иммуноглобулины являются бифункциональными протеинамиИммуноглобулины взаимодействуют лишь с
- 7. Сохранение структуры и возможность к изменениям
- 8. Гены, кодирующие Ig доменыХотя первыми были открыты
- 9. Домены –компактно уложенные структуры, устойчивые к действию
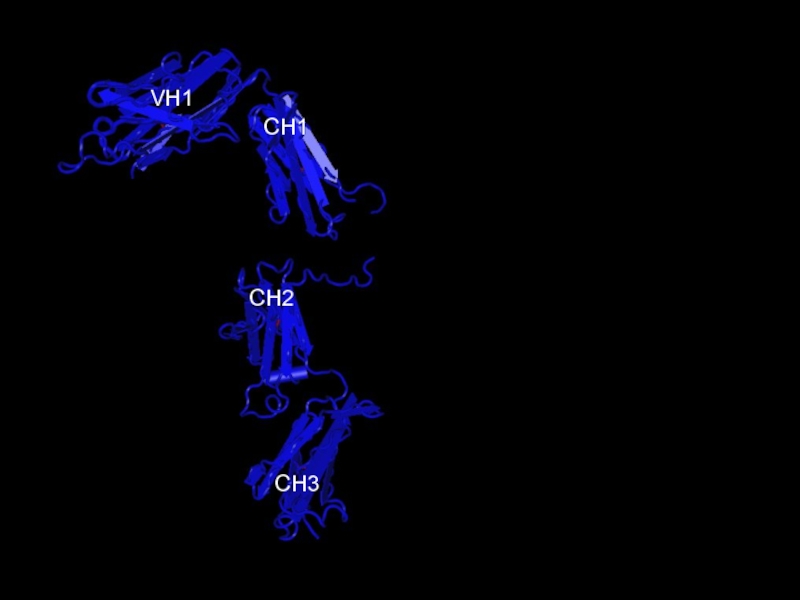
- 10. CH3
- 11. CH3CH2
- 12. CH3CH2CH1
- 13. CH3CH2CH1VH1
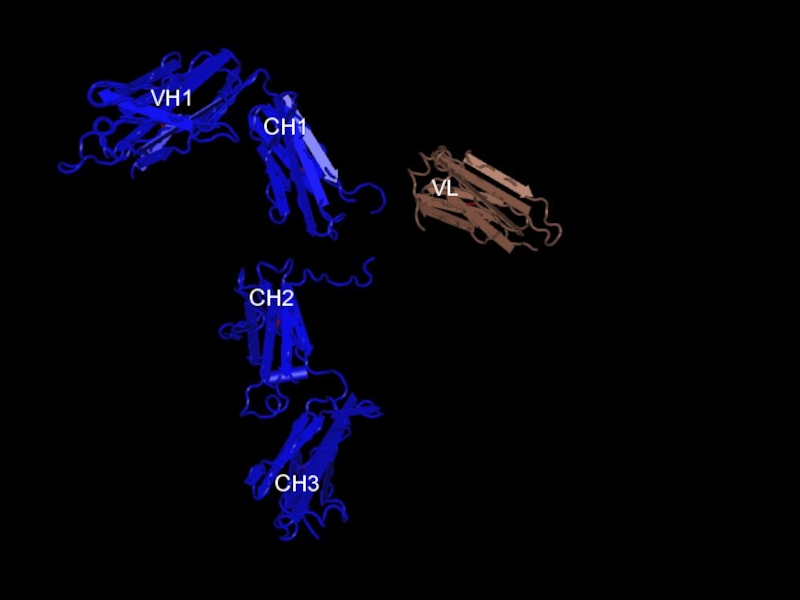
- 14. CH3CH2CH1VH1VL
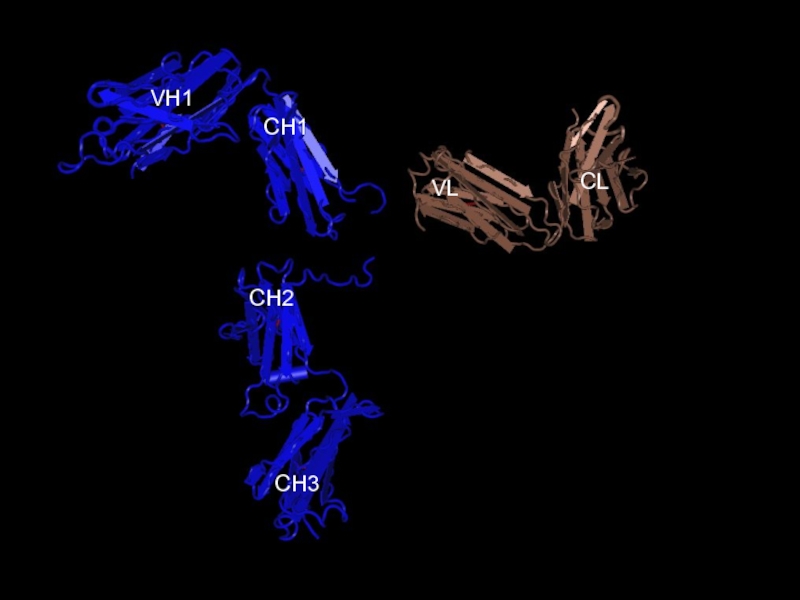
- 15. CH3CH2CH1VH1CLVL
- 16. CH3CH2CH1VH1CLVL
- 17. CH3CH2CH1VH1VLCL
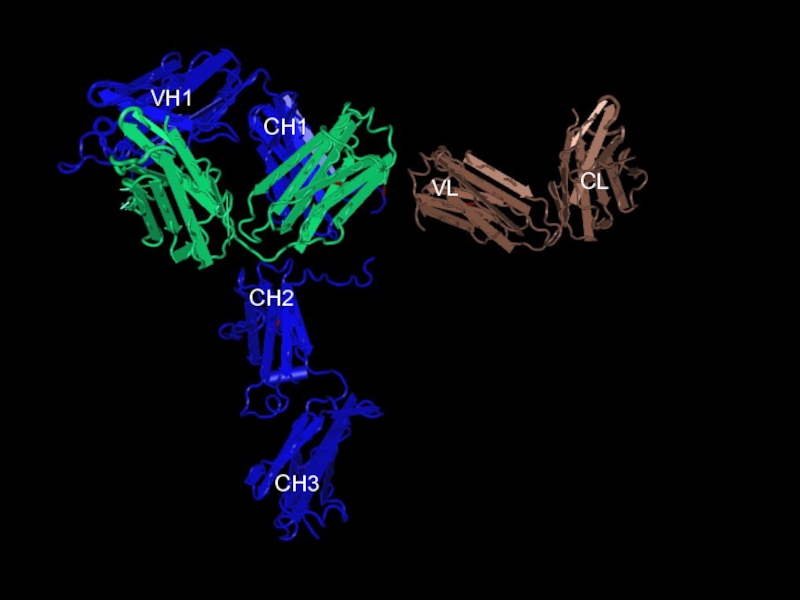
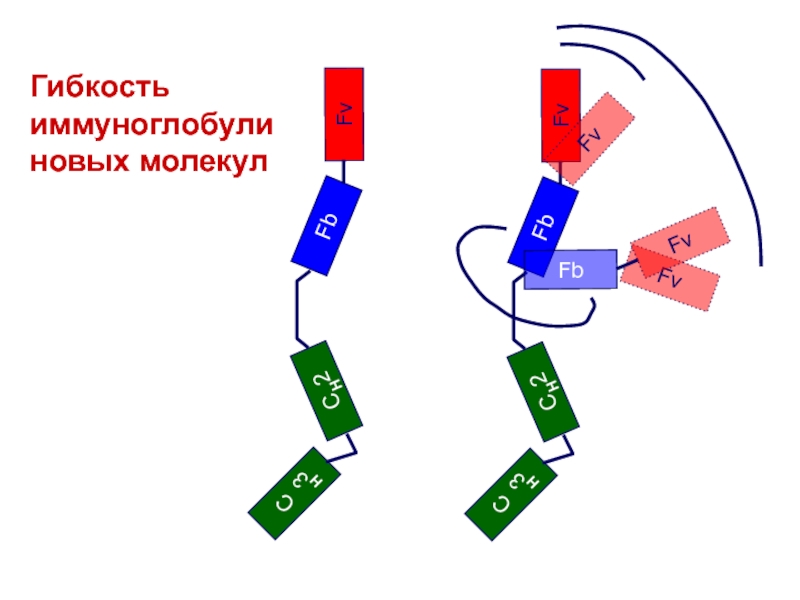
- 18. FvГибкость иммуноглобулиновых молекул
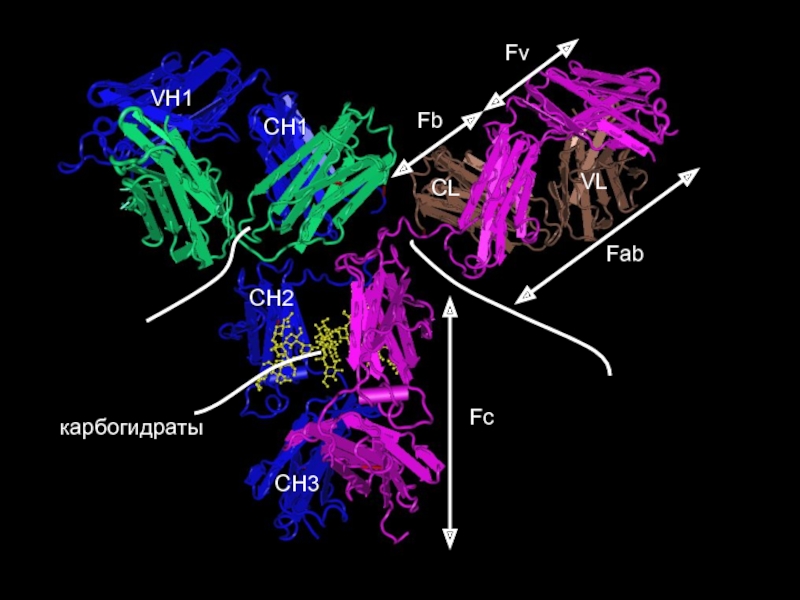
- 19. FvFbFabCH3CH2CH1VH1VLCLFcкарбогидраты
- 20. View structures
- 21. View structures
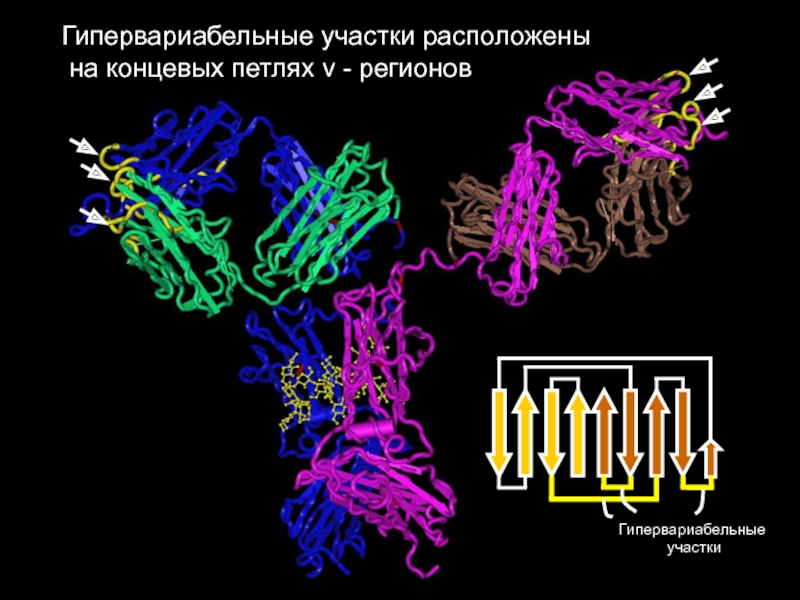
- 22. Гипервариабельные участки расположены на концевых петлях v - регионов
- 23. модель (Fab)2, расположение гипервариабельных участков Легкая цепь зеленые и коричневыеТяжелая цепь фиолетовые и голубыеГипервариабельные зоны желтые
- 24. Антигены различаются размером и структурой
- 25. Антитела взаимодействуют с антигенами разными способамиАнтиген покружается в «карман» антителаАг взаимодействует с выступающей поверхностью петли АТ
- 26. Слайд 26
- 27. Слайд 27
- 28. Слайд 28
- 29. Нековалентные взаимодействия между антителами и антигенамиЭлектростатические силы
- 30. функции (Fab – antigen binding) фрагментов в
- 31. Структура и функции Fc фрагментаСтруктура Fc общая
- 32. Мономерный IgMНа поверхности в клетки IgM существует
- 33. МУЛЬТИМЕРИЗАЦИЯ IgM1. 2 мономера IgM (показаны только Fc)2.
- 34. Изменения конформации молекулы IgM, вызванные антигеном
- 35. IgMТяжелая цепь: m - MюВремя полужизни: 5 -
- 36. IgDIgD ко-экспрессируется вместе с IgM на В
- 37. IgA - димеризация и секреция IgA –основной
- 38. секреторный IgA и трансцитозкомплекс pIgR разрушается, освобождается IgA с частью pIgR - секреторным компонентом
- 39. IgAТяжелые цепи: a1 или a2 - альфа 1
- 40. IgEIgE появился позже в эволюции в связи
- 41. высокоаффинные IgE рецепторы (FceRI)IgE - FceRI взаимодействия
- 42. IgGТяжелые цепи: g 1 g 2 g3 g4
- 43. Слайд 43
- 44. Fcg рецепторыРецептор тип клеток эффекты связыванияFcgRI мф, нф, эо,
- 45. Различия в аминокислотной последовательности молекул антител1. Изотипические
- 46. Методы определения В-лимфоцитов в клинической практике
- 47. Методы определения антител в клинической практике
- 48. Понятия аффинности и авидности антител. Эпитоп –наименьшая
- 49. Контроль аффинитета связи АГ с АТТолько эта
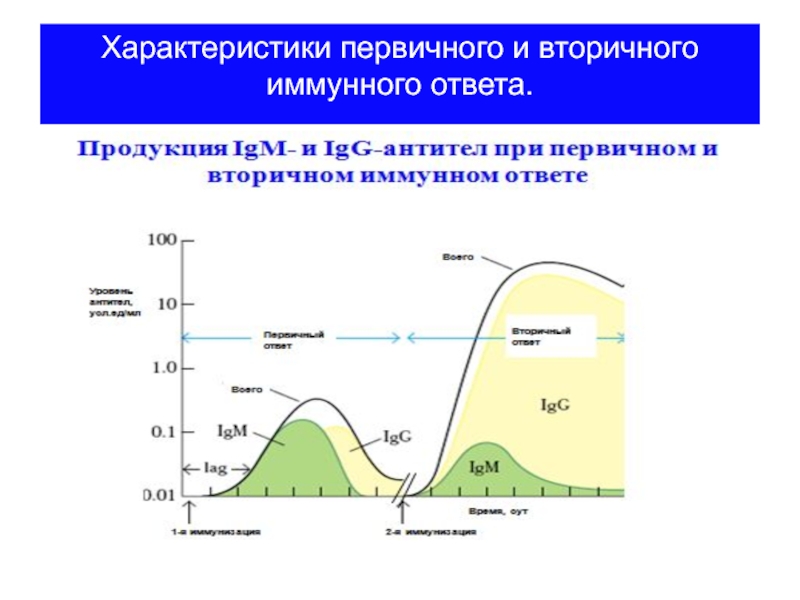
- 50. Характеристики первичного и вторичного иммунного ответа.
- 51. Сравнительная характеристика первичного и вторичного иммунного ответа
- 52. Серопрофилактика и серотерапия в клинической практике. Экстренная
- 53. Серопрофилактика и серотерапия в клинической практике. Нормальные
- 54. Пассивная иммунизация генно-инженерным препаратом паливизумабЗащита недоношенных детей:
- 55. 1. 14 мая 1796 года Дженнер в присутствии врачей
- 56. Луи ПастерИдеи Дженнера почти через 100 лет
- 57. Хронология создания вакцин: оспа;бешенство; чума; холера;
- 58. Вакцинация от гепатита В. Всего в
- 59. Карта распространения разных штаммов вируса гриппа в
- 60. Активная иммунотерапия (Иммунопрофилактика)Иммунопрофилактика – комплекс мер по
- 61. Классификация вакцин. Инактивированные вакцины :Конъюгированные вакцины (антиген
- 62. Классификация вакцин. 5.Вакцины на основе поверхностных антигенов
- 63. Классификация вакцин. По количеству видов антигенов вакцины
- 64. Дополнительные составляющие вакцин. Кроме антигенов в состав
- 65. Иммунологические механизмы вакцинации. После первого введения вакцины
- 66. Применение вакцин в клинической практике. Методы вакцинации:Парентеральный
- 67. Применение вакцин в клинической практике. Врачи в
- 68. Применение вакцин в клинической практике: принципы вакцинопрофилактики
- 69. Критерии эффективности вакцинЭффективная вакцина способна:Активировать антигенпрезентирующие клетки.Активировать
- 70. ВопросыДвойственная роль В-лимфоцита в гуморальном иммунном ответе
- 71. Тестовые вопросыИммуноглобулины - это:Сигнальные межклеточные молекулыМолекулы главного
- 72. Тестовые вопросыВ1-лимфоциты:Секретируют в основном IgMЯвляются CD5+ лимфоцитамиЯвляются
- 73. Тестовые вопросыДля идентификации В-лимфоцитов в клинической практике
- 74. Тестовые вопросыВ результате гипермутации (соматического гипермутагенеза) при
- 75. Тестовые вопросыОсновными иммуноглобулинами вторичного ответа являются: IgAIgGIgMIgEIgD
- 76. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1 Государственное бюджетное образовательное учреждение высшего профессионального образования «ПЕРВЫЙ САНКТ-ПЕТЕРБУРГСКИЙ ГОСУДАРСТВЕННЫЙ
МЕДИЦИНСКИЙ УНИВЕРСИТЕТ имени академика И.П. Павлова» МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ Российской федерАции
иммунологииСлайд 2« Первичный и вторичный гуморальный иммунный ответ. Переключение изотипов антител.
Клетки памяти. Аффинность и авидность антител. Механизмы действия вакцин. Клинические
примеры».Практическое занятие № 8
Слайд 3Вопросы
Фазы иммунного ответа.
Типы иммунного ответа и факторы, их определяющие.
В-лимфоцит
как антигенпредставляющая клетка.
Взаимодействие В-лимфоцита и Т-лимфоцита-хелпера.
Активация и пролиферация В-лимфоцитов.
Дифференцировка В-лимфоцитов
в плазматические клетки и клетки памяти.Общая характеристика и строение молекулы иммуноглобулина.
Слайд 5Рецепторы к антигенам на поверхности В клетки:
Позволяют В клеткам «чувствовать»
их антигенное микроокружение
Связывают внеклеточное пространство с механизмами внутриклеточного сигналлинга
СЕКРЕТИРУЕМЫЕ АНТИТЕЛА
– функции:нейтрализация
привлечение эффекторных клеток
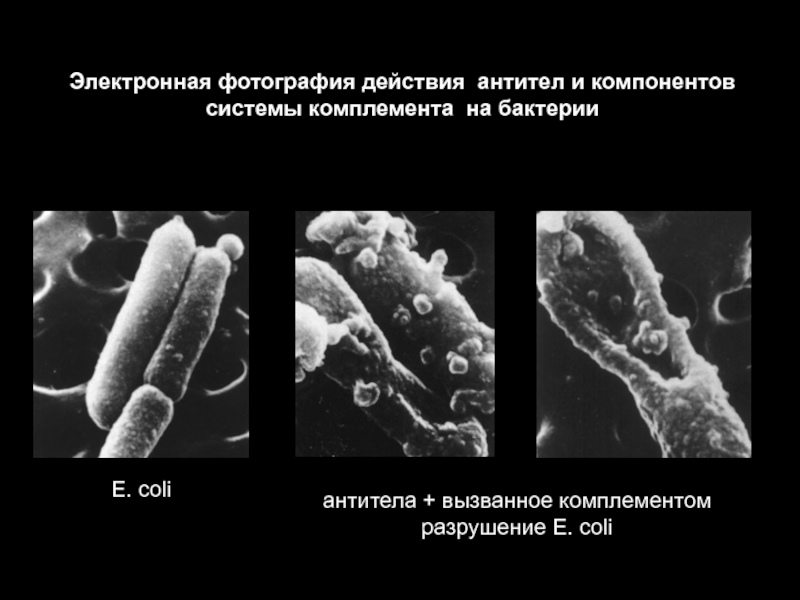
фиксация комплемента
Иммуноглобулины: структурно – функциональные взаимоотношения
Слайд 6Иммуноглобулины являются бифункциональными протеинами
Иммуноглобулины взаимодействуют лишь с небольшим числом специализированных
молекул -
Fc рецепторами на поверхности клеток
компонентами системы комплемента
внутриклеточными сигнальными молекулами
Распознают
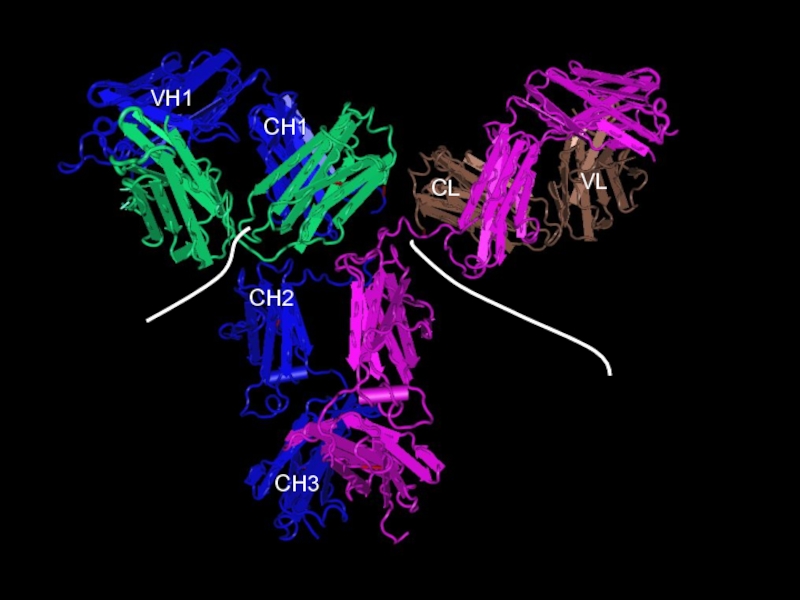
определенные антигенные детерминантыСлайд 7Сохранение структуры и возможность к изменениям в каждой молекуле
иммуноглобулина обеспечивают глобулярные структуры - ДОМЕНЫ
Легкая цепь молекулы Ig (212
остатков аминокислот) стереотипно сворачивается, формируя 2 домена – вариабельный и константный.Тяжелая цепь молекулы IgG, A и D (450 остатков аминокислот) стереотипно сворачивается, формируя 4 домена –1 вариабельный и 3 константных.
Антигенсвязывающие центры (Fab)2 молекул образованы вариабельными доменами легких и тяжелых цепей - VL и VH.
Иммуноглобулиновые домены
Слайд 8Гены, кодирующие Ig домены
Хотя первыми были открыты иммуноглобулины, позже было
обнаружено целое суперсемейство молекул, кодируемых этими генами. Среди таких молекул
-молекулы межклеточных взаимодействий и молекулы распознающих систем.Суперсемейство генов Ig обнаружено во многих клетках организма.
Суперсемейство генов Ig
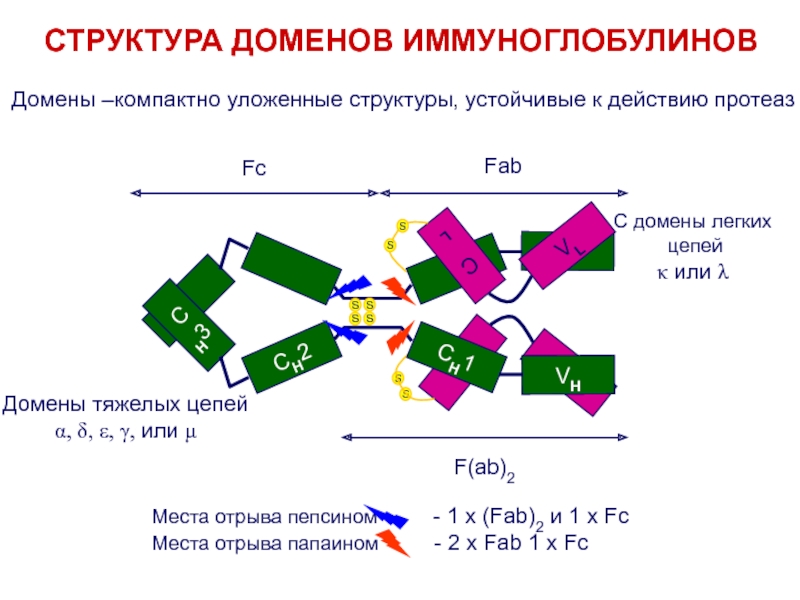
Слайд 9Домены –компактно уложенные структуры, устойчивые к действию протеаз
СТРУКТУРА ДОМЕНОВ ИММУНОГЛОБУЛИНОВ
С
домены легких
цепей
k или l
Домены тяжелых цепей
a, d, e, g,
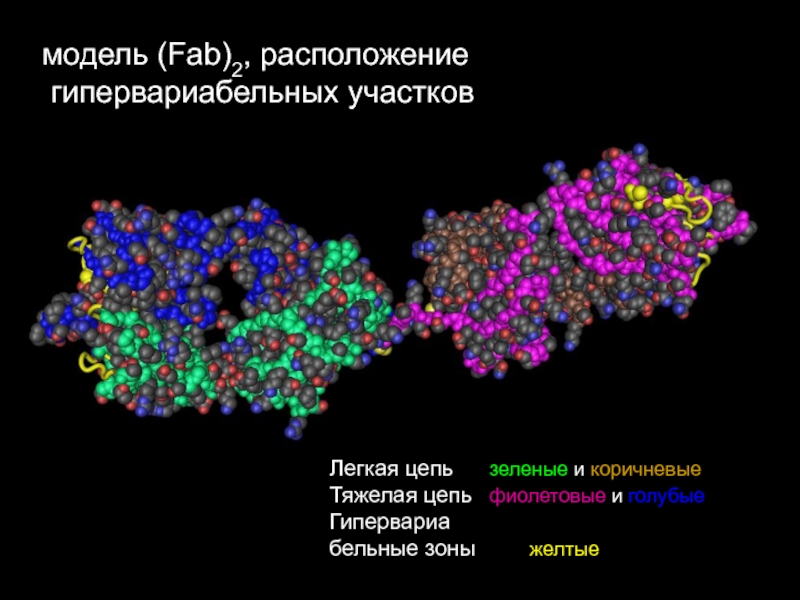
или mСлайд 23модель (Fab)2, расположение
гипервариабельных участков
Легкая цепь зеленые и коричневые
Тяжелая цепь фиолетовые
и голубые
Гипервариа
бельные зоны желтые
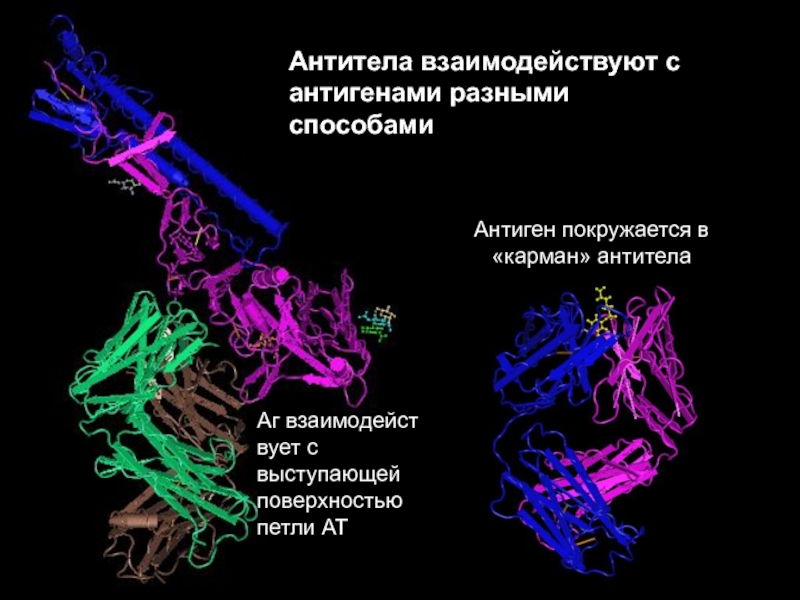
Слайд 25Антитела взаимодействуют с антигенами разными способами
Антиген покружается в «карман» антитела
Аг
взаимодейст
вует с выступающей поверхностью петли АТ
Слайд 29Нековалентные взаимодействия между
антителами и антигенами
Электростатические силы притяжение противоположно заряженных
структур
Водородные мостики водородные «сшивки»
Силы Ван дер Ваальса слабые электоростатические взаимодействия
Гидрофобные
силы гидрофобные группы собираются вместе, для исключения водыСлайд 30функции (Fab – antigen binding) фрагментов в молекулах Ig
Распознавать антиген
Преципитировать
антиген
Блокировать активные сайты токсинов
или патоген - ассоциированных молекул
Блокировать взаимодействие
между организмом –хозяиноми чужеродными молекулами
(Fab)2 фрагмент способен:
Воспаление и эффекторные функции клеток
Воспаление и эффекторные функции комплемента
Запускать процессинг антигенов
Но (Fab)2 не может активировать:
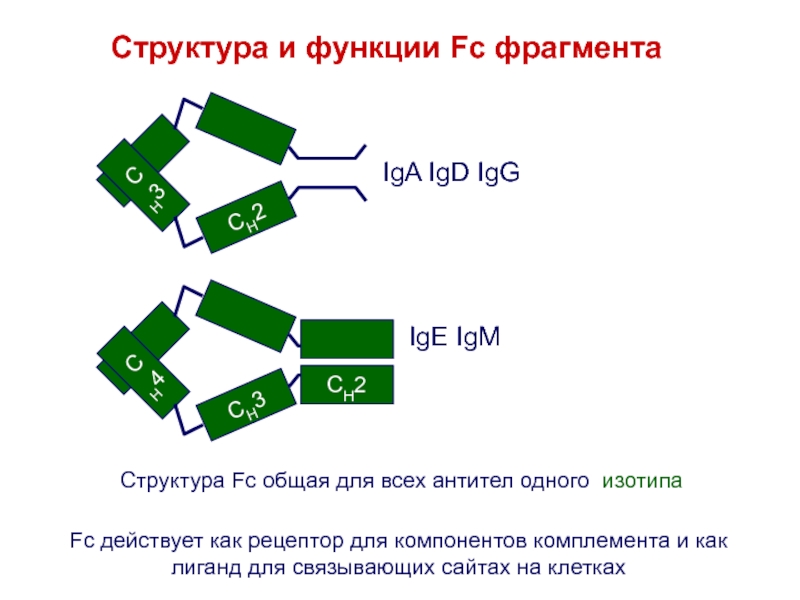
Слайд 31Структура и функции Fc фрагмента
Структура Fc общая для всех антител
одного изотипа
Fc действует как рецептор для компонентов комплемента и как
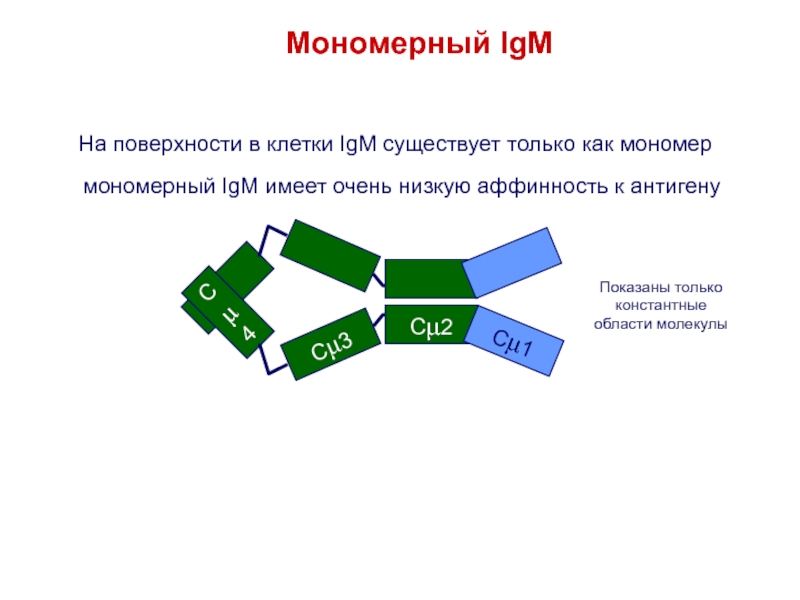
лиганд для связывающих сайтах на клеткахСлайд 32Мономерный IgM
На поверхности в клетки IgM существует только как мономер
мономерный
IgM имеет очень низкую аффинность к антигену
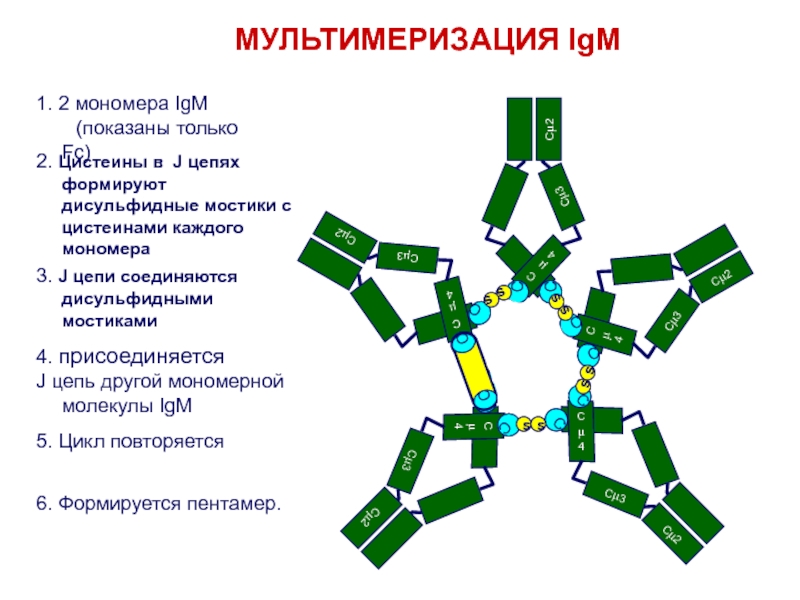
Слайд 33МУЛЬТИМЕРИЗАЦИЯ IgM
1. 2 мономера IgM
(показаны только Fc)
2. Цистеины в J
цепях формируют дисульфидные мостики с цистеинами каждого мономера
3. J цепи
соединяются дисульфидными мостиками4. присоединяется
J цепь другой мономерной молекулы IgM
5. Цикл повторяется
6. Формируется пентамер.
Слайд 35IgM
Тяжелая цепь: m - Mю
Время полужизни: 5 - 10 дней
% от
Ig сыворотки: 10
Уровень в ыворотке 0.25 - 3.1 ( мг мл-1):
Активация комплемента: ++++ классический путь
Взаимодействие с клетками: фагоцитоз через C3b рецепторы эпителиальные клетки = полимерный IgR
Перенос через плаценту : нет
Аффинниость к Аг: мономерный IgM –– валентность = 2 пентамерный IgM - валентность = 10
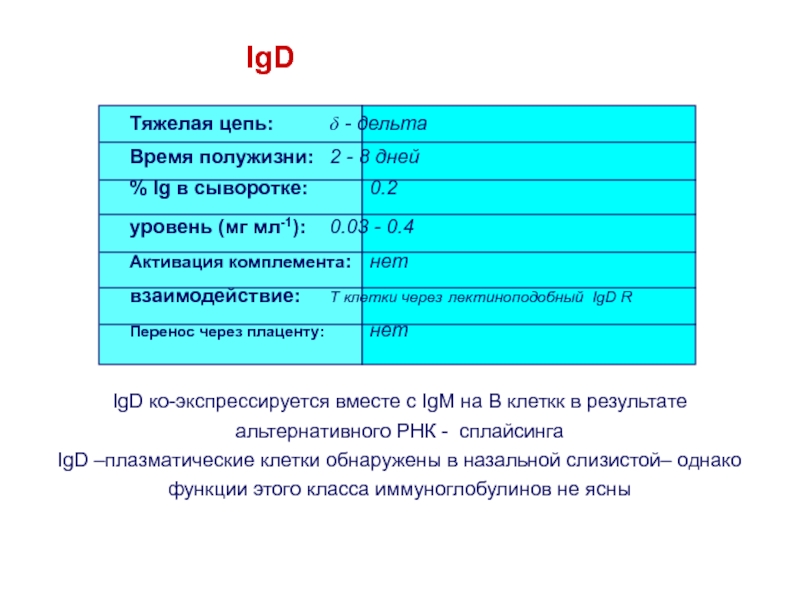
Слайд 36IgD
IgD ко-экспрессируется вместе с IgM на В клеткк в результате
альтернативного РНК - сплайсинга
IgD –плазматические клетки обнаружены в назальной слизистой–
однако функции этого класса иммуноглобулинов не ясныТяжелая цепь: d - дельта
Время полужизни: 2 - 8 дней
% Ig в сыворотке: 0.2
уровень (мг мл-1): 0.03 - 0.4
Активация комплемента: нет
взаимодействие: T клетки через лектиноподобный IgD R
Перенос через плаценту: нет
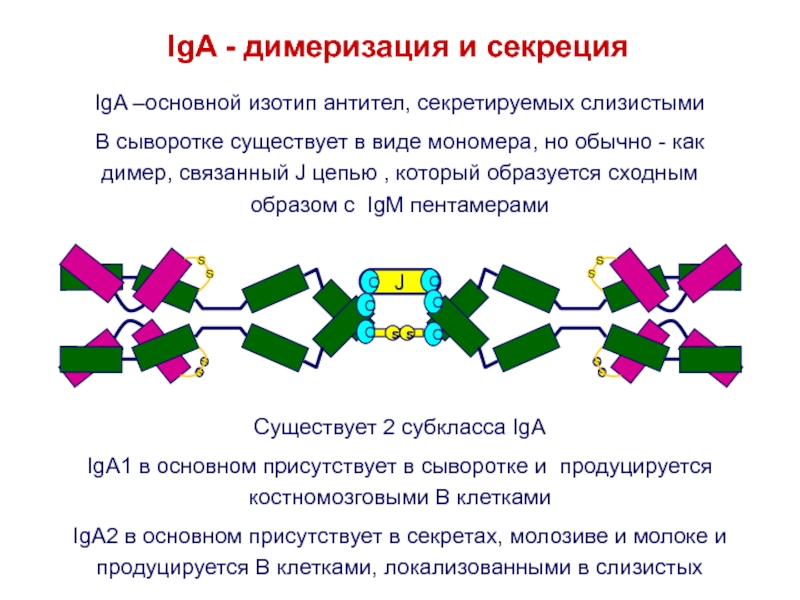
Слайд 37IgA - димеризация и секреция
IgA –основной изотип антител, секретируемых
слизистыми
В сыворотке существует в виде мономера, но обычно - как
димер, связанный J цепью , который образуется сходным образом с IgM пентамерамиСуществует 2 субкласса IgA
IgA1 в основном присутствует в сыворотке и продуцируется костномозговыми B клетками
IgA2 в основном присутствует в секретах, молозиве и молоке и продуцируется B клетками, локализованными в слизистых
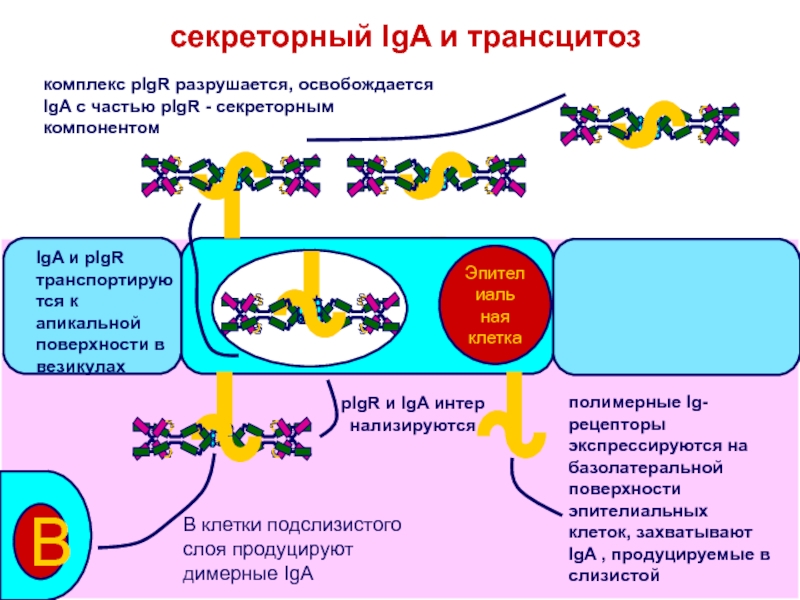
Слайд 38секреторный IgA и трансцитоз
комплекс pIgR разрушается, освобождается IgA с частью
pIgR - секреторным компонентом
Слайд 39IgA
Тяжелые цепи: a1 или a2 - альфа 1 or 2
Время полужизни:
IgA1 5 - 7 дней
IgA2 4 - 6 дней
Уровень в
сыворотке IgA1 1.4 - 4.2
(мг мл-1): IgA2 0.2 - 0.5% от Ig сыворотки : IgA1 11 - 14 IgA2 1 - 4
Активация комплемента: IgA1 – альтернативный и лектиновый путь IgA2 - нет
Взаимодействие с клетками: эпителий - через pIgR фагоциты -через IgAR
перенос через плаценту : нет
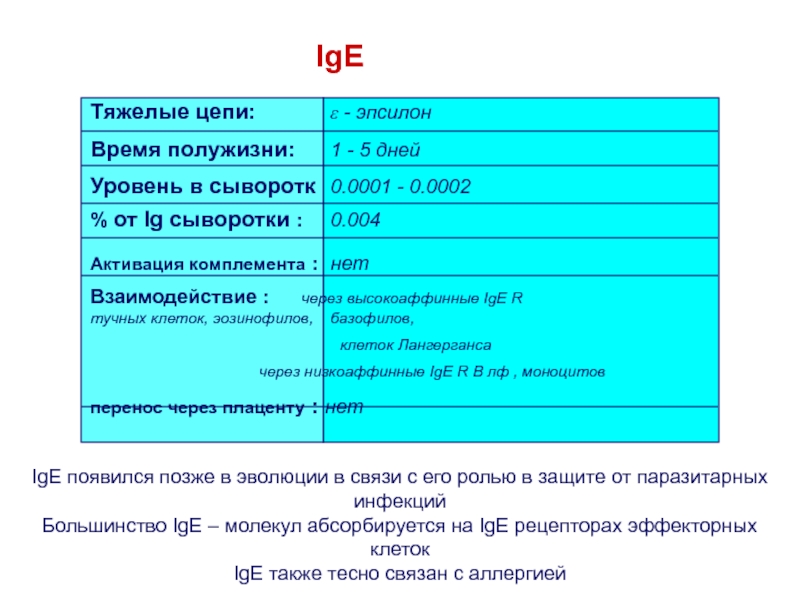
Слайд 40IgE
IgE появился позже в эволюции в связи с его ролью
в защите от паразитарных инфекций
Большинство IgE – молекул абсорбируется на
IgE рецепторах эффекторных клетокIgE также тесно связан с аллергией
Тяжелые цепи: e - эпсилон
Время полужизни: 1 - 5 дней
Уровень в сыворотк 0.0001 - 0.0002
% от Ig сыворотки : 0.004
Активация комплемента : нет
Взаимодействие : через высокоаффинные IgE R тучных клеток, эозинофилов, базофилов,
клеток Лангерганса
через низкоаффинные IgE R В лф , моноцитов
перенос через плаценту : нет
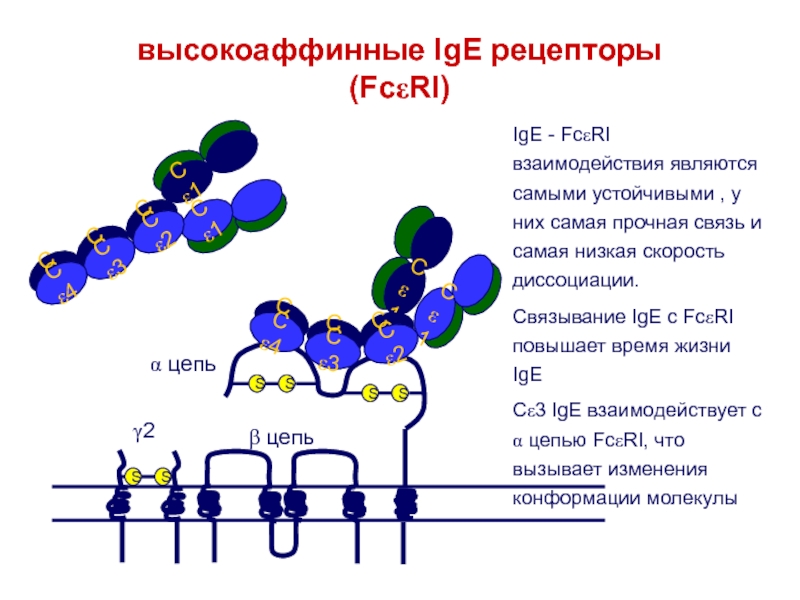
Слайд 41высокоаффинные IgE рецепторы (FceRI)
IgE - FceRI взаимодействия являются самыми устойчивыми
, у них самая прочная связь и самая низкая скорость
диссоциации.Связывание IgE с FceRI повышает время жизни IgE
Ce3 IgE взаимодействует с a цепью FceRI, что вызывает изменения конформации молекулы
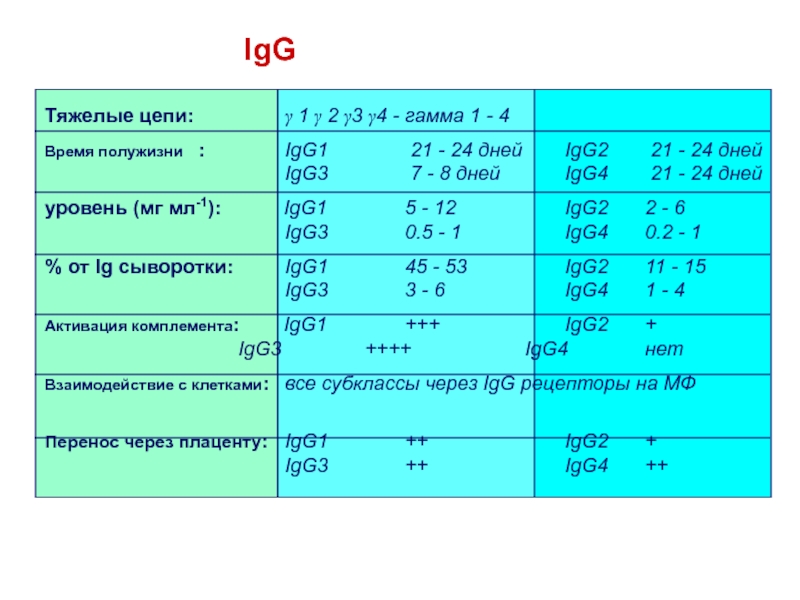
Слайд 42IgG
Тяжелые цепи: g 1 g 2 g3 g4 - гамма 1
- 4
Время полужизни : IgG1 21 - 24 дней
IgG2 21 - 24 дней
IgG3 7 - 8 дней IgG4 21 - 24 днейуровень (мг мл-1): IgG1 5 - 12 IgG2 2 - 6 IgG3 0.5 - 1 IgG4 0.2 - 1
% от Ig сыворотки: IgG1 45 - 53 IgG2 11 - 15 IgG3 3 - 6 IgG4 1 - 4
Активация комплемента: IgG1 +++ IgG2 + IgG3 ++++ IgG4 нет
Взаимодействие с клетками: все субклассы через IgG рецепторы на МФ
Перенос через плаценту: IgG1 ++ IgG2 + IgG3 ++ IgG4 ++
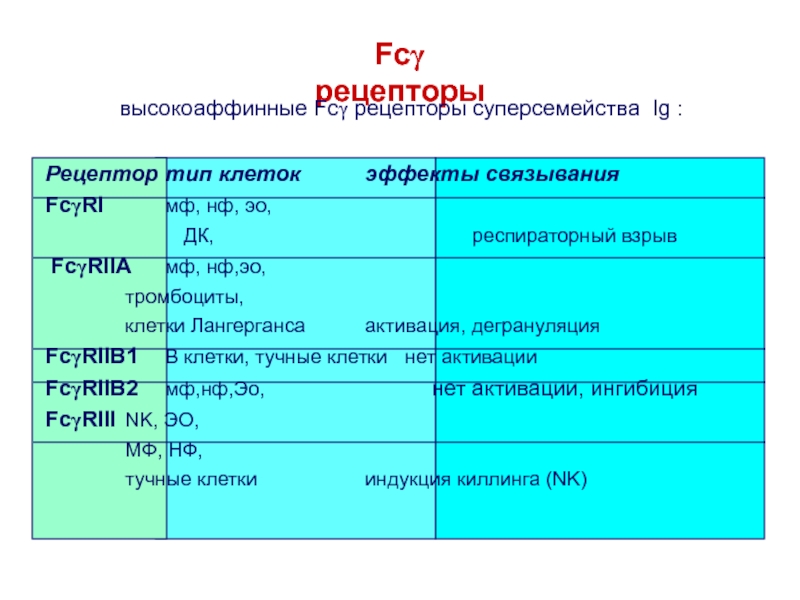
Слайд 44Fcg рецепторы
Рецептор тип клеток эффекты связывания
FcgRI мф, нф, эо,
ДК,
респираторный взрывFcgRIIA мф, нф,эо,
тромбоциты, клетки Лангерганса активация, дегрануляция
FcgRIIB1 В клетки, тучные клетки нет активации
FcgRIIB2 мф,нф,Эо, нет активации, ингибиция
FcgRIII NK, ЭО, МФ, НФ, тучные клетки индукция киллинга (NK)
высокоаффинные Fcg рецепторы суперсемейства Ig :
Слайд 45Различия в аминокислотной последовательности молекул антител
1. Изотипические различия – у
всех изотипов одинаковая аминокислотная последовательность в антигенсвязывающем центре (IgM, IgD,
IgG, IgA, IgE).Аллотипические различия – разные последовательности аминокислот в константных областях тяжелых цепей у разных особей 1 вида.
Идиотипы – различия в аминокислотных последовательностях в антигенсвязывающих центрах молекул Ig (в гипервариабельных участках).
Слайд 46Методы определения В-лимфоцитов в клинической практике
Для определения В-лимфоцитов используется метод
проточной цитофлуориметрии.
К клеткам крови добавляют моноклональные антитела, меченые флуорохромом.
В
зависимости от типа флуорохрома выбирают каналы для фотодетекции.Пробирки инкубируют 30 минут –за это время моноклональные антитела связываются с поверхностными маркерами клеток: для В-лимфоцитов –это CD 19; для Т-лимфоцитов -CD 3.
Суспензия клеток проходит через систему проточного цитофлуориметра. Программное обеспечение прибора строит гистограммы распределения клеток по интенсивности флуоресценции клеток с определяемыми маркерами.
Фенотип В-лимфоцита CD3-CD 19+
Слайд 47Методы определения антител в клинической практике
Для определения уровней иммуноглобулинов в
биологических жидкостях используют разные методы :
Иммуноферментный анализ (ИФА).
Иммунохемилюминесценция.
Турбодиметрия.
Слайд 48Понятия аффинности и авидности антител.
Эпитоп –наименьшая часть антигена, способная вызвать
иммунный ответ.
Паратоп –участок молекулы антитела, образованный вариабельными доменами и плотно
связывающий эпитоп антигена.Афинность антител (affinity-англ. сродство) –прочность взаимодействия антигена и антитела. Показатель силы связи между эпитопом и паратопом.
Авидность антител(avidity-англ. жадность) –функциональная афинность целой молекулы антитела, определяемая числом антитигенсвязывающих участков и их способностью взаимодействовать с эпитопами. Чем больше антитело связывает эпитопов, тем выше его авидность.
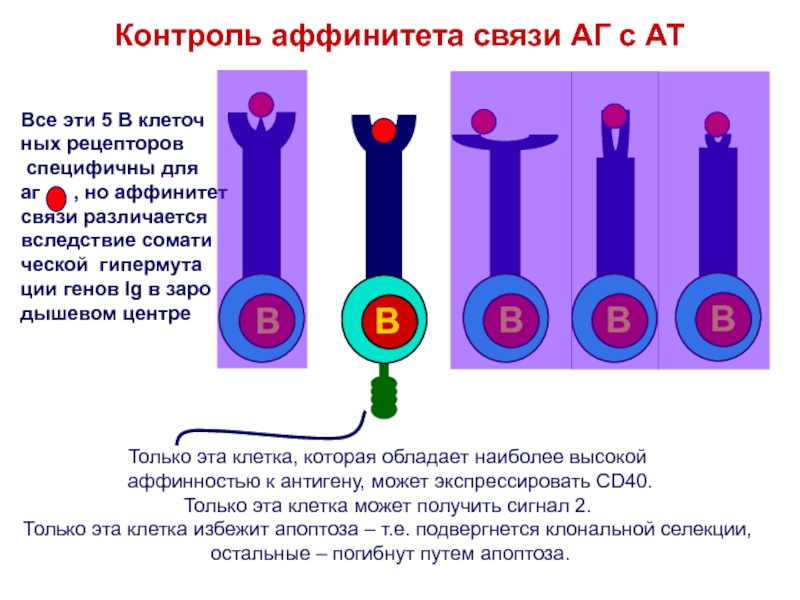
Слайд 49Контроль аффинитета связи АГ с АТ
Только эта клетка, которая обладает
наиболее высокой
аффинностью к антигену, может экспрессировать CD40.
Только эта клетка
может получить сигнал 2.Только эта клетка избежит апоптоза – т.е. подвергнется клональной селекции,
остальные – погибнут путем апоптоза.
Слайд 52Серопрофилактика и серотерапия в клинической практике.
Экстренная профилактика –применение нормальных или
специфических иммуноглобулинов или сывороток.
Цель: создание пассивного иммунитета для предупреждения развития
инфекционного заболевания в условиях высокого риска заражения столбняком, дифтерии, гепатита В, цитомегаловирусной инфекции, сибирской язвы, чумы, ботулизма и других инфекций.Слайд 53Серопрофилактика и серотерапия в клинической практике.
Нормальные иммуноглобулины человека используют с
целью профилактики кори, гепатита А, коклюша, полиомиелита, менингококковой инфекции, а
также назначают лицам с сепсисом и иммунодефицитными состояниями.Гетерологические препараты иммуноглобулинов (лошадиная сыворотка) –обогащена антителами –противодифтерийная, противостолбнячная, противогангренозная, противобутулиническая сыворотки. Также сыворотки, обогащенные иммуноглобулинами против бешенства, клещевого энцефалита, сальмонеллеза, сибирской язвы и др.
Слайд 54Пассивная иммунизация генно-инженерным препаратом паливизумаб
Защита недоношенных детей:
с очень низкой
массой тела,
с врожденными пороками сердца,
с бронхолегочной дисплазией
от смертельно
опасной для них респираторно-вирусной инфекции.Слайд 551. 14 мая 1796 года Дженнер в присутствии врачей привил коровью оспу
здоровому восьмилетнему мальчику: сделал два небольших надреза на его руке и внес
в ранки экстракт оспенных пустул. Вскоре у мальчика появились симптомы легкой (коровьей) оспы, а через 10 дней он был уже совершенно здоров. Когда же через месяц Дженнер заразил мальчика человеческой оспой, он оказался к ней невосприимчивым.Спустя несколько месяцев введение натуральной оспы повторили, а через 5 лет — еще раз. Результат остался все тем же: мальчик был невосприимчивым к этой болезни . 2. Русский ученый Владимир Хавкин, работая в Индии, в 1896 году организовал лабораторию, в которой создал первую в мире противочумную вакцину . Владимир Хавкин проводит вакцинацию местного населения от чумы. Калькутта, 1893 годСлайд 56Луи Пастер
Идеи Дженнера почти через 100 лет развил великий французский
иммунолог Луи Пастер, который доказал, что искусственно вводя в кровь ослабленные
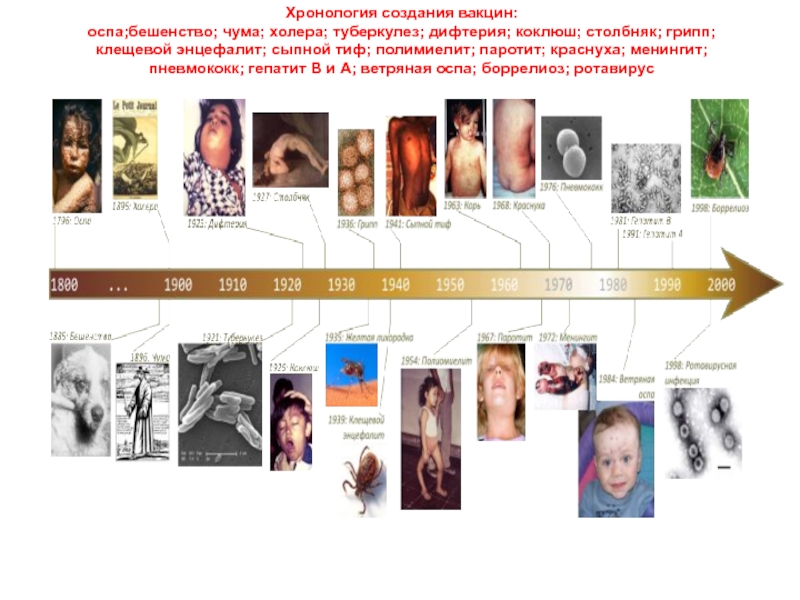
инфекционные агенты, можно вызвать формирование иммунитета у животных и человека. С именем Пастера связаны первые вакцины — от бешенства у человека; от холеры, сибирской язвы и краснухи у животных. Именно он ввел сам термин «вакцина» (от латинского vacca — корова); при нем вакцины стали вводить не с помощью надрезов кожи, а шприцами. Именно он после ряда публичных опытов убедил мир в том, что вакцинация — это единственный способ уберечься от многих страшных болезней.Слайд 57Хронология создания вакцин: оспа;бешенство; чума; холера; туберкулез; дифтерия; коклюш; столбняк;
грипп; клещевой энцефалит; сыпной тиф; полимиелит; паротит; краснуха; менингит; пневмококк;
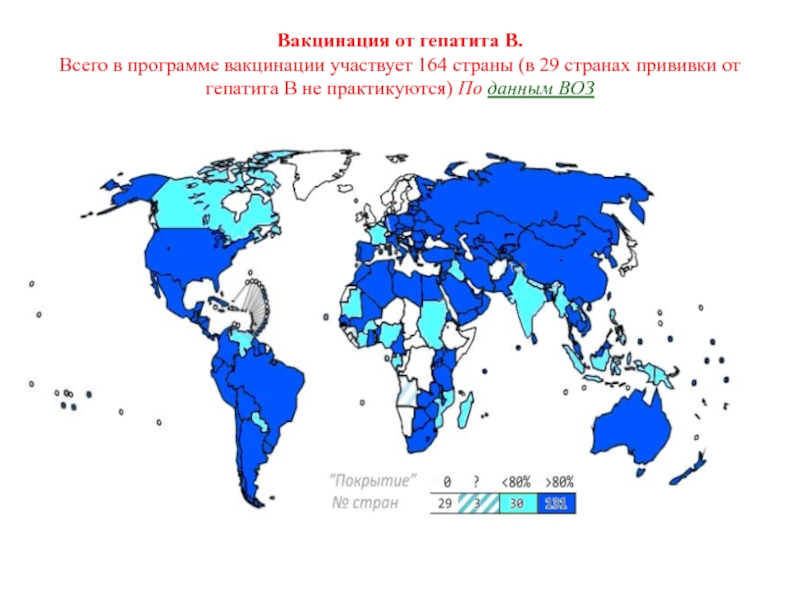
гепатит В и А; ветряная оспа; боррелиоз; ротавирусСлайд 58Вакцинация от гепатита В. Всего в программе вакцинации участвует 164
страны (в 29 странах прививки от гепатита B не практикуются)
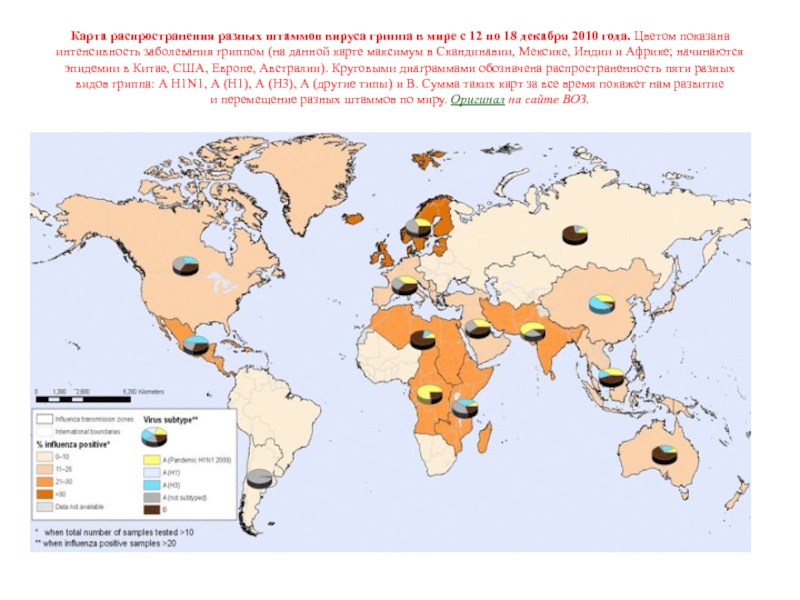
По данным ВОЗСлайд 59Карта распространения разных штаммов вируса гриппа в мире с 12
по 18 декабря 2010 года. Цветом показана интенсивность заболевания гриппом
(на данной карте максимум в Скандинавии, Мексике, Индии и Африке; начинаются эпидемии в Китае, США, Европе, Австралии). Круговыми диаграммами обозначена распространенность пяти разных видов гриппа: А H1N1, А (Н1), А (Н3), А (другие типы) и В. Сумма таких карт за все время покажет нам развитие и перемещение разных штаммов по миру. Оригинал на сайте ВОЗ.Слайд 60Активная иммунотерапия (Иммунопрофилактика)
Иммунопрофилактика – комплекс мер по созданию искусственного иммунитета.
Цель вакцинации: создание невосприимчивости организма к инфекции путем имитации естественного
инфекционного процесса с благоприятным исходом.Иммунологическая основа вакцинации:формирование иммунологической памяти о патогенах, которая при инфицировании позволяет развивать опережающий иммунный ответ.
Вакцины – иммунобиологические препараты, основа которых –антигены (живые , ослабленные или убитые бактерии, вирусы, токсины, а также антигены,полученные с помощью генно-инженерных технологий).
Адъюванты –различные вещества, которые при связывании с антигеном вакцины –усиливают ее иммуногенность (гидроокись алюминия. Фосфат алюминия и др.)
Слайд 61Классификация вакцин.
Инактивированные вакцины :
Конъюгированные вакцины (антиген одного микроорганизма связан с
носителем в виде протеинов или анатоксинов другого микроорганизма).Иммунный ответ развивается
на укрупненный антиген, а не на белок-носитель. Пример: менингококковая, гемофильная, пневмококковая вакцины.Анатоксины: обезвреженные экзотоксины (столбняк и дифтерия).
Цельноклеточные или цельновирионные вакцины –обезвреженные химическим путем или нагреванием микроорганизмы(коклюш; грипп; полиомиелит).
Сплит-вакцины( расщепленные) –у цельного вируса путем обработки детергентами удаляется липидный слой. Вакцина содержит поверхностные белки вируса –гемагглютинин и нейроаминидазу; а также белки матрикса и нуклеопротеины (вакцина против вируса гриппа).
Слайд 62Классификация вакцин.
5.Вакцины на основе поверхностных антигенов –содержат только гемаглютинин и
нейроминидазу вируса гриппа.
6. Синтетические вакцины –части вируса соединяют с синтетическим
препаратом –например, с иммуномодулятором полиоксидонием.7. Рекомбинантные генно-инженерные вакцины против гепатита В и др: искусственное введение генетического материала вируса в бактериальные клетки ; наработка белков вируса бактериальными клетками, очистка белков.
Слайд 63Классификация вакцин.
По количеству видов антигенов вакцины могут быть:
Моновалентными (моновакцины против
кори, паротита,ветряной оспы , краснухи, гемольфильной инфекции и др.).
Поливалентными (содержат
разные штаммы одного микроорганизма –против папилломовируса,полиомиелита, гриппа).Комбинированными (ассоциированными) 4-валентная вакцина АКДС (адсорбированная коклюшно-дифтерийно-столбнячная вакцина, 5-валентная вакцина Пентаксим (коклюшно-дифтерийно-столбнчно- полиомиелитно-гемофильная вакцина); 6-валентная вакцина Интраксим Гекса(к пентаксиму добавлен антиген вируса гепатита В);
Пневмо 23 и другие комбинированные вакцины.
Слайд 64Дополнительные составляющие вакцин.
Кроме антигенов в состав вакцин входят:
Адъюванты.
Консерванты.
Антибиотики.
Стабилизаторы.
Жидкая основа.
Вспомогательные вещества.
Роль
адъювантов: дополнительная активация АПК, создание депо антигена в месте его
введения с целью замедления процесса его всасывания, появления воспалительной реакции, усиления процессинга и презентации антигенов.Слайд 65Иммунологические механизмы вакцинации.
После первого введения вакцины (прайминг) развивается первичный иммунный
ответ. Антитела класса М –преобладают.
Формируется популяции долгоживущих Т и в
клеток памяти.После повторного введения вакцины(брустер) – синтезируются высокоаффинные антитела класса G.
Для разные патогенов число повторных введений антигенов (V) –различное. Цель: достичь устойчивый уровень защитные антител:
Для кори, паротита, краснухи – 1 введение антигена (V1).
Для вируса гепатита В, дифтерии, столбняка, коклюша и др. – трехкратное введение антигена - (V1) (V2) (V3) .
Повторные введения антигенов - ревакцинации или бустеризации.
Слайд 66Применение вакцин в клинической практике.
Методы вакцинации:
Парентеральный путь: большинство вакцин вводится
внутримышечно под углом 90 о к поверхности (инактивированные вакцины, анатоксины)–у
детей до 2-х лет в переднебоковую поверхность бедра.Подкожно , под углом 45 о к поверхности тела - у детей более старшего возраста - в дельтовидную мышцу плеча (живые ослабленные вакцины против кори, краснухи. паротита, ветряной оспы) или
Внутрикожно ( БЦЖ)
Энтеральный путь используют с целью активации мукозального и общего иммунитета –живые вакцины против полиомиелита и ротавируса
Интраназальный путь –введение живой противовирусной вакцины.
Слайд 67Применение вакцин в клинической практике.
Врачи в своей практике используют
Национальный
календарь прививок РФ (Приказ № 125н Министерства здравоохранения Российской Федерации
от 21 марта 2014 года).Слайд 68Применение вакцин в клинической практике: принципы вакцинопрофилактики
Массовая вакцинопрофилактика: 95% охват
населения позволяет достичь полного контроля над инфекционными заболеваниями
Ограниченный перечень противопоказаний
(отводов) –аллергия на вспомогательные вещества, иммунодефицитные состояния и др.Иммунизация лиц с хроническими заболеваниями и особыми состояниями. Ряду таких лиц требуется дополнительная (не входящая в календарь прививок) иммунизация –против мнингококковой инфекции, против гемофильной инфекции, против ветряной оспы.
Постоянный мониторинг поствакцинальных реакций.
Организационные вопросы: условия организации проведения вакцинации.
Слайд 69Критерии эффективности вакцин
Эффективная вакцина способна:
Активировать антигенпрезентирующие клетки.
Активировать антигенспецифические Т и
В лимфоциты.
Вызывать образование Т и В клеток памяти.
Обеспечивать длительное сохранение
антигенов вакцины в организме с целью поддержания протективного иммунитета.Слайд 70Вопросы
Двойственная роль В-лимфоцита в гуморальном иммунном ответе (основной эффектор и
одновременно антигенпрезентирующая клетка-АПК).
Взаимоотношения В-лимфоцит (АПК) –Т-хелпер.
Характеристика субпопуляций В-лимфоцитов-В1 и В2
клетки.Активация В-лимфоцитов при взаимодействии с Т-независимыми антигенами.
Структура антител: понятия «изотипы антител»; «аллотипы антител»; «идиотипы антител».
Методы определения В-лимфоцитов и антител в клинической практике.
Понятия аффинности и авидности антител.
Характеристики первичного и вторичного иммунного ответа.
Классификация вакцин.
Применение вакцин в клинической практике.
Слайд 71Тестовые вопросы
Иммуноглобулины - это:
Сигнальные межклеточные молекулы
Молекулы главного комплекса гистосовместимости
Адгезионные молекулы
Пептидные
молекулы, способные специфически связываться с антигеном
Протеолитические ферменты
Молекулы антител синтезируют:
Т-лимфоциты-хелперы
Незрелые
В-лимфоциты (предшественники)Плазматические клетки - потомки В-лимфоцитов
Естественные киллеры
Цитотоксические Т-лимфоциты
Слайд 72Тестовые вопросы
В1-лимфоциты:
Секретируют в основном IgM
Являются CD5+ лимфоцитами
Являются CD5- лимфоцитами
Распознают в
основном тимусзависимые антигены
Распознают в основном тимуснезависимые антигены
В2-лимфоциты:
Секретируют иммуноглобулины разных классов
Являются
CD5+ лимфоцитамиЯвляются CD5- лимфоцитами
Распознают тимусзависимые антигены
Распознают тимуснезависимые антигены
Слайд 73Тестовые вопросы
Для идентификации В-лимфоцитов в клинической практике наиболее часто используют
маркер:
CD 4
CD 19
CD 20
CD 21
CD 34
Гипермутация (соматический гипермутагенез)
происходит:В рецепторах незрелых В-лимфоцитов
в V-областях генов иммуноглобулинов пролиферирующих В-лимфоцитов
в костномозговых предшественниках миелоцитов
в геноме естественных киллеров
в клетках моноцитарно-макрофагального ряда
Слайд 74Тестовые вопросы
В результате гипермутации (соматического гипермутагенеза) при развитии гуморального иммунного
ответа происходит:
Формирование клона цитотоксических Т-лимфоцитов
Многократно возрастает афинность антител
Гибель плазматических клеток
Усиление
фагоцитарной активности макрофаговПовышение цитотоксической активности естественных киллеров
Основными иммуноглобулинами первичного ответа являются:
IgA
IgG
IgM
IgE
IgD