Слайд 1
Государственное бюджетное учреждение высшего профессионального образования «Тюменский государственный медицинский университет»
Министерства
здравоохранения Российской Федерации
(ГБОУ ВПО ТюмГМУ Минздрав России)
Кафедра клинической иммунологии и
аллергологии
Дендритные клетки
Выполнил: студент 3го курса
Педиатрического факультета
Мачитова Н. А. 340гр
Слайд 2Что такое дендритные клетки?
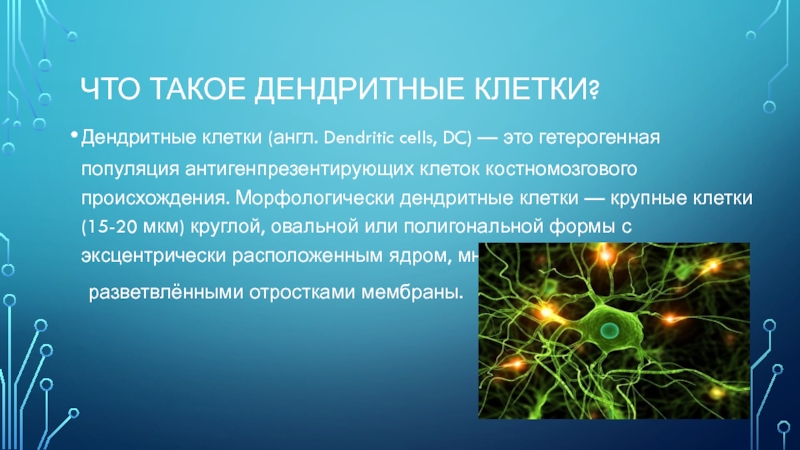
Дендритные клетки (англ. Dendritic cells, DC) —
это гетерогенная популяция антигенпрезентирующих клеток костномозгового происхождения. Морфологически дендритные клетки
— крупные клетки (15-20 мкм) круглой, овальной или полигональной формы с эксцентрически расположенным ядром, многочисленными
разветвлёнными отростками мембраны.
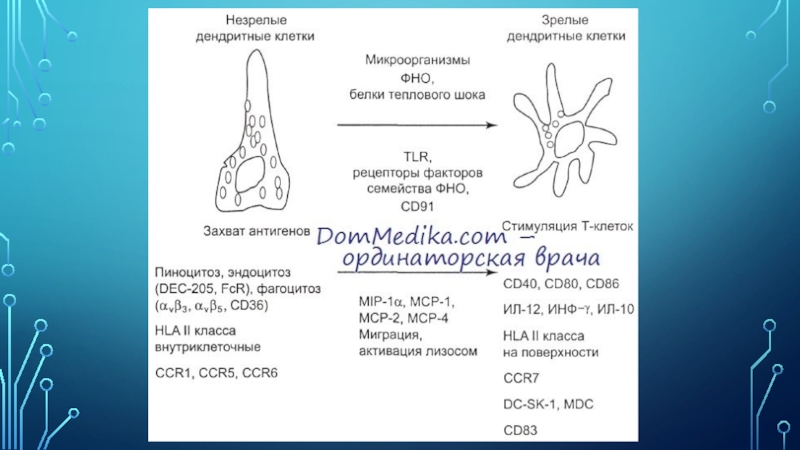
Слайд 3Функции дендритных клеток
Основной функцией дендритных клеток является презентация антигенов Т-клеткам.
Дендритные клетки также выполняют важные иммунорегуляторные функции, такие как контроль
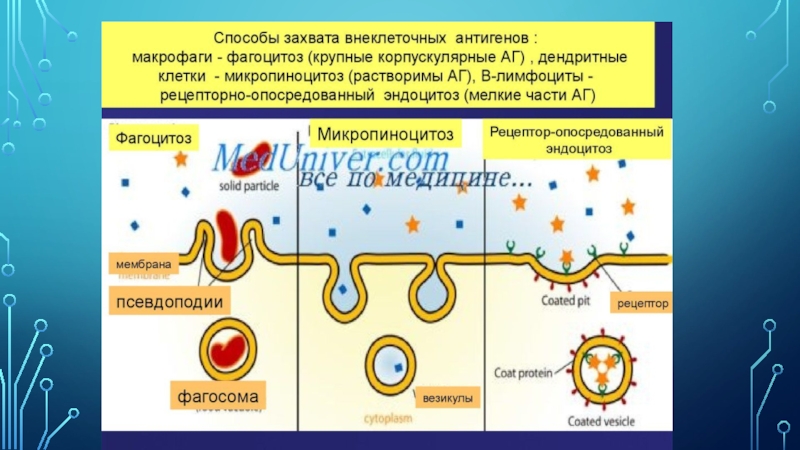
за дифференцировкой Т-лимфоцитов, регуляция активации и супрессии иммунного ответа. Важной особенностью дендритных клеток является способность захватывать из окружающей среды различные антигены при помощи пиноцитоза и рецептор-опосредованного эндоцитоза. Больше всего дендритных клеток находится в тканях, которые соприкасаются с внешней средой, например в толще эпителиального слоя слизистой оболочки кишечника, в подслизистой респираторного, желудочно-кишечного и урогенитального трактов.
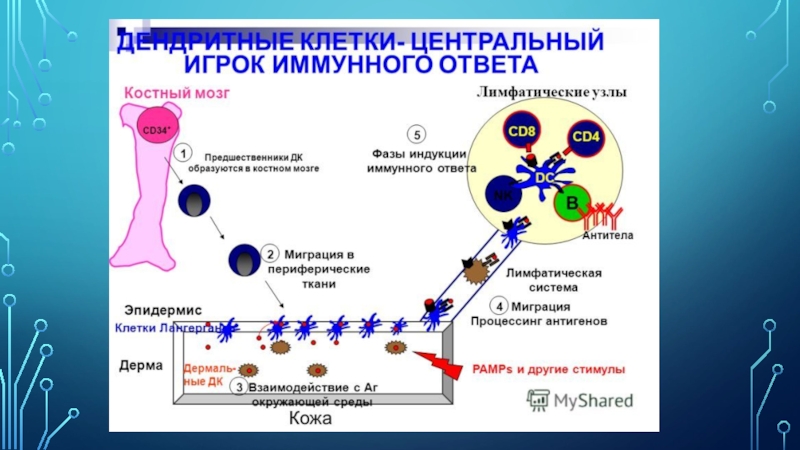
Слайд 5Дендритные клетки поглощают антигены, процессируют и представляют на своей поверхности
в комплексе с MHC I или MHC II классов. Только
в таком виде Т-клетки способны распознать антиген и вслед за этим активироваться и развить иммунный ответ. В зависимости от типа патогена дендритные клетки способны направлять дифференцировку наивных Т-хелперов (Th0) в сторону Т-хелперов 1 типа, Т-хелперов 2 типа, регуляторных Т-клеток или же Т-хелперов 17.
Слайд 6Дендритные клетки экспрессируют набор поверхностных молекул, характерный для других антигенпредставляющих
клеток:
патоген-распознающие рецепторы, в том числе рецепторы для компонентов клеточной стенки
и нуклеиновых кислот микроорганизмов, рецепторы к компонентам комплемента (CD205, CD206, CD14), Толл-подобные рецепторы;
молекулы II класса гистосовместимости (ГКС);
костимуляторные молекулы CD40, B7.1 (CD80), B7.2 (CD86), ICOS-L;
коингибиторные молекулы B7-DC (CD274), B7-H1 (CD274) и др.;
молекулы межклеточной адгезии (ICAM-1), CD11b, CD11c;
комплекс хемокиновых рецепторов (CD193, CD197 и многие другие).
Слайд 7К молекулам, которые представлены преимущественно на дендритных клетках, относят:
молекулы LAMP-семейства
CD208 (DC-LAMP), BAD-LAMP;
высокоспецифичный маркер зрелых ДК — молекулу CD83;
ГКС-подобные молекулы
CD1a, CD1c, участвующие в презентации липидных антигенов ;
молекулы CD209 (DC-SIGN), CD207 (лангерин).
Слайд 9Виды дендритных клеток
В зависимости от происхождения выделяют миелоидные (CDllc+) и
плазмоцитоидные (CDllc~CD123b) ДК, имеющие общих предшественников с марофагами и лимфоцитами,
соответственно, и обладающие различными фукциональными свойствами. Популяции различаются по экспрессии TLR, но способны стимулировать наивные Т-лимфоциты. ДК широко представлены в организме. Миелоидные ДК находятся в дерме, эпидерме, дыхательных путях, кишечнике, тимусе, селезенке, печени, лимфоидной ткани. Плазмоцитоидные ДК локализуются в лимфоидных органах, печени, легких, коже.
Слайд 11Миелоидные дк: клетки Лангерганса, интерстициальные ДК, находящиеся преимущественно в различных
тканях, и ДК, происходящие из моноцитов.
Дендритные клетки, происходящие из моноцитов,
обычно получают из фракции моно-цитарных клеток in vitro. Для этих целей СБ14+-моноциты, выделенные из периферической крови, стимулируются в течение 6-7 сут in vitro в присутствии ГМ-КСФ и ИЛ-4 или других комбинаций цитокинов (М-КСФ, ГМ-КСФ и ФНО-а). Созревание ДК оценивают по экспрессии на их поверхности CD83.
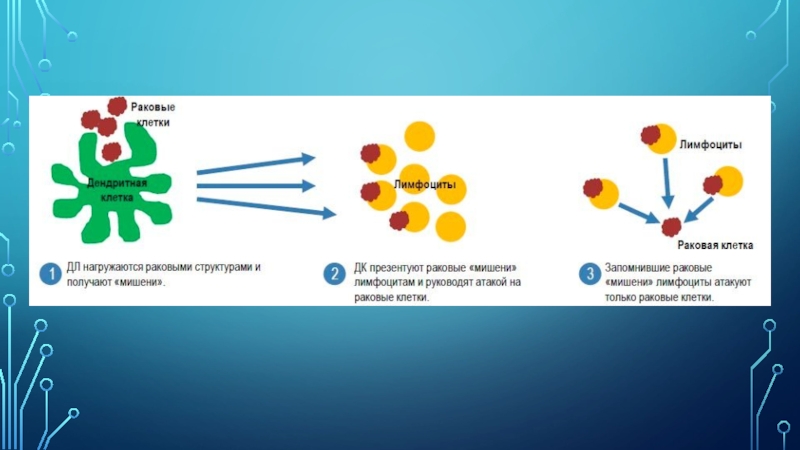
Слайд 12Индуцированные in vitro дендритные клетки находят всё большее распространение в
качестве вакцин при многих заболеваниях, в первую очередь при раке.
Приготовление такой вакцины состоит из нескольких этапов: выделение моноцитов из крови конкретного больного, стимуляция их цитокинами in vitro для дифференцировки в ДК, добавление в культуру иммуногенного пептида, происходящего из опухоли больного (клеточный лизат или стандартный антиген), продолжение культивирования до созревания ДК и, наконец, возвращение зрелых ДК в организм больного. Лечебный эффект такой вакцины связывают с активацией клонов ЦТЛ, активность которых обычно снижена у больных раком. Возможно, это происходит за счет подавления регуляторных Т-лимфоцитов.
Слайд 13Обнадеживающий лечебный эффект получен при раке предстательной железы, некоторых формах
рака почки и в некоторых других случаях. Плазмоцитоидные ДК развиваются
из СD34+-гемопоэтических предшественников, по морфологии подобны плазматическим клеткам, локализуются в Т-клеточных зонах лимфоидной ткани, миндалинах, тимусе и др. У них отсутствуют маркеры миелоидных клеток. Для таких клеток характерен фенотип CDllc CD14 CD123 BDCA2+ (CD303 ) HLA-DR+ TLR7+ TLR9+. Плазмоцитоидные ДК экспрессируют рецептор ИЛ-3 (CD 123) и созревают в присутствии ИЛ-3. Предшественники плазмоцитоидных ДК составляют около 0,5% мононуклеарных клеток периферической крови.
Слайд 14Клетки Лангерганса из кожи и других плоскоэпителмальных покровов тела, захватив
антиген, мигируют в виде "вуалевидных" клеток по афферентным лимфатическим сосудам
в паракортикальные T-зависимые области региональных сосудов, чтобы презентировать этот антиген T-клеткам CD4 . (Клетки Лангерганса богаты молекулами MHC класса II ).
В T-областях они меняют свою морфологию и уже как интердигитатные клетки они контактируют с T-клетками и презентируют им антиген. Особенно велико их содержание в мозговой зоне тимуса .
Слайд 16Плазмоцитоидные дендритные клетки вырабатывают большое количество ИФН-а в ответ на
стимуляцию и оказывают существенное влияние на врожденный иммунитет против патогенов.
Считают, что циркулирующий в крови ИФН-а — продукт плазмоцитоидных ДК.
Слайд 17Применение в медицине
В последнее десятилетие дендритные клетки вызывают повышенный интерес
исследователей благодаря лёгкости их получения из моноцитов периферической крови или
стволовых клеток костного мозга и способности эффективно представлять антиген Т-лимфоцитам. К настоящему времени проведено множество исследований по модуляции иммунного ответа у больных хроническими инфекционными и онкологическими заболеваниями с использованием праймированных антигеном дендритных клеток. Результаты большинства исследований обнадеживающие, показана безопасность применения ДК, активация иммунной системы в ответ на проводимую терапию и неплохой клинический эффект.
Слайд 19Дендритные клетки получают из примерно 250 мл крови пациента при
определенных лабораторных условиях. Закон предписывает их изготовление по стандарту GMP
в помещении, соответсвующему ГОСТ Р ИСО 14644-1. Собственные аутологичные дендритные клетки пациента созревают в лаборатории в течение 7 дней, прежде чем их инъецируют обратно пациенту.
Как только дендритные клетки введены в тело пациента, они тут же находят дорогу к лимфоузлам или циркулирующих по крови хелперные клетки и клетки-киллеры. Здесь они непосредственно предъявляют им клетки опухоли. Таким образом, качество собственного иммунного ответа организма может быть заметно улучшено, а невосприимчивость защитной системы организма к опухолям преодолена. Инъекция дендритными клетками может применяться на любой стадии заболевания.
Слайд 20Список литературы
1. Воробьев А.А., Быков А.С., А.В. Караулов. Иммунология и
аллергология / М.: Практическая медицина, 2006
2. Прокопович С.К., Винницкий В.Б.
Дендритные клетки и перспективы их использования в иммунотерапии злокачественных новообразований // Онкология, 2001, №2-3.
3. Телетаева Г.М. Цитокины и противоопухолевый иммунитет // Практ. Онкология, 2007, №4