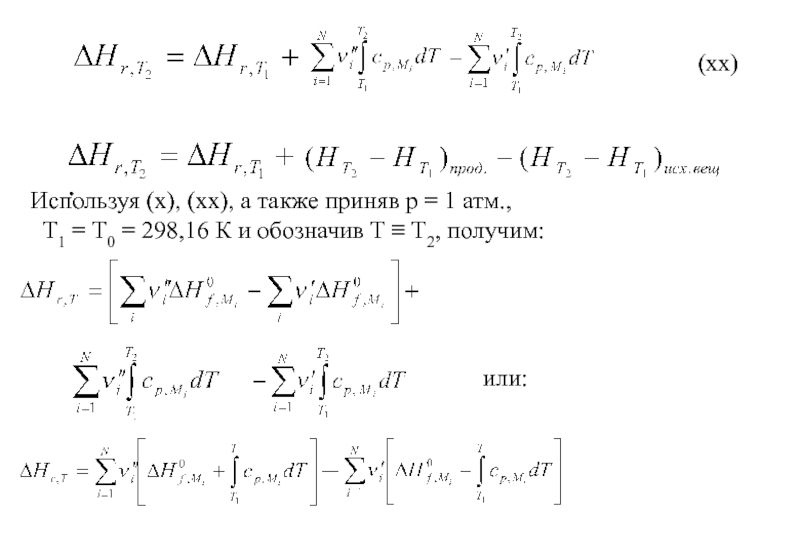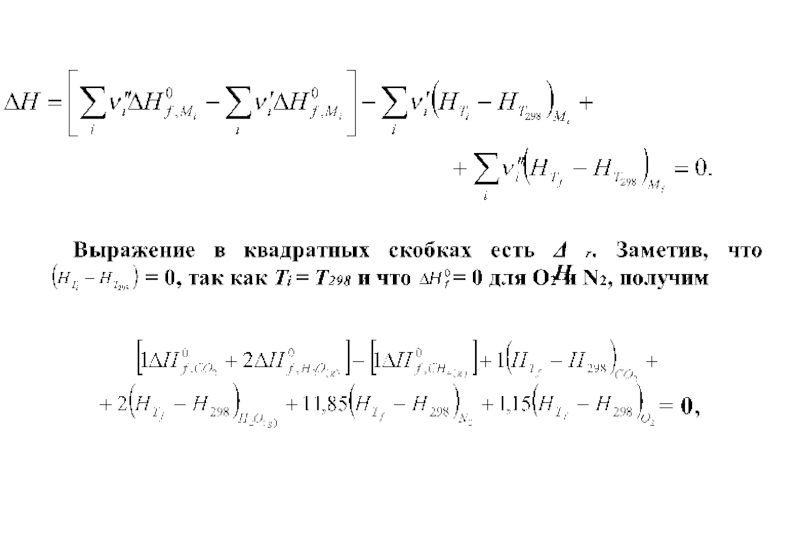Слайд 1ХИМИЧЕСКАЯ ФИЗИКА ГОРЕНИЯ
ЛЕКЦИИ
НГУ 2012 г.
Слайд 2Программа курса
Вводная лекция. История изучения процессов горения и современное состояние
исследований.
Термодинамика процессов горения, температура и химический состав системы в равновесии.
Химическая
кинетика. Скорость химических реакций. Элементарные химические реакции, теория переходного состояния. Кинетика обратимых, параллельных, последовательных и цепных реакций.
Роль диффузии и теплопередачи в процессах горения.
Основы и математическое описание теории горения. Самовоспламенение и зажигание. Теория теплового взрыва Семенова и Франк-Каменецкого. Цепной взрыв.
Теория распространения пламени в газах. Тепловая теория Малляра–Ле-Шателье, Зельдовича–Франк-Каменецкого. Теория цепного распространения пламени Зельдовича. Пределы распространения пламени. Поджигание пламени искрой.
Слайд 3Программа курса
Численное моделирование многокомпонентных реагирующих газовых потоков с применением многостадийных
механизмов реакций и детальной кинетики для описания скорости распространения и
структуры ламинарных пламен с помощью пакета CHEMKIN. Определение лимитирующих стадий процесса и характерных путей реакций.
Экспериментальные методы изучения горения газовых пламен.
Измерение нормальной скорости распространения пламен.
Измерение структуры пламен – профили концентрации веществ и температуры в волне горения.
Методы управления процессом горения - ингибирование и промотирование горения.
Ламинарные диффузионные пламена.
Образование вредных веществ при горении, методы уменьшения их выбросов.
Горение конденсированных систем, экспериментальные методы исследования.
Исследование кинетики термического разложения конденсированных веществ как первичного этапа процесса их горения.
Горение энергетических материалов.
Слайд 5Горение – это сложный физико-химический процесс, при котором превращение вещества
сопровождается интенсивным выделением тепла, ярким свечением и тепломассообменом с окружающей
средой.
Слайд 6ИСТОРИЯ РАЗВИТИЯ ЗНАНИЙ О ГОРЕНИИ
люди начали пользоваться огнем для
обогрева и приготовления пищи 600 тысяч лет назад
получать огонь
– 30 тысяч лет назад
Слайд 7Порох – Китай, Япония - IX век
Слайд 8Огню отводилось значительное место в ранних мифах и легендах, например,
в греческом мифе о Прометее, похитившем огонь у богов и
отдавшем его людям.
Слайд 9Огонь — наиболее динамичная, изменчивая из всех стихий, первоначало мира,
в то время как вода — лишь одно из его
состояний.
Огонь сгущается в воздух, воздух превращается в воду, вода — в землю («путь вниз», который сменяется «путём вверх»). Сама Земля, на которой мы живём, была некогда раскалённой частью всеобщего огня, но затем — остыла.
Геракли́т Эфе́сский (544—483 гг. до н. э) — древнегреческий философ-досократик
Слайд 10Одна из первых теорий, объясняющих сущность процесса горения - теория
флогистона. Иоганн Иоахим Бехер, 1703 г
Процесс горения заключается в разложении
вещества на флогистон и остаток – землю.
Слайд 11Роберт Бойль считал, что при нагревании металлов «огненная материя» соединяется
с металлами и превращает их в окалину. Так как вес
окалины больше веса металла, из которого она получена, то, по мнению Бойля, флогистон имеет вес.
Роберт Бойль
(1627-1691)
Слайд 12Ломоносов М.В. 1711-1765
Антуа́н Лора́н Лавуазье́
1743-1794
Закон сохранения массы вещества (Ломоносов
-1756 г, Лавуазье - 1773 г).
Слайд 13Майкл Фарадей
1791 - 1867
История свечи (1861)
Слайд 14Ро́берт Ха́тчингс Го́ддард (1882—1945 ) один из пионеров современной ракетной
техники
Эра жидкостных ракетных двигателей - 1926
Слайд 15Разработка в России ракет ГИРД-9 и ГИРД-10, первый запуск 17
августа 1933г
Тихонра́вов М.К. 1900-1974
Королев С.П. 1907-1966
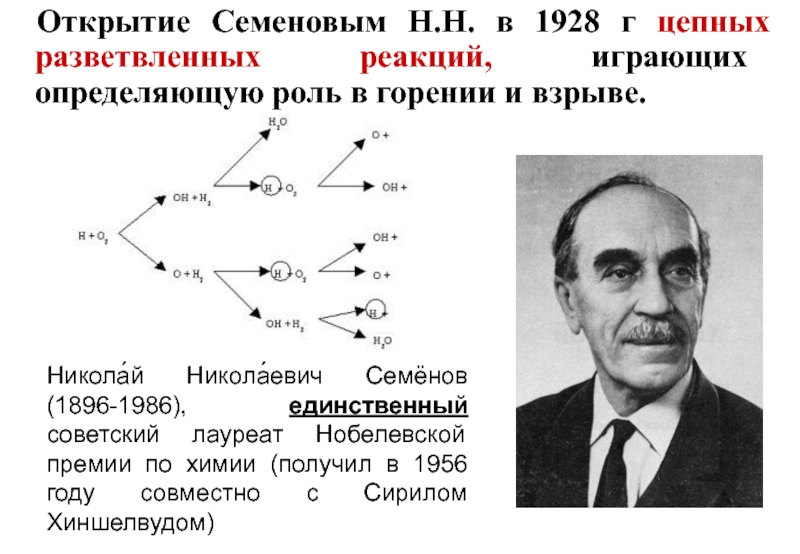
Слайд 16Никола́й Никола́евич Семёнов (1896-1986), единственный советский лауреат Нобелевской премии по
химии (получил в 1956 году совместно с Сирилом Хиншелвудом)
Открытие Семеновым
Н.Н. в 1928 г цепных разветвленных реакций, играющих определяющую роль в горении и взрыве.
Слайд 17 Зельдо́вич Я́ков Бори́сович
(1914-1987)
Установление связи между скоростью распространения
пламени и кинетикой химических реакций
Условия поджигания смеси накаленной поверхностью, определение
фронта распространения пламени и др.
Механизм химич. реакции в детонационной волне, обосновывающий расчет скорости и давления детонации.
Теория распространения пламени
Слайд 18Основные области применения горения
Тепловые электростанции на горении угля, жидкого
топлива.
Печи для получения стали, цветных металлов, стекла, керамики, цемента, сажи
углерода.
Двигатели для автомобилей, самолетов, ракет, судов.
Артиллерия, стрелковое оружие и другое вооружение.
Взрывные работы.
Уничтожение мусора, отходов, вредных веществ.
Слайд 19В настоящее время горение является основным источником энергии.
Более 85%
потребляемой энергии в мире имеет своим источником горение, большинство современных
технологий основано на использовании горения.
Количественное описание этого явления представляет не только чисто научный интерес, но также имеет большое практическое значение.
Слайд 21.
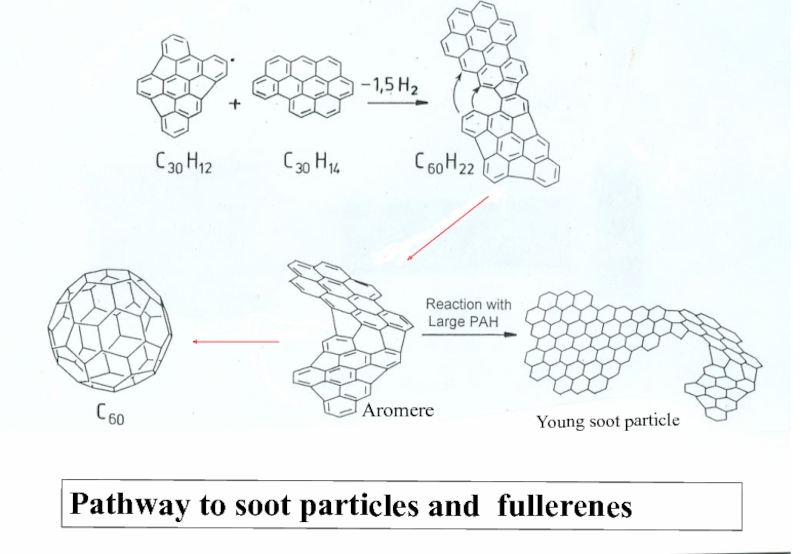
Pathway to soot particles and fullerenes
Young soot particle
Aromere
Слайд 24Процедуры разработки теоретической модели
1. Укажи общие цели модели
2. Разработай физическую
модель, основанную на понимании главных механизмов и подходящих предположениях (гипотезах)
3.
Сконструируй главные рамки математической модели, используя подходящие уравнения сохранения и транспорта
4. Проведи анализ порядков величин, чтобы упростить модель
5. Задай другие компоненты модели – начальные и граничные условия, константы скорости, термодинамические и транспортные свойства
6. Сделай математическую модель безразмерной, идентифицируй безразмерные параметры .
7. Исследуй способность модели генерировать точное решение для простых предельных случаев
8. Сравни теоретическое решение с экспериментом для подтверждения модели
Слайд 25Основные соотношения в теории горения
Сохранение масс. Химическую реакцию можно
записать как
где Мi – химический символ элемента, νi – стехиометрические
коэффициенты. Например, СО + 1/2О2 → СО2, здесь
М1 = CO, М2 = O2, М3 = CO2;
Уравнение состояния для идеального - рV= nRT,
где р – давление [Па], V – объем [м3], n – число молей [моль], T – температура [К], R – универсальная газовая постоянная (R = 8,314 Дж/(моль K)).
Для смеси идеальных газов справедлив закон Дальтона:
где N – полное число компонентов смеси
Слайд 26Массовый баланс для одностадийной реакции
.
где Wi – молекулярный вес i-й
компоненты смеси.
Определение долей реактантов
Массовая доля i-го реагента Yi с
массой mi
причем
Аналогично, мольная доля
Топливо-окислитель отношение
Стехиометрический коэффициент (equivalence ratio)
Слайд 27индекс st соответствует стехиометрической реакции, например:
CH4 + 2O2 → CO2
+ 2H2O.
Для бедных топливом смесей
< 1;
для стехиометрических смесей = 1
для богатых топливом > 1.
Стандартная теплота образования [ккал/моль] теплота, необходимая, чтобы один моль вещества был образован из элементов при стандартных условиях
.
(Т = 298,16 К, Р = 1 атм);
индекс f означает образование из элементов,
Надстрочный индекс “0” означает стандартные
условия
Слайд 28СТАНДАРТНЫЕ ТЕПЛОТЫ ОБРАЗОВАНИЯ ВЕЩЕСТВ
Вещество
ΔНf0 ккал/моль
Атом кислорода О (г) 59,5
Окись азота NО (г) 21,6
Молекула кислорода О2 (г) 0
Двуокись азота NO2 (г) 8,0
Озон О3 (г) 34,0
Атом водорода Н (г) 52,1
Молекула водорода Н2 (г) 0
Вода Н2О (г) –57,8
Закись азота N2O(г) 19,5
Н2О (ж) –68,3
NH (г) 81,2
Радикал НО2 (г) 3,9
NH2 (г) 42,3
Перекись водорода Н2О2 (ж) –44,7
Аммиак NН3 (г) –11,0
Гидроксил ОН (г) 9,3
Слайд 29Теплота реакции
Рассмотрим реакцию
Теплота реакции при стандартных условиях при температуре
Т0:
Во многих случаях требуется определить ΔНr при некоторой температуре T2
, если известна теплота реакции при температуре Т1. В этом случае имеем два равновесных состояния (ΔН)А = (ΔН) В. Таким образом, можно записать:
(х)
Используя (х), (хх), а также приняв р = 1
атм.,
Т1 = Т0 = 298,16 К и обозначив Т ≡ Т2, получим:
или:
(хх)
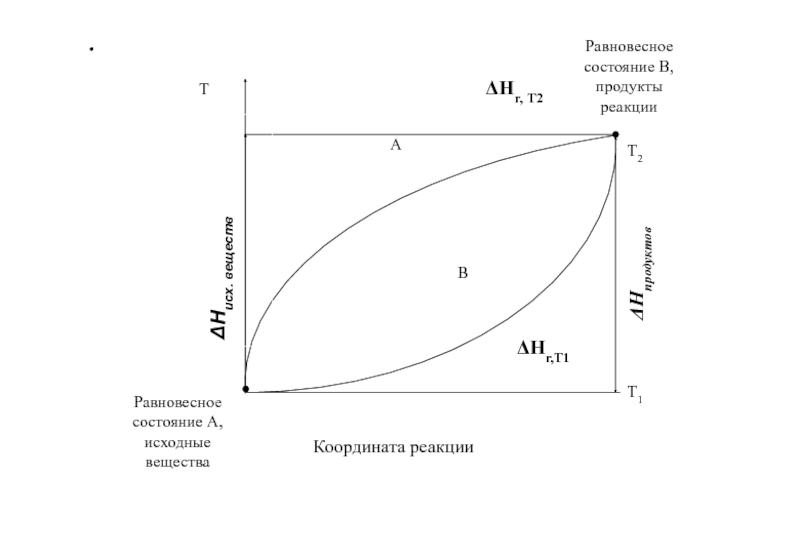
Слайд 31.
А
В
Равновесное состояние А, исходные вещества
Координата реакции
Равновесное состояние В, продукты реакции
ΔHr,T1
Т1
ΔНпродуктов
Т2
ΔHr,
T2
Т
ΔНисх. веществ
Слайд 33 Пример 1. Найти теплоту реакции окисления этана С2Н6.
С2Н6
+ 3,5O2 2CO2 + 3H2O.
ΔН = Σνi΄΄ΔHf Mi0 – Σνi΄ΔHf
Mi0 = 2ΔHf CO20 + 3ΔHf H2O0 –
– ΔHf C2H6 0 – 0 = –2 ∙ 94 – 3 ∙ 57,8 – (–20,24) = –341,16 ккал.
Пример 2. Определить адиабатическую температуру пламени метановоздушной смеси состава: 1 моль метана + 15 молей воздуха и концентрации продуктов без учета их диссоциации:
Слайд 34Решение. Уравнения сохранения элементов:
С:
O: 15(0,21∙2) =
N: 15(0,79∙2) =
H:
Решая эти уравнения, получим
значения для Адиабатическая температура пламени может быть вычислена, с учетом
того, что ΔН = 0, и следующего уравнения:
Слайд 37УЧЕТ ДИССОЦИАЦИИ ПРОДУКТОВ РЕАКЦИИ
Приведенный выше метод вычисления приемлем только, если
Тf < 1200 K. При более высоких температурах продукты реакции
диссоциируют и образуются другие соединения. Так, описанную реакцию следовало бы заменить на
Слайд 38Химический состав системы в равновесии
Рассмотрим обратимую реакцию:
При условии, что все
компоненты находятся в газообразном состоянии, в состоянии равновесия при постоянном
давлении можно записать выражение для константы равновесия:
где pi,e – парциальное давление компонентов системы в равновесии,
p0 – общее давление в системе, p0= pi
Слайд 39По определению, свободная энергия Гиббса:
G ≡ H - TS
В химических
процессах одновременно действуют два противоположных фактора — энтропийный (TΔS) и энтальпийный
(ΔH). Суммарный эффект этих противоположных факторов в процессах, протекающих при постоянном давлении и температуре, определяет изменение энергии Гиббса (G):
ΔG = ΔH – TΔS
Если энергия Гиббса в исходном состоянии системы больше, чем в конечном, то процесс принципиально может протекать (ΔG<0),
если наоборот (ΔG>0) — то не может.
Если ΔG=0, то система находится в состоянии химического равновесия.
Слайд 40Существует соотношение, связывающее изменение свободной энергии Гиббса в ходе химической
реакции с её константой равновесия:
или
позволяющее находить состав системы в
равновесии
Слайд 41Пример 3. Рассмотрим реакцию окисления метана при недостатке кислорода
CH4+1.5O2=CO+2H2O,
которая благодаря реакции водяного газа
СО + Н2О = СО2 +
Н2
идет по уравнению
СН4 + 1,5О2 (1 – )CO + (2 – )H2O + CO2 + H2.
Необходимо найти соотношения для нахождения равновесного состава и определения адиабатической температуры пламени.
Слайд 43Для химической реакции в адиабатической системе
CH4+1.5O2=(1-)CO+(2- )H2O+ CO2+
H2
Можно записать уравнение сохранения энтальпии
Слайд 44Это выражение можно переписать для индивидуальных соединений:
(Б)
Слайд 45Зная Кр, из выражения (А) может быть найдена . Подставляя
полученную величину , энтальпии образования и энтальпию реакции в левую
часть выражения (Б), сопоставляем сумму с 0. Если она не равна 0, снова предполагаем некоторое значение Tf и повторяем процесс. Проводя таким образом последовательные итерации находят значение Tf и .
Предполагая некоторое значение Tf, константа равновесия Кр(Tf) может быть определена из констант равновесия реакций образования СО2, СО и Н2О,