Слайд 1ХИМИЧЕСКАЯ ТЕХНОЛОГИЯ ТОПЛИВ И УГЛЕРОДНЫХ МАТЕРИАЛОВ
Слайд 2Рекомендуемая литература
Капустин В.М., Гуреев А.А. Технология переработки нефти. Часть 2.
Физико-химические процессы. (2015 г.)
Смидович Е.В. Технология переработки нефти и газа.
Ч.2.
Суханов В.П. Каталитические процессы в нефтепереработке
Ахметов С.А. Технология глубокой переработки нефти и газа.
Макаров Г.Н. и др. Химическая технология твердых горючих ископаемых.
Рябов В.Д. Химия нефти и газа.
Магарил Р.З. Теоретические основы химической переработки нефти и газа
Слайд 3ВВЕДЕНИЕ В ХИМИЧЕСКУЮ ТЕХНОЛОГИЮ ТОПЛИВ И УГЛЕРОДНЫХ МАТЕРИАЛОВ
Слайд 41 Классификация химических (деструктивных) процессов
2 Теоретические основы химических процессов
3 Технологические
основы процессов
4 Скорость процессов и тепловые эффекты
ПЛАН ЛЕКЦИИ
Слайд 5Физические
Химические (деструктивные)
Классификация технологических процессов
Слайд 6Термические процессы
Термокаталитические процессы
Гидрогенизационные (термогидрокаталитические) процессы
Процессы по переработке легких углеводородных фракций
Классификация
химических процессов переработки нефти
Классификация по родственным признакам
Слайд 8Термокаталитические процессы
Слайд 10Процессы переработки легких углеводородных фракций
Слайд 11Классификация химических процессов переработки нефти
Направленные на углубление переработки нефти
Направленные на
облагораживание нефтепродуктов для повышения их качества
Направленные на получение специальных продуктов
или сырья нефтехимии
Классификация по назначению
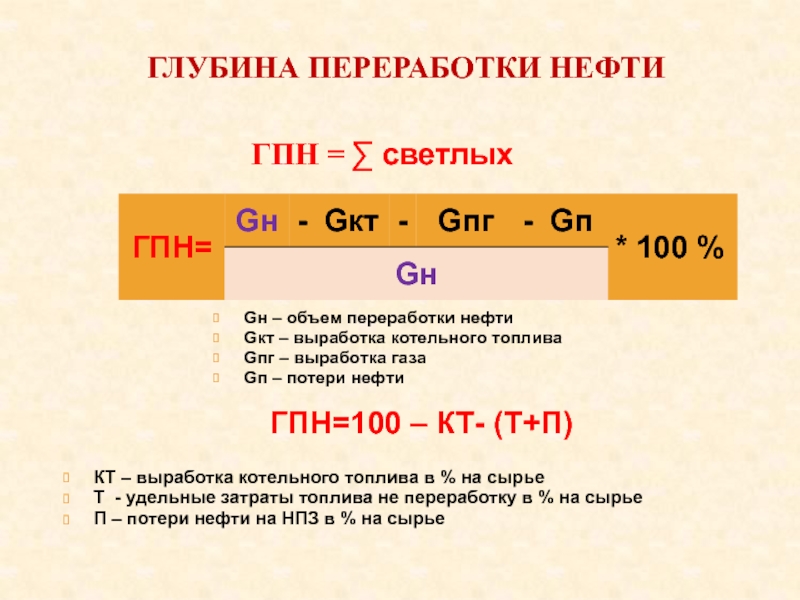
Слайд 12глубина переработки нефти
Gн – объем переработки нефти
Gкт – выработка котельного
топлива
Gпг – выработка газа
Gп – потери нефти
ГПН=100 – КТ- (Т+П)
КТ
– выработка котельного топлива в % на сырье
Т - удельные затраты топлива не переработку в % на сырье
П – потери нефти на НПЗ в % на сырье
ГПН =
∑ светлых
Слайд 13Увеличение Глубины переработки
Нефть
АВТ
Г Б К
ДТ ВГ
Гудрон
2 10 15 15 20 35
40 % на нефть
ВГ
КК
Г Б ЛГ ТГ Кокс
20 45 20 10 5
65 на ВГ (65*0,2=13 % на нефть)
Гудрон
Коксование
Г Б ЛГ ТГ Кокс
10 15 25 25 25
40 на Гудрон (40*0,35=14 % на нефть)
Слайд 14Направленные на углубление переработки нефти
Технологические процессы
Термический крекинг
Висбрекинг
Каталитический крекинг
Коксование
Гидрокрекинг
Пиролиз остаточного сырья
Слайд 15Направленные на облагораживание нефтепродуктов, повышение их качества
Технологические процессы
Изомеризация
Алкилирование
Каталитический риформинг
Гидрогенизационные процессы:
гидроочистка (ГО) , гидрокрекинг (ГК)
Слайд 16Направленные на получение спецпродуктов или сырья для нефтехимии
Технологические процессы
Коксование
Каталитический
риформинг
Пиролиз
Производство битумов
Производство пеков
Олигомеризация
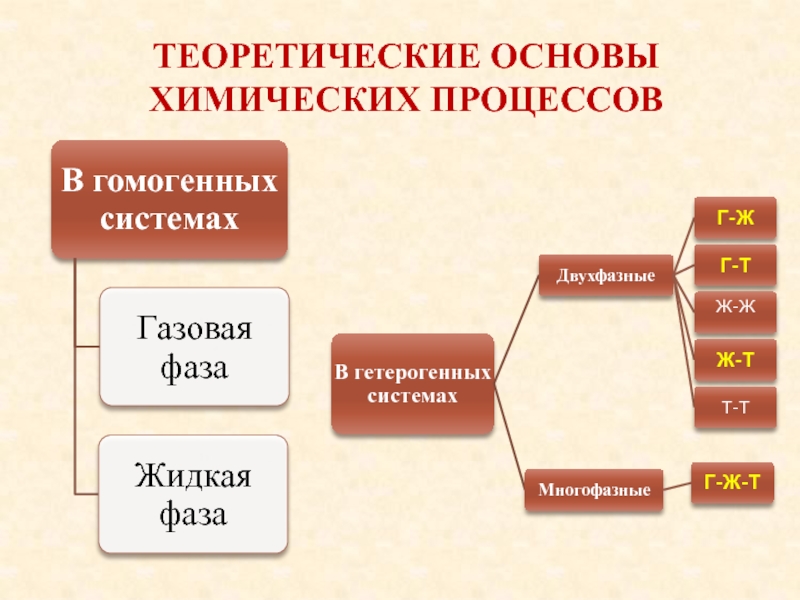
Слайд 17Теоретические основы химических процессов
С позиций изменения структуры молекул углеводородного сырья
протекают химические процессы:
Термолиз
Катализ
Крекинг
Конденсация и др.
Слайд 18Теоретические основы химических процессов
Суммарный технологический процесс состоит из стадий:
Подвод реагирующих
компонентов в зону реакции
Химические реакции
Разделение и отвод полученных продуктов из
зоны реакции
Слайд 19Теоретические основы химических процессов
Подвод реагирующих компонентов в зону реакции
Молекулярная диффузия
Конвекция
(при интенсивном перемешивании – турбулентная диффузия)
Многофазные системы – группа веществ,
находящихся в любом взаимодействии
Фаза – совокупность однородных частей системы, одинаковых по составу, химическим и физическим свойствам, разделенных поверхностью раздела от других частей
Слайд 20Теоретические основы химических процессов
В многофазных системах – подвод реагирующих компонентов
совершается:
- Абсорбцией
- Адсорбцией или десорбцией паров и газов
- Конденсацией паров
-
Плавлением твердых веществ или растворением их в жидкости
- Испарением или возгонкой
Стадия перехода реагирующих компонентов из одной фазы в другую – наиболее медленный этап технологического процесса, определяет общую скорость процесса
Слайд 21Теоретические основы химических процессов
Химические реакции – основа физико-химического процесса
Превращение вещества
проходит через ряд последовательных (а иногда и параллельных) химических реакций
В
результате образуются – основной продукт, побочные продукты, отходы
Побочные продукты и отходы образуются как в результате основных так и побочных реакций
Слайд 22Теоретические основы химических процессов
Отвод полученных продуктов из зоны реакции:
- Диффузией
-
Конвекцией
Суммарная скорость процесса определяется скоростью перечисленных элементарных стадий
Элементарные процессы протекают
с различными скоростями
Общая скорость процесса лимитируется скоростью наиболее медленной стадией
Слайд 23Теоретические основы химических процессов
Процесс протекает в кинетической области – если
наиболее медленно происходит сама химическая реакция, лимитирующая суммарную скорость
Для ускорения
применяют: увеличение концентрации, температуры или давления, катализатор.
Процесс протекает в диффузионной области – если общая скорость процесса лимитирует подвод реагирующих компонентов или отвод продуктов реакции
Для ускорения применяют: увеличение скорости диффузии (турбулизация системы), диспергирование фаз, повышение температуры и концентрации, гомогенизация системы
Если скорости всех стадий соизмеримы - процесс протекает в переходной области
Слайд 24Теоретические основы химических процессов
Технологический режим – совокупность основных факторов (параметров),
влияющих на скорость процесса, выход и качество продукта
Основные параметры: температура,
давление, применение катализатора и его активность, концентрация взаимодействующих веществ, способ и степень перемешивания реагентов
Параметры определяют принципы конструкции реакторов
Оптимальным параметрам соответствуют максимальная производительность
Слайд 25Теоретические основы химических процессов
Агрегатное состояние реагирующих веществ определяет способы их
технологической переработки и принципы конструирования аппаратов
Слайд 26Теоретические основы химических процессов
Слайд 27ТехНОЛОГИЧЕСКИЕ основы процессов
1. Равновесие реакций
- Все реакции обратимы
- Во многих
реакциях равновесие смещено полностью в сторону продуктов реакции
Технологические процессы делят
на:
- Обратимые
- Необратимые
Необратимые процессы протекают лишь в одном направлении
Слайд 28ТеХНОЛОГИЧЕСКИЕ основы процессов
Все обратимые процессы стремятся к равновесию (Wпр=Wобр)
Соотношение компонентов
во взаимодействующих системах остается постоянным до изменения параметров технологического процесса
(температура, давление, концентрация)
Влияние основных параметров на равновесие определяется принципом Ле Шателье-Брауна
«В системе, выведенной внешним воздействием из состояния равновесия, самопроизвольно происходят изменения, стремящиеся вернуть систему к новому состоянию равновесия»
Слайд 29ТеХНОЛОГИЧЕСКИЕ основы процессов
Примеры
1. А+Б=В+Q (в газовой фазе)
2. А=Б+В-Q ( в
газовой фазе)
3. А+Б=В+Q (в жидкой фазе)
4. А+Б=В+С+Q (в жидкой фазе)
Для увеличения выхода готового продукта
T-?, Р-?, С-?, Q-?
Слайд 30ТеХНОЛОГИЧЕСКИЕ основы процессов
2. Выход продукта – в зависимости от условий
процесса определяется как степень превращения, равновесный выход и фактический выход.
Степень
превращения (степень конверсии) – отношение фактически полученного продукта Gф к максимальному (или теоретическому) количеству Gм, которое можно было бы получить их данного исходного вещества
Слайд 31ТеХНОЛОГИЧЕСКИЕ основы процессов
Равновесный выход – отношение количества основного исходного вещества,
фактически превращенного в продукт Gр, к общему его количеству Gм
Для
необратимых процессов Для обратимых процессов
Слайд 32ТеХНОЛОГИЧЕСКИЕ основы процессов
Фактический выход – отношение фактически полученного продукта Gф
к его количеству, которое получалось бы в состоянии равновесия Gр
(в долях или %)
Выход продукта – единственная мера оценки скорости и полноты протекания процесса
Слайд 33ТеХНОЛОГИЧЕСКИЕ основы процессов
3. Глубина процесса (степень превращения сырья) – характеризуется
долей превращенного сырья
«Условно непревращенное сырье» - та часть жидких
продуктов процесса, которая выкипает в пределах испарения исходного сырья
Доля «условно непревращенного сырья»
Процесс с рециркуляцией – процесс, сопровождаемый возвращением «условно непревращенного сырья» в зону реакции
Рециркулят (рисайкл) - «условно непревращенная» часть сырья, которая возвращается в зону реакции
Коэффициент рециркуляции – отношение количества рециркулята к количеству свежего сырья (К)
Коэффициент загрузки – отношение общей загрузки реактора к количеству свежего сырья (К1)
К1=К+1
Слайд 34Скорость процессов и тепловые эффекты
1. Скорость процессов
Скорость гомогенных реакций Wi
– количество одного из реагентов или продуктов ni, прореагировавшее или
образовавшееся в единицу времени в единице реакционного пространства V
- Скорость химической реакции пропорциональна концентрациям реагентов;
- Суммарная скорость последовательных превращений определяется скоростью наиболее медленной стадии
Слайд 35Скорость процессов и тепловые эффекты
Температура (технологический параметр) описывается уравнением Аррениуса,
где k – константа скорости
Е - энергия активации, это минимальный
избыток энергии, который необходим для протекания химической реакции
- В области более низких температур кинетические реакции более чувствительны к изменению температуры
- При изменении температуры скорость реакции с более высокой энергией активации меняется в большей степени
Слайд 36Скорость процессов и тепловые эффекты
Скорость гетерогенного процесса
Wа – скорость процесса
по реагенту А
а- стехиометрический коэффициент реагента А
S – площадь полифазной
(реакционной) поверхности
В гомогенных процесса при хорошем перемешивании диффузия протекает очень быстро и не влияет на суммарную скорость
В гетерогенных системах – диффузия самая медленная стадия, определяет общею скорость всего процесса
Слайд 37Скорость процессов и тепловые эффекты
Способы увеличения скорости процесса
Увеличение константы скорости
процесса
Увеличение движущей силы процесса
Увеличение поверхности соприкосновения (контакта) фаз
Слайд 38Увеличение константы скорости процесса
Слайд 39Увеличение движущей силы процесса
Слайд 40Увеличение поверхности соприкосновения (контакта) фаз
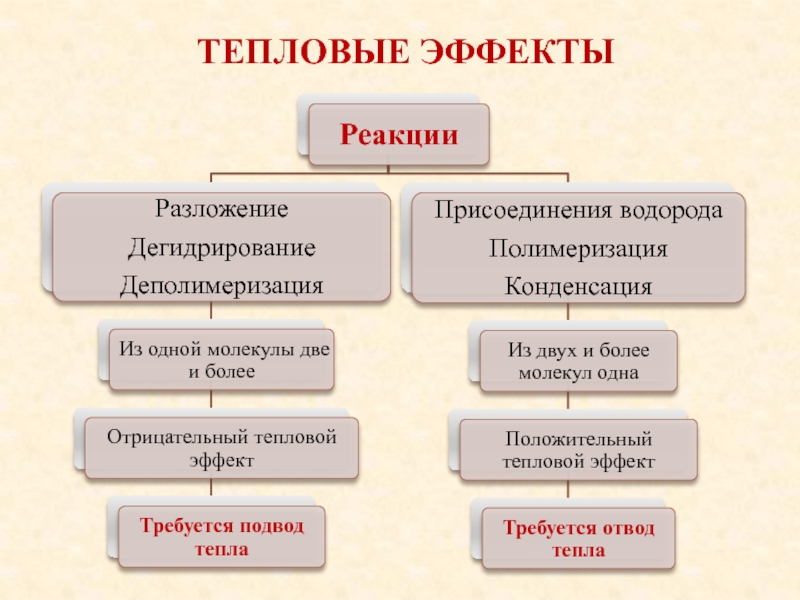
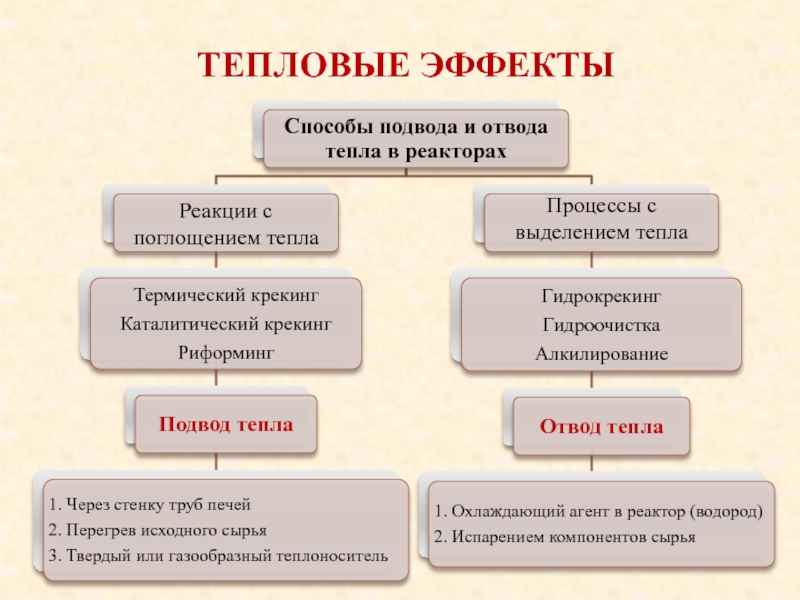
Слайд 41Тепловые эффекты
Отрицательный – для осуществления процесса необходимо затрачивать некоторое количество
теплоты
Положительный – происходит выделение теплоты, и для сохранения изотермичности необходимо
отводить теплоту из зоны реакции
∆Нхр = ∑ ∆Нобр.прод - ∑ ∆Нобр. исх. реагентов
∆Нпроц = ∑ ∆Нцелевых + ∑ ∆Нпобочных
Слайд 42Тепловые эффекты
Тепловой эффект химической реакции не зависит от пути перехода
одного вещества в другое, а зависит от начального и конечного
состояния веществ
Например: