Слайд 3р-Элементы
р-элементы включают в себя все благородные газы, кроме гелия, все неметаллы, кроме водорода, все металлоиды, и даже
несколько металлов, в том числе Al, Sn и РЬ
O, Si и Al –
наиболее распространенные элементы в земной коре
C, N, O, P, S и Cl – среди элементов, составляющих большую часть живой материи
C и S могут встречаться в свободном виде
Слайд 4Общая характеристика
p - элементов
Общая электронная формула:
[…] ns 2(n–2)f 14(n–1)d
10np 16
Степени окисления (от –IV до +VII).
Отличие свойств последнего
элемента группы (6 период): стабилизация низшей степени окисления. Например, в 13 группе таллий (I); в 14 группе свинец (II); в 15 группе висмут (III) и т.д.
Характерно образование кратных (- и -) связей; тип гибридизации атомных орбиталей преимущественно sp3.
Слайд 5р - элементы:
Для простых и сложных веществ: катенация –
образование структур типа –Э—Э—Э– … (O3, P4, S8, Na2Se5, HN3
…) и –Э—О—Э—О—Э– … (H2S2O7, Na2B4O7 ...).
Неметаллические свойства: склонность к образованию одноатомных анионов (S2–, Cl– и т.д.), к образованию только сложных катионов (NH4+, NO+ и т.д.), окислительные свойства.
С увеличением порядкового номера элемента (сверху вниз по группе) усиливается металличность.
Слайд 6 Металлический характер элементов уменьшается слева направо в периодах в связи с увеличением
энергии ионизации.
Максимальная степень окисления увеличивается в периодах.
Ионный характер галогенидов и оксидов
уменьшается в каждом периоде.
Кислотный характер оксидов возрастает в каждом периоде.
Ионный характер оксидов и галогенидов увеличивается (сверху вниз по группе) и они становятся более основными.
Слайд 7Общая характеристика элементов 13-группы.
Слайд 8Элементы 13 группы
Общая электронная формула:
[…] ns 2 (n –1)d
10 np 1
Степени окисления: 0, +I, +III
(TlIII
– с. ок-ль)
Валентные возможности: B 3, 4; Al, Ga, In, Tl 3 6
Слайд 9Физические свойства простых веществ
Слайд 11Распространение в природе. Минералы
3. Al 7,57 % масс.
37. B 2·10–3
%. масс.
38. Ga
65. Tl
68. In
Al: боксит AlO(OH)
каолин Al4(Si4O10)(OH)8
корунд Al2O3
(рубин и сапфир)
криолит Na3[AlF6]
алунит (K,Na)Al3(SO4)2(OH)6
полевые шпаты – ортоклаз K(AlSi3O8)
нефелин K,Na(AlSiO4)
Слайд 12B: бура Na2B4O7 . 10H2O
кернит Na2B4O7 . 4H2O
борацит Mg3(B7O13)Cl
сассолин
B(OH)3
Слайд 14Открыт в 1808 г. Два известных французских ученых Жозеф Гей-Люссак и
Луи Тенар «отняли» воду у борной кислоты и на полученный
оксид подействовали металлическим калием. Гей-Люссак и Тенар объявили об открытии нового элемента.
Спустя несколько месяцев бор открыли вторично. Великий английский химик Хэмфри Дэви получил его при электролизе расплавленного борного ангидрида.
Своим названием элемент обязан латинскому слову borax, что значит бура.
Слайд 16Свойства бора
1. Единственный неметалл в 13 группе
2. Очень высокие т.пл.
(2573 оС) и т.кип. (3660 оС)
3. d = 2.35
г/см3 - черный, кристаллический бор
d = 1.73 г/см3 - коричневый, аморфный бор
4. Кристаллический бор очень твердый
(9.5 по шкале Мооса)
5. Кристаллический бор - полупроводник, Еg = 1.55 эВ
6. Бор имеет 2 стабильных изотопа 10В, 11В
10
5В + 110n = 42He + 73Li
замедление нейтронов
7. Бор - восстановитель, Е0(Н3ВО3/В) = -0.87 В
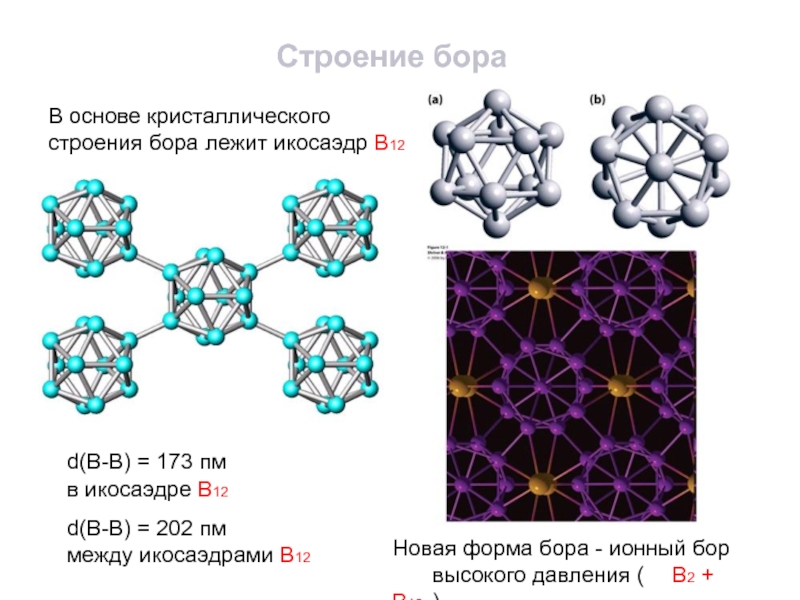
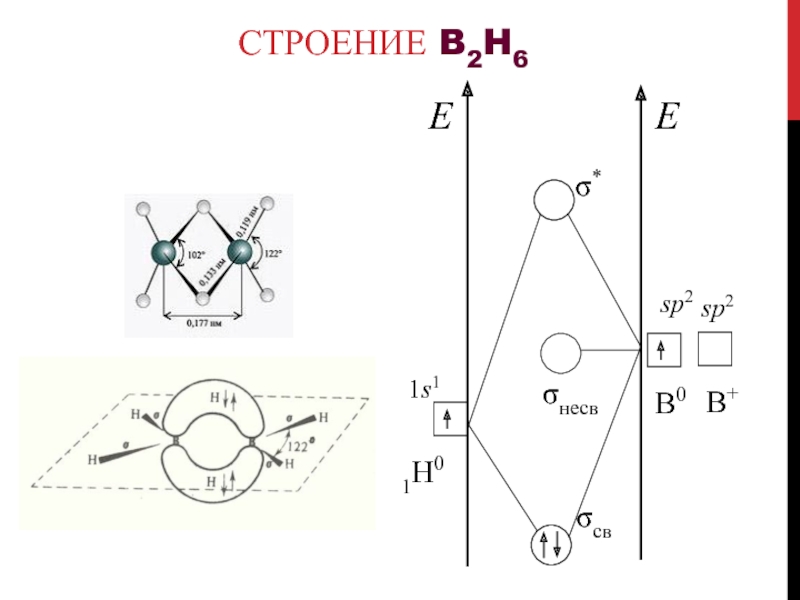
Слайд 17Строение бора
В основе кристаллического
строения бора лежит икосаэдр В12
d(B-B) = 173
пм
в икосаэдре В12
d(B-B) = 202 пм
между икосаэдрами В12
Новая форма бора
- ионный бор
высокого давления ( В2 + В12 )
Слайд 18ПОЛУЧЕНИЕ
Наиболее чистый бор получают пиролизом:
B2H6 = 2B + 3H2
Термическое разложение
паров бромида бора на раскаленной (1000—1200°С) танталовой проволоке в присутствии
водорода:
2BBr3 + 3H2 = 2B + 6HBr
Метод металлотермии (чаще восстановление
магнием или натрием):
B2O3 + 3Mg = 3MgO + 2B ΔG= −525 кДж
KBF4 + 3Na = 3NaF + KF + B ΔG= −377 кДж
Слайд 20 1808 году Хэмфри Дэви получил сплав алюминия с железом. Он
писал: «Если бы мне посчастливилось получить металлическое вещество, которое я ищу, я бы предложил
для него название — алюминий».
Впервые алюминий был получен датчанином Гансом Эрстедом в 1825 году действием амальгамы калия на хлорид алюминия с последующей отгонкой ртути.
Название элемента образовано от латинского aluminis — квасцы.
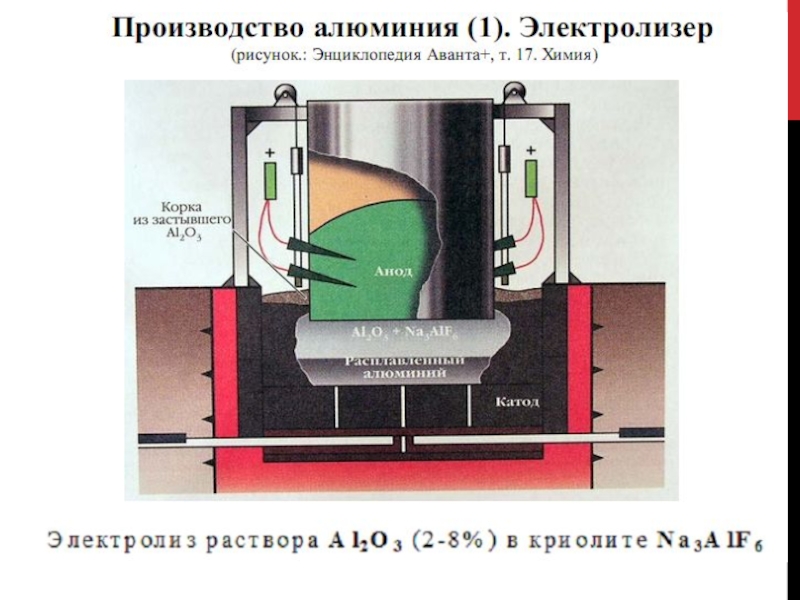
Слайд 23 Температуру ванны поддерживают в пределах 950—970°С за счет тепла,
выделяющегося при прохождении постоянного тока через электролит.
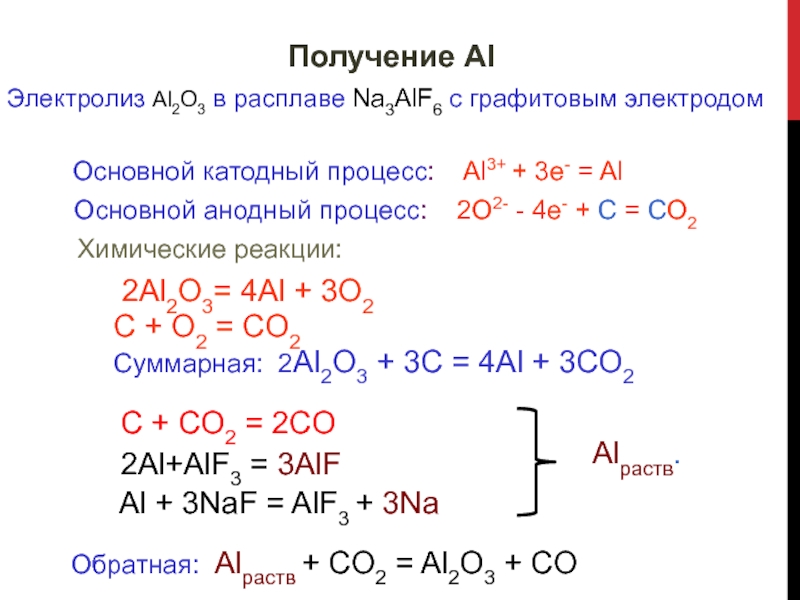
Слайд 24Получение Al
Электролиз Al2O3 в расплаве Na3AlF6 с графитовым электродом
Основной катодный
процесс: Al3+ + 3e- = Al
Основной анодный процесс:
2O2- - 4e- + C = CO2
Химические реакции:
2Al2O3= 4Al + 3O2
C + O2 = CO2
Суммарная: 2Al2O3 + 3C = 4Al + 3CO2
C + CO2 = 2CO
2Al+AlF3 = 3AlF
Alраств.
Al + 3NaF = AlF3 + 3Na
Обратная: Alраств + CO2 = Al2O3 + CO
Слайд 25Производительность современных электролизных ванн составляет 500—1200 кг алюминия в
сутки. Для получения 1 т алюминия расходуется:
1,95 т глинозема,
25 кг криолита,
25 кг фтористого алюминия,
0,5—0,6 т анодной массы,
14—16 МВт • ч электроэнергии.
Слайд 26Галлий, индий, таллий
В 1875 году Лекок де
Буабодран исследовал спектр цинковой обманки. В этом спектре и была
обнаружена новая фиолетовая линия. После длительных опытов удалось получить новый элемент, но в очень небольшом количестве, что не позволило изучить его физические и химические свойства.
Он назвал элемент в честь своей родины Франции, по её латинскому названию — Галлия (Gallia). Символ Франции — петух (по-французски — le coq), так что в названии элемента его первооткрыватель неявно увековечил и свою фамилию. Кроме того на латыни «петух» — gallus.
Слайд 28Индий был обнаружен Фердинандом Рейхом и Теодором Рихтером в 1863 году при
спектроскопическом исследовании цинковой обманки. Спектроскопическая линия индия — цвета индиго. Отсюда
и происхождение названия.
Таллий был открыт спектральным методом в 1861 году английским ученым Уильямом Круксом. Название элемент получил по характерным зеленым линиям своего спектра и зеленой окраске пламени. От греч. θαλλος — молодая, зелёная ветвь.
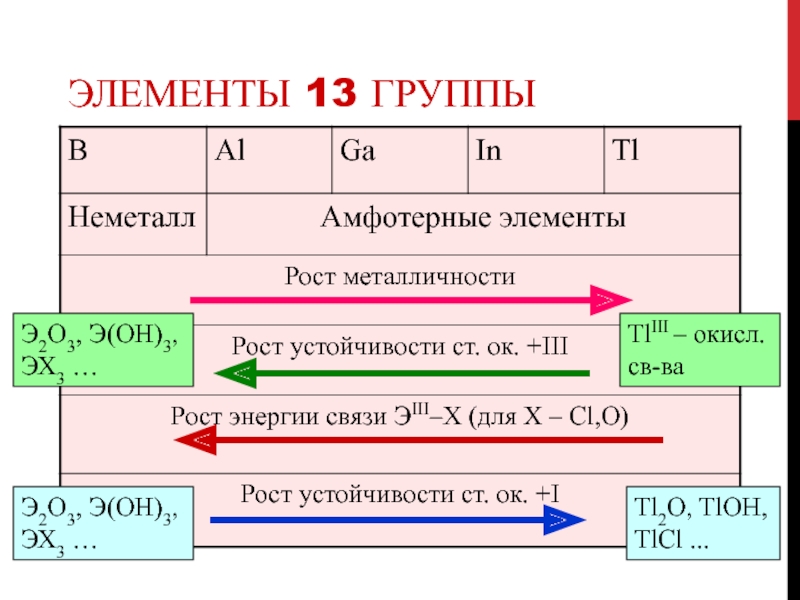
Слайд 29Элементы 13 группы
Tl2O, TlOH, TlCl ...
TlIII – окисл. св-ва
Э2O3,
Э(OH)3, ЭХ3 …
Э2O3, Э(OH)3, ЭХ3 …
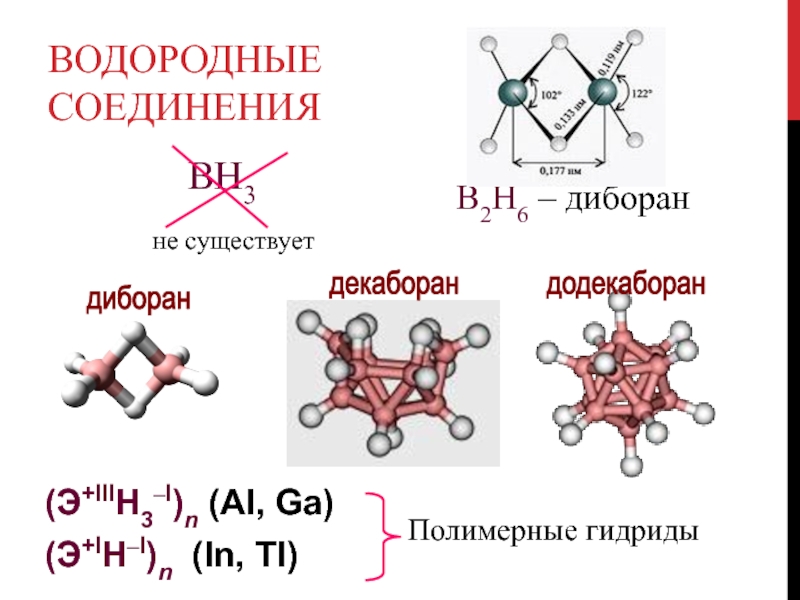
Слайд 30Водородные соединения
(Э+IIIН3–I)n (Al, Ga)
(Э+IН–I)n (In, Tl)
BH3
B2H6
– диборан
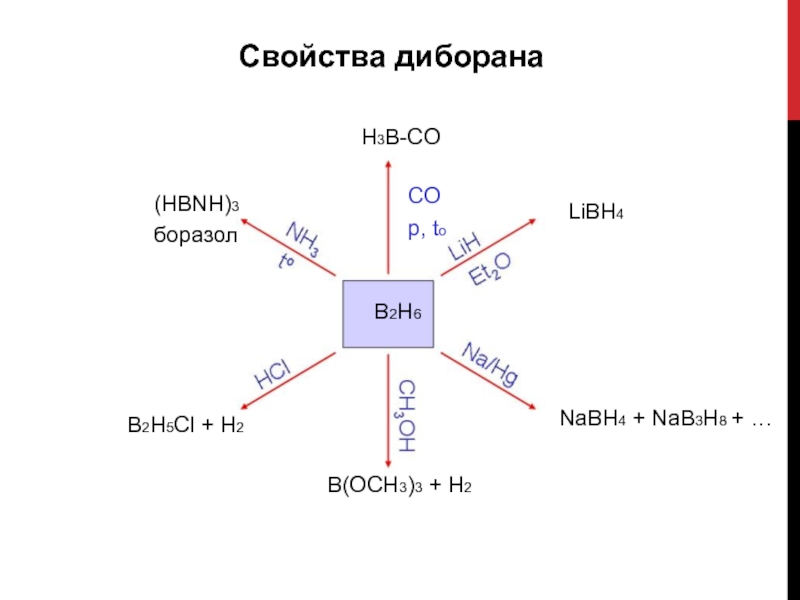
Слайд 31Свойства диборана
H3B-CO
(HBNH)3
боразол
B2H5Cl + H2
CO
p, to
B2H6
B(OCH3)3 + H2
LiBH4
NaBH4 + NaB3H8 +
…
Слайд 33Гидридные комплексы
Na[BH4] – тетрагидридоборат натрия
Li[AlH4] – тетрагидридоалюминат лития
Восстановительные свойства
[AlH4]
+ 4H2O = [Al(OH)4] + 4H2
Li[AlH4] + RCHO = RCH2OH
+ LiOH + Al(OH)3
ЭН3 + H– = [ЭH4]
B Al Ga In Tl
Слайд 34Химические свойства простых веществ
B + 3HNO3 = B(OH)3 +
3NO2
4B + 4NaOH(т) + 3O2 = 4NaBO2 + 2H2O
(сплавление)
2Ga + 6H3O+ + 6H2O = 2[Ga(H2O)6]3+ + 3H2
2Ga + 2OH + 6H2O = 2[Ga(OH)4] + 3H2
Слайд 35Простые вещества
ЭГ3 (Al2Cl6)
Э2О3 (Tl2O)
Э2S3 (Tl2S)
Э3+ + H2 [Al(H2O)6]3+
(Al In)
[Э(OH)4]– + H2 [Al(H2O)2(OH)4]– (Al In)
Э13
Слайд 36Кислородные соединения
Э2O3(т) + 2NaOH (т) = 2NaЭO2(т) + H2O(г)
(Э = B Tl,
сплавление)
Э2O3(т) + 6H3O+(р) = 2Э3+(р) + 9H2O
(Э = Al Tl)
Э2О3
B Al Ga In Tl
Tl2O – основный оксид, TlOH – сильное основание
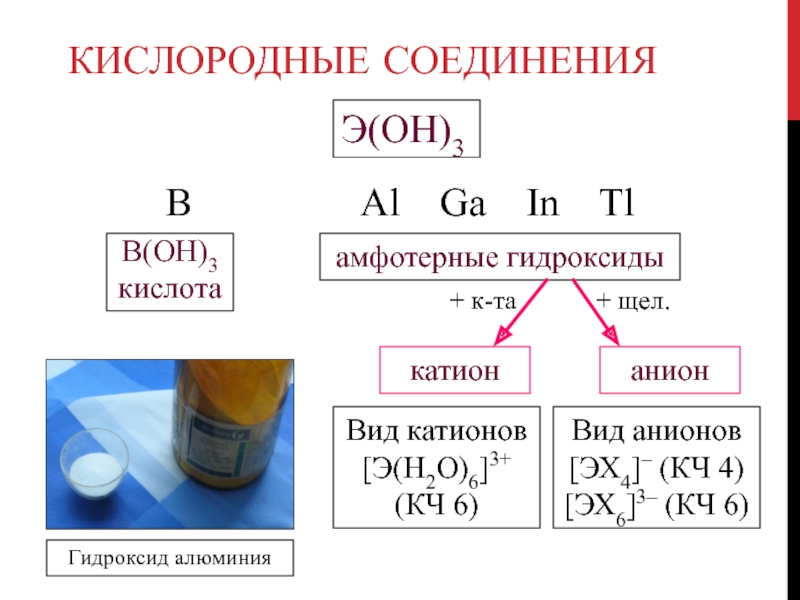
Слайд 37Кислородные соединения
Э(OH)3
B
Al Ga In Tl
B(OH)3 кислота
амфотерные гидроксиды
катион
анион
Вид
катионов [Э(H2O)6]3+ (КЧ 6)
Вид анионов [ЭХ4]– (КЧ 4) [ЭХ6]3– (КЧ 6)
Слайд 38Кислородные соединения бора
B2O3 – кислотный оксид
B2O3 + 3H2O =
2B(OH)3
Гидроксид бора B(OH)3 (борная кислота)
Растворение и гидратация:
B(OH)3(т) +
H2O = [B(H2O)(OH)3](р)
Протолиз
[B(H2O)(OH)3] + H2O [B(OH)4] + H3O+
Слайд 39Строение B(OH)3 и [B(H2O)(OH)3]
t°
t° t°
B(OH)3 (HBO2)3 (HBO2)n B2O3
–H2O –H2O –H2O
sp2-гибр.
sp3-гибр.
: OH2
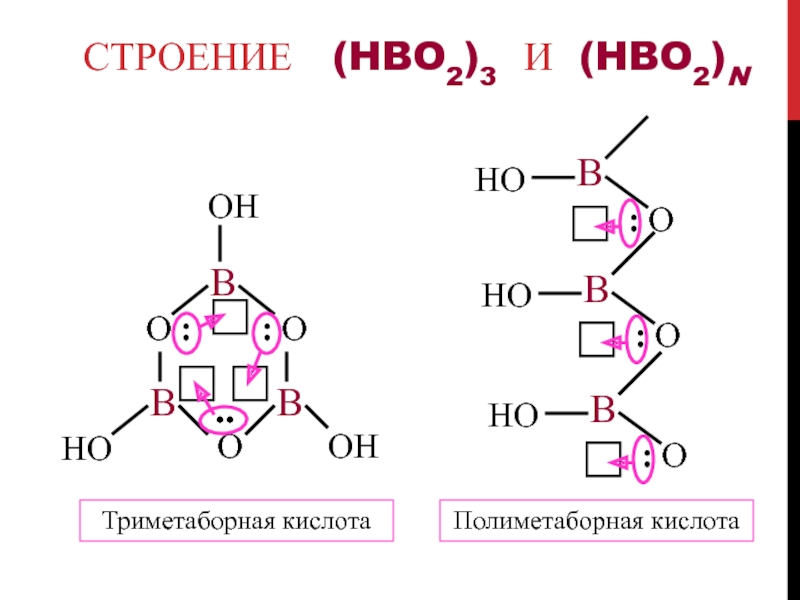
Слайд 40Строение (HBO2)3 и (HBO2)n
Триметаборная кислота
Полиметаборная кислота
Слайд 41Тетраборат натрия Na2B4O7·10H2O (бура)
Na2B4O7 + 2H2O = 2Na+ + [B4O72–
· 2H2O]
(диссоциация и гидратация)
Слайд 42Гидролиз тетрабората натрия
[B4O5(OH)4] 2 + 2H2O 4B(OH)3 ·H2O +
2OH–
pH > 7
Слайд 43Получение B(OH)3
BCl3 + 3H2O = B(OH)3 + 3HCl
(лаб.)
Na2B4O7 + H2SO4 + 5H2O =
= 4B(OH)3 +
Na2SO4 (лаб., пром.)
Слайд 44Обнаружение соединений бора
Na2B4O7 + 12C2H5OH + 2H2SO4 =
=
4B(OC2H5)3 + 7H2O + 2NaHSO4
2B(OC2H5)3 + 18 O2 =
B2O3 + 15H2O + 12CO2
Получение и горение борноэтилового эфира.
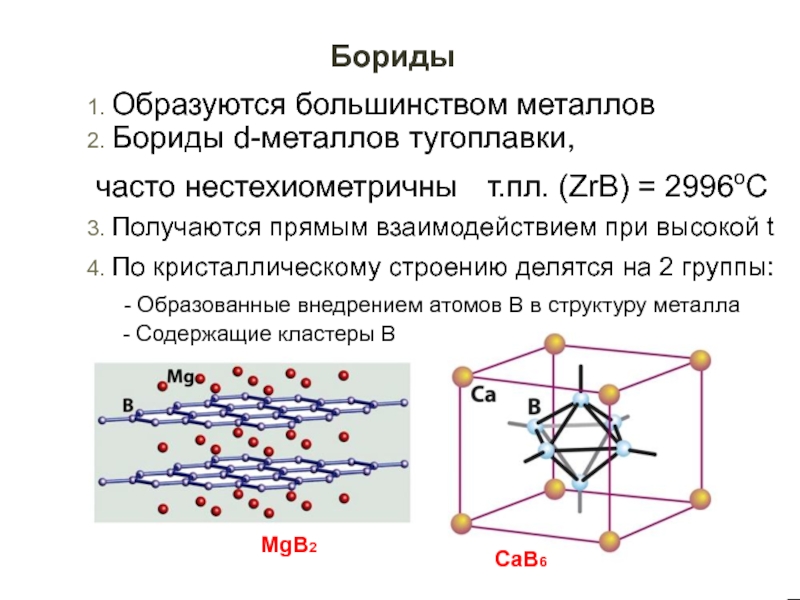
Слайд 45Бориды
1. Образуются большинством металлов
2. Бориды d-металлов тугоплавки,
часто нестехиометричны т.пл.
(ZrB) = 2996оС
3. Получаются прямым взаимодействием при высокой t
4. По
кристаллическому строению делятся на 2 группы:
- Образованные внедрением атомов B в структуру металла
- Содержащие кластеры В
MgB2
CaB6
Слайд 46Алюминий
Al2Г6
Al2О3
Al2S3
Al3+ + H2
[Al(OH)4]– + H2
AlN
Al(OH)3 + H2
Al
Слайд 47Окисление амальгамированного алюминия
Алюминиевая ложка, погруженная в раствор Hg(NO3)2, покрывается амальгамой
– сплавом Al и Hg.
Алюминий теряет защитную оксидную плёнку и
окисляется, превращаясь в белые хлопья Al(OH)3.
Слайд 48 2Al + 6H3O+ + 6H2O = 2[Al(H2O)6]3+ + 3H2
2Al
+ 2OH + 6H2O = 2[Al(OH)4] + 3H2
2Al +
6H2O = 2Al(OH)3 + 3H2
В щелочной среде восст. св-ва сильнее:
8Al + 30 HNO3(оч. разб.) =
= 8Al(NO3)3 + 3NH4NO3 + 9H2O
8Al + 18H2O + 5KOH + 3KNO3 =
= 8K[Al(OH)4] + 3NH3
Слайд 49Al2O3 и Al(OH)3
Al3+ + 3 NH3·H2O
Al2O3
Al(OH)3 – амфолит:
Al(OH)3(т)
+ 3H2O [Al(H2O)3(OH)3](р)
[Al(H2O)3(OH)3] + H2O
[Al(H2O)2(OH)4]– +
H3O+
[Al(H2O)3(OH)3] + H2O
[Al(H2O)4(OH)2]+ + OH–
Слайд 50Формы существования AlIII в растворах
рН < 4 (изб. к-ты): [Al(H2O)6]3+
sp3d 2
(октаэдр)
рН > 4 (гидролиз):
[Al(H2O)6]3+ + H2O [Al(H2O)5OH]2+ + H3O+
рН > 7: [Al(H2O)2(OH)4 ] sp3d 2
(искаж. октаэдр)
рН > 7 (изб. щелочи): [Al(OH)4 ] sp3
(тетраэдр)
Слайд 55ХИМИЧЕСКИЕ СВОЙСТВА Ga, In, Tl
Характерная степень окисления Ga и
In +3, для Tl +1. От галлия к таллию увеличивается
активность. С углеродом и азотом эти элементы не взаимодействуют.
Галлий растворяется в смеси азотной и плавиковой кислот, легко растворяется в щелочах и даже в аммиаке:
2Ga + 2NaOH + 6H2O = 2Na[Ga(OH)4] + 3H2
2Ga + 2NH4OH + 6H2O = 2NH4[Ga(OH)4] + 3H2
Индий хорошо растворим и в кислотах и щелочах:
2In + 6HCl = 2InCl3 + 3H2
Слайд 56Таллий в щелочах не растворяется, хорошо растворим в кислотах:
Tl
+ 2HNO3 = TlNO3 + NO2
+ H2O
Оксиды Ga2O3, In2O3, Tl2O получают термическим разложением гидроксидов.
2Ga(ОН)3 = Ga2O3 + 3Н2О
Оксиды галлия и индия в воде не растворимы, Tl2O при взаимодействии с водой образует гидроксид TlOH - сильное основание
Tl2O + Н2О = 2TlОН
Слайд 57В чистом виде галлий применяется для изготовления высококачественных зеркал, в
полупроводниковой промышленности. Оксид галлия при добавлении в стекло дает эффект
высокого блеска.
Индий применяется в полупроводниковой технике и для изготовления сплавов особого назначения.
Таллий – в виде соединений в приборах ночного видения.
Слайд 58Общая характеристика элементов 14 группы.
Слайд 59Общая электронная формула:
[…] ns 2 (n–1)d 10np2
Валентные возможности:
С: 2, 4; Si, Ge, Sn, Pb: 2 6
Степени окисления: –IV, 0, +II, +IV
Устойчивые ст.ок.: С, Si, Ge, Sn: +IV
(PbIV – сильн.окисл.). Уст. ст.ок.: Pb: +II
Слайд 60Элементы 14 группы
Неметаллы
Амфотерные элементы
Слайд 61Распространение в природе и важнейшие минералы
2. Si 25,80%
(27,72% в литосфере)
13. C 0,087%
(0,032% в литосфере)
31. Sn
0,0035%
35. Pb 0,0018%
46. Ge 6 ·10–4% (РРЭ)
Кремний: кварц, яшма, агат, опал, силикаты, алюмосиликаты
Слайд 62Углерод: графит, алмаз, каменный уголь, нефть, природный газ, орг. в-ва,
карбонаты
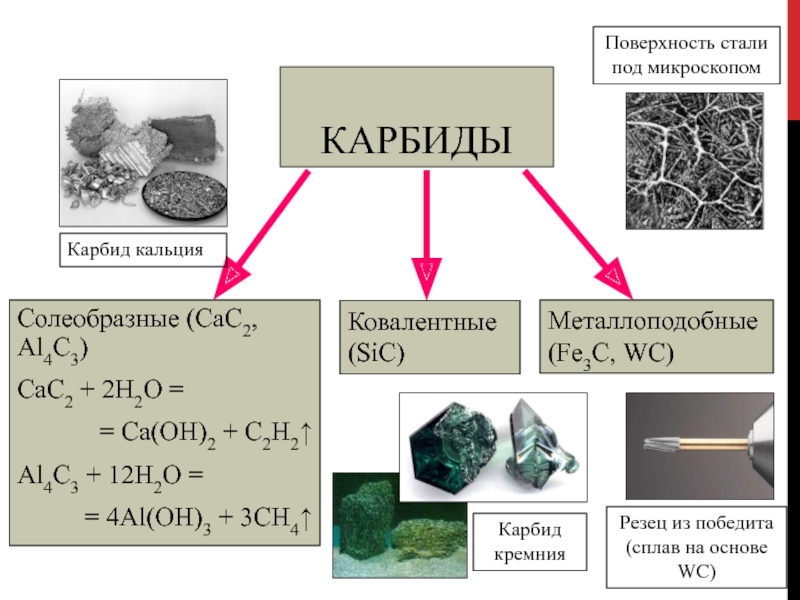
Слайд 64КРЕМНИЙ
В 1825 году шведский химик Йенс Якоб Берцелиус действием металлического калия на фтористый кремний SiF4 получил чистый элементарный
кремний.
Новому элементу было дано название «силиций» (от лат. silex — кремень).
Русское
название «кремний» введено в 1834 году российский химиком Германом Ивановичем Гессом. В переводе c греческого kremnos — «утес, гора».
Слайд 65Кремний в природе содержится во многих минералах в виде оксида
SiO2, из которого элементарный кремний можно получить восстановлением магнием или
углеродом:
SiO2 + 2Mg = 2MgO + Si
В чистом виде кремний тверд, хрупок, имеет алмазоподобную структуру.
Слайд 66ГЕРМАНИЙ
Элемент был предсказан Д.И.Менделеевым (эка-кремний) и открыт в 1885 году немецким химиком Клеменсом Винклером
при анализе минерала - аргиродита Ag8GeS6.
Германий выделяют в виде оксида
GeO2,который восстанавливают водородом при 600 оС до простого вещества:
GeO2 + 2H2 = Ge + 2H2O
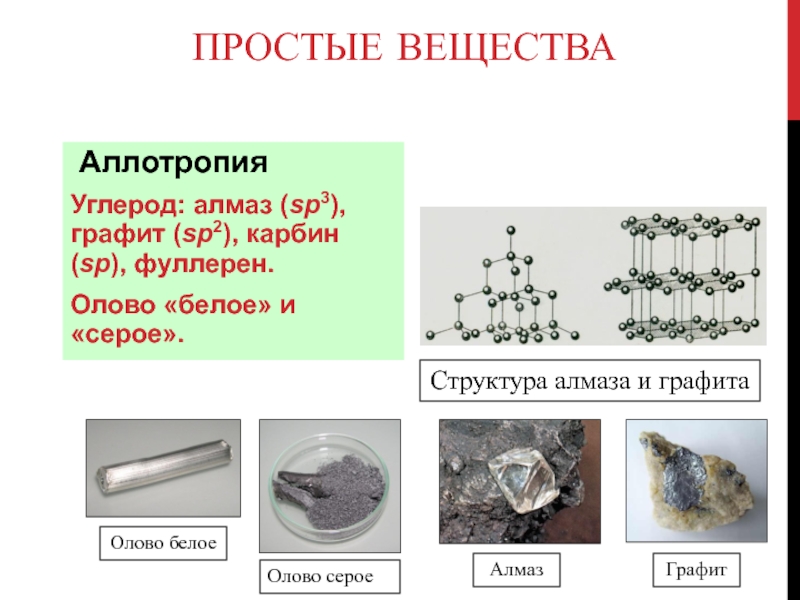
Слайд 67Простые вещества
Аллотропия
Углерод: алмаз (sp3), графит (sp2), карбин (sp), фуллерен.
Олово
«белое» и «серое».
Структура алмаза и графита
Слайд 68Графит
Т. пл. 3800 С, т. кип. 4000 С, плотность 2,27
г/см3, электропроводен, устойчив.
Типичный восст-ль (реагирует с водородом, кислородом, фтором, серой,
металлами).
Кристаллическая решетка слоистая (sp2-гибридизация).
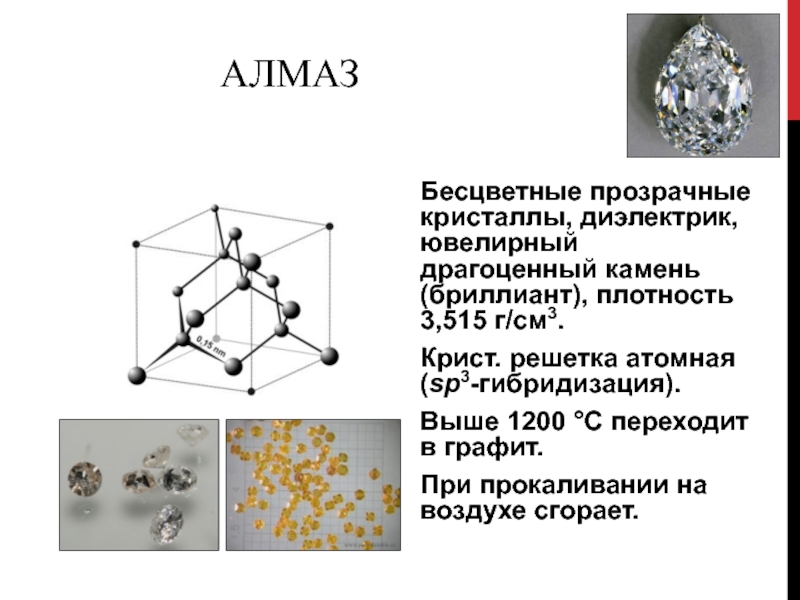
Слайд 69Алмаз
Бесцветные прозрачные кристаллы, диэлектрик, ювелирный драгоценный камень (бриллиант), плотность 3,515
г/см3.
Крист. решетка атомная (sp3-гибридизация).
Выше 1200 С переходит в графит.
При прокаливании на воздухе сгорает.
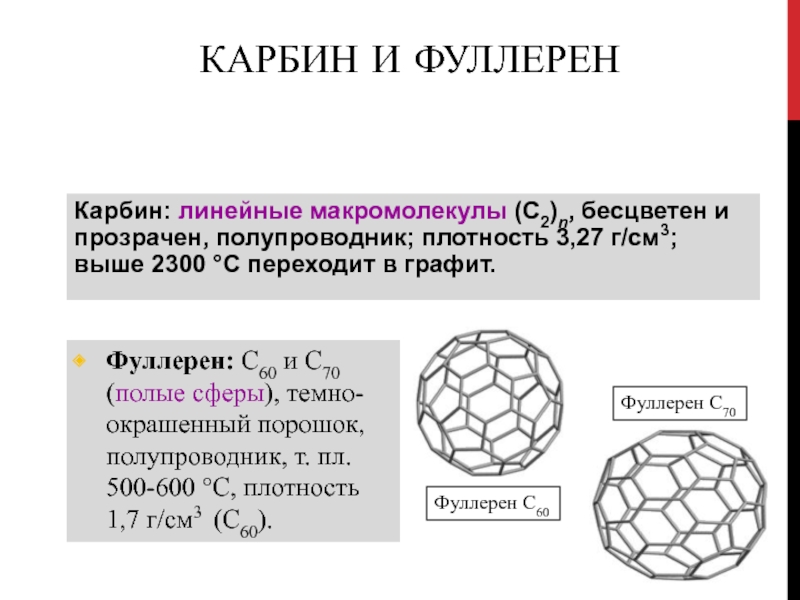
Слайд 70Карбин и фуллерен
Карбин: линейные макромолекулы (С2)n, бесцветен и прозрачен, полупроводник;
плотность 3,27 г/см3; выше 2300 С переходит в графит.
Фуллерен:
С60 и С70 (полые сферы), темно-окрашенный порошок, полупроводник, т. пл. 500-600 C, плотность 1,7 г/см3 (С60).
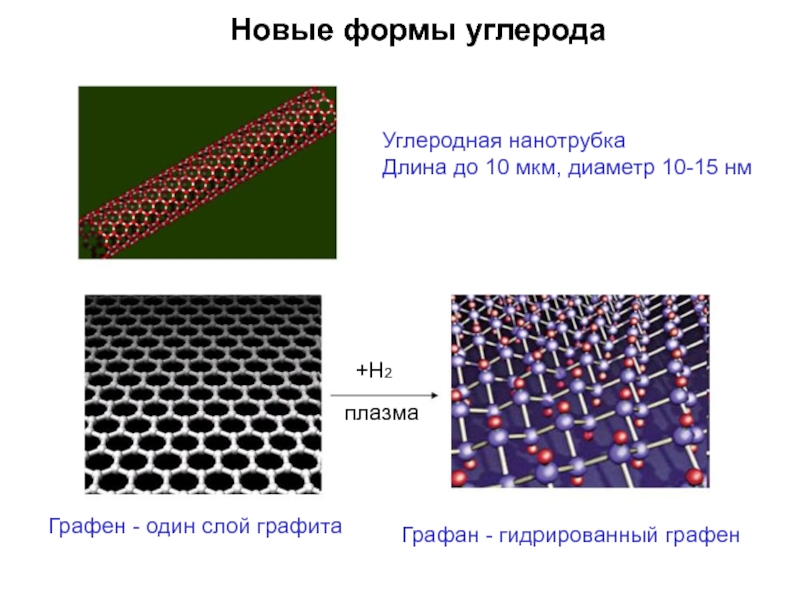
Слайд 71Новые формы углерода
Углеродная нанотрубка
Длина до 10 мкм, диаметр 10-15 нм
+Н2
плазма
Графен
- один слой графита
Графан - гидрированный графен
Слайд 72Новые формы углерода
Нобелевская премия по физике 2010 года
Андрей Гейм
Константин Новоселов
«За
новаторские эксперименты с двумерным материалом - графеном»
Слайд 73Химические свойства
При комнатной температуре
С, Si, Ge + H2O
С, Si,
Ge + H3O+
Sn, Pb + H2O
Sn + H3O+
Sn2+ + H2
Pb + H3O+ Pb2+ + H2
Слайд 74Химические свойства
С(т) + KOH
Si + 4NaOH = Na4SiO4 +
2H2
Si + 8OH– –4e – = SiO44– + 4H2O
2H2O +
2e – = H2 + 2OH–
Ge + 2KOH + 2H2O2 = K2[Ge(OH)6]
Ge + 6OH– –4e – = [Ge(OH)6]2–
H2O2 + 2e – = 2OH–
Sn + NaOH + 2H2O = Na[Sn(OH)3] + H2
Sn + 3OH– –2e – = [Sn(OH)3]–
2H2O + 2e – = H2 + 2OH–
Слайд 75Простые вещества
Э14
ЭГ2, ЭГ4 (Sn, Pb)
ЭO, ЭO2 (Sn, Pb)
ЭS, ЭS2
SiO44–
[Э(OH)3]– +
H2
(Sn, Рb)
Э2+ + H2 (Sn, Pb)
CO2, Pb2+, SnO2 ·
nH2O
Sn2+, Pb2+
Слайд 76Шкала степеней окисления углерода
CO2, CO32, H2CO3, Na2CO3, CS2, CF4,
CCl2O
CO, HCN, C2F4
C (графит, алмаз, карбин, фуллерен)
СH4, Be2C,
Al4C3, SiC
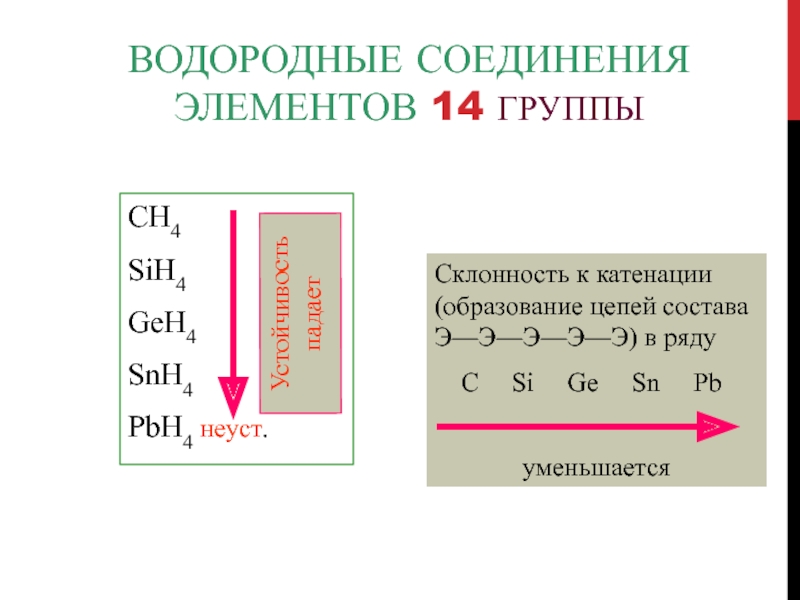
Слайд 77Водородные соединения элементов 14 группы
СH4
SiH4
GeH4
SnH4
PbH4 неуст.
Склонность к катенации (образование цепей
состава Э—Э—Э—Э—Э) в ряду
C Si
Ge Sn Pb
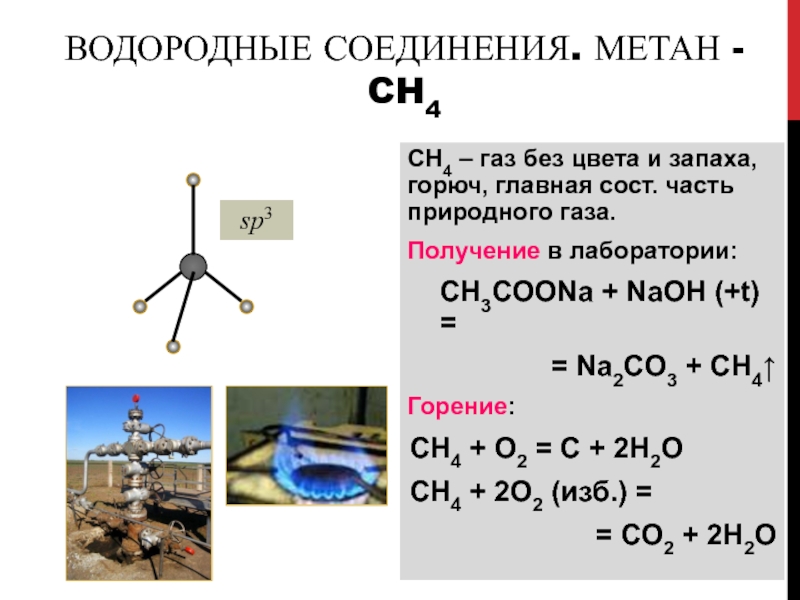
Слайд 78Водородные соединения. Метан - CH4
СН4 – газ без цвета
и запаха, горюч, главная сост. часть природного газа.
Получение в
лаборатории:
CH3COONa + NaOH (+t) =
= Na2CO3 + CH4
Горение:
CH4 + O2 = С + 2H2O
CH4 + 2O2 (изб.) =
= СO2 + 2H2O
sp3
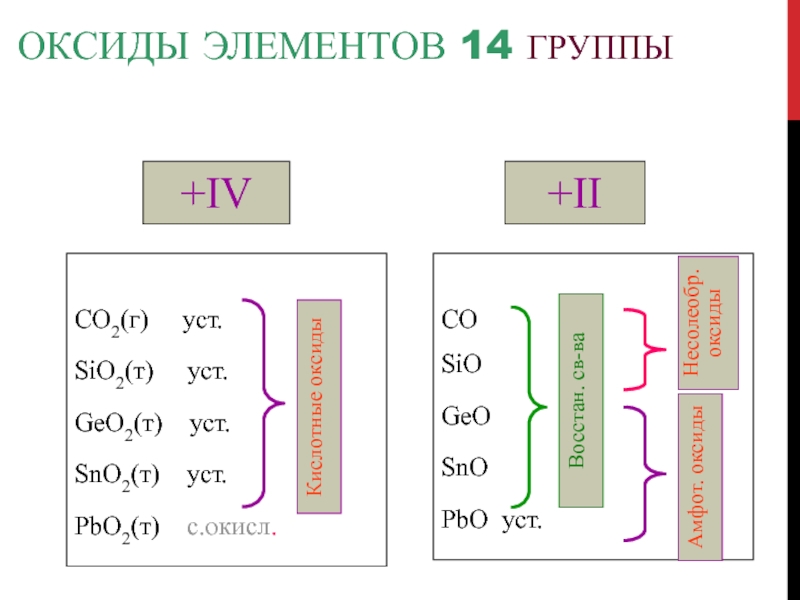
Слайд 80Оксиды элементов 14 группы
+IV
CO2(г) уст.
SiO2(т) уст.
GeO2(т)
уст.
SnO2(т) уст.
PbO2(т) с.окисл.
+II
CO
SiO
GeO
SnO
PbO уст.
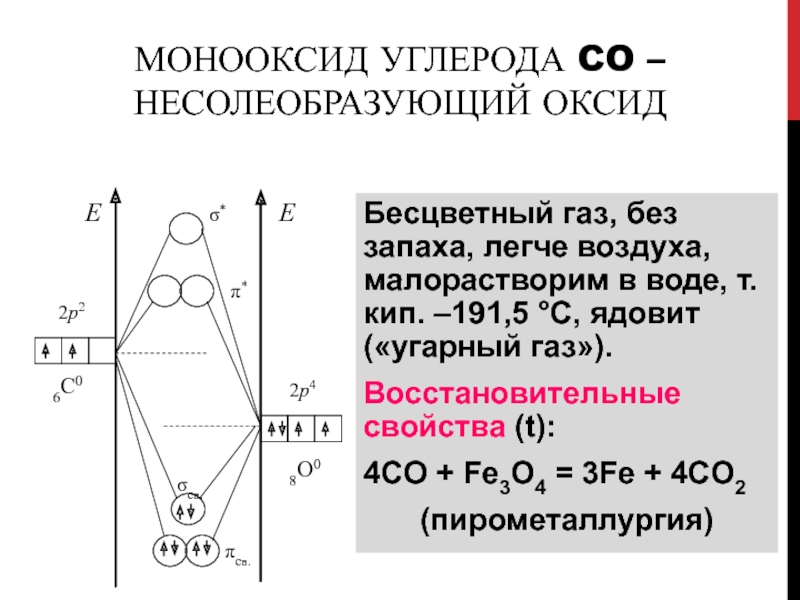
Слайд 81Монооксид углерода CO – несолеобразующий оксид
Бесцветный газ, без запаха,
легче воздуха, малорастворим в воде, т.кип. –191,5 С, ядовит («угарный
газ»).
Восстановительные свойства (t):
4CO + Fe3O4 = 3Fe + 4CO2
(пирометаллургия)
Слайд 82Монооксид углерода CO
Донорные свойства:
CO образует прочные комплексы, например [Fe(CO)5].
: C
::: O
Обнаружение:
PdCl2 + CO + H2O = Pd +
CO2 + 2HCl
I2O5 + 5CO = I2 + 5CO2
Слайд 83Диоксид углерода CO2 (кислотный оксид)
Бесцветный газ, без запаха, тяжелее воздуха,
умеренно растворим в воде (при комн. т-ре в 1 л
воды – около 1,7 л CO2).
В тв. сост. («сухой лёд») – молекулярная крист. решетка; т. возгонки –78 С, т.пл. –57 С (р = 5 атм).
sp-гибридизация
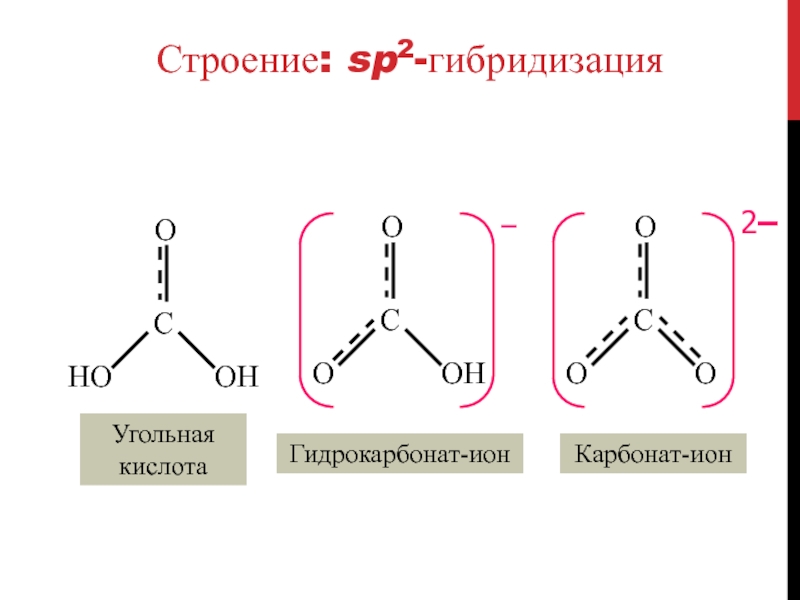
Слайд 84Моногидрат CO2 . H2O и
угольная кислота H2CO3
В водном
растворе:
CO2 (г) + H2O CO2 . H2O H2CO3
H2CO3 – слабая двухосновная кислота:
H2CO3 + H2O HCO3– + H3O+ ; KK = 4,27 · 10–7
HCO3– + H2O CO32– + H3O+ ; KK = 4,68 · 10–11
Соли – карбонаты и гидрокарбонаты M2CO3 и MHCO3 подвергаются гидролизу (рН > 7).
Термическое разложение гидрокарбонатов:
2NaHCO3 = Na2CO3 + CO2 + H2O
Слайд 87Псевдогалогениды
Циановодород HCN – бесцв.ж., т. пл. –13,3 С, т.кип.
+25,6С).
В водн. р-ре – слабая «синильная кислота»:
HCN + H2O
CN– + H3O+
KK = 4,93 · 10–10
Цианид-ион CN : донорные св-ва, образует прочные комплексы, ядовит.
: C:::N–
HCN – производное дициана C2N2
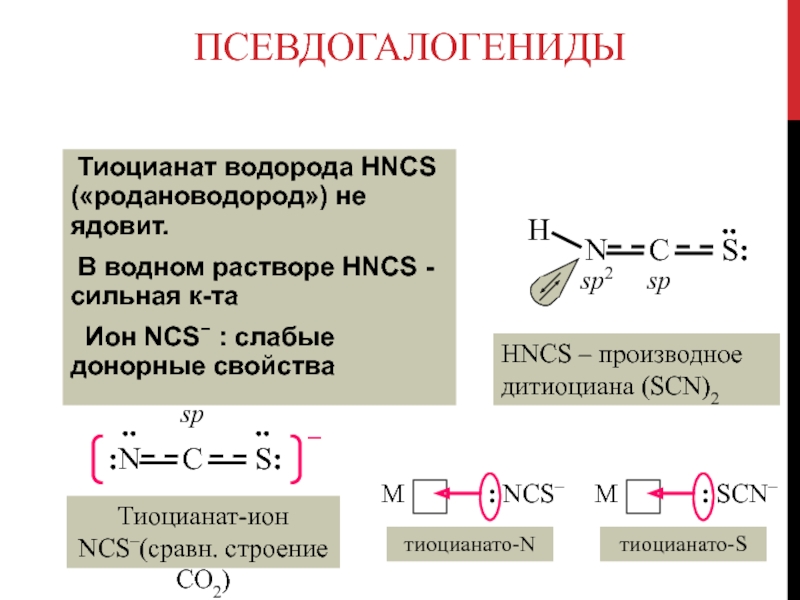
Слайд 89Псевдогалогениды
Тиоцианат водорода HNCS («родановодород») не ядовит.
В водном
растворе HNCS - сильная к-та
Ион NCS : слабые
донорные свойства
HNCS – производное дитиоциана (SCN)2
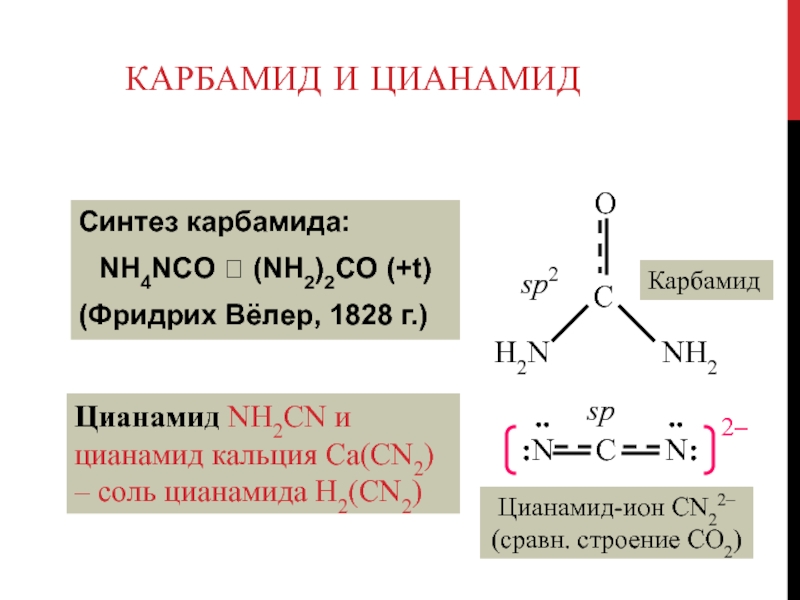
Слайд 91Карбамид и цианамид
Синтез карбамида:
NH4NCO (NH2)2CO (+t)
(Фридрих Вёлер,
1828 г.)
Цианамид NH2CN и цианамид кальция Ca(CN2) – соль цианамида
H2(CN2)
Слайд 93Кремний
Химическое растворение
3Si + 4HNO3 + 18HF = 3H2[SiF6] + 4NO
+ 8H2O
Si + 4NaOH = Na4SiO4 + 2H2
Получение кремния
SiO2 + 2Mg = 2MgO + Si
SiCl4 + 2H2 = Si + 4HCl (кремний ос.ч.)
Слайд 94Водородные соединения SinH2n+2 (силаны)
Моносилан SiH4:
SiH4 + 2O2 =
SiO2 + 2H2O
Получение силанов:
SiO2 + 4Mg(изб) = Mg2Si +
2MgO
(силицид магния)
Mg2Si + 4H2O = 2Mg(OH)2 + SiH4
Mg2Si + 4H3O+ = 2Mg2+ + 4H2O + SiH4
Слайд 95Кислородные соединения
Полиморфизм диоксида кремния:
кварц
тридимит
кристобалит
SiO2(ж) (расплав)
SiO2
GeO2
+ H2O
SiO2 + 4NaOH(р) = Na4SiO4 + 2H2O
(ортосиликат натрия)
GeO2 + 2NaOH(т) = Na2GeO3 + H2O (метагерманат натрия)
SiO2
GeO2
+ H3O+
Слайд 96Травление стекла
SiO2 + 4HF = SiF4 + 2H2O
SiO2 +
6HF (изб.) = H2[SiF6] + 2H2O
(гексафторосиликат водорода)
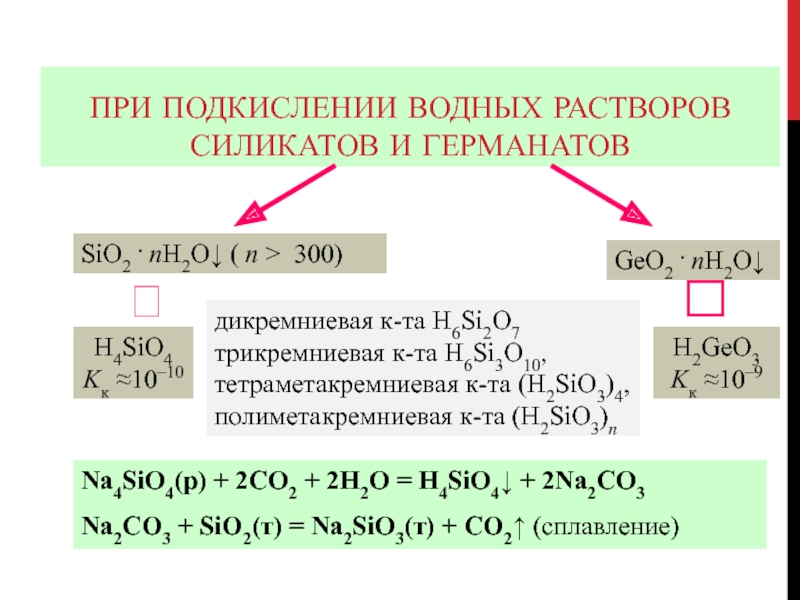
Слайд 97При подкислении водных растворов силикатов и германатов
SiO2 . nH2O (
n 300)
дикремниевая к-та H6Si2O7 трикремниевая к-та H6Si3O10, тетраметакремниевая
к-та (H2SiO3)4, полиметакремниевая к-та (H2SiO3)n
GeO2 . nH2O
H4SiO4 Kк 10–10
H2GeO3 Kк 10–9
Na4SiO4(р) + 2CO2 + 2H2O = H4SiO4 + 2Na2CO3
Na2CO3 + SiO2(т) = Na2SiO3(т) + CO2 (сплавление)
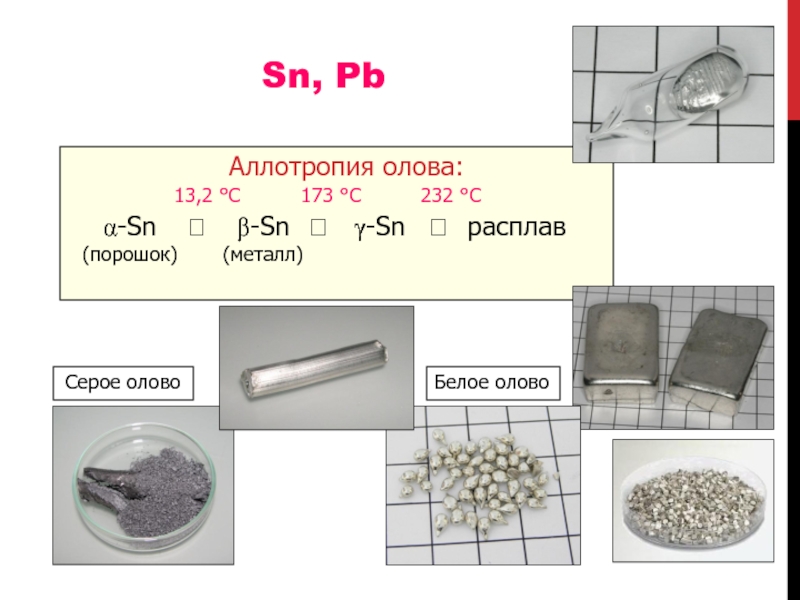
Слайд 100Sn, Pb
Аллотропия олова:
-Sn (порошок)
13,2 °С
-Sn (металл)
-Sn
173 °С
расплав
232
°С
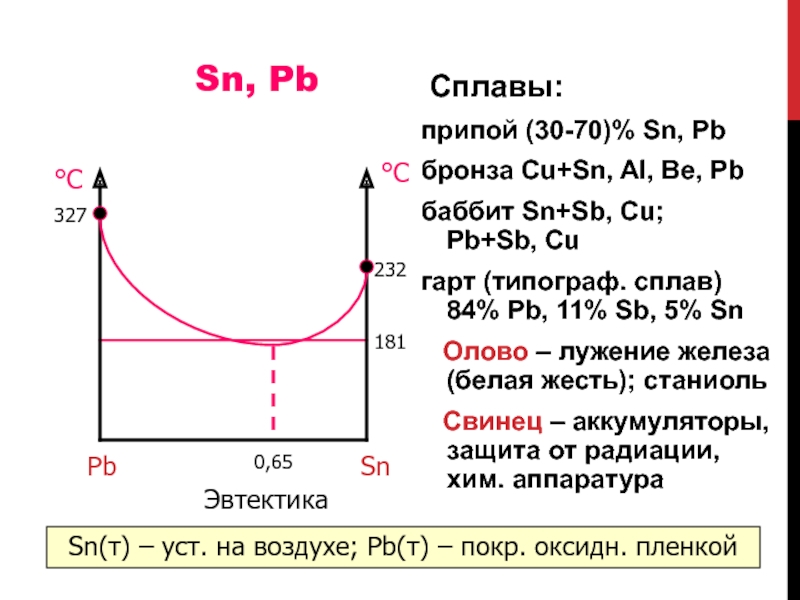
Слайд 101Sn, Pb
Cплавы:
припой (30-70)% Sn, Pb
бронза Cu+Sn, Al, Be, Pb
баббит Sn+Sb, Cu; Pb+Sb, Cu
гарт
(типограф. сплав) 84% Pb, 11% Sb, 5% Sn
Олово – лужение железа (белая жесть); станиоль
Свинец – аккумуляторы, защита от радиации, хим. аппаратура
181
232
327
Эвтектика
0,65
Sn(т) – уст. на воздухе; Pb(т) – покр. оксидн. пленкой
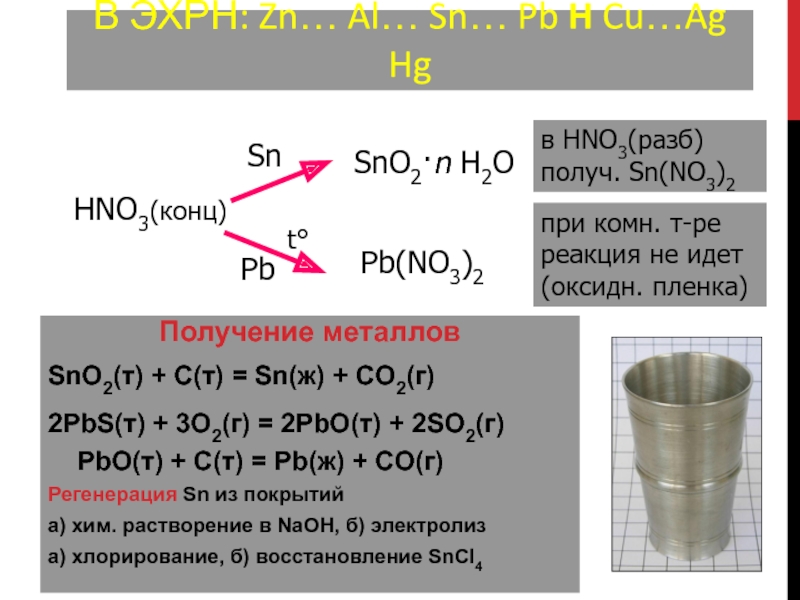
Слайд 102В ЭХРН: Zn… Al… Sn… Pb H Cu…Ag Hg
Получение металлов
SnO2(т)
+ C(т) = Sn(ж) + CO2(г)
2PbS(т) + 3O2(г) = 2PbO(т)
+ 2SO2(г)
PbO(т) + C(т) = Pb(ж) + CO(г)
Регенерация Sn из покрытий
а) хим. растворение в NaOH, б) электролиз
а) хлорирование, б) восстановление SnCl4
HNO3(конц)
SnO2·n H2O
Pb(NO3)2
при комн. т-ре реакция не идет (оксидн. пленка)
в HNO3(разб) получ. Sn(NO3)2
Слайд 103 ЭII Оксиды - ЭО
SnO
PbO (устойчив: глёт, массикот)
Sn(OH)2(т) +
2H3O+ = [Sn(H2O)3]2+ + H2O
Sn(OH)2(т) + OH = [Sn(OH)3]
Pb(OH)2 (т) + 2H3O+ = [Pb(H2O)3]2+ + H2O
Pb(OH)2(т) + OH = [Pb(OH)3]
Гидроксиды Sn(OH)2 и Pb(OH)2 малорастворимы и амфотерны:
Устойчивость ст.ок. +II растет
Слайд 104Соли SnII
Соли PbII
[Pb2+]: PbSO4 > PbCrO4 > PbS
PbSO4(т) + CrO42– = PbCrO4(т) + SO42–
белый
желтый
PbCrO4(т) + S2– = PbS(т) + CrO42–
жёлтый черный
Растворение осадков:
PbSO4(т) + H2SO4 = Pb(HSO4)2
2PbCrO4(т) + 4HNO3 = 2Pb(NO3)2 + H2Cr2O7 + H2O
PbCrO4(т) + 3NaOH = Na[Pb(OH)3] + Na2CrO4
Слайд 105 ЭIV Оксиды - ЭО2
амфотерн. с преобладанием кислотн. св-в
полигидраты ЭO2.n H2O (уст. при рН
= [Э(OH)6]2 + (n –2)H2O
Получение
SnCl4 + 2H2O = SnO2 + 4HCl
PbCl4 = PbCl2 + Cl2
(вода – катализатор ОВР)
SnO2 - устойч.
PbO2 - c. окислитель
Слайд 106Окислительно-восстановительные свойства
Sn2+ – мягкий восстановитель
рН < 7 (HCl):
[SnCl3]– + 3Cl– –2e – = [SnCl6]2–
рН > 7:
[Sn(OH)3] + 3OH 2e – = [Sn(OH)6]2
Sn2+ – слабый окислитель (восстановители – Ti3+, Cr2+)
рН < 7: (HCl): [SnCl3]– + 2e – = Sn(т) + 3Cl–
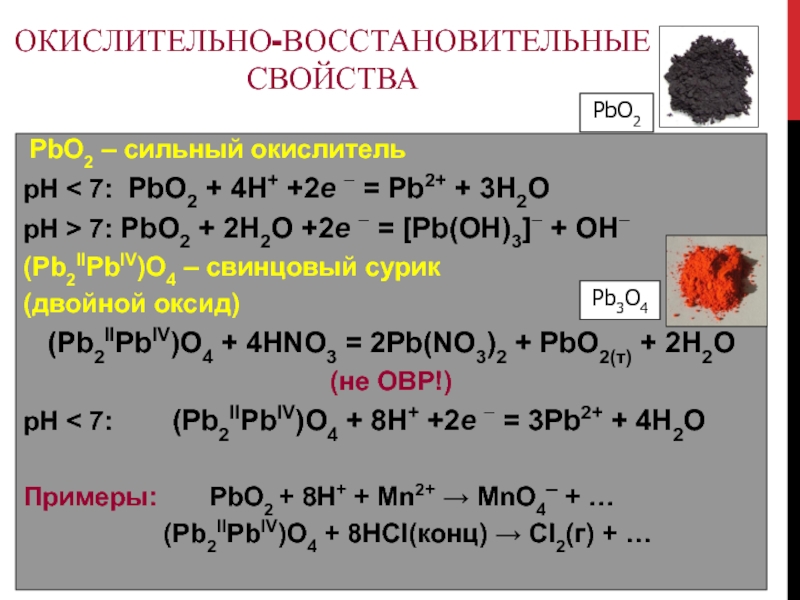
Слайд 107Окислительно-восстановительные свойства
PbO2 – сильный окислитель
рН < 7: PbO2 +
4H+ +2e = Pb2+ + 3H2O
рН > 7: PbO2
+ 2H2O +2e = [Pb(OH)3] + OH
(Pb2IIPbIV)O4 – свинцовый сурик
(двойной оксид)
(Pb2IIPbIV)O4 + 4HNO3 = 2Pb(NO3)2 + PbO2(т) + 2H2O
(не ОВР!)
рН < 7: (Pb2IIPbIV)O4 + 8H+ +2e = 3Pb2+ + 4H2O
Примеры: PbO2 + 8H+ + Mn2+ MnO4– + …
(Pb2IIPbIV)O4 + 8HCl(конц) Cl2(г) + …
Слайд 108Разделение олова и свинца (сульфидный метод)
Осаждение сульфидов (+H2S):
SnS(т)
PbS(т)
2. Растворение сульфида, образование Na2[SnS3] (тиокомплекс)
Na2S2: S–I +1e
– = S–II
SnS [SnS3]2– :
Sn+II –2e – = Sn+IV
3. Осаждение [SnS3]2– + 2H+ SnS2(т) + H2S
+Na2S2
+ HCl
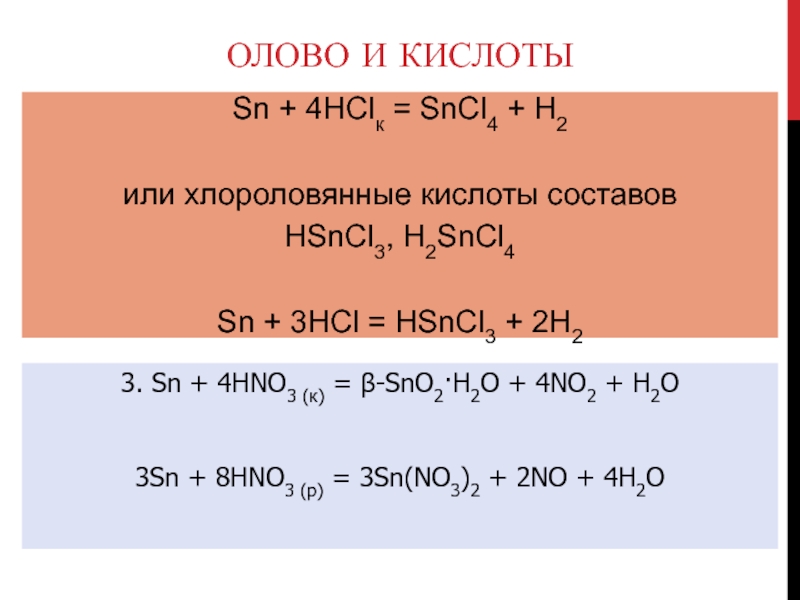
Слайд 109Олово и кислоты
3. Sn + 4HNO3 (к) = β-SnO2·H2O + 4NO2 + H2O
3Sn
+ 8HNO3 (р) = 3Sn(NO3)2 + 2NO + 4H2O
Sn + 4HClк
= SnCl4 + H2
или хлороловянные кислоты составов
HSnCl3, H2SnCl4
Sn + 3HCl = HSnCl3 + 2H2
Слайд 110SnCl4 + 4NH3 + 6H2O = H2[Sn(OH)6] + 4NH4Cl
H2[Sn(OH)6] = a-SnO2·nH2O + 3H2O
Свежеполученная a-оловянная
кислота амфотерна
a-SnO2·nH2O + KOH = K2[Sn(OH)6]
a-SnO2·nH2O + HNO3 = Sn(NO3)4 + H2O


![Химия р-элементов Общая характеристика p - элементовОбщая электронная формула:[…] ns 2(n–2)f 14(n–1)d 10np Общая характеристика p - элементовОбщая электронная формула:[…] ns 2(n–2)f 14(n–1)d 10np 16Степени окисления (от –IV до](/img/thumbs/a19fe0fb58cf31aa451d460a99807071-800x.jpg)



![Химия р-элементов Элементы 13 группы Общая электронная формула:[…] ns 2 (n –1)d 10 Элементы 13 группы Общая электронная формула:[…] ns 2 (n –1)d 10 np 1 Степени окисления: 0, +I,](/img/thumbs/8b6474bdf6fc062d5faeb3d0795bbcde-800x.jpg)















![Химия р-элементов Гидридные комплексыNa[BH4] – тетрагидридоборат натрияLi[AlH4] – тетрагидридоалюминат литияВосстановительные свойства [AlH4] + Гидридные комплексыNa[BH4] – тетрагидридоборат натрияLi[AlH4] – тетрагидридоалюминат литияВосстановительные свойства [AlH4] + 4H2O = [Al(OH)4] + 4H2Li[AlH4] +](/img/thumbs/07689eaf201f0f639a995e21b9620b1b-800x.jpg)

![Химия р-элементов Простые веществаЭГ3 (Al2Cl6)Э2О3 (Tl2O) Э2S3 (Tl2S) Э3+ + H2 [Al(H2O)6]3+ (Al Простые веществаЭГ3 (Al2Cl6)Э2О3 (Tl2O) Э2S3 (Tl2S) Э3+ + H2 [Al(H2O)6]3+ (Al In) [Э(OH)4]– + H2 [Al(H2O)2(OH)4]–](/img/thumbs/b0e83ce8d03575359a0c60ece33c2807-800x.jpg)


![Химия р-элементов Строение B(OH)3 и [B(H2O)(OH)3] t° Строение B(OH)3 и [B(H2O)(OH)3] t°](/img/thumbs/fc7bac6606e133285e703e657bf87bd2-800x.jpg)
![Химия р-элементов Тетраборат натрия Na2B4O7·10H2O (бура)Na2B4O7 + 2H2O = 2Na+ + [B4O72– · Тетраборат натрия Na2B4O7·10H2O (бура)Na2B4O7 + 2H2O = 2Na+ + [B4O72– · 2H2O]](/img/thumbs/a9e32fdfd969ba32daa244c6a92a1f56-800x.jpg)
![Химия р-элементов Гидролиз тетрабората натрия[B4O5(OH)4] 2 + 2H2O 4B(OH)3 ·H2O + 2OH–pH > 7 Гидролиз тетрабората натрия[B4O5(OH)4] 2 + 2H2O 4B(OH)3 ·H2O + 2OH–pH > 7](/img/thumbs/566dd6e6d5d4adac495f985355806b63-800x.jpg)


![Химия р-элементов Алюминий Al2Г6Al2О3Al2S3Al3+ + H2[Al(OH)4]– + H2AlNAl(OH)3 + H2Al Алюминий Al2Г6Al2О3Al2S3Al3+ + H2[Al(OH)4]– + H2AlNAl(OH)3 + H2Al](/img/thumbs/5ba5ab1cce4ca195bb7e910c68e5e2cf-800x.jpg)

![Химия р-элементов 2Al + 6H3O+ + 6H2O = 2[Al(H2O)6]3+ + 3H22Al + 2Al + 6H3O+ + 6H2O = 2[Al(H2O)6]3+ + 3H22Al + 2OH + 6H2O = 2[Al(OH)4] +](/img/thumbs/c395ae65cc36c11c16b88c6c680e0661-800x.jpg)
[Al(H2O)3(OH)3] + H2O ](/img/thumbs/b12e2b45320cb3c912fd42072da71ea6-800x.jpg)
![Химия р-элементов Формы существования AlIII в растворахрН < 4 (изб. к-ты): [Al(H2O)6]3+ sp3d Формы существования AlIII в растворахрН < 4 (изб. к-ты): [Al(H2O)6]3+ sp3d 2](/img/thumbs/6c81c85ff2f7b08b037579f96e27748f-800x.jpg)








![Химия р-элементов Общая электронная формула: […] ns 2 (n–1)d 10np2Валентные возможности: Общая электронная формула: […] ns 2 (n–1)d 10np2Валентные возможности:](/img/thumbs/66563a5615588a5e4266c785b4f9edb5-800x.jpg)











![Химия р-элементов Простые веществаЭ14ЭГ2, ЭГ4 (Sn, Pb)ЭO, ЭO2 (Sn, Pb)ЭS, ЭS2SiO44–[Э(OH)3]– + H2 Простые веществаЭ14ЭГ2, ЭГ4 (Sn, Pb)ЭO, ЭO2 (Sn, Pb)ЭS, ЭS2SiO44–[Э(OH)3]– + H2 (Sn, Рb)Э2+ + H2 (Sn, Pb)CO2,](/img/thumbs/379d22a9d138eb4d79048cf1ea08f5e4-800x.jpg)

![Химия р-элементов Монооксид углерода COДонорные свойства:CO образует прочные комплексы, например [Fe(CO)5].: C ::: Монооксид углерода COДонорные свойства:CO образует прочные комплексы, например [Fe(CO)5].: C ::: O Обнаружение:PdCl2 + CO + H2O](/img/thumbs/af9632b7078d89c23f800100757fe302-800x.jpg)






![Химия р-элементов КремнийХимическое растворение3Si + 4HNO3 + 18HF = 3H2[SiF6] + 4NO + КремнийХимическое растворение3Si + 4HNO3 + 18HF = 3H2[SiF6] + 4NO + 8H2OSi + 4NaOH = Na4SiO4 +](/img/thumbs/a6b5ebd5bcb173bece1e01d44d5ed713-800x.jpg)


![Химия р-элементов Травление стекла SiO2 + 4HF = SiF4 + 2H2OSiO2 + 6HF Травление стекла SiO2 + 4HF = SiF4 + 2H2OSiO2 + 6HF (изб.) = H2[SiF6] + 2H2O (гексафторосиликат](/img/thumbs/8f1accd54360cc3abe0a3d857f44774e-800x.jpg)


![Химия р-элементов ЭII Оксиды - ЭОSnOPbO (устойчив: глёт, массикот) Sn(OH)2(т) + 2H3O+ = ЭII Оксиды - ЭОSnOPbO (устойчив: глёт, массикот) Sn(OH)2(т) + 2H3O+ = [Sn(H2O)3]2+ + H2O Sn(OH)2(т) +](/img/thumbs/a925f2d2ea6e22652825fc63efa968e8-800x.jpg)
![Химия р-элементов Соли SnII Соли PbII [Pb2+]: PbSO4 > PbCrO4 > PbS PbSO4(т) Соли SnII Соли PbII [Pb2+]: PbSO4 > PbCrO4 > PbS PbSO4(т) + CrO42– = PbCrO4(т) + SO42–](/img/thumbs/c918113b643d76965dffef804ba955de-800x.jpg)

![Химия р-элементов Окислительно-восстановительные свойстваSn2+ – мягкий восстановительрН < 7 (HCl): [SnCl3]– + Окислительно-восстановительные свойстваSn2+ – мягкий восстановительрН < 7 (HCl): [SnCl3]– + 3Cl– –2e – =](/img/thumbs/4f3f8b06d3e8013c63657bed0fef14fa-800x.jpg)
![Химия р-элементов Разделение олова и свинца (сульфидный метод)Осаждение сульфидов (+H2S):SnS(т) PbS(т)2. Разделение олова и свинца (сульфидный метод)Осаждение сульфидов (+H2S):SnS(т) PbS(т)2. Растворение сульфида, образование Na2[SnS3]](/img/thumbs/94ba5866e1252fb0822eee630b2e91c4-800x.jpg)
![Химия р-элементов SnCl4 + 4NH3 + 6H2O = H2[Sn(OH)6] + 4NH4ClH2[Sn(OH)6] = a-SnO2·nH2O + 3H2OСвежеполученная a-оловянная кислота SnCl4 + 4NH3 + 6H2O = H2[Sn(OH)6] + 4NH4ClH2[Sn(OH)6] = a-SnO2·nH2O + 3H2OСвежеполученная a-оловянная кислота амфотернаa-SnO2·nH2O + KOH = K2[Sn(OH)6]a-SnO2·nH2O +](/img/thumbs/d6a01696fff7eb288c9a4b92d37e31a5-800x.jpg)