Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ИК у новорожденных
Содержание
- 1. ИК у новорожденных
- 2. Искусственное кровообращение подразумевает экстракорпоральный контур, который обеспечивает
- 3. Первую операцию с помощью функционирующего аппарата искусственного
- 4. Слайд 4
- 5. ОЦК у детей маленький, поэтому диаметр магистралей
- 6. Слайд 6
- 7. Начало перфузииГепарин вводится в дозе 3 мг/кг.
- 8. канюляция Канюлю обычно устанавливается в восходящей аорте
- 9. Слайд 9
- 10. Нормы среднего артериального давления во время перфузии у детей
- 11. У новорожденных рО2а не должно превышать
- 12. Слайд 12
- 13. Во время перфузии у детей раннего возраста
- 14. Первичный объем заполнения равен 30% от ОЦКОбъемная
- 15. Расчет гематокритаКак правило, используется стандартная техника первичного
- 16. Расчет уровня фибриногенаМинимальный уровень фибриногена во время
- 17. Расчет коллоидного осмотического давленияНормальное коллоидно-осмотическое давление равно
- 18. ОПл – объем добавленной донорской плазмыОАл –
- 19. Для удобства расчета объема компонентов первичного заполнения
- 20. Лекарственные препараты
- 21. При достижении расчетной скорости, адекватного артериального давления,
- 22. В детской кардиохирургии применяют более глубокую гипотермию,
- 23. Степень охлаждения определяется характером и объёмом оперативного
- 24. Окклюзия аортыНепосредственно в момент наложения зажима на
- 25. В зависимости от объёма вмешательства, степени снижения
- 26. Состав кровяной кардиоплегииСостав на 1 литр раствора
- 27. Функция почекНормальная функция почек – показатель адекватности
- 28. СогреваниеСогревание начинается по команде оперирующего хирурга после
- 29. Окончание перфузииВремя реперфузии составляет не менее 10 минут.
- 30. Циркуляторный арестОборудование, канюли и подготовка к перфузии
- 31. Показания к циркуляторному арестуНевозможность хирургической коррекции в
- 32. Безопасная длительность ареста по данным большинства авторов
- 33. Low flowОборудование, канюли и подготовка к перфузии
- 34. Показания к low flowНевозможность хирургической коррекции в
- 35. После команды хирурга перфузиолог снижает объемную скорость
- 36. МОДИФИЦИРОВАННАЯ УЛЬТРАФИЛЬТРАЦИЯМУФ проводится после остановки искусственного кровообращения
- 37. Показания к проведению МУФ:ИК у детей первого
- 38. Осложнения. Эмболия сосудов Эмболия сосудов головного мозга,
- 39. Осложнения. Эмболия сосудов Эмболия сосудов головного мозга
- 40. Осложнения. Гипоксия Гипоксия жизненно важных органов может
- 41. Гематологические осложнения Гематологические осложнения могут быть вызваны
- 42. Гематологические осложнения Более редким, но опасным осложнением
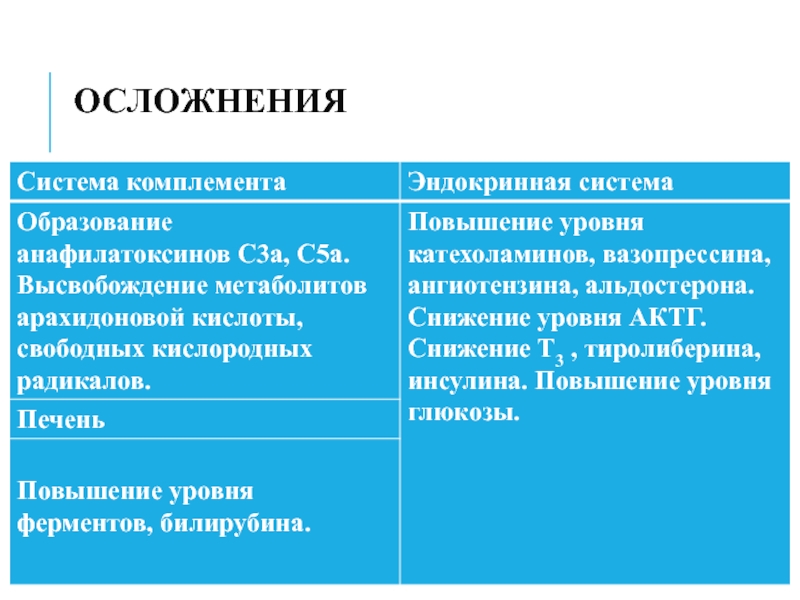
- 43. Осложнения
- 44. Осложнения
- 45. Скачать презентанцию
Искусственное кровообращение подразумевает экстракорпоральный контур, который обеспечивает системный кровоток в организме в то время, когда сердце и легкие не функционируют.Организм ребенка имеет много анатомических и физиологических отличий от организма взрослого. Сердце
Слайды и текст этой презентации
Слайд 1ИК у новорожденных
Резидент второго года обучения по специальности «Анестезиология и
реанимация» Ильясова А.Т.
Слайд 2Искусственное кровообращение подразумевает экстракорпоральный контур, который обеспечивает системный кровоток в
организме в то время, когда сердце и легкие не функционируют.
Организм
ребенка имеет много анатомических и физиологических отличий от организма взрослого. Сердце у детей относительно больше, чем у взрослых, ОЦК меньше, сосуды более эластичны. Мозговой кровоток новорожденного составляет 34% от системного, значительно больше чем у взрослого. Частота дыхания новорожденного доходит до 40 в 1 мин. Гипотермия при педиатрических операциях значительно глубже, а уровень метаболизма выше.Слайд 3Первую операцию с помощью функционирующего аппарата искусственного кровобращения выполнил американский
хирург Gibbon в 1953 году (закрытие ДМПП у маленькой девочки).
Аппарат
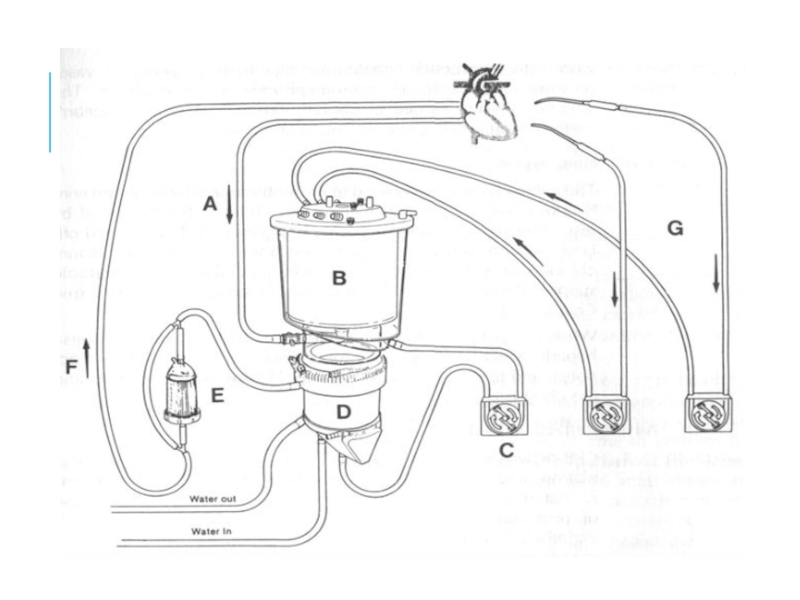
искусственного кровообращения состоит из:Оксигенатора (искусственного лёгкого): 1) пузырьковые и пленочные. 2) мембранные
Теплообменника, обеспечивающего поддержание необходимого температурного режима (трубчатый и щелевой),
Регулируемого артериального насоса (искусственного сердца),
Артериальной и венозной магистралей для тока крови,
Одного либо нескольких микрофильтров, улавливающих во время искусственного кровообращения из крови агрегаты форменных элементов, пузырьки газа и другие микроэмболы,
Коронарный отсос. Его задача отсасывать излившуюся кровь из раны и возвращать в циркуляторный контур аппарата ИК.
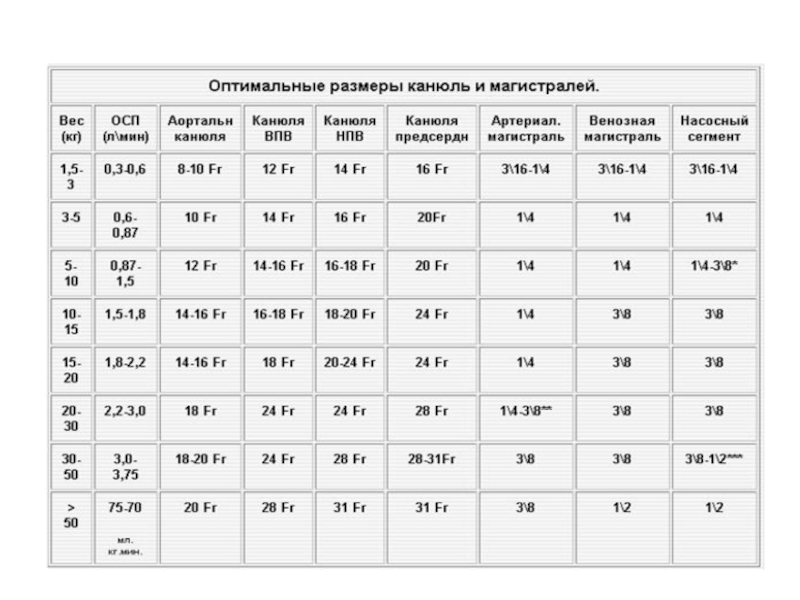
Слайд 5ОЦК у детей маленький, поэтому диаметр магистралей должен быть минимальным,
чтобы избежать чрезмерной гемодилюции. Нужно стремиться к использованию магистралей наименьшего
диаметра, обеспечивающих адекватный кровоток.Исходя из расчетной ОСП, выбирают оксигенатор.
Диаметр магистралей определяют, исходя из расчетной объемной скорости. Затем вычисляют объем заполнения с учетом объема магистралей, оксигенатора, артериального фильтра, венозного резервуара, антропометрических данных пациента. Исходя из известного объема заполнения, вычисляют расчетную гемодилюцию.
Состав перфузата определяется индивидуально, исходя из объёма операции, состояния пациента и используемого оборудования.
Слайд 7Начало перфузии
Гепарин вводится в дозе 3 мг/кг. Гепарин вводится анестезиологом
в центральную вену. Через 3-5 минуты после введения гепарина взять
пробу на АСТ и анализ газов крови. Выполнение канюляции аорты и полых вен (правого предсердия). После достижения АСТ = 300 секунд можно начинать перфузию. Уровень АСТ во время ИК должен быть не менее 480 секунд.Больным с дефицитом антитромбина III вследствие длительного лечения гепарином может потребоваться введение дополнительной его дозы, иногда достаточно высокой. Если дополнительное введение гепарина не дает результата, возможно, потребуется введение свежезамороженной плазмы, содержащей антитромбин III, или его препарат.
Слайд 8канюляция
Канюлю обычно устанавливается в восходящей аорте проксимальнее безымянной артерии.
Иногда необходимо канюлировать бедренную артерию или несколько артерий для обеспечения
адекватного кровотока в головном мозге и жизненно важных органах.Канюлируют верхнюю и нижнюю полые вены, если присутствует левая ВПВ, может потребоваться ее канюляция. У детей отток по бассейну ВПВ относительно больше, чем у взрослых.
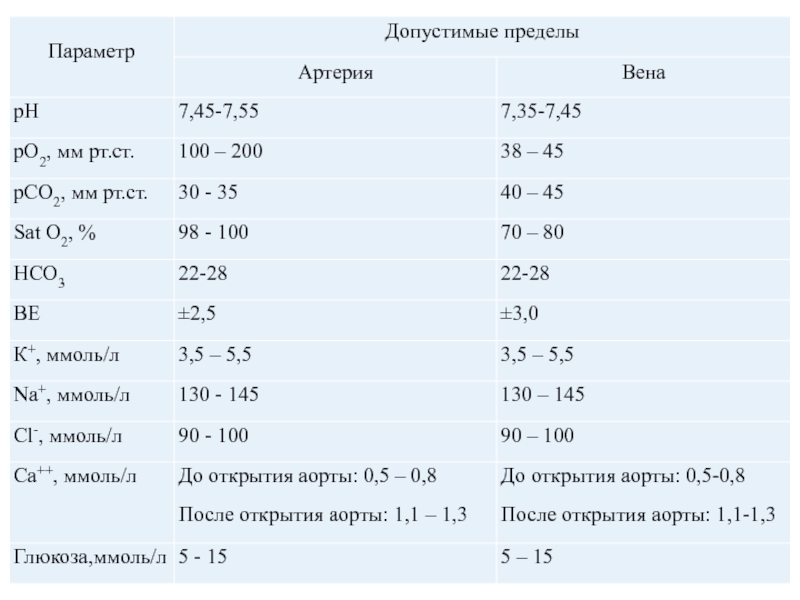
Слайд 11 У новорожденных рО2а не должно превышать 110 мм рт.ст.
более 2 часов (опасность ретинопатии).
Во время гипотермической перфузии
допускается повышение рО2v выше 45 мм рт.ст. и венозной сатурации выше 80%Во время окклюзии аорты К+ может составлять 5,5 – 7,0 ммоль/л
Слайд 13Во время перфузии у детей раннего возраста поддерживается:
гематокрит на
уровне 28%-30%,
гемоглобин 95-100 г/л,
фибриноген не ниже 1 г/л,
КОД не менее 25 мм рт.ст.Слайд 14Первичный объем заполнения равен 30% от ОЦК
Объемная скорость перфузии =
ПТ х ПИ
ПИ у детей 2,5-3,0 л/мин/м2
Слайд 15Расчет гематокрита
Как правило, используется стандартная техника первичного заполнения физиологического блока
АИК для достижения у пациента во время перфузии показателя гематокрита,
равного 28-30% (в зависимости от температурного режима перфузии).ОЦК – объем циркулирующей крови
ОЗА – объем первичного заполнения
ОЕrm – объем добавляемой эритроцитарной массы
Гематокрит эритроцитарной массы принимается за 70% (коэффициент 0,7 в формуле)
Слайд 16Расчет уровня фибриногена
Минимальный уровень фибриногена во время ИК - 1
г/л
ОПл – объем добавленной плазмы
Уровень фибриногена в донорской плазме считается
2 г/л (коэффициент 2 в формуле)Fban – исходный уровень фибриногена больного
Т.к. фибриноген до операции не определяется, то условно можно считать исходный уровень фибриногена больного как 2 г/л
Для точного расчета необходимо учитывать, что в эритроцитарной массе (но не в отмытых эритроцитах!) содержится 30% плазмы с фибриногеном 2 г/л.
Слайд 17Расчет коллоидного осмотического давления
Нормальное коллоидно-осмотическое давление равно 25 мм рт.ст.
КОД 1 мл плазмы – 25 мм рт.ст.
КОД 1 мл 10% альбумина – 50 мм рт.ст., 20% альбумина – 100 мм рт.ст.Расчет без использования коллоидов (кроме альбумина):
Расчет с использованием других коллоидов:
Раствор альбумина и эритроцитарная масса могут блокировать фильтр предварительной очистки, поэтому вводятся после его отключения.
Слайд 18ОПл – объем добавленной донорской плазмы
ОАл – объем добавленного10% альбумина
ОК
– объем добавленного коллоидного раствора
КОДк – коллоидноосмотическое давление коллоидного раствора
(см. табл.)ОErm – объем добавленной эритроцитарной массы
Для прецизионного расчета необходимо учитывать, что в эритроцитарной массе (но не в отмытых эритроцитах!) содержится 30% плазмы
Альбумин, покрывая внутренние поверхности магистралей, препятствует агрегации тромбоцитов. При добавлении большого количества кристаллоидных растворов жидкость мигрирует в ткани, затрудняя выведение продуктов метаболизма. Коллоидные вещества повышают КОД и способствуют выходу жидкости из тканей в кровоток.
Слайд 19Для удобства расчета объема компонентов первичного заполнения можно использовать следующие
формулы:
Необходимый объем эритроцитарной массы для достижения Ht = 30%:
Эрмасса(мл) =
(ОЦК + ОЗА - 3,3*ОЦК*Htп)*0,5Необходимое количество плазмы для достижения Fb=1г/л:
ОПл (мл)=(2ОЦК*Ht + ОЗА – ОЦК)*0,5
Необходимое количество 10% альбумина для достижения КОД = 25 мм рт.ст.:
ОАльб (мл) = (ОЗА - ОЭрмасса – ОПл)*0,5
Слайд 21При достижении расчетной скорости, адекватного артериального давления, достаточного притока при
необходимости начинается охлаждение. При охлаждении температурный градиент «вода/кровь» не должен
превышать 100С. По достижению заданной температуры охлаждение прекращается, и температура поддерживается на нужном уровне.Слайд 22В детской кардиохирургии применяют более глубокую гипотермию, из-за большей сложности
операций и, возможно, необходимой остановки кровообращения. Градиент температуры между артериальной
и венозной кровью при охлаждении не должен превышать 8C. Больший температурный градиент может привести к резкому понижению растворимости газов в крови и выделению их в виде пузырьков.Давление в кардиоплегической магистрали должно быть меньше. Время безопасной остановки кровообращения зависит от температуры тела больного.
Электрическая активность головного мозга подавляется при температуре 15-20C.
Гипотермия и остановка кровообращения
Слайд 23Степень охлаждения определяется характером и объёмом оперативного вмешательства. Применяются следующие
режимы:
нормотермическая перфузия (до 35,5-36С);
поверхностная гипотермическая перфузия (34-32С)
умеренная гипотермическая перфузия (32-28С):
-
с пассивным охлаждением,- с активным охлаждением.
глубокая гипотермическая перфузия (до 16-14С):
- с остановкой искусственного кровообращения;
- без остановки искусственного кровообращения;
- искусственное кровообращение со сниженной объёмной скоростью перфузии.
Слайд 24Окклюзия аорты
Непосредственно в момент наложения зажима на аорту ОСП снижается
до 50 – 70% от расчетной. После наложения зажима на
аорту необходимо проконтролировать давление в системе (возможность пережатия артериальной канюли!). В случае резкого повышения давления в системе снизить ОСП и потребовать от хирурга переложить зажим на аорте.Слайд 25В зависимости от объёма вмешательства, степени снижения резервных возможностей миокарда,
применяются различные виды кардиоплегии – кристаллоидная и кровяная, антеградная и
ретроградная, постоянная и дробная. Дробная кардиоплегия проводится непосредственно после окклюзии аорты и повторяется по мере возможности каждые 15-25 минут.Показания к кровяной плегии:
дети до 1 года (кроме ДМПП)
дети с ВЛГ
сложные пороки с предполагаемой окклюзией аорты более 40 минут
Противопоказание к кровяной кардиоплегии
Холодовая гемагглютинация.
Слайд 26Состав кровяной кардиоплегии
Состав на 1 литр раствора NaCl 0,9%
Соотношение раствор:кровь
– 1:4
Содержание К+ в кровяной плегии на основе высококалиевого раствора
около 20 ммоль/л, на основе низкокалиевого – около 8 ммоль/л (зависит от уровня К+ крови)Объем кардиоплегии: 1 плегия – 30 мл/кг, последующие – 10 мл/кг
Слайд 27Функция почек
Нормальная функция почек – показатель адекватности перфузии. Почечный кровоток
составляет 27% от системного, потребление кислорода – лишь 7%. Для
нормальной почечной фильтрации необходимо постоянное поступление большого объема крови, поэтому при гипоперфузии функция почек страдает в первую очередь, На 15-20 минуте перфузии диурез должен составлять не менее 0,02 мл/кг/мин (1,0-2,0 мл/кг/ч). При отсутствии мочи в течение 30 мин необходимо применять меры. Часто бывает достаточно введения 0,05 мг/кг маннитола, если это не помогает, вводится лазикс в дозе 0,25 мг/кг. Отсутствие мочи может быть вызвано выходом жидкости в ткани из сосудистого русла, гипотонией.. Почка переносит ишемию в течение 90-120 мин.При отсутствии эффекта от указанных мероприятий и высоком уровне перфузата (не менее 150 мл) и низкого гематокрита (менее 28%) – использовать гемоконцентратор (подключение артерио–венозное).
Слайд 28Согревание
Согревание начинается по команде оперирующего хирурга после снятия зажима с
аорты. Температурный градиент «вода/носоглотка» в первые 5 минут не должен
превышать 50С, в дальнейшем – 100С, максимальная температура воды не превышает 420С. При необходимости добавляется маннитол в дозе 0,25 г/л за 5 – 10 минут до открытия аорты. Согревание продолжается до достижения температуры не ниже 36,50С и не выше 37,50С. Если у пациента во время согревания определяется низкая венозная сатурация при 100% артериальной, метаболический ацидоз, то необходимо повышение ОСП на 20-50%.Слайд 30Циркуляторный арест
Оборудование, канюли и подготовка к перфузии не отличается от
прочих. Обязательна установка ультрафильтра для проведения МУФ.
После начала перфузии начинается
охлаждение до заданной температуры:температурный градиент «вода/кровь» может достигать 150С (после закрытия аорты)
время охлаждения при предполагаемом аресте циркуляции (особенно длительном) должно быть не меньше 20 минут (при меньшем времени увеличивается риск мозговых осложнений)
во время охлаждения для ареста используется -stat
Температура для проведения ареста – 180С.
Слайд 31Показания к циркуляторному аресту
Невозможность хирургической коррекции в условиях перфузии даже
с минимальной скоростью (например: Norwood stage 1)
Возможность выполнения хирургической коррекции
в течение 45 минут циркуляторного арестаПеред началом ареста производится обязательный контроль газов крови:
SatO2v желательно не менее 95%
pCO2a не более 30
отсутствие метаболического ацидоза
Слайд 32Безопасная длительность ареста по данным большинства авторов ограничивается 45 минутами
при 180С.
Большая длительность ареста не всегда приводит к негативным последствиям.
«Слабое
звено» при аресте – головной мозг. Реальная оценка изменений его функций (особенно ментально-когнитивных) после ареста у детей раннего возраста практически невозможна. Возможна лишь диагностика грубых неврологических компликаций.Хореоатетоз отмечается у некоторых детей раннего возраста не только после ареста (иногда и менее 45 минут), но и при low flow с температурой менее 200С. Критический возраст в отношении появления хореоатетоза – от 3 до 9 месяцев.
По окончании перфузии производится МУФ.
Слайд 33Low flow
Оборудование, канюли и подготовка к перфузии не отличается от
прочих.
Обязательна установка ультрафильтра для проведения МУФ.
После начала перфузии начинается
охлаждение до заданной температуры:температурный градиент «вода/кровь» может достигать 150С (после закрытия аорты)
Минимальная (рекомендованная) объемная скорость при 18-200С составляет 50 мл/кг/мин (у детей до года). Время ограничено только хирургом
Слайд 34Показания к low flow
Невозможность хирургической коррекции в условиях перфузии с
полной объемной скоростью (например: ТФ с БАЛК)
Слайд 35После команды хирурга перфузиолог снижает объемную скорость до желаемого минимума
(ограничивается только возможностью выполнения коррекции). После появления возможности увеличить объемную
скорость хирург информирует перфузиолога и ОСП повышается до расчетной.После повышения ОСП вводится маннитол 0,25 г/кг.
После контроля газов крови и электролитов производится необходимая коррекция.
Согревание и дальнейшее ведение пациентов с low flow не отличается от остальных случаев. По окончании перфузии производится МУФ.
Слайд 36МОДИФИЦИРОВАННАЯ УЛЬТРАФИЛЬТРАЦИЯ
МУФ проводится после остановки искусственного кровообращения для:
удаления из тканей
пациента излишнего количества жидкости;
фильтрации медиаторов воспаления связанные с
системным воспалительным ответом;уменьшения необходимости послеоперативной гемотрансфузии, достижения желаемого гематокрита;
улучшения постперфузионной органной функции;
Слайд 37Показания к проведению МУФ:
ИК у детей первого года жизни (кроме
ДМПП); Длительное время ИК (более 3 часов); Синдром постперфузионной капиллярной
утечки; Циркуляторный арест, Low flow, Легочная гипертензия после операцииПреимущества техники МУФ:
ультрафильтруется пациент; гемоконцентрируется контур; контур поддерживается заполненным все время, можно всегда заново начать ИК
Отрицательные эффекты МУФ:
задержка на 10-20 минут удаления канюль из пациента; задержка по времени введения протамина и более длительная постоперационная кровоточивость; возможность гемодинамической нестабильности.
Слайд 38Осложнения. Эмболия сосудов
Эмболия сосудов головного мозга, коронарных сосудов и
сосудов других жизненно важных органов может быть вызвана газом, тромботическими
массами, частицами кальция, каплями жира и другого. В качестве универсальной меры профилактики воздушной эмболии многие хирурги применяют подачу углекислого газа в операционную рану перед герметизацией полостей сердца. Углекислый газ хорошо растворяется в жидкостях и быстрее, чем воздух, покидает просвет сосуда.Попадание пузырьков кислорода из оксигенатора в артериальную линию аппарата - вторая возможная причина газовой эмболии. Для предупреждения эмболии применяют микропористые артериальные фильтры однократного пользования. Эти фильтры устанавливаются в артериальной линии АИК. Они способны задержать частицы размером до 40 мкм.
Слайд 39Осложнения. Эмболия сосудов
Эмболия сосудов головного мозга может иметь различные
симптомы (от незначительных неврологических знаков до глубокой мозговой комы) и
нередко заканчивается смертью больного. Терапия этого осложнения должна быть направлена прежде всего на профилактику и лечение отека мозга.Одним из самых эффективных лечебных мероприятий при газовой эмболии является немедленное помещение больного в камеру с повышенным барометрическим давлением.
Слайд 40Осложнения. Гипоксия
Гипоксия жизненно важных органов может быть следствием двух
основных причин: недостаточной производительности оксигенатора или артериального насоса и нарушением
микроциркуляции.Клиническим признаком гипоксии является нарастание метаболического ацидоза в ходе перфузии. Причинами могут быть выход из строя иерфузионной аппаратуры и слишком большое шунтирование нагнетаемой в кровеносное русло больного крови через пораженный аортальный клапан или бронхиальные анастомозы. Резкое снижение кровотока в организме может привести в этом случае к необратимым изменениям в жизненно важных органах. Профилактикой постгипоксического отека мозга во время искусственного кровеобращения является немедленное охлаждение нагнетаемой крови с помощью теплообменника.
Слайд 41Гематологические осложнения
Гематологические осложнения могут быть вызваны групповой или белковой
несовместимостью крови донора и больного, реакцией больного на массивную гемотрансфузию
цитратной крови, повышенной травмой крови в аппарате, нарушением свертывания крови и водно-электролитного баланса. Реакция больного на чужеродную кровь проявляется целым комплексом симптомов, часто объединяемых под названием «синдром гомологичной крови».Профилактика осложнений, связанных с введением в организм консервированной крови, должна быть направлена прежде всего на уменьшение ее количества. Решающую роль здесь играют применение аппаратов с малым объемом заполнения и использование гемодилюции. Степень травматизации крови зависит от ряда факторов: длительности и способа сохранения донорской крови, совершенства перфузионной аппаратуры и методики ее применения, продолжительности перфузии. Современные аппараты искусственного кровеобращения сравнительно мало травмируют кровь, и величина гемолиза при работе с ними обычно не превышает 30—40 мг% свободного гемоглобина плазмы при перфузии длительностью до 1 часа, что, как правило, хорошо переносится больными