Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Множественная миелома (миеломная болезнь, болезнь Рустицкого-Калера)
Содержание
- 1. Множественная миелома (миеломная болезнь, болезнь Рустицкого-Калера)
- 2. Миеломная болезнь – Прогрессирующее, неопластическое заболевание из
- 3. История открытия ММ Vc.Intyre и Watson, 1845.
- 4. проявляется обычно у людей пожилого возраста ,
- 5. Этиология миеломной болезни неизвестна.Отмечена повышенная частота заболевания
- 6. Основные дефиницииПарапротеинемия – состояние нарушенного белкового состава
- 7. Парапротеинемические гемобластозы: группа опухолевых заболеваний крови В-лимфоидной природы
- 8. Миелома характеризуется неопластической пролиферацией плазматических клеток с
- 9. Классификация миеломы по морфологии ККМВ зависимости от
- 10. Клиническая картина. Заболевание может длительно протекать бессимптомно,
- 11. Поражение костейРазрушение кости при миеломе обусловлено пролиферацией
- 12. Поражение костейОпухолевые инфильтраты (экстрамедуллярные очаги) чаще всего
- 13. Поражение костейКлиническая картина.Боли в костях (оссалгии) являются
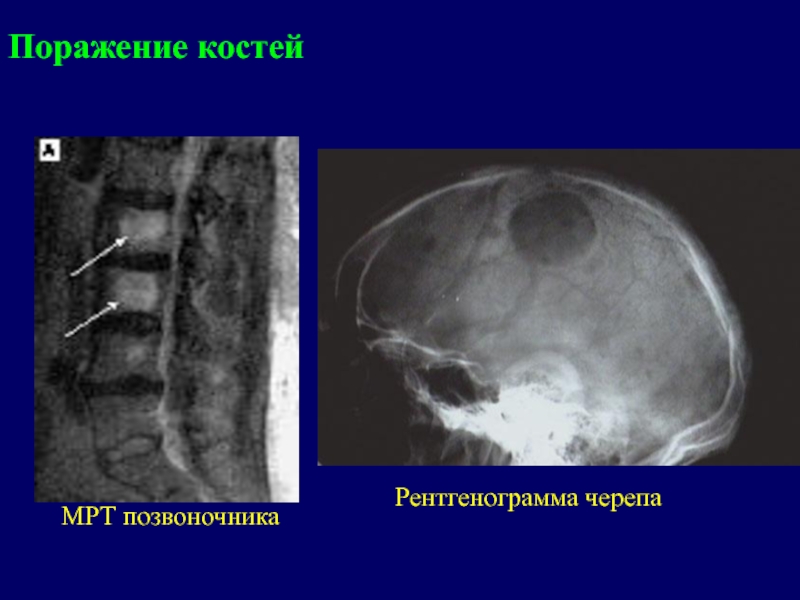
- 14. МРТ позвоночникаРентгенограмма черепаПоражение костей
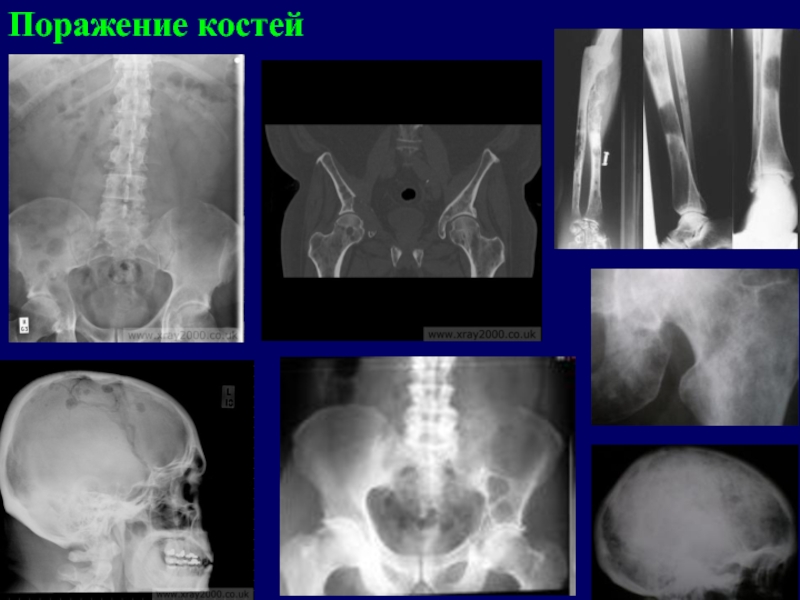
- 15. Поражение костей
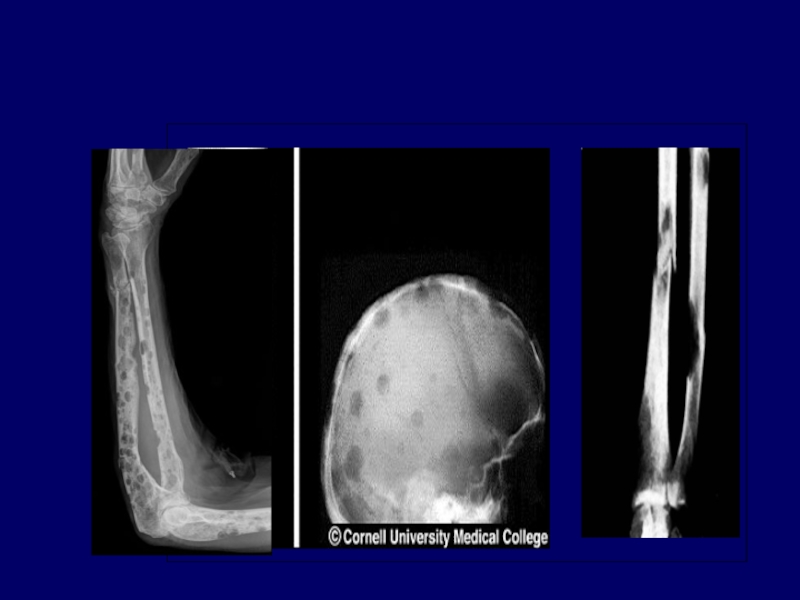
- 16. Слайд 16
- 17. Поражение почекПри миеломной болезни в связи с
- 18. ГиперкальциемияНарушение вязкости кровиИнфекцииУратный диатезПоражение почек (другие причины)
- 19. Клиническая картина.Cиндром повышенной вязкости крови
- 20. Клиническая картина.Миеломноклеточные инфильтраты отмечаются во внутренних органах.У
- 21. Клиническая картина.Частым клиническим признаком миеломной болезни является
- 22. Клинико-лабораторные методы диагностикиКлинический анализ периферической кровирезкое и
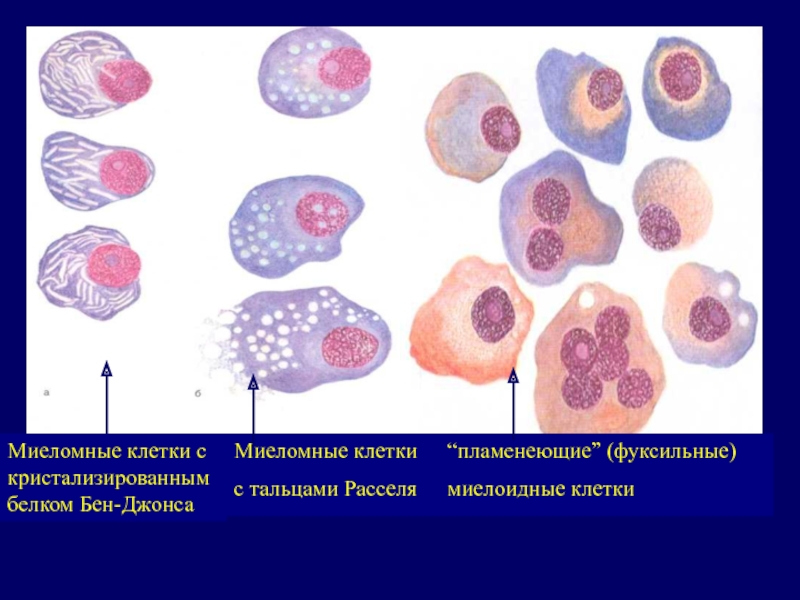
- 23. Миеломные клетки с кристализированным белком Бен-ДжонсаМиеломные клетки с тальцами Расселя“пламенеющие” (фуксильные) миелоидные клетки
- 24. Клинико-лабораторные методы диагностикиЦитологическое исследование пунктата костного мозгахарактерно
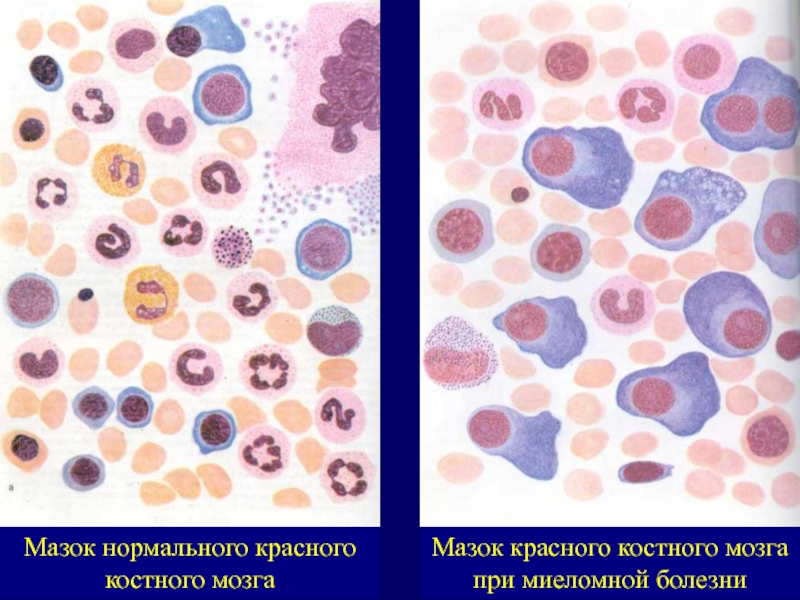
- 25. Мазок нормального красного костного мозгаМазок красного костного мозга при миеломной болезни
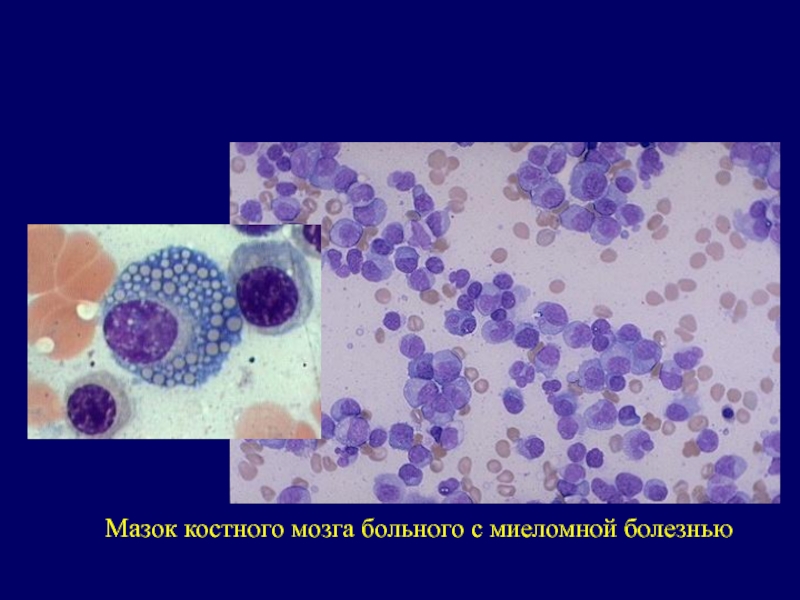
- 26. Мазок костного мозга больного с миеломной болезнью
- 27. Клинико-лабораторные методы диагностикиБиохимические тестыЭлектрофорез позволяет выявить М-градиент
- 28. Клинико-лабораторные методы диагностикиНа рентгенограммах выявляют: очаги деструкции
- 29. Критерии множественной миеломы 1. Наличие более 10%
- 30. 1. Множественная миелома. Рак костного мозга. Справочник
- 31. Пример формулировки диагноза.Миеломная болезнь, миелома G, диффузно-узловая
- 32. Лечение миеломной болезни.Выбор лечения и его объем
- 33. Показанием для назначения лечения являются признаки прогрессирования
- 34. Перед началом проведения химиотерапии все больные
- 35. 9. колониеобразующая способность клеток костного мозга10. общий
- 36. Этапы лечения множественной миеломы:I Индукция ремиссииII
- 37. лечение множественной миеломыМелфалан. Первое лекарственное средство
- 38. Бортезомиб. Основной механизм действия — обратимое подавление
- 39. Леналидомид. Имеет двойной механизм действия: активирует иммунные
- 40. Эффективность терапии, критерии ответа.лечение считается эффективным
- 41. Принципы лечения миелоидной болезни:ЦитостатикиГлюкокортикоидыЛучевая терапияСимптоматическое лечение пораженных
- 42. Оценка эффективности лечения
- 43. Истинная полная ремиссия – полное исчезновение парапротеина
- 44. Продолжительность жизни больных зависит от стадии, на
- 45. Тактика поведения врача поликлиники.При подозрении на миелому
- 46. Экспертиза нетрудоспособности. Все пациенты парапротеинемическими гемобластозами нуждаются в присвоении группы инвалидности.
- 47. Случай из практики Пациент 30 лет, обратился
- 48. Интерактивные вопросы1. Уровень альбуминемии при миеломе:снижаетсяповышаетсяНе меняется
- 49. Интерактивные вопросы2. Парапротеин при миеломе:поликлональныймоноклональный
- 50. Интерактивные вопросы3. Какой синдромокомплекс НЕ характерен для меломы:поражение костейнарушение иммунитетаизменение в почкахлейкоцитозповышение вязкости крови
- 51. Интерактивные вопросы4. Какое состояние НЕ соответствует понятию
- 52. Интерактивные вопросы5. Определение М-градиента это метод для:Выявление
- 53. ЛитератураГоленков А.К., Шабалин В.Н. Множественная миелома. -
- 54. ЛитератураАбдулкадыров К.М. с соавт. Гематологические синдромы в
- 55. Скачать презентанцию
Слайды и текст этой презентации
Слайд 3История открытия ММ
Vc.Intyre и Watson, 1845. Первое описание ММ сделано
о больном умершем от болезни проявившей себя болями в костях
и отеками.H. Bence-Jones, 1848. Описывает живую материю белкового происхождения, полученную из мочи вышеуказанного пациента и обладающую способностью выпадать при нагревании до определенной температуры, а затем вновь растворяться при кипячении.
О.А. Рустицкий, 1873. Описал патологическую анатомию и гистологию заболевания названного им «множественной миеломой».
O. Kahler, 1889. Связал миелому Рустицкого с протеинурией Бенс-Джонса
Д.Райт, 1900. Связал заболевание с увеличением количества и изменением количества плазматических клеток, пролиферацией плазматических клеток, характеризующихся полиморфизмом самих клеток, их ядер, анаплазией и разной степенью зрелости.
Слайд 4проявляется обычно у людей пожилого возраста , средний возраст –
62 года
случаи заболевания в возрасте до 40 лет редки (
миеломной болезни составляет 1,5-3 на 100 000 населения в год в Европе ( у чернокожих до 10)мужчины болеют несколько чаще, 1,5:1 (R.Niesvizky,1993)
Продолжительность жизни зависит от злокачественности течения заболевания и в среднем составляет около 8 лет
Эпидемиология миеломы:
Слайд 5Этиология миеломной болезни неизвестна.
Отмечена повышенная частота заболевания среди японцев, переживших
ядерную бомбардировку во время второй мировой войны.
Имеются также свидетельства о
генетической предрасположенности к этому виду гемобластоза (семейные случаи). Прямые доказательства вовлечения онкогенов при миеломе человека отсутствуют
Слайд 6Основные дефиниции
Парапротеинемия – состояние нарушенного белкового состава сыворотки крови за
счет появления белков аномальной структуры (парапротеинов), представляющих собой иммуноглобулины или
фрагменты их молекул.Моноклональный парапротеин – аномальный белок, синтезируемый одним, чаще измененным, клоном иммуноглобулинсинтезирующих клеток, сходный по структуре и биохимических свойствам с нормальными Ig, но отличающийся высокой гомогенностью.
Слайд 7Парапротеинемические гемобластозы:
группа опухолевых заболеваний крови В-лимфоидной природы при которых имеет
место повышенная продукция моноклональных парапротеинов.
Данную группу заболеваний составляют:
миеломная
болезньмакроглобулинемия Вандельстрема
Болезнь тяжелых цепей
Хронический лимфолейкоз
Лимфома
особенностью данных гемобластозов является сохранение способности В-лимфоцитов к дифференцировке до стадии иммуноглобулинсекретирующих клеток.
Слайд 8Миелома характеризуется неопластической пролиферацией плазматических клеток с продукцией моноклоновых иммуноглобулинов
(парапротеинов) или легких цепей.
В зависимости от класса и типа
синтезируемых и секретируемых парапротеинов выделяют следующие иммунохимические варианты: G-, A-, D-, E-, М-миелому, миелому Бенс-Джонса (болезнь легких цепей).Клинические и морфологические проявления вариантов сходны, кроме миеломы Бенс-Джонса .
Слайд 9Классификация миеломы по морфологии ККМ
В зависимости от характера миеломных инфильтратов
в красном костном мозге различают следующие формы заболевания:
узловую;
диффузную;
диффузно-узловую
склерозирующую
висцеральную
Классификация
миеломы по распространенностиМиелома может протекать в солитарной форме, в виде одиночного узла, но чаще она бывает множественной.
Слайд 10Клиническая картина. Заболевание может длительно протекать бессимптомно, сопровождаясь лишь увеличением
СОЭ.
Выделяют следующие симптомы заболевания:
Синдром костной патологии
Синдром гуморального иммунодефицита
Синдром почечной
патологииАнемия
Синдром повышенной вязкости
Геморрагический синдром
Синдром гиперкальциемии
Неврологический синдром
Слайд 11Поражение костей
Разрушение кости при миеломе обусловлено пролиферацией опухолевого клона и
активацией остеокластов под влиянием остеокластактивирующего фактора (ФНО-а, IL-1, IL-3, IL-6),
выделяемого миеломными клетками.Лизис костей приводит к мобилизации кальция из костей и гиперкальциемии с развитием осложнений (тошнота, рвота, сонливость, сопорозное состояние, кома).
Опухолевые пролифераты могут пальпироваться, особенно в области черепа, ключиц и грудины. Оседание позвонков обусловливает появление признаков компрессии спинного мозга.
Слайд 12Поражение костей
Опухолевые инфильтраты (экстрамедуллярные очаги) чаще всего появляются в
- плоских костях (ребра, кости черепа)
- позвоночнике, реже – в трубчатых костях (плечевая, бедренная кость).Разрастающаяся опухолевая ткань ведет к деструкции костной ткани и развитию патологических переломов. При диффузном разрастании опухолевой кроветворной ткани наблюдается остеолизис и остеопороз – образование гладкостенных, как бы штампованных дефектов.
Слайд 13Поражение костей
Клиническая картина.
Боли в костях (оссалгии) являются наиболее частым признаком
миеломы и отмечаются почти у 70% больных.
Боли чаще всего
локализуются в позвоночнике и ребрах, мигрируютвозникают главным образом при движении (в отличие от болей при метастазах опухолей в кости, которые усиливаются по ночам)
Непрекращающиеся локализованные боли обычно указывают на формирование патологических переломов
Слайд 17Поражение почек
При миеломной болезни в связи с секрецией опухолевыми клетками
парапротеина часто развивается AL-амилоидоз.
Наибольшее значение среди парапротеинемических изменений имеет
парапротеинемический нефроз.В основе парапротеинемического нефроза лежит избыточное накопление в канальцах и в строме мозгового, а затем и коркового вещества парапротеина Бенс-Джонса, ведущее к нефросклерозу. Такие почки получили название “миеломные сморщенные почки”. Развивающаяся уремия является в 30% случаев причиной смерти больных миеломой.
Слайд 18Гиперкальциемия
Нарушение вязкости крови
Инфекции
Уратный диатез
Поражение почек (другие причины)
Слайд 19Клиническая картина.
Cиндром повышенной вязкости крови
не является частым проявлением миеломной болезни.
При образовании криоглобулинов отмечается синдром Рейно и нарушение микроциркуляции
вязкость крови обусповливает неврологические симптомы: головную боль, усталость, нарушение зрения, ретинопатию (вплоть до парапротеинемической комы)
Слайд 20Клиническая картина.
Миеломноклеточные инфильтраты отмечаются во внутренних органах.
У 5 – 13
% больных выявляют спленомегалию и(или) гепатомегалию вследствие инфильтрации плазматическими клетками,
а также нередко и миелоидной метаплазии.Слайд 21Клиническая картина.
Частым клиническим признаком миеломной болезни является подверженность больных бактериальным
инфекциям в связи с гипогаммаглобулинемией, снижением продукции нормальных антител.
Слайд 22Клинико-лабораторные методы диагностики
Клинический анализ периферической крови
резкое и стабильное увеличение СОЭ,
порой до 80 – 90 мм/ч
анемия нормохромного типа
возможна
лейкопения (нейтропения)иногда в крови можно выявить плазматические (миеломные) клетки
Слайд 23Миеломные клетки с кристализированным белком Бен-Джонса
Миеломные клетки с тальцами Расселя
“пламенеющие”
(фуксильные) миелоидные клетки
Слайд 24Клинико-лабораторные методы диагностики
Цитологическое исследование пунктата костного мозга
характерно наличие более 10%
плазматических атипических клеток типа плазмобластов (миеломных) клеток, отличающихся большим многообразием
структурных особенностейСлайд 25Мазок нормального красного костного мозга
Мазок красного костного мозга при миеломной
болезни
Слайд 27Клинико-лабораторные методы диагностики
Биохимические тесты
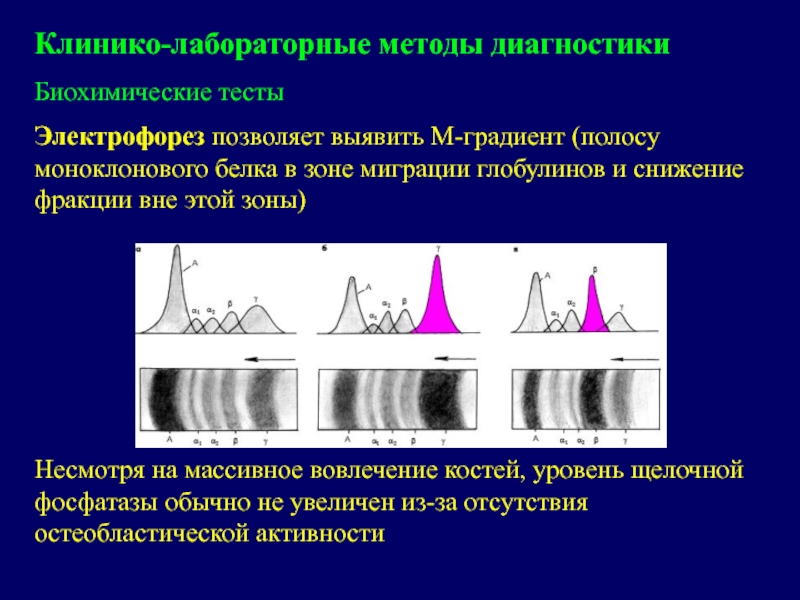
Электрофорез позволяет выявить М-градиент (полосу моноклонового белка
в зоне миграции глобулинов и снижение фракции вне этой зоны)
Несмотря
на массивное вовлечение костей, уровень щелочной фосфатазы обычно не увеличен из-за отсутствия остеобластической активности Слайд 28Клинико-лабораторные методы диагностики
На рентгенограммах выявляют:
очаги деструкции костной ткани,
общий остеопороз, в первую очередь в плоских костях затем в
проксимального отделах трубчатых костейСлайд 29Критерии множественной миеломы
1. Наличие более 10% плазматических клеток
в миелограмме и (или) биоптате пораженной ткани;
2. Моноклональный Ig при
иммуноэлектрофорезе (в сыворотке содержание IgG более 35 г/л, или IgA – более 20 г/л, в моче κ- или λ-легкие цепи более 1 г в сутки)3. Наличие остеолитических поражений скелета и (или) диффузный остеопороз.
Диагноз множественной миеломы устанавливается только при сочетании не менее двух из этих трех основных критериев, наличие первого критерия обязательно.
Слайд 301. Множественная миелома. Рак костного мозга. Справочник пациента. International Myeloma
Foundation 2007
2. http://www.myeloma-euronet.org/en/multiple-myeloma/faq.php
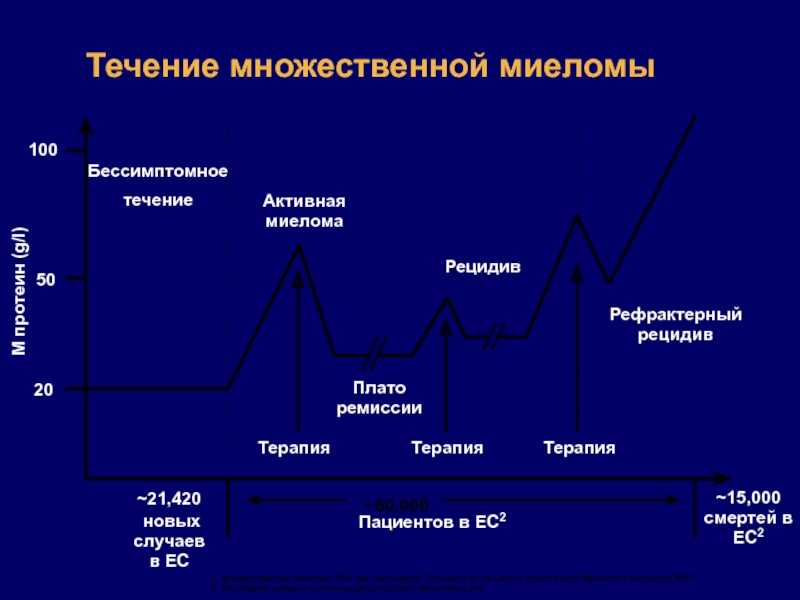
Бессимптомное
течение
20
50
100
Рефрактерный рецидив
Плато ремиссии
Рецидив
Терапия
~60,000
~21,420
новых случаев в ЕС
~15,000
смертей в ЕС2Пациентов в ЕС2
M протеин (g/l)
Терапия
Терапия
Активная миелома
Течение множественной миеломы
Слайд 31Пример формулировки диагноза.
Миеломная болезнь, миелома G, диффузно-узловая форма, стадия II
А
Миеломная болезнь, миелома Бенс-Джонса, диффузная форма, стадия I B.
Слайд 32Лечение миеломной болезни.
Выбор лечения и его объем зависят от стадии
(распространенности) процесса.
У 10 % больных миеломой наблюдается медленное
прогрессирование болезни в течение многих лет, редко требующее противоопухолевой терапии.У больных с солитарной миеломой эффективна лучевая локальная терапия.
У больных с начальными стадиями рекомендуется выжидательная тактика, так как у части из них возможна медленно развивающаяся форма болезни.
Слайд 33Показанием для назначения лечения являются признаки прогрессирования заболевания:
отрицательная динамика показателей
при повторных исследованиях с интервалом 2 -4 недели
-
нарастает общий белок крови за счет нарастания моноклонального белка, увеличение количества плазматических клеток в костном мозге,
нарастание остеодеструктивного синдрома.
Слайд 34 Перед началом проведения химиотерапии все больные должны быть обследованы.
Необходимый перечень обследования:
клинический анализ крови с подсчетом количества тромбоцитов
пункция грудины
гистологическое
исследование трепанбиоптата костного мозгабиохимическое исследование крови
коагулограмма
иммунологическое исследование крови (Ig A, G, M, D, E)
ЭКГ
сонография органов брюшной полости, почек, сердца с определением функциональной способности левого и правого желудочков
Слайд 359. колониеобразующая способность клеток костного мозга
10. общий анализ мочи
11. проба
Реберга
12. проба Зимницкого
13. рентгенография органов грудной клетки
14. рентгенография плоских
костей при наличии показаний - трубчатый костей15. биопсия периферических лимфоузлов или опухолевидных образований в мягких тканях, если таковые обнаруживаются
16. определение белка Бенс-Джонса в моче и типа легких цепей
17. определение содержания кальция и фосфора
18. определение массы тела, роста, площади тела больного
Слайд 36Этапы лечения множественной миеломы:
I Индукция ремиссии
II Период консолидации
III
Поддерживающее лечение
IV Терапия в периоде рецидива
V Терапия резистентных и
быстропрогрессирующих форм множественной миеломы.Слайд 37 лечение множественной миеломы
Мелфалан. Первое лекарственное средство для специфической терапии
миеломы, внедрено в практику в 60-е г.г. прошлого века. До
сих пор достаточно широко используется как в монотерапии, так и в комбинации с преднизолоном (МР), особенно для лечения пожилых больных. Ответ на терапию наблюдается не выше, чем у 50 % больных множественной миеломой.Слайд 38Бортезомиб
. Основной механизм действия — обратимое подавление апоптоза Ответ наступает
в 43 % случаев у пациентов с рецидивом миеломы, время
до ответа около 2 месяцев, длительность ремиссии (время до прогрессии) — 7 месяцев, выживаемость — 29 месяцев. Используется как в монотерапии,[6] так и в сочетании с другими препаратами: VMP — велкейд + мелфалан + преднизолон — зарегистрирован для лечение в первой линии терапии; VD — велкейд + дексаметазон для рецидивов болезни; PAD — велкейд + адриабластин + дексаметазон и другие. Его применение не исключает трансплантацию стволовых клеток. Вводится внутривенно, предпочтительно в стационарных условиях.Слайд 39Леналидомид
. Имеет двойной механизм действия: активирует иммунные клетки организма, что
приводит к гибели опухолевых клеток, и подавляет ангиогенез опухоли. При
раннем использовании (вторая линия терапии) увеличивает ремиссиию (время до прогрессии) до 17,1 месяцев, общую выживаемость — до 42 месяцев. Эффективен у 60 % пациентов. При длительном применении у пациентов, получивших ответ, общая выживаемость достигает 51 месяца (San Miguel, 2010). Применяется в комбинации со стероидным гормоном — дексаметазоном, а также алкилирующими агентами (циклофосфаном). Монотерапия леналидомидом рекомендована группой экспертов по миеломе NCCN в качестве поддерживающей терапии после ТСК. Имеет пероральную форму, удобен для амбулаторного приёма.Слайд 40Эффективность терапии, критерии ответа.
лечение считается эффективным
только у тех больных у которых:
достигнута положительная динамика дополнительных опухолевых клеток в пунктате грудины до 5%,
стабильные или нарастающие показатели красной крови,
снижение уровня кальция до 3 ммоль/л
Отсутствие видимого увеличения количества и размеров остеодеструкции.
Слайд 41Принципы лечения миелоидной болезни:
Цитостатики
Глюкокортикоиды
Лучевая терапия
Симптоматическое лечение пораженных органов
Бисфосфонаты
Заместительная терапия иммуноглобулинами
При
нефропатия – гемодиализ
Плазмаферез
Препараты кальция, вит Д (при нормальном уровне Ca)
Слайд 43Истинная полная ремиссия – полное исчезновение парапротеина из сыворотки крови
и мочи, доказанное методом иммунофиксации, нормальную морфологическую картину костного мозга
(плазмоцитов менее 5%).Достигнутый уровень ответа должен сохраняться не менее 2 мес и должен быть подтвержден дважды
Фаза плато – стабилизация болезни с максимально низким уровнем парапротеина в сыворотке крови и (или) моче, с минимально выраженными клиническими проявлениями и независимостью от гемотрансфузий не менее 6 мес. Определение фазы важно для решения вопроса о прекращении лечения и выявления рецидива.
Слайд 44Продолжительность жизни больных зависит от стадии, на которой диагностирована опухоль.
Причинами
смерти могут быть:
прогрессирование миеломы
почетная недостаточность
Сепсис
часть больных умирает от инфаркта миокарда,
инсульта и других причин. Слайд 45Тактика поведения врача поликлиники.
При подозрении на миелому – срочная госпитализация
пациента
Регулярный контроль биохимических тестов, отражающих активность процесса.
При активации заболевания –
повторное стационарное лечение.Профилактика и лечение осложнений химиотерапии.
Оценка степени инвалидизации пациентов.
Слайд 46Экспертиза нетрудоспособности.
Все пациенты парапротеинемическими гемобластозами нуждаются в присвоении группы инвалидности.
Слайд 47Случай из практики
Пациент 30 лет, обратился с жалобами на
выраженные отеки на лице . При обследовании выявлены повышение цифр
АД .Заболевание прогрессирует в течение 6 месяцев , снижается масса тела. При обследовании в клиническом анализе крови : эритроциты 3.4*19\л, гемоглобин 100 г\л, лейкоциты 4,5*10\л, соэ 70 мм\ч.Общий анализ мочи: цвет темно- желтый, мутн., белок 2,5 мг\л, плотность 1002, глюкоза ++, ураты, гиперкальциурия.
Экскреторная урография :очаги расплавления в проекции подвздошных костей, диаметром до 2,5см, нарушение концентрационно- выделительной функции почек.
Рентгенография легких: дефекты плоских костей .
Слайд 50Интерактивные вопросы
3. Какой синдромокомплекс НЕ характерен для меломы:
поражение костей
нарушение иммунитета
изменение
в почках
лейкоцитоз
повышение вязкости крови
Слайд 51Интерактивные вопросы
4. Какое состояние НЕ соответствует понятию «миеломная почка»:
Амилоидоз почки
Сморщенная
почка
Парапротеинемический нефроз
Cиндром Де Тони – Дебре – Фанкони
Селективная протеинурия
Слайд 52Интерактивные вопросы
5. Определение М-градиента это метод для:
Выявление миеломных клеток
Определения уровня
парапротеина
Выявления остеолитических дефектов
Определения степени нарушения реологии крови
Слайд 53Литература
Голенков А.К., Шабалин В.Н. Множественная миелома. - Санкт-Петербург, 1995. -
142 с.
Рейд К.Д. Патология плазматических клеток // Болезни крови
у пожилых / Под ред. М.Дж. Денхэма и И. Чанарина. - М., 1989. - С. 255 - 283. Бессмельцев С.С., Абдулкадыров К.М. Ультразвуковая диагностика в гематологической практике. - Санкт-Петербург, 1997. - 178 с.
Abdulkadyrov К., Bessmeltsev S. Renal insufficiency in multiple myeloma: basic mechanisms in its development and methods for treatment // Renal Failure. - 1996. - Vol. 18. - P. 139 - 146.
Слайд 54Литература
Абдулкадыров К.М. с соавт. Гематологические синдромы в общей клинической практике
// «Элби», Санкт-Петербург.-1999.-С.83-94
Гематологические синдромы в клинической практике, под редакцией
Вягорской Я.И., Киев «Здорье» 1981 одВоробьёв А.И. Руководство по гематологии.// «Ньюдиамед», Москва.-2003.-Т1.
Вуд М.Э., Банн П.А. Секреты гематологии и онкологии// «Бином»- Москва.-2001.-С.85-93.
Гусева С.А., Вознюк В.П. Болезни системы крови. Справочник. // «МЕДпресс-информ».-Москва.-2004.-С.317-356.
Внутренние болезни под редакцией Рябва С.И., Алмазова В.А., Шляхто Е.В., Санкт-Петербург, СпецЛит, 2000 год
Клиническая онкогематология, под редакцией Волковой М.А., Москва, «Медицина,» 2001 год
Шиффман Ф.Д. Патофизиология крови. // «Бином».-Москва.-2000.-С.71-123, 343-358
М.Вецлер, К.Блумфильд МИЕЛОИДНЫЕ ЛЕЙКОЗЫ. From Harrison's Principles of Internal Medicine. 14-th edition,2002.
Г.И. Абелев. Механизмы дифференцировки и опухолевый рост. Биохимия, 2000, 65, 127- 138
Болезни крови, «издательство энциклопедия», Москва, 2005 год
Диагностика и лечение ДВС крови, Лычев В.Г., москва, «медицина» 1993 год
Диагностика и контролируемая терапия нарушений гемостаза, Баркаган З.С., Момот А.П., «Ньюдиамед», москва 2001 год
Актуальный гемостаз , Воробьев П.А., «Ньюдиамед», москва 2004 год