Слайд 1
Кардиотонические гликозиды (КГ).
Лекарственные растения и сырье, содержащие сердечные гликозиды (СГ)
Слайд 2
• В предыдущих лекциях были рассмотрены продукты обмена растений -
первичного : углеводы, липиды, витамины,
а также некоторые продукты вторичного: терпеноиды,
эфирные масла, в том числе с ароматическими (фенольными) компонентами
и начато рассмотрение гликозилированных соединений, или гликозидов, таких веществ
как иридоиды (горечи), S-гликозиды.
Изучены также лекарственные растения (ЛР)
и лекарственное растительное сырье (ЛРС), содержащие эти соединения.
• Сейчас мы переходим к рассмотрению новой группы биологически активных веществ (БАВ), которые относятся к стероидам, и первыми среди них будут кардиогликозиды.
Слайд 3
Определение.
Кардиотоническими гликозидами (КГ)
называют вещества растительного, реже животного происхождения, агликоны которых
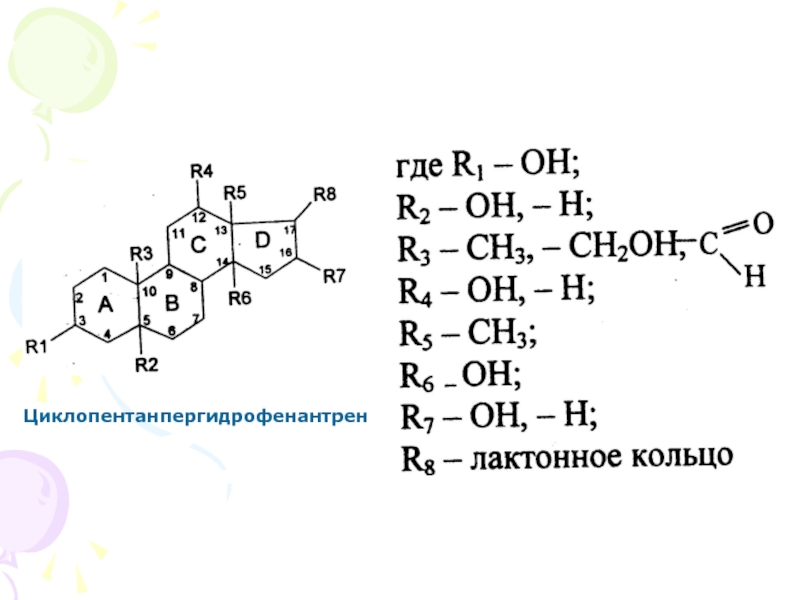
являются стероидами – производными циклопентанпергидрофенантрена, имеющими у С17 ненасыщенное 5-
или 6-членное лактонное кольцо, и оказывающими специфическое действие на сердечную мышцу.
КГ вызывают задержку и остановку сердечного ритма в стадии систолы. В больших дозах КГ являются сердечными ядами.
Однако в малых дозах эти вещества улучшают деятельность сердца, урежая сокращения и делая их более сильными.
Слайд 4Американские биохимики (Джэкобс, Чэш и др., 1930) установили, что агликоны
сердечных гликозидов относятся к стероидным соединениям, которые весьма близки к
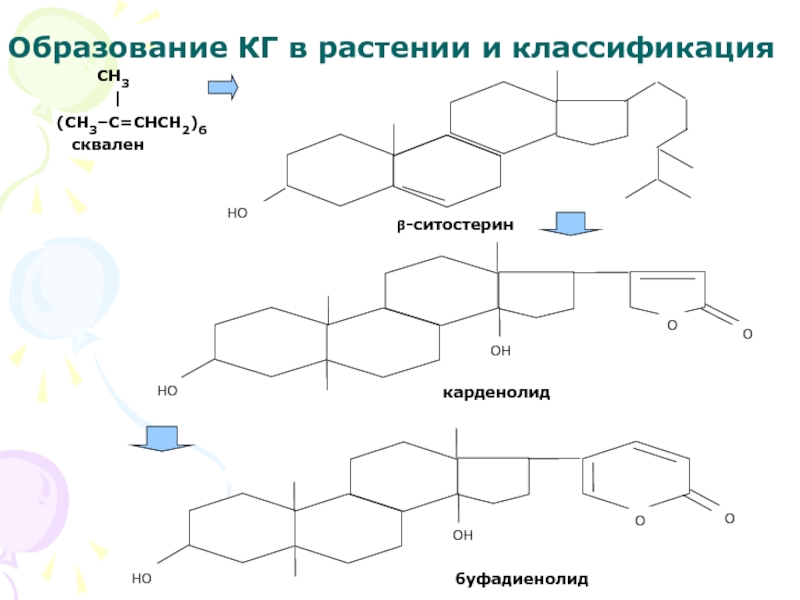
таким важным соединениям животного организма как холестерин, желчные кислоты, половые гормоны коры надпочечников, витамин Д. Это обстоятельство ускорило исследование образования сердечных гликозидов в растениях. Как оказалось, предшественниками фитостеринов являются молекулы непредельного алифатического углеводорода сквалена, циклизирующиеся в β-ситостерин, из которого затем путем изменения структуры боковой цепи в молекуле у С17 образуются
два типа сердечных гликозидов –
карденолиды и буфадиенолиды.
Слайд 5Образование КГ в растении и классификация
CH3
|
(CH3–C=CHCH2)6
сквален
О
О
ОН
НО
карденолид
НО
ОН
О
О
буфадиенолид
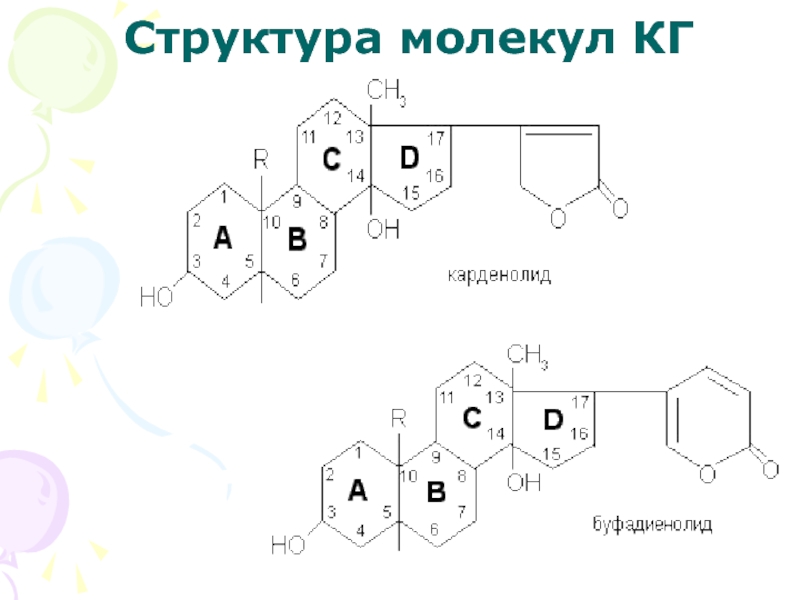
Слайд 6Таким образом, в химическом отношении кардиотонические гликозиды достаточно сходны, поскольку
все они в агликоновой части имеют одну базовую структуру циклопентанпергидрофенантрена,
в которой у атома С17 обнаруживается еще лактонное кольцо:
5-членное с одной ненасыщенной связью или
6-членное с двумя ненасыщенными связями.
В циклопентанпергидрофенантреновом остове молекул С-атомы нумеруют, начинают с верхнего в кольце А, далее против часовой стрелки, переходя на кольцо В (С5) до С10 в месте сочленения колец А и В, затем с С9 на С11 в кольце С и по часовой стрелке до С14, далее на кольцо D (С14-С15) до С17, где появляется радикал R8 – 5- или 6-членное лактонное кольцо.
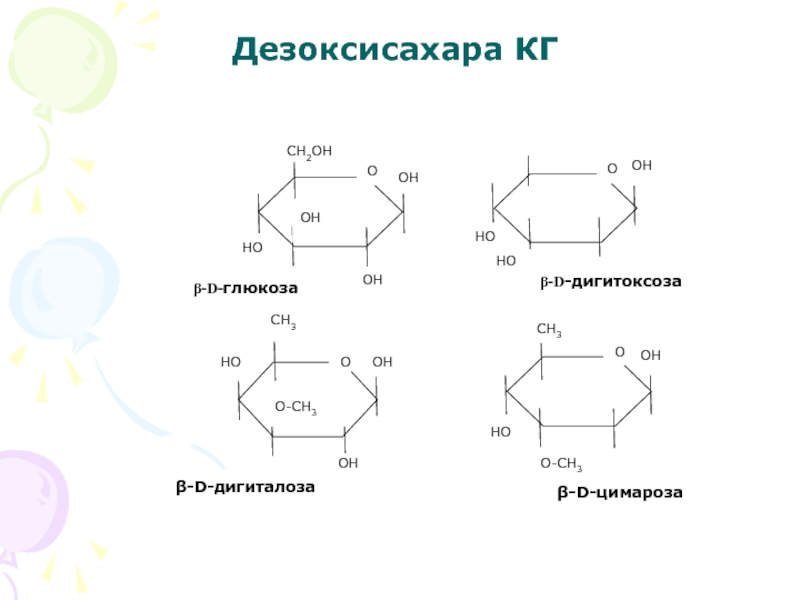
Слайд 9Дезоксисахара КГ
НО
ОН
ОН
ОН
О
НО
ОН
ОН
О
НО
ОН
ОН
О
СН3
О-СН3
CH3
O-CH3
HO
HO
O
β-D-глюкоза
β-D-дигитоксоза
СН2ОН
β-D-дигиталоза
β-D-цимароза
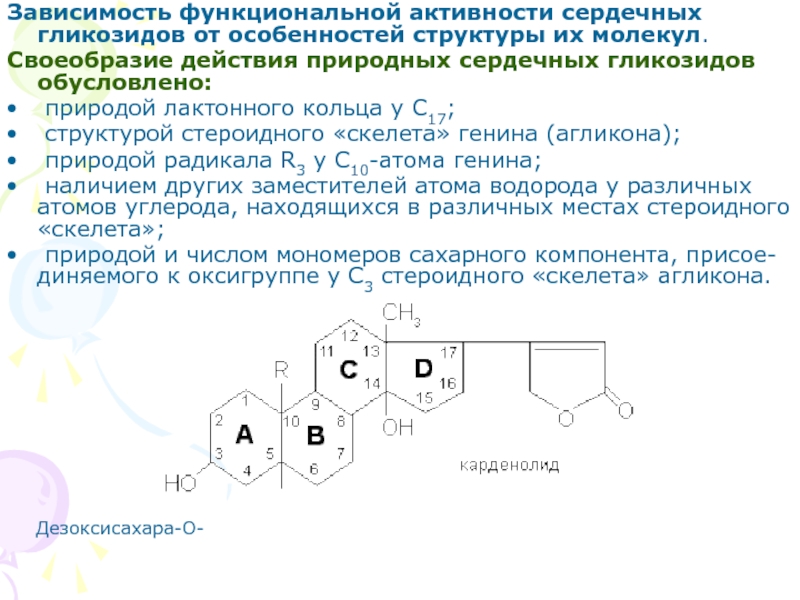
Слайд 11Зависимость функциональной активности сердечных гликозидов от особенностей структуры их молекул.
Своеобразие действия природных сердечных гликозидов обусловлено:
природой лактонного кольца
у С17;
структурой стероидного «скелета» генина (агликона);
природой радикала R3 у С10-атома генина;
наличием других заместителей атома водорода у различных атомов углерода, находящихся в различных местах стероидного «скелета»;
природой и числом мономеров сахарного компонента, присое-диняемого к оксигруппе у С3 стероидного «скелета» агликона.
Дезоксисахара-О-
Слайд 12Вначале о влиянии структурных особенностей агликона (генина),
точнее даже его
циклопентанпергидрофенантреновой основы,
на функциональную активность сердечных гликозидов.
Циклопентанпергидрофенантреновый «скелет» генина
– тетрациклическое образование, состоящее из колец, обозначаемых буквами А, В, С и D.
Здесь важное значение имеет размещение колец:
в транс- или в цис-положении.
В цис-положении кольца сближены: А и В, С и D;
в транс-положении они несколько дистанцированы
и потому более подвижны в целой конструкции, например В и С.
Кардиотонической активностью обладают только те КГ,
у которых кольца А и В находятся в цис-сочленении.
Это пространственное положение колец отличает сердечные гликозиды от других природных стероидов, где положение колец может быть иным.
Слайд 13У С17 имеется важная связь – ответвление на еще одно
кольцо – лактонное: 5-членное бутенолидное или 6-членное кумалиновое.
Следует подчеркнуть,
что специфическое кардиотоническое действие сердечных гликозидов на сердце обусловлено
именно наличием в их молекуле
5- или 6-членного лактонного цикла. Изменения в структуре лактонного кольца (например, раскрытие его под действием NaOH) ведут к утрате этими веществами характерного сердечного действия.
Карденолидам, в сравнении с буфалиенолидами,
свойственно более сильное и резкое влияние на сердечную мышцу,
тогда как буфадиенолидам – более слабое и мягкое действие.
Слайд 14Третьим важным фактором, влияющим на характер и степень кардиотонической активности
сердечных гликозидов, является радикал R3 у С10 циклопентанпергидрофенантрена: метильный, альдегидный
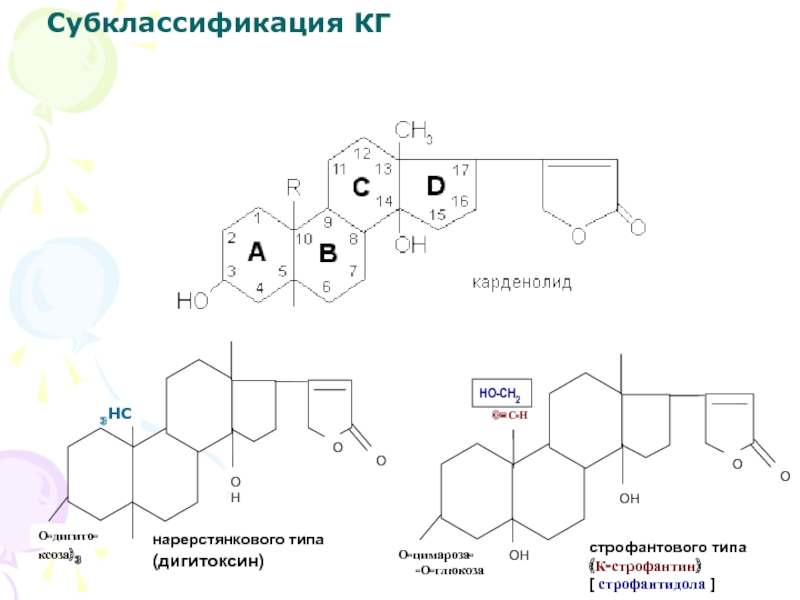
или карбонильный (спиртовой). Подавляющее большинство природных агликонов в этом положении имеет метильную или альдегидную группу, на основании которых все кардиогликозиды подразделяют на две подгруппы:
▫ наперстянковые (с –СН3);
▫ строфантовые (с –С=О или –СН2ОН).
\
Н
Отметим также, что изменение у строфантовых сердечных гликозидов альдегидной группы на карбонильную значительно ослабляет их кардиотонический эффект на сердечную мышцу.
Меньшее влияние на активность молекулы сердечных гликозидов оказывают другие заместители у атома углерода генина.
Слайд 15
Как правило, присоединение сахаристых остатков к агликону у С3
всегда происходит через кислород гидроксила, т.е. это – О
гликозиды.
Длина цепочки сахарных мономеров у разных гликозидов составляет от 1 до 5 и более остатков.
При гидролизе отщепление звеньев от сахаристой цепочки происходит постепенно.
В ЛРС содержатся сразу первичные и вторичные гликозиды кардиотонических генинов.
Сахара в цепочке относится в основном к D-типу
(это – глюкоза, ксилоза, рамноза).
Однако кроме обычных сахаров в молекулах сердечных гликозидов присутствуют и необычные, которые больше нигде не встречаются. Особенность их в том, что они
бедны кислородом, т.е. представляют собой дезоксисахара,
что связано с заменой ОН-групп водородом или метильной (–СН3)
группой, благод.к-рым в целой молекуле изменяется соотношение
гидрофильных (–ОН) и гидрофобных липофильных (–СН3) групп.
При гликозилировании к генину у С3 сначала присоединяются дезоксисахара, а конечным звеном в цепочке, как правило, является глюкоза.
Слайд 16
Более неполярные (липофильные) сердечные гликозиды,
основным представителем которых является наперстянковый
дигитоксин, благодаря
метильным группам и небольшому числу
гидроксильных групп хорошо растворимы в липидах
и легко
всасываются из ЖКТ – их рекомендуется принимать перорально.
Наоборот, более полярные (более гидрофильные) сердечные
гликозиды, основным представителем которых является
К-строфантин, благодаря преобладанию полярных групп
(альдегидной, гидроксильных) над неполярными (метильными)
плохо проникают через клеточную мебрану и всасываются из ЖКТ
– их рекомендуется вводить парентерально (в кровь вены).
Агликоны не удерживаются в сердечной мышце, их эффект кратковременный. Кроме того, они токсичны (за исключением буфадиенолидов).
На скорость и силу кардиотонического эффекта влияют также число сахарных мономеров в гликозидной цепочке: наиболее сильное, но кратковременное действие оказывают монозиды;
удлинение углеводной цепочки действие сердечных гликозидов делает более мягким и продолжительным.
Слайд 17Таким образом, сахарные компоненты кардиогликозидов кардинально не меняют характер действия
генинов, но гидрокси- и метильные группы сахаров могут усиливать либо
ослаблять действие аналогичных групп агликона.
Углеводные части существенно влияют на растворимость, всасывание и фиксацию (задержку) кардиогликозидов в клетках сердечной мышцы, т.е. на способность сердечных гликозидов проникать в мышцу сердца и аккумулироваться в ней, а также
на силу и длительность кардиотонического действия, делая эффект этих веществ более или менее пролонгированным и резким.
Слайд 18Физико-химические свойства сердечных гликозидов
В чистом виде выделенные из ЛРС
сердечные гликозиды представляют собой бесцветные или бело-кремовые кристаллические вещества без
запаха и горького вкуса. Для них характерна определенная точка плавления (около 200 ºС) и оптическая активность (обусловленная присутствием в молекуле гликозильной части), многие кардиогликозиды флуоресцируют в УФ-свете.
Сердечные гликозиды плохо растворимы в органических растворителях (хлороформе, эфире), но хорошо – в воде, а еще лучше – в водных растворах этанола и метанола.
Чем длиннее сахарная цепочка КГ, тем их растворимость в воде лучше. Агликоны, наоборот, растворимы в неполярных растворителях и нерастворимы в воде.
Молекулы сердечных гликозидов легко гидролизуются: как ферментами-гидролазами, так и неферментным путем в диапазоне кисл. рН, в результате их гликозильная цепочка ступенчато или полностью отщепляется от генина. Как правило, при ферментном гидролизе углеводный фрагмент расщепляется постепенно и мягко, одно звено за другим, при кислотном – более резко, часто с отрывом больших кусков или даже всей сахаристой цепочки от агликона.

Слайд 19Многие сердечные гликозиды достаточно быстро окисляются кислородом воздуха.
К разрушению КГ
приводит и нахождение их при повышенной температуре.
В щелочной среде,
вследствие наступающего раскрытия лактонного кольца, сердечные гликозиды теряют свою кардиотоничекую активность и превращаются в биологически малоактивные изо-соединения.
Таким образом, если кислая среда ведет к отделению сахаристой части от агликона, то щелочная – к утере сердечными гликозидами своих специфических кардиотонических свойств.
Лучше всего эти свойства у сердечных гликозидов сохраняются при нейтральных показаниях рН.
Эти обстоятельства следует учитывать при заготовке и сушке ЛРС и при технологии выделения из него кардиогликозидов.
Слайд 20Выделение сердечных гликозидов из ЛРС.
Обычно используют упрощенный
способ выделения КГ.
Для этого определенное количество измельченного
ЛРС (напр.,
листьев ландыша) в течение суток подвергают экстракции 50%-м
или 70%-м этанолом. Спирт одновременно препятствует ферментному гидролизу сердечных гликозидов, отделению сахаристой части от агликона.
В этих концентрациях спирта растворятся гликозиды и агликоны сердечных гликозидов. Полученный экстракт выпаривают под вакуумом при температуре 50–60 ºС (выпаривание при более высоких значениях ведет к инактивации сердечных гликозидов – потере ими качественных свойств).
Густой экстракт разбавляют водой и многократно обрабатывают хлороформом или другим органическим растворителем.
Очистку можно проводить методом фильтрации через колонку с оксидом алюминия, которая при этом поглощает хлорофилл, флавоноиды, смолистые и другие липофильные балластные вещества, делая раствор более прозрачным. Далее проводят разделение суммы сердечных гликозидов на хроматографических колонках с Al2O3, силикагелем или другим сорбентом. Образующиеся на сорбенте нужные зоны берут и элюируют определенным растворителем.

Слайд 21
Сегодня еще не существует достоверных методов химического анализа сердечных гликозидов.
Кроме того, нет и общепризнанных химических способов выявления молекул этих
веществ.
Потому используют качественные реакции на те или иные части структуры молекул КГ
Реакции по выявлению КГ
1. На 5-членное лактонное кольцо:
- Балье: пикриновая к-та в щелочной среде с КГ дает красное окрашивание;
- Легаля: нитропруссидом Na КГ окрашиваются в оранжево-красный цвет;
- Кедде: 3,5-динитробензойной к-той в щелоч.рН КГ дают красно-фиолетовое окрашив.
2. На стероидное ядро молекулы:
- Либермана-Бурхардта: КГ в лядяной уксусной к-те+уксус.ангидрид и конц.H2SO4
(50:1 по объему) дает изменяющуюся окраску – от розовой к зеленой и синей;
- Розенгейма: КГ в хлороформе+90% водный р-р трихлоруксусной к-ты ведет к появлению изменяющейся окраски: от розовой до лиловой и синей.
3. На дезоксисахара гликозидной цепочки:
- Келлер-Килиани: КГ в ледяной уксусной к-те (со следами Fe3+)+ конц.H2SO4: на границе слоев появляется бурое кольцо, а верхний слой становится сине-зеленым;
- Пезеца: нагрев КГ с ксантгидролом в ледяной уксусной к-те+капли H2SO4 дает красное окрашивание;
- если дезоксисахара в КГ закрыты, проводят предварительный гидролиз с помощью
трихлоруксусной к-ты. Освобождаемый дезоксисахар можно выявить также в реакции с
нитрофенилгидразином и щелочью – раствор развивает голубую окраску.
4. На буфадиенолиды:
- Татье: к спиртовому экстракту КГ добавляют 2-3 капли конц. HCl со следами FeCl3 и нагревают. Агликоны буфадиенолидов дают красное окрашивание.
- КГ растворяют в хлороформе + 3 капли SbCl3 (треххлористой сурьмы) и нагревают: появляется лиловое окрашивание.
Определение активности КГ и стандартизация ЛРС
Валор – это количество единиц действия (КЕД, ГЕД или ЛЕД) в 1г ЛРС.

Слайд 22Определение активности сердечных гликозидов и стандартизация ЛРС. Активность сердечных гликозидов
в ЛРС, в лекарственных формах и в ЛС определяют биометодом.
Активность устанавливают, сравнивая опытный образец с препаратом-стандартом (кристаллическим сердечным гликозидом с известным количеством единиц действия) и выражают в особых единицах действия. Таковыми являются: кошачьи единицы действия (КЕД), голубиные единицы действия (ГЕД) или лягушачьи единицы действия (ЛЕД) – все зависит от того, сердца каких из этих животных используют для испытания активности ЛРС. В результате этих испытаний устанавливают наименьшие дозы стандарта и испытуемого образца, которые вызывают систолическую остановку сердца. Цифовые значения активности выражают в пересчете на 1 г препарата.
Поскольку КЕД>ГЕД>ЛЕД, то валор 1 г ЛРС будет зависеть от природы сердец, в частности, он будет больше при выражении в ЛЕД и меньше при выражении в ГЕД или КЕД.
Слайд 23Сердечные гликозиды по их молекулярной структуре делят на подгруппы:
1)
карденолиды:
▫ наперстянковые,
▫ строфантовые,
▫ строфантидоловые;
2) буфадиенолиды.
Классификация.
Слайд 24КГ Наперстянки пурпурной
1) Пурпуреагликозид А: дигитоксигенин–О-(дигитоксоза)3–глюкоза;
Дигитоксин: дигитоксигенин–О-(дигитоксоза)3;
2) Пурпуреагликозид
В: гитоксигенин–О-(дигитоксоза)3–глюкоза;
Гитоксин: гитоксигенин–О-(дигитоксоза)3;
3) Глюкогиталоксин: гиталоксигенин–О-(дигитоксоза)3–глюкоза;
Гиталоксин: гиталоксигенин–О-(дигитоксоза)3.
Слайд 25КГ Наперстянки крупноцветковой
Н. крупноцветковая содержат 3 карденолида:
ланатозиды А, В и
С (дигиланиды А, В и С),
у которых агликонами являются,
соответственно: дигитоксигенин, гитоксигенин и дигоксигенин. Их вторичные гликозиды, которые образуются при сушке сырья и связаны с отщеплением конечной глюкозы в цепочке первичных гликозидов, названы как
ацетилдигитоксин, ацетилгитоксин, ацетилдигоксин, а третичные гликозиды, которые образуются после отщепления еще одного звена дигитоксозы, названы соответственно как дигитоксин, гитоксин и дигоксин.
Слайд 261) Ланатозид А: дигитоксигенин–О-(дигитоксоза)2–ацетилдигитоксоза–глюкоза;
Ацетилдигитоксин: дигитоксигенин–О-(дигитоксоза)2–ацетилдигитоксоза;
Дигитоксин: дигитоксигенин–О-(дигитоксоза)2;
2) Ланатозид В:
гитоксигенин–О-(дигитоксоза)2–ацетилдигитоксоза–глюкоза;
Ацетилгитоксин: гитоксигенин–О-(дигитоксоза)2–ацетилдигитоксоза;
Гитоксин: гитоксигенин–О-(дигитоксоза)2;
3) Ланатозид С: дигоксигенин–О-(дигитоксоза)2–ацетилдигитоксоза–глюкоза;
Ацетилдигоксин: дигоксигенин–О-(дигитоксоза)2–ацетилдигитоксоза;
Дигоксин: дигоксигенин–О-(дигитоксоза)2.
Слайд 27
Digitalis purpurea L. - Наперстянка пурпурная
Digitalis purpureae folia
– сем.
Норичниковые (Scrophulariaceae).
Двулетнее травянистое растение высотой до 1,2 м. Произрастает в
Западной Европе, Карпатах. Во флоре Беларуси в диком виде не отмечено, но иногда культивируется как декоратив-ное или ЛР. Розеточные и стеблевые листья удиненно-обратно-яйцевидные, черешковые длиной до 30 см и шириной до 15 см. Стеблевые нижние – черешковые, верхние – сидячие. Края листьев неравномерно-городчатые. Листовые пластинки сверху темно-зеленые, морщинистые, снизу – серо-зеленые (из-за обилия волосков) и с сильно выступающими жилками, показывающими сетчатый рисунок. Соцветие – однобокая кисть, состоящая из поникающих наперстковидных крупных колокольчатых цветков – пурпурных снаружи и бело-розовых внутри с пурпурными пятнами в зеве.
Слайд 281- Digitalis purpurea L. - наперстянка пурпуровая
2- D. grandiflora Mill.
- наперстянка крупноцветковая
3- D. lanatae Ehrh. - наперстянка шерстистая
4- D. ferruginea L. - наперстянка ржавая
Слайд 29
Наперстянка крупноцветковая – Digitalis grandiflora L.
Digitalis grandiflorae folia -
наперстянки крупноцветковой листья
Наперстянка шерстистая – Digitalis lanatae Ehrh.
Digitalis lanatae folia
– наперстянки шерстистой листья
сем.Норичниковые (Scrophulariaceae).
Многолетнее травянистое растение высотой 40–100 см. Во флоре Беларуси встречается редко (внесено в Красную книгу).
Н. крупноцветковую, как и н. пурпурную, в ботанических садах выращивают как 2-летние, свето-любивые, засухоустойчивые растения, имеющие декоративную
и лекарственную значимость.
У н. крупноцветковой, в отличие
от н. пурпурной, листья с острой верхушкой, продолговато-ланцетные, края неравномерно-пильчатые, цвет листовой плас-тинки с обеих сторон темно-зеленый. Цветки колокольчатые, бело-желтые, образуют в июне–июле поникающую однобокую кисть.
Многолетнее травянистое растение высотой до 60–80 см. В культуре выращивается обычно как 2-летнее растение, высотой до 2 м. Естественно произрастает на Кавказе, Балканах, но считается редким, исчезающим видом. В РБ известно только в культуре. Стебли прямостоячие, красно-фиолетовые, вверху густо опушенные, особенно цветочная кисть. Прикорневые розеточные и нижние стеблевые листья продолговато-ланцетные, цельнокрайние, опушенные, верхние стеблевые – ланцетные, сидячие, уменьшающиеся в размере и переходящие в прицветники, покрытые волосками. Цветет в июне–августе. Соцветие – густая длинная и многосторонняя кисть из цветков шаровидной формы буро-желтого цвета с лиловыми жилками.
Листья наперстянки (пурпурной и крупноцветковой) содержат 2 % стероидных сапонинов, флавоноиды (рутин, производные апигенина и лютеолина), антрахиноны, фенолкарбоновые кислоты (ванилиновую, кумаровую, кофейную и др.), 5 % иридоидов, дубильные вещества, алкалоиды. В отношении КГ у н. пурпурной и н. крупноцветковой есть некоторые различия

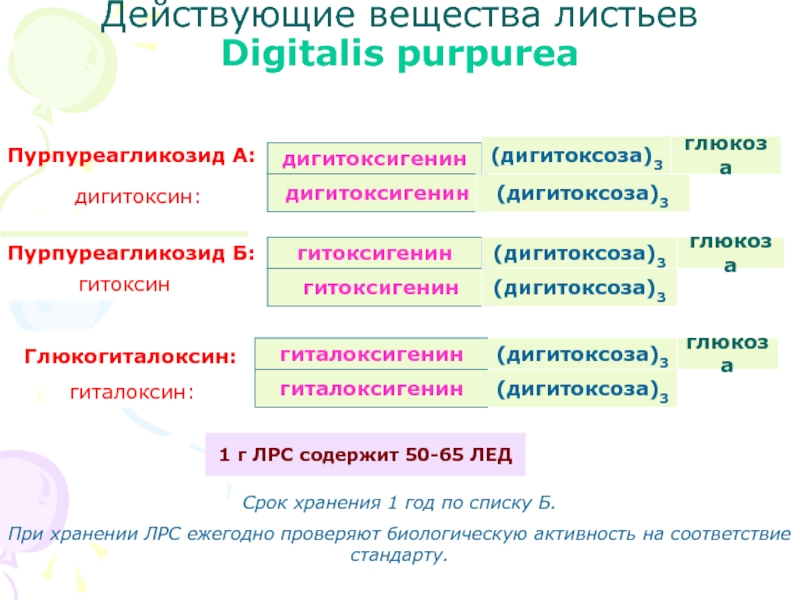
Слайд 30Действующие вещества листьев
Digitalis purpurea
Пурпуреагликозид А:
дигитоксигенин
(дигитоксоза)3
глюкоза
дигитоксин:
дигитоксигенин
(дигитоксоза)3
Пурпуреагликозид Б:
гитоксигенин
(дигитоксоза)3
глюкоза
гитоксин
гитоксигенин
(дигитоксоза)3
Глюкогиталоксин:
гиталоксигенин
(дигитоксоза)3
глюкоза
гиталоксин:
гиталоксигенин
(дигитоксоза)3
1 г
ЛРС содержит 50-65 ЛЕД
Срок хранения 1 год по списку Б.
При хранении ЛРС ежегодно проверяют биологическую активность на соответствие стандарту.
Слайд 31Действующие вещества листьев
Digitalis grandiflora
Ланатозид А: дигитоксигенин-(дигитоксоза)2- ацетил-дигитоксоза-глюкоза
Ланатозид B: гитоксигенин-(дигитоксоза)2-
ацетилдиги-токсоза-глюкоза
Ланатозид C: дигоксигенин-(дигитоксоза)2- ацетилдиги-токсоза-глюкоза
У листьев Digitalis lanatae
Ланатозид А, Ланатозид B,
Ланатозид C и еще
Ланатозид D: дигинатигенин-(дигитоксоза)2- ацетилдиги-токсоза-глюкоза
Ланатозид E: гиталоксигенин-(дигитоксоза)2- ацетилдиги-токсоза-глюкоза
1г листев D. grandiflora содержит 60 ЛЕД, а D. lanatae – 100 ЛЕД
Слайд 32Из листьев н. пурпурной и н. крупноцветковой получают ЛС Дигитоксин
и Кордигит, который по действию аналогичен Дигитоксину, но обладает меньшим
куммулятивным эффектом. ЛС применяют при хронической сердечной недостаточности, требующей длительного лечения, тахикардии, мерцательной аритмии. Кроме названных ЛС, можно использовать также водные настои из листьев, которые способствуют исчезновению отеков, одышки, уменьшению застойных явлений, урежению пульса, увеличению скорости кровотока, повышению диуреза и улучшению общего состояния.
Из листьев н. шерстистой получают кардиотонические ЛС Целанид, Дигоксин, Дигален-нео, а также Лантозид (70 %-й спиртовой раствор суммы гликозидов из листьев н. шерстистой – т. е. ланатозидов А, В, С, D и Е и др.). Они меньше куммулируют, быстрее всасываются и быстрее выводятся, чем кардиогликозиды из н. пурпурной и н. крупноцветковой.
Слайд 33Strophantus kombe Oliv. – строфант комбе,
S.gratus (Hook.)Franch – с. привлекательный,S.
hispidus DC – с. щетинистый
Strophanthi semina
Сем. Apocinaceae
- Кутровые
Многолетние лианы. Имеют супротивные эллиптические листья. Произрастают в тропиках Восточной (первый вид) и Западной (два других вида) Африки. Плод – двулистовка, достигающая в длину 1 м, содержит многочисленные продолговатые семена длиной 18 мм, шириной 3–6 мм, с перистой летучкой на конце. Семена продолговатые, с одного конца закругленные, с другого вытянутые. У S. kombe они серебристо-зеленые, с прижатыми шелковистыми волосками; S. hispidus – бурые, менее опушенные; S. gratus – желто-бурые, голые.
Семена строфанта хранят три года по списку А.
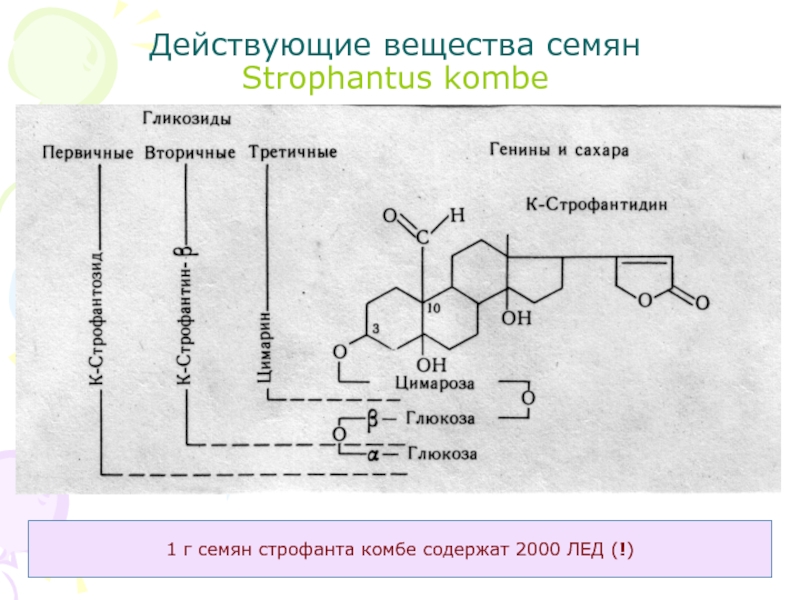
Слайд 34Действующие вещества семян
Strophantus kombe
1 г семян строфанта комбе содержат
2000 ЛЕД (!)
Слайд 35
Х и м и ч е с к и й
с о с т а в Л Р
С . Семена с. Комбе содержат кардиотонические гликозиды, производные агликона строфантидина: первичный – К-строфантозид, вторичный – К-строфантин-β и третичный – цимарин, а также гликозид цимарол. Общее количество сердечных гликозидов в семенах с. Комбе составляет около 10 %, с. привлекательного – 4–8 %, причем 90 % их приходится на рамнозид G-строфантин (уабаин). В семенах всех видов строфанта содержится жирное масло (30 %), сапонины, холин.
О с н о в н о е д е й с т в и е : кардиотоническое.
И с п о л ь з о в а н и е . Из семян с. Комбе получают два основных ЛС: Строфантин К, который состоит из смеси К-строфантозида и К-строфантина-β и Строфантидин-ацетат. ЛС характеризуются высокой эффективностью и быстротой действия (эффект проявляется через 5–10 минут, максимум достигается через 15–30 минут, продолжительность действия небольшая), практически не обладают куммулятивным влиянием и быстро выводятся из организма. Их рекомендуют вводить в кровь больным при неэффективности применения наперстянковых сердечных гликозидов, при острой сердечно-сосудистой недостаточности, остром инфаркте миокарда, тяжелых формах хронической недостаточности кровообращения и т. д.

Слайд 36Convallaria majalis L. - ландыш майский
cем. ландышевые - Convallariaceae
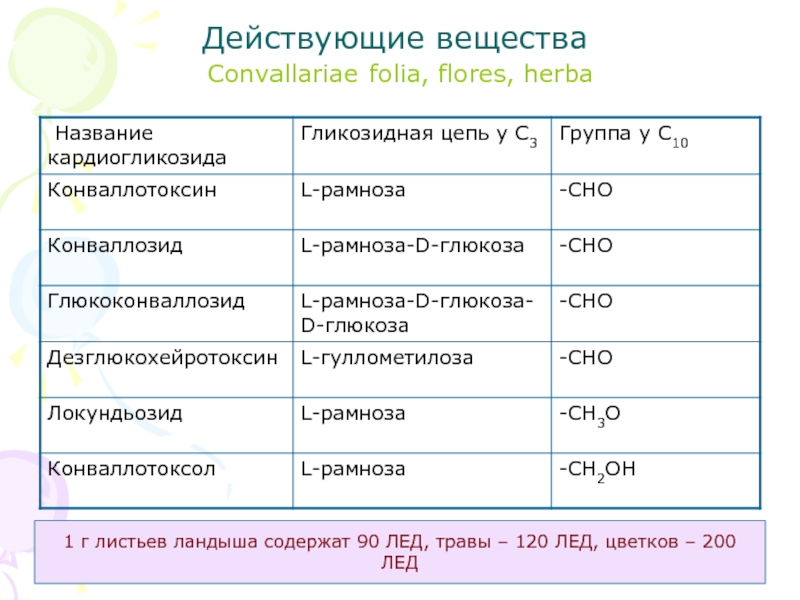
Convallariae folia, flores, herba
Ландыш майский, а также л. закавказ-ский и
л. японский - многолетние травянистые растения. Благодаря горизонтальному корневищу с корнями сохраняются зимой в почве. Весной от корневища отрастают два или четыре листа удлиненно-эллиптической формы с дугонервным жилкованием и цветочная стрелка высотой 10–30 см, несущая редкую одностороннюю поникающую кисть белых душистых цветков диаметром до 1 см. Цветут в апреле–мае, плоды (оранжево-красные ягоды) созревают в августе. Л. майский растет в смешанных и широколиственных лесах Европейской части СНГ; в Крыму и на Кавказе произрастает л. закавказский, а в Забайкалье, Приамурье и Приморском крае – л. японский, которые отличаются от л. майского более крупными листьями и бóльшими по размеру цветками. Траву и цветки ландыша заготавливают во время цветения, а листья – после цветения. ЛРС сушат при температуре 40–50 ºС в тени.
Слайд 37Действующие вещества
Convallariae folia, flores, herba
1 г листьев ландыша содержат
90 ЛЕД, травы – 120 ЛЕД, цветков – 200 ЛЕД
Слайд 38Х и м и ч е с к и й
с о с т а в Л Р
С . Главные действую-щие вещества – кардиотонические гликозиды, производные агликона строфантидина и строфантидола, но генин – локундьозид наперстянкового типа. Выявлено около 20 КГ, а также флавоноиды (производные кверцетина, лютеолина, кемпферола), стероидные сапонины, эфирное масло (в цветках). Содержание КГ в цветках составляет до 5 %.
О с н о в н о е д е й с т в и е : кардиотоническое, диуретическое.
И с п о л ь з о в а н и е . Из листьев, цветков и травы ландыша получают ЛС Коргликон и Конвафлавин (в состав последнего кроме кардиогликозидов входят флавоноиды, он обладает также спазмолитическим и желчегонным действием). Коргликон оказывает успокаи-вающее действие и усиливает сокращения сердечной мышцы, в тканях не куммулируется. Применяют при неврозах сердца, кардиосклерозе, острой и хронической сердечной недостаточности. Настойка ландыша, а также настойка ландыша, валерианы, белладоны и ментола в составе капель Зеленина оказывают на сердце успокаивающее и слабое тоническое действие.

Слайд 39Adonis vernalis L. - Горицвет весенний
cем. Ranunculaceae –
лютиковые
Adonidis vernalis herba
Многолетнее травянистое растение с коротким многоглавым корневищем,
которое весной образует несколько ветвистых полулежащих стеблей, голых у основания и олиственных вверху. Листья очередные, сидячие, многократно-рассе-ченные на линейно-шиловидные голые сегменты. Цветки верхушечные, одиноч-ные, крупные, желтые. Появляются в числе первых весенних цветов в апреле–мае. Горицвет весенний естественно произрас-тает в лесостепной и степной зоне от Венгрии до Сибири, в Беларуси культиви-руется (в основном для фармацевтических нужд). Траву срезают на высоте 5–10 см от почвы, сушат на продуваемых стеллажах под навесом либо в сушилках при темпе-ратуре 40–50 ºС.
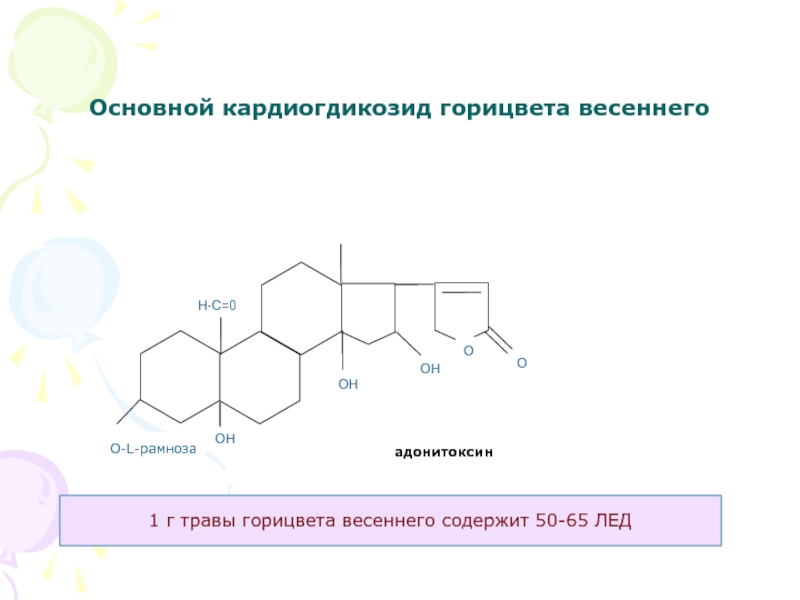
Слайд 40Основной кардиогдикозид горицвета весеннего
О
О
ОН
Н-С=0
ОН
OH
О-L-рамноза
адонитоксин
1 г травы
горицвета весеннего содержит 50-65 ЛЕД
Слайд 41Х и м и ч е с к и й
с о с т а в Л Р
С . В траве г. весеннего содержится ряд карденолидов, но основными являются адонитоксин (гидролизующийся на адонитоксигенин строфантового типа и L-рамнозу), цимарин, К-строфантин-β, адонитоксол и другие кардиогликозиды. Имеются сапонины, фитостерины, флавоноиды, дубильные в-ва, органич. кислоты.
О с н о в н о е д е й с т в и е : кардиотоническое, умеренно седативное, слабое мочегонное.
И с п о л ь з о в а н и е . Трава г. весеннего применяется для получения настоя, сухого экстракта, который входит в состав таблеток Бехтерева. Получаемые из травы сердечные гликозиды, в частности адонитоксин, входят в состав ЛС Адонизид, Адонис-бром, а Адонизид также является компонентом комплексного ЛС Кардивален. ЛС из горицвета применяют при сравнительно легких формах недостаточности кровообращения. В терапевтических дозах эти препараты не куммулируются. Кроме того, они используются как успокаиваю-щие средства при терапии неврозов и вегетодистонии, а также для лечения почечных заболеваний с симптомами недостаточ-ности сердечно-сосудистой системы.
П р о т и в о п о к а з а н и я . Настой травы горицвета и получаемые из него ЛС нельзя применять при беременности.

Слайд 42
Erysimum diffusum Ehrh.(=canescens Roth.)
Erysimi diffusi herba recens
cем.
Brassicaceae – Капустные
Двулетнее травянистое растение высотой 30–80 см. Стеблей несколько,
они ветвистые. Листья очередные, линейно-продолговатые или ланцетные, цельнокрайние. Все растение выглядит сероватым от покрывающих его коротких прижатых волосков. Цветки собраны в верхушечные рыхлые кисти, венчик четырехлепестный, бледно-желтый, длиной 10–14 мм, вдвое длиннее чашечки. Плод – 4-гранный стручок длиной до 7 см, направлен косо вверх или параллельно стеблю. Цветение происходит в мае–июне. Ж. раскидистый произрастает в зоне лесостепи Европейской части СНГ, в Беларуси культивируется. Вместе с травой ж. раскидистого (серого) допускается использование травы ж. левкойного (E. cheiranthoides L.), произрастающего как сорняк, который представляет собой однолетнее травянистое растение с ветвистым стеблем и очередными продолговато-ланцетными цельнокрайними или зубчатыми листьями ярко-зеленой окраски; все растение также опушенно короткими прижатыми волосками. Цветки в верхушечных кистях с ярко-желтыми лепестками длиной 5 мм, вдвое длиннее чашелистиков. После отцветания они образуют стручки длиной 1–3 см на отклоненных ножках, направленные косо вверх. Заготовку ЛРС ведут во время цветения растений. Траву скашивают, сразу собирают и сырую немедленно прессуют.

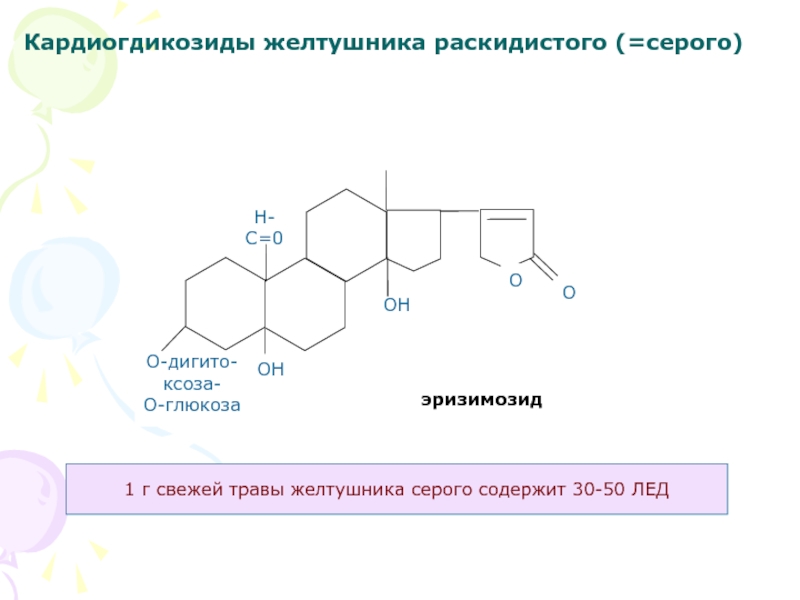
Слайд 43Кардиогдикозиды желтушника раскидистого (=серого)
эризимозид
ОН
ОН
Н-С=0
О-дигито-
ксоза-
О-глюкоза
1 г свежей травы желтушника серого содержит
30-50 ЛЕД
Слайд 44Х и м и ч е с к и й
с о с т а в Л Р
С . Надземная часть желтушника раскидистого (серого) содержит карденолиды строфантового типа (листья – 1–1,5 %, стебли – 0,5 %, семена – 2–6 %), в которых генином является строфантин, а в гликозильной части находится дигитоксоза, присутствующая у сердечных гликозидов наперстянки, но конечным звеном цепочки является глюкоза. Основные КГ травы желтушника – эризимозид и эризимин. Присутствуют также флавоноиды (производные изорамнетина и кверцетина). В семенах имеются эризимозид (2,5 %), гликозиды строфантина (1,4 %), масло (30–40 %) с содержанием олеиновой (50 %), эруковой (30 %), линоленовой (5 %) и других непредельных жирных кислот.
О с н о в н о е д е й с т в и е : кардиотоническое.
И с п о л ь з о в а н и е . Сок ж. раскидистого (серого) входит в состав ЛС Кардиовален (вместе с экстрактом плодов боярышника, корней валерианы, адонизидом, камфорой, натрия бромидом) и применяется при ревматических пороках сердца, кардиосклерозе с нарушением кровообращения, неврозах, аритмии, стенокардии. Семена ж. раскидистого идут также на приготовление получаемого главным образом из семян строфанта Комбе ЛС Строфантидина ацетат. В медицине препараты желтушника применяются, как и строфантин, при острой и хронической сердечной недостаточности II–III степени с тяжелым нарушением кровообращения.

Слайд 45
Тот факт, что на протяжении столетий и до настоящего времени
ЛР, содержащие сердечные гликозиды, не утратили своего значения как источники
ФАВ, позволяет выделить два перспективных направления будущей работы:
1) изучать виды – возможные потенциальные источники сердечных гликозидов: растения рода Морозник (Helleborus), Морской лук (Urginea), Бовиейя (Bowiea), Джут (Corhus), Кендырь (Apocynum), Обвойник (Periploca), Олеандр (Nerium), Купена (Polygonatum)и др. Филогенетический (хемотаксономический) принцип может облегчить поиск таких видов;
2) разрабатывать получение сердечных гликозидов биотехнологическим способом:
из культуры клеток и тканей растений, синтезирующих эти соединения.
Слайд 46Нефармакопейные лекарственные растения – потенциальные источники кардиотонических гликозидов
Helleborus niger
L.
Polygonatum officinalis L.
Морозника корневища с корнями
Купены лекарственной плоды
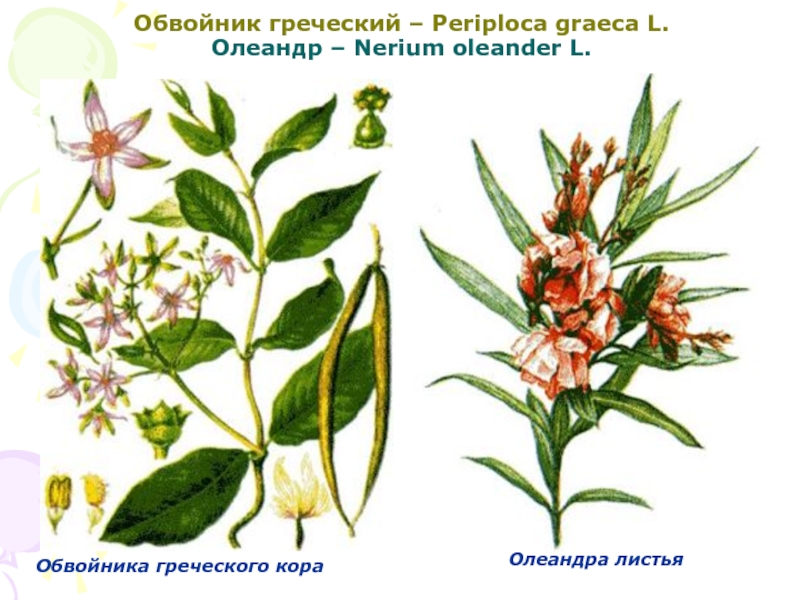
Слайд 47Обвойник греческий – Periploca graeca L.
Олеандр – Nerium oleander L.
Обвойника
греческого кора
Олеандра листья