Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Классификация и номенклатура ферментов
Содержание
- 1. Классификация и номенклатура ферментов
- 2. Номенклатура ферментов. На первых этапах развития энзимологии
- 3. Первая попытка ввести правило для названий ферментов
- 4. В 1961 г. V Международный биохимичекий конгресс
- 5. Итак, все ферменты разделяют на 6 классов
- 6. НОМЕНКЛАТУРА ОКСИДОРЕДУКТАЗСтруктура систематического названия оксидоредуктаз такова: название
- 7. Тривиальные (рабочие) названия оксидоредуктаз имеют следующую структуру:
- 8. 4. Монооксигеназы – оксидоредуктазы, катализирующие внедрение одного
- 9. Примеры:1) Восстановление пирувата до лактата:Донор электронов -
- 10. 2) Восстановление сульфит-иона до сероводорода с помощью
- 11. 4) Окисление цистеина кислородом с включением в
- 12. НОМЕНКЛАТУРА ТРАНСФЕРАЗТрансферазы катализируют реакции переноса различных радикалов
- 13. Например, метилтрансферазы (реакции биологического метилирования – перенос
- 14. Систематические названия ферментов класса трансфераз строятся следующим
- 15. 1) Превращение серина в глицин (перенос оксиметильной группы)Систематическое название фермента КФ 2.1.2.1.– L-серин:тетрагидрофолат-5,10-оксиметилтрансфераза, тривиальное – серин-оксиметилтрансфераза
- 16. 2) Образование ацетилфосфата (перенос ацетильной группы):Фермент катализирующий
- 17. 3) Образование аланина из пирувата:Систематическое название КФ 2.6.1.2. – аланин:2-оксоглутарат-аминотрансфераза; тривиальное –аланин-аминотрансфераза.
- 18. Самый большой подкласс трансфераз составляют ферменты, катализирующие
- 19. тривиальная номенклатура - киназы, систематическая –фосфотрансферазами. тривиальная
- 20. Образование глюкозо-6-фосфата из глюкозы и АТФ (первая
- 21. НОМЕНКЛАТУРА ГИДРОЛАЗСистематические названия гидролаз содержат наименование гидролизуемого
- 22. Гидролазы, катализирующие гидролиз сложноэфирных связей, образуют подкласс
- 23. Гидролиз жировПо систематической номенклатуре фермент КФ 3.1.1.3. называется триацилглицерин-моноацилатгидролаза, по тривиальной - триацилглицерин-липаза.
- 24. Более значительную группу гидролаз образуют протеазы(протеолитические ферменты),
- 25. НОМЕНКЛАТУРА ЛИАЗФерменты четвертого класса – лиазы. Катализируют
- 26. Наиболее обширный подкласс образуют углерод-углеродлиазы, среди которых
- 27. НОМЕНКЛАТУРА ИЗОМЕРАЗПервый подласс изомераз (КФ 5.1.) составляют
- 28. Если в молекуле субстрата имеется несколько хиральных
- 29. Отдельный подкласс изомераз образуют ферменты, катализирующие реакции
- 30. Подкласс 5.4. изомераз образуют ферменты, катализирующие внутримолекулярный
- 31. НОМЕНКЛАТУРА ЛИГАЗШестой класс ферментов (лигазы, синтетазы) недаром
- 32. Например, ферменты подкласса 6.3. катализируют многочисленные реакции
- 33. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Номенклатура ферментов.
На первых этапах развития энзимологии названия ферментам давали
их первооткрыватели по случайным признакам (тривиальная номенклатура).
относятся названия ферментов: пепсин, трипсин, химотрипсин. Слайд 3Первая попытка ввести правило для названий ферментов была предпринята Е.
Дюкло в 1898 г. (рациональная номенклатура).
Согласно рациональной номенклатуре, простой
фермент называли по названию субстрата с добавлением окончания -аза (ДНКаза, РНКаза, амилаза, уреаза). Для названия холофермента по рациональной номенклатуре использовали название кофермента (пиридоксальфермент, геминфермент).
Позднее в названии фермента стали использовать название субстрата и тип катализируемой реакции (алкогольдегидрогеназа).
Слайд 4В 1961 г. V Международный биохимичекий конгресс (IUBМВ) , проходивший
в Москве, утвердил систематическую номенклатуру ферментов.
Систематическая классификация учитывает реакционную
и субстратную специфичность ферментов. Все ферменты включены в «Каталог ферментов» под своим классификационным номером (КФ), состоящим из четырех цифр.1-я цифра КФ указывает на принадлежность фермента к одному из шести главных классов, в зависимости от типа реакции.
2-я цифра – подкласс (в зависимости от субстрата).
3-я цифра – подподкласс (в зависимости от типа кофермента, реагента или особенностей реакции)
4-я цифра - порядковый номер фермента в пределах данного подподкласса.
Слайд 5Итак, все ферменты разделяют на 6 классов в зависимости от
типа реакции:
1. Оксидоредуктазы, катализирующие окислительно-восстанови-тельные реакции.
2. Трансферазы, катализирующие реакции межмолекулярного
переноса различных химических групп и остатков.3. Гидролазы, катализирующие реакции гидролиза внутри-молекулярных связей.
4. Лиазы, катализирующие расщепление или образование связи без участия окисления или гидролиза
5. Изомеразы, катализирующие реакции изомеризации.
6. Лигазы, катализирующие реакции присоединения,
сопряженные с разрывом макроэргической связи в АТФ или ГТФ, ЦТФ, УТФ, ТТФ.
Слайд 6НОМЕНКЛАТУРА ОКСИДОРЕДУКТАЗ
Структура систематического названия оксидоредуктаз такова:
название субстрата – донора
электронов (восстановителя): название акцептора электронов (окислителя) – название класса (оксидоредуктаза.).
Таким образом, приступая к построению названия фермента необходимо:
установить субстрат;
установить акцептор электронов.
Поскольку многие окислительно-восстановительные реакции обратимы, а прямую и обратную реакцию катализирует один и тот же фермент, то условлено,
что в качестве субстрата для построения названия фермента выбирается метаболит, являющийся донором электронов, т.е. субстрат, подвергающийся
окислению.
Слайд 7Тривиальные (рабочие) названия оксидоредуктаз имеют следующую структуру:
приставка - название
субстрата, корень – название группы оксидоредуктаз.
Наиболее распространенные группы оксидоредуктаз
следующие: 1. Дегидрогеназы – оксидоредуктазы, катализирующие дегидрирование субстрата с использованием в качестве акцептора водорода любых молекул кроме кислорода.
2. Если перенос водорода от молекулы донора трудно доказуем, то такие оксидоредектазы называют редуктазами.
3. Оксидазы – оксидоредуктазы, катализирующие окисление субстратов с молекулярным кислородом в качестве акцептора электронов без включения
кислорода в молекулу субстрата.
Слайд 84. Монооксигеназы – оксидоредуктазы, катализирующие внедрение одного атома кислорода в
молекулу субстрата с молекулярным кислородом в качестве донора кислорода.
5.
Диоксигеназы – оксидоредуктазы, катализирующие внедрение 2 атомов кислорода в молекулу субстрата с молекулярным кислородом в качестве донора кислорода. 6. Пероксидазы – оксидоредуктазы, катализирующие реакции с пероксидом водорода в качестве акцептора электронов.
Окисление органических соединений может быть связано:
1) с потерей электрона;
2) с отрывом водорода от окисляемого субстрата;
3) с замещением атомов на другие, более электроотрицательные атомы.
Слайд 9Примеры:
1) Восстановление пирувата до лактата:
Донор электронов - лактат, акцептор электронов,
т.е. окислитель - НАД+.
Систематическое название фермента КФ 1.1.1.27. –
лактат:НАД+-оксидоредуктаза, тривиальное –лактатдегидрогеназа.
Слайд 102) Восстановление сульфит-иона до сероводорода с помощью НАДФН:
Систематическое название этого
фермента – сероводород:НАДФ+-оксидоредуктаза,
тривиальное – сульфитредуктаза.
3) Окисление β-D-глюкозы кислородом без
включения в его молекулу атомов кислорода: Систематическое название этого фермента –
β-D-глюкоза:кислород-оксидоредуктаза,
тривиальное – глюкозооксидаза.
Слайд 114) Окисление цистеина кислородом с включением в молекулу цистеина обоих
атомов кислорода:
Систематическое название фермента КФ 1.13.11.20.– цистеин:кислород-оксидоредуктаза,
тривиальное – цистеиндиоксигеназа.
Слайд 12НОМЕНКЛАТУРА ТРАНСФЕРАЗ
Трансферазы катализируют реакции переноса различных радикалов от молекулы-донора к
молекуле-акцептору, общая схема которых приведена ниже:
Д-Г + А ↔Д +
Г-Агде:
Д-Г –молекула донор группы Г,
А –молекула акцептор,
Г –переносимая группа
А, Д ≠ Н2О - реакции гидролиза, которые также соответствуют этой схеме, выделены в отдельный класс.
Слайд 13Например,
метилтрансферазы (реакции биологического метилирования – перенос метильных групп),
гликозилтрансферазы
(катализируют реакции переноса остатков сахаров на различные акцепторы),
ферменты переносящие
азотисные группы (трансаминазы – играют важную роль в обмене аминокислот), ферменты переносящие фосфатные группы.
Слайд 14Систематические названия ферментов класса трансфераз строятся следующим образом:
название донора
группы: название акцептора группы –
название переносимой группы – название класса
(тире между названием переносимой группы и названием класса не ставится). В тривиальные названия трансфераз включают название донора группы и название переносимой группы.
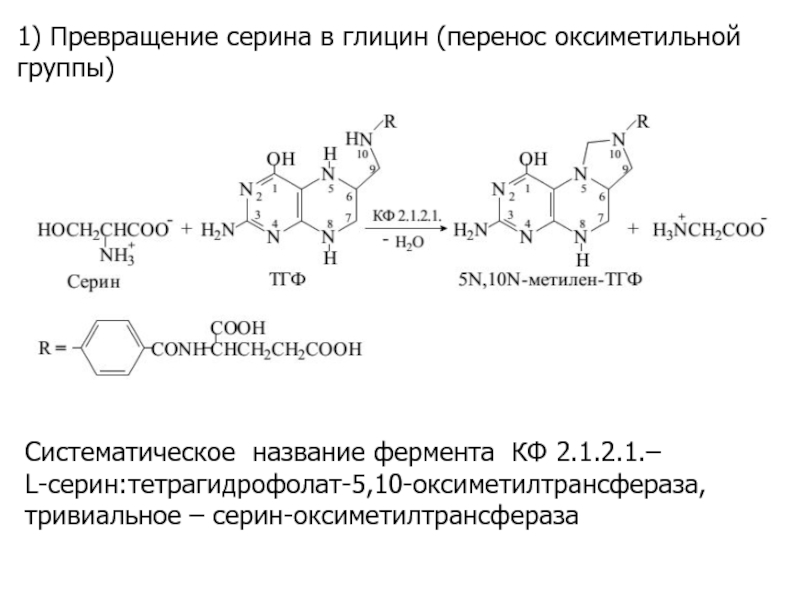
Слайд 151) Превращение серина в глицин (перенос оксиметильной группы)
Систематическое название фермента
КФ 2.1.2.1.–
L-серин:тетрагидрофолат-5,10-оксиметилтрансфераза, тривиальное – серин-оксиметилтрансфераза
Слайд 162) Образование ацетилфосфата (перенос ацетильной группы):
Фермент катализирующий эту реакцию по
систематической номенклатуре называется –
ацетил-КоА:ортофосфат-ацетилтрансфераза и имеет
классификационный номер КФ
2.3.1.8. Тривиальное название этого фермента –
фосфат-ацетилтрансфераза.
Слайд 173) Образование аланина из пирувата:
Систематическое название КФ 2.6.1.2. – аланин:2-оксоглутарат-аминотрансфераза;
тривиальное –аланин-аминотрансфераза.
Слайд 18Самый большой подкласс трансфераз составляют ферменты, катализирующие перенос остатков фосфорной
кислоты, её ангидридов и эфиров
(КФ 2.7.).
В подавляющем большинстве случаев
донором фосфата, дифосфата и нуклеотидного остатка является АТФ. Тривиальные названия ферментов, катализирующих реакции переноса фосфорсодержащих групп определяются фрагментом молекулы АТФ, которая переносится на субстрат.
Слайд 19тривиальная номенклатура - киназы, систематическая –
фосфотрансферазами.
тривиальная – пирофосфокиназами, систематическая
-дифосфотрансферазами.
если переносится остаток нуклетида, то такие ферменты и по
систематической и по тривиальной номенклатурам называются нуклеотидилтрансферазами.
Слайд 20Образование глюкозо-6-фосфата из глюкозы и АТФ (первая реакция процесса гликолиза):
Систематическое
название КФ 2.7.1.1. –АТФ:глюкоза-6-фосфотрансфераза;
тривиальное – гексокиназа.
Приставка гексо в
тривиальном названии означает, что этот фермент катализирует фосфорилирование не только глюкозы, но и других гексоз.
Слайд 21НОМЕНКЛАТУРА ГИДРОЛАЗ
Систематические названия гидролаз содержат наименование гидролизуемого субстрата и наименование
отщепляемой группы в сочетании со словом гидролаза.
Рекомендованные тривиальные названия многих
гидролаз образуют из названия гидролизуемого субстрата с добавлением окончания – аза.Подклассы гидролаз образованы в зависимости от природы гидролизуемой связи. Известны гидролазы катализирующие гидролиз сложноэфирных, пептидных, гликозидных, ангидридных и других связей.
Слайд 22Гидролазы, катализирующие гидролиз сложноэфирных связей, образуют подкласс КФ 3.1 –
эстеразы. Э
стеразы в зависимости от природы сложноэфирной
связи и класса
субстрата делятся на следующие подподклассы и группы:катализирующие гидролиз жиров называются – липазы;
моноэфиров фосфорной кислоты – фосфатазы;
диэфиров фосфорной кислоты – фосфодиэстеразы;
лактонов – лактоназы;
эфиров серной кислоты – сульфатазы;
ДНК – дезоксирибонуклеазы;
РНК -рибонуклеазы и др.
Слайд 23Гидролиз жиров
По систематической номенклатуре фермент КФ 3.1.1.3. называется триацилглицерин-моноацилатгидролаза,
по
тривиальной - триацилглицерин-липаза.
Слайд 24Более значительную группу гидролаз образуют протеазы
(протеолитические ферменты), катализирующие гидролиз пептидных
связей в белках и полипептидах (КФ 3.4.).
По месту атаки
молекулы субстрата протеолитические ферменты делятся на эндопептидазыи экзопептидазы.
Эндопептидазы еще называют протеиназами.
Протеиназы классифицируются по механизму действия, а точнее по строению активного центра.
В настоящее время известны: сериновые протеиназы (КФ 3.4.21.N), цистеиновые протеиназы (КФ 3.4.22.N), аспартатные протеиназы (КФ 3.4.23.N), металлопротеиназы (КФ 3.4.24.N).
Экзопептидазы гидролизуют пептиды с конца цепи: аминопептидазы с H2N-конца, карбоксипептидазы – с HOOC-конца
Слайд 25НОМЕНКЛАТУРА ЛИАЗ
Ферменты четвертого класса – лиазы. Катализируют негидролитическое расщепление субстрата
с образованием кратной связи или цикла и соответственно обратные реакции
– присоединение по кратным связям или реакции раскрытия цикла.Систематическое название фермента складывается из названия расщепляемого субстрата, названия отщепляемого фрагмента и слова «лиаза»
Слайд 26Наиболее обширный подкласс образуют углерод-углеродлиазы, среди которых основную массу составляют
ферменты, катализирующие реакции декарбоксилирования. По тривиальной номенклатуре эти ферменты называют
декарбоксилазами.Декарбоксилирование пирувата:
По систематической номенклатуре фермент, катализирующий эту реакцию – КФ 4.1.1.1., называется пируват:ацетальдегид-лиаза,
по тривиальной – пируватдекарбоксилаза.
Слайд 27НОМЕНКЛАТУРА ИЗОМЕРАЗ
Первый подласс изомераз (КФ 5.1.) составляют различные ферменты, катализирующие
процессы обращения конфигурации при хиральном атоме
углерода.
Если такой центр
в молекуле субстрата один, то происходит обращение конфигурации молекулы в целом. Поскольку оптические изомеры термодинамически эквивалентны, по крайней мере, в отсутствие других хиральных молекул, способных давать комплекс предпочтительно с одним из энантиомеров, то фермент в равной мере катализирует обращение конфигурации
в обоих направлениях. Конечным итогом действия такого фермента является образование рацемической смеси, поэтому такие ферменты называют
рацемазами.
Слайд 28Если в молекуле субстрата имеется несколько хиральных атомов углерода, то
обращение конфигурации при одном из них приводит к образованию нового
диастереомера. Ферменты, катализирующие такие процессы (реакцииэпимеризации), называют эпимеразами.
Эпимеризация рибулозо-5-фосфата
Систематическое название фермента КФ 5.1.3.1 D-рибулозо-5-фосфат-3-эпимераза.
Тривиальное название фермента рибулозофосфат-3-эпимераза.
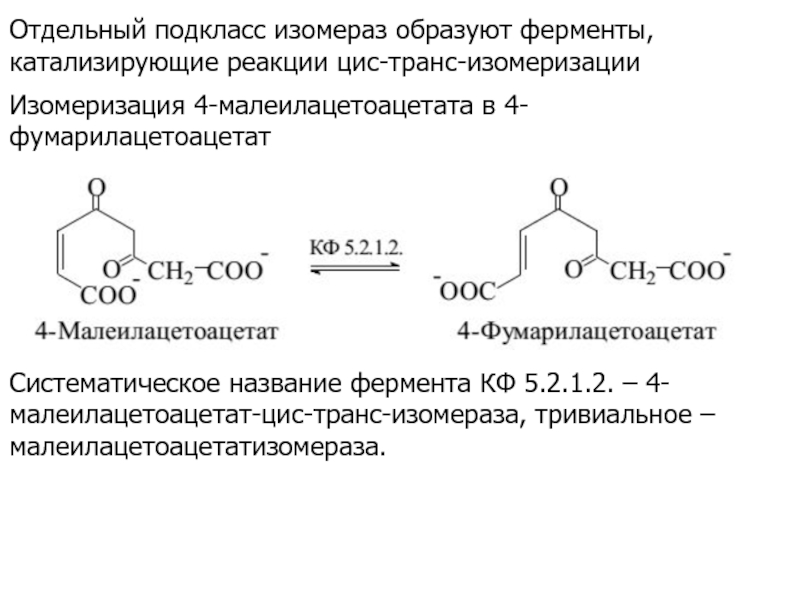
Слайд 29Отдельный подкласс изомераз образуют ферменты, катализирующие реакции цис-транс-изомеризации
Изомеризация 4-малеилацетоацетата в
4-фумарилацетоацетат
Систематическое название фермента КФ 5.2.1.2. – 4-малеилацетоацетат-цис-транс-изомераза, тривиальное –малеилацетоацетатизомераза.
Слайд 30Подкласс 5.4. изомераз образуют ферменты, катализирующие внутримолекулярный перенос различных фрагментов
без изменения степеней окисления атомов (внутримолекулярные трансферазы). Тривиальное название внутримолекулярных
трансфераз – мутазы.Слайд 31НОМЕНКЛАТУРА ЛИГАЗ
Шестой класс ферментов (лигазы, синтетазы) недаром имеет название похожее
на название четвертого класса ферментов (лиазы), поскольку класс лигаз составляют
ферменты, катализирующие реакции конденсации илиприсоединения, как и лиазы, но сопряженные с реакциями расщепления одной из пирофосфатных связей в молекуле нуклеозидтрифосфата (обычно АТФ или ГТФ).
Таким образом, в реакциях, катализируемых лигазами, обязательно участвует АТФ или ГТФ.
Слайд 32Например, ферменты подкласса 6.3. катализируют многочисленные реакции введения азотсодержащих групп
в органические соединения, т.е. катализируют образование связи углерод-азот.
Образование аспарагина из
аспарагиновой кислотыСистематическое название – аспарагинат:аммоний-лигаза
Тривиальное - аспарагинсинтетаза