Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Клеточные факторы врождённого иммунитета. Фагоцитоз и его стадии
Содержание
- 1. Клеточные факторы врождённого иммунитета. Фагоцитоз и его стадии
- 2. План занятияКлеточные факторы и определение фагоцитозаВиды и
- 3. Клеточные факторыКлеточные факторы – это молекулярные компоненты
- 4. Фагоцитоз — процесс поглощения и переваривания инородных
- 5. Виды фагоцитовНейтрофилы (палочко- и сегментоядерные)Мононуклеарные лейкоциты (промоноциты, моноциты и тканевые макрофаги)ЭозинофилыБазофилыДендритные клетки (ДК)
- 6. Нейтрофилы (15 суток) (палочко- и сегментоядерные) –
- 7. Слайд 7
- 8. Мононуклеарные лейкоциты (40-60 суток) (промоноциты, моноциты и
- 9. Слайд 9
- 10. Слайд 10
- 11. Эозинофилы (8-12 суток) - полиморфно-ядерные лейкоциты. Обладают
- 12. Слайд 12
- 13. Базофилы (8-12 суток) – очень крупные гранулоциты
- 14. Слайд 14
- 15. Дендритные клетки (DC) —популяция антигенпредставляющих крупных клеток ККМ с овальным
- 16. Слайд 16
- 17. Опсонины – белки сыворотки крови, обволакивающие микробы
- 18. Слайд 18
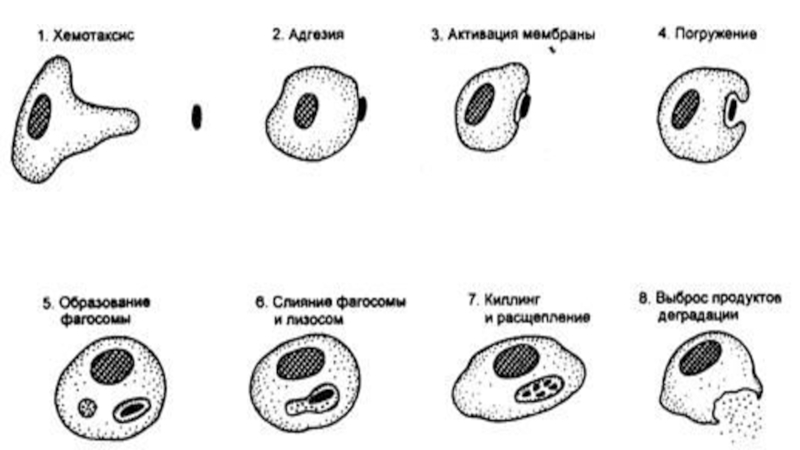
- 19. Основные этапы фагоцитарной реакции ХемотаксисАдгезияАктивация мембраныПогружениеОбразование фагосомыОбразование фаголизосомыКиллинг и расщеплениеВыброс продуктов деградации
- 20. 1. Хемотаксис — направленное движение клеток друг к
- 21. Слайд 21
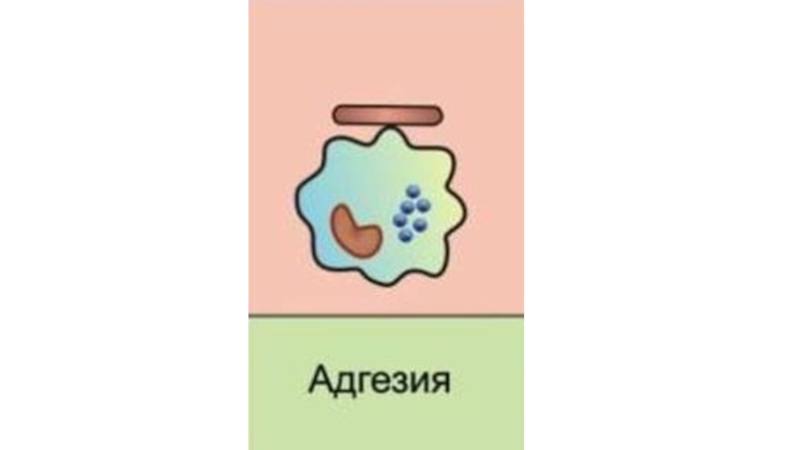
- 22. 2. Адгезия к объекту (сближение). Обусловлена наличием рецепторов для
- 23. Слайд 23
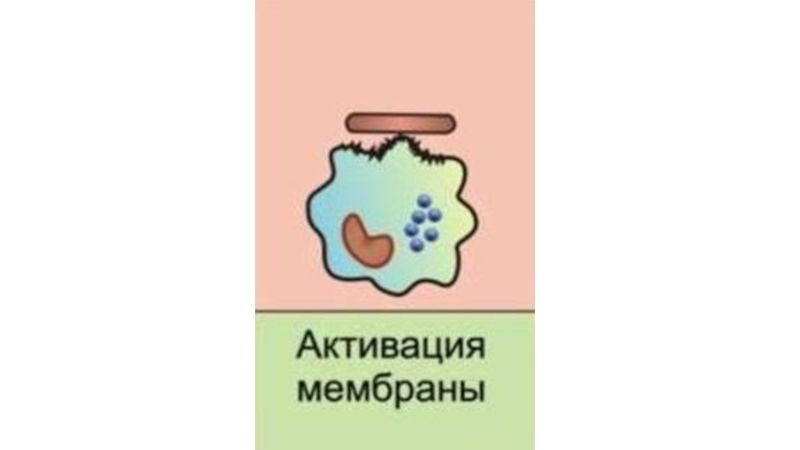
- 24. 3. Активация мембраны. Подготовка объекта к поглощению путём активации протеинкиназы С и выхода ионов кальция из внутриклеточных депо.
- 25. Слайд 25
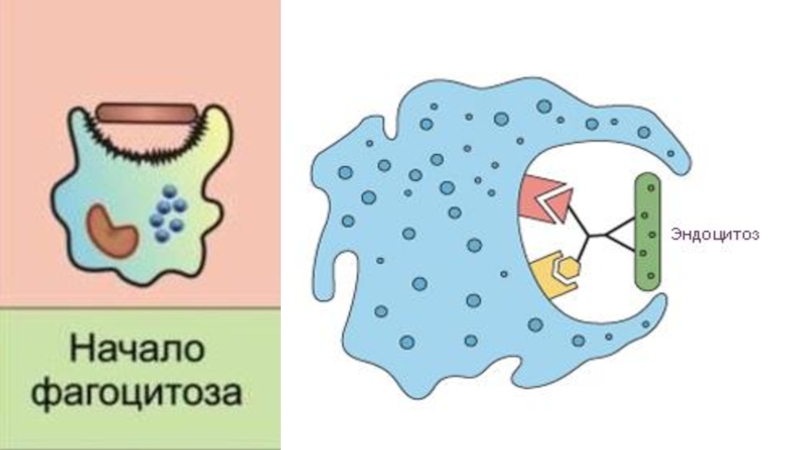
- 26. 4. Погружение. Обволакивание объекта.Взаимодействие опсонинов и поверхностных рецепторов
- 27. Слайд 27
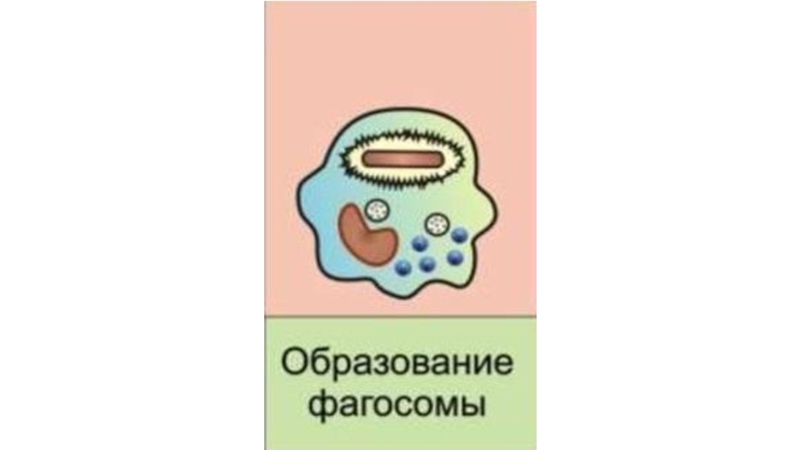
- 28. 5. Образование фагосомы. Замыкание мембраны, погружение объекта с частью мембраны фагоцита внутрь клетки.
- 29. Слайд 29
- 30. 6. Образование фаголизосомы. Слияние фагосомы с лизосомами. Содержимое лизосом
- 31. Слайд 31
- 32. 7. Киллинг и расщепление. Использование пероксида водорода, лизоцима и
- 33. Слайд 33
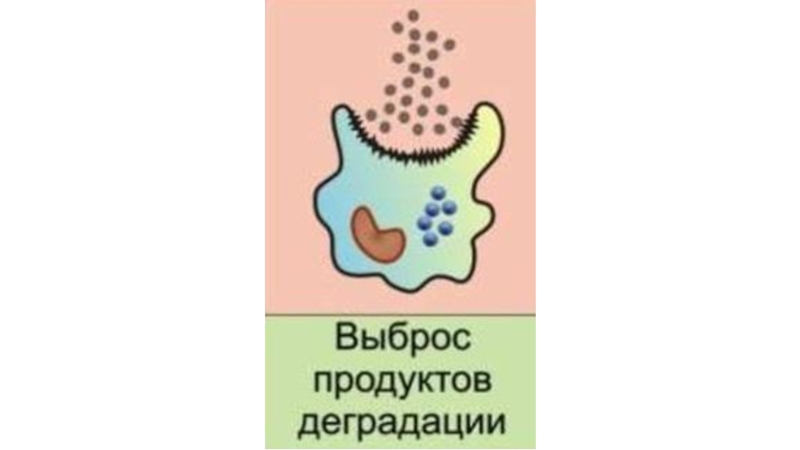
- 34. 8. Выброс продуктов деградации.
- 35. Слайд 35
- 36. Слайд 36
- 37. Компоненты: рецепторы фагоцитовПаттерн-распознающие рецепторы (ПРР)Лектиновые рецепторыФагоцитарные рецепторыРецепторы для хемокинов и хемотрактантовГликопротеиновые рецепторы для цитокинов
- 38. Паттерн-распознающие рецепторы (ПРР) врожденного иммунитета - обеспечивают
- 39. Слайд 39
- 40. Лектиновые рецепторы:маннозно-фукозные рецепторы, распознающие углеводные компоненты поверхностных
- 41. Слайд 41
- 42. Фагоцитарные рецепторы - опосредованное распознавание опсонизированных антителами
- 43. Рецепторы для Fc-фрагментов IgG:FcγRI (CD64) - характеризуется
- 44. Слайд 44
- 45. Рецепторы для хемокинов и других хемоаттрактантов. Взаимодействие
- 46. Слайд 46
- 47. Слайд 47
- 48. Гликопротеиновые рецепторы для цитокинов. Служит первым звеном
- 49. Молекулы адгезииМолекулы адгезии – молекулы, отвечающие за контакт
- 50. Селектины— поверхностные молекулы, тканевые лектины (трансмембранные белки),
- 51. Слайд 51
- 52. Интегрины — многофункциональные молекулы адгезии, которые проводят внутренние
- 53. Хемокины - обширная группа цитокинов (полипептиды). На ряду
- 54. Слайд 54
- 55. Молекулы суперсемейства иммуноглобулинов (IgSF) – молекулы, связывающие
- 56. Слайд 56
- 57. Скачать презентанцию
План занятияКлеточные факторы и определение фагоцитозаВиды и функции фагоцитирующих клетокОсновные этапы фагоцитарной реакцииКомпоненты: рецепторы фагоцитовМолекулы адгезии: селектины, интегрины и хемокиныДемонстрация фагоцитоза
Слайды и текст этой презентации
Слайд 1Клеточные факторы врождённого иммунитета.
Фагоцитоз и его стадии
Преподаватель: м.н.с., аспирант
Григорьев Артём Геннадьевич
Слайд 2План занятия
Клеточные факторы и определение фагоцитоза
Виды и функции фагоцитирующих клеток
Основные
этапы фагоцитарной реакции
Компоненты: рецепторы фагоцитов
Молекулы адгезии: селектины, интегрины и хемокины
Демонстрация
фагоцитозаСлайд 3Клеточные факторы
Клеточные факторы – это молекулярные компоненты ряда специализированных клеток,
а также выделяемые ими биологические вещества. Такие клетки обладают внутриклеточным
киллингом или фагоцитозом.Фагоцитоз осуществляют полиморфно-ядерные лейкоциты и мононуклеарные фагоциты (профессиональные фагоциты). Нейтрофилы и мононуклеарные фагоциты (тканевые макрофаги и их предшественники моноциты, промоноциты и монобласты) имеют общее миелоидное происхождение из стволовой кроветворной клетки, но различаются рядом свойств.
Слайд 4Фагоцитоз — процесс поглощения и переваривания инородных частиц. Является одним
из видов эндоцитоза и пиноцитоза. Явление фагоцитоза впервые открыл в 1883
г. И.И. Мечников. За объяснение и демонстрацию фагоцитоза был удостоен в 1909 г. Нобелевской премии.Слайд 5Виды фагоцитов
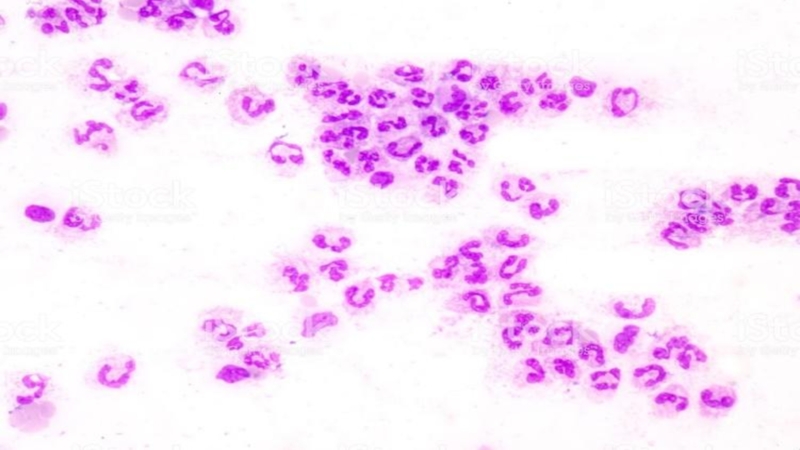
Нейтрофилы (палочко- и сегментоядерные)
Мононуклеарные лейкоциты (промоноциты, моноциты и тканевые
макрофаги)
Эозинофилы
Базофилы
Дендритные клетки (ДК)
Слайд 6Нейтрофилы (15 суток) (палочко- и сегментоядерные) – многочисленная, способная к
передвижению популяция фагоцитов, созревание которых начинается и заканчивается в ККМ.
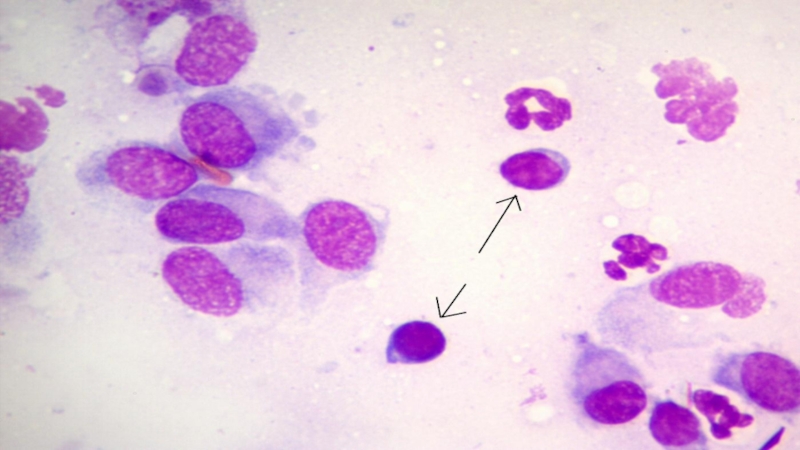
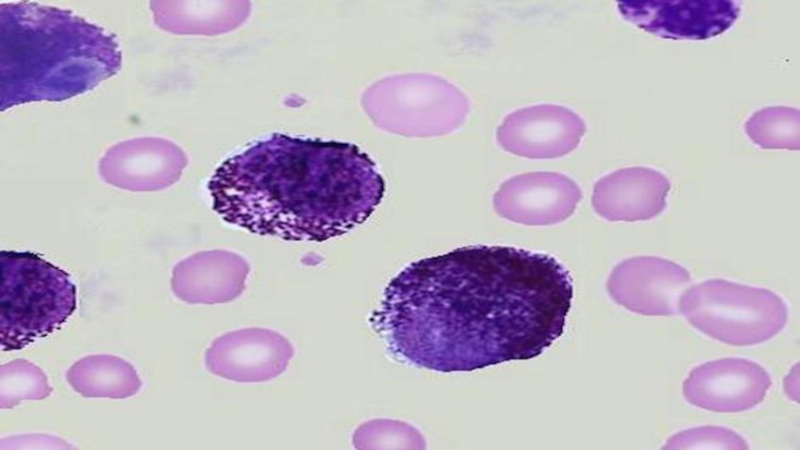
70% всех нейтрофилов существуют как резерв, а под действием биологических медиаторов могут перемещаться через кровь в патологический очаг (органы и ткани) и развивать острый воспалительный ответ, где и погибают.Слайд 8Мононуклеарные лейкоциты (40-60 суток) (промоноциты, моноциты и тканевые макрофаги). Самый
крупный вид лейкоцитов в крови с большой цитоплазмой, в которой
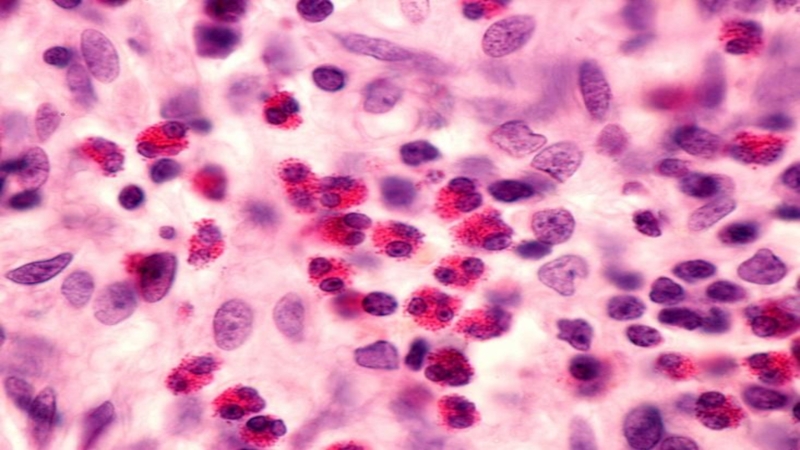
много лизосом. Состоят из одного полиморфного рыхлого ядра бобовидной формы. Эти клетки являются самыми активными фагоцитами среди остальных. Моноциты ещё незрелые клетки, но попадая в ткани через кровь, созревают в тканевые макрофаги.Слайд 11Эозинофилы (8-12 суток) - полиморфно-ядерные лейкоциты. Обладают слабой фагоцитарной активностью.
Эозинофилы способны к фагоцитозу, но его активность и эффективность значительно
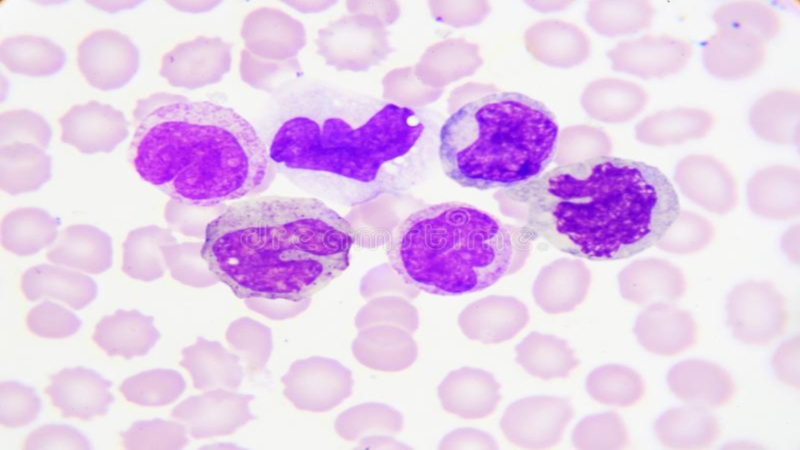
ниже, чем у нейтрофилов. Защищают от паразитарных организмов. Активация этих клеток приводит к выделению токсичных продуктов гранул, оказывающих губительное действие на гельминтов. Оказываю противопаразитарный иммунный ответ.Слайд 13Базофилы (8-12 суток) – очень крупные гранулоциты с базофильным S-образным
ядром, которое не видно из-за цитоплазмы с гранулами. Дегрануляция содержимого
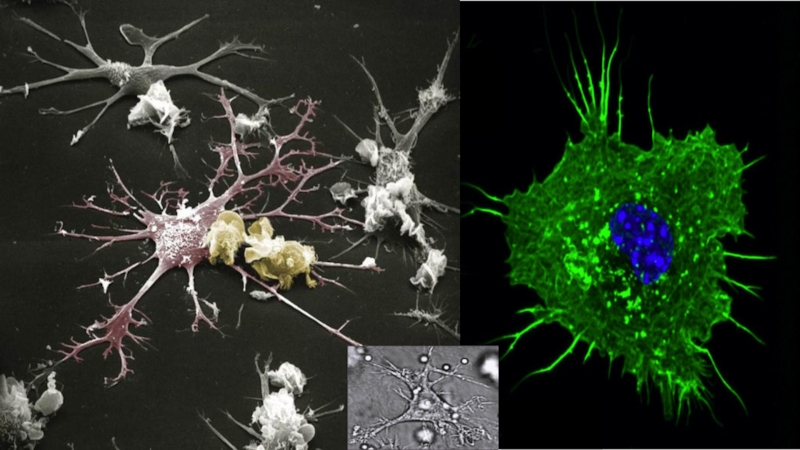
гранул усиливает кровоток и проницаемость сосудов для привлечения в очаг новых клеток.Слайд 15Дендритные клетки (DC) —популяция антигенпредставляющих крупных клеток ККМ с овальным или круглым ядром
и с многочисленными отростками мембраны. Осуществляют презентацию антигенов Т-клеткам и ведут
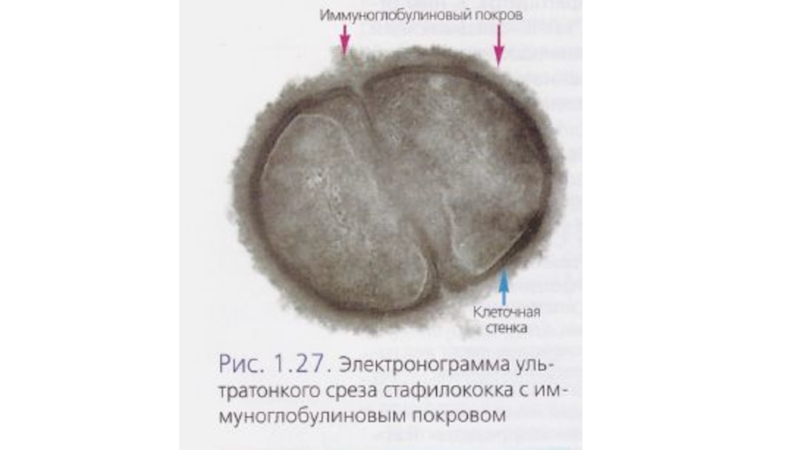
контроль за дифференцировкой Т-лимфоцитов, регуляцией активации и супрессии иммунного ответа. Захватыватывают из окружающей среды различные антигены при помощи пиноцитоза и рецептор-опосредованного эндоцитоза. Поглощают антигены, процессируют и представляют на своей поверхности в комплексе с MHC I (все ядросодержащие клетки) или MHC II (только в антигенпрезентирующих клетках (ДК, МФ, В-лимфоциты) классов.Слайд 17Опсонины – белки сыворотки крови, обволакивающие микробы и корпускулярные АГ
и усиливающие их фагоцитоз (IgG1, IgG3, частично IgA, белки острой
фазы)Слайд 19Основные этапы фагоцитарной реакции
Хемотаксис
Адгезия
Активация мембраны
Погружение
Образование фагосомы
Образование фаголизосомы
Киллинг и расщепление
Выброс продуктов
деградации
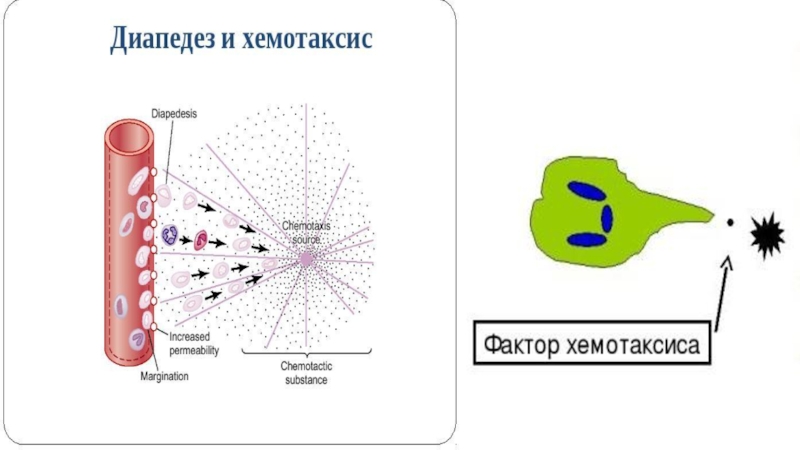
Слайд 201. Хемотаксис — направленное движение клеток друг к другу или наоборот
за счёт химических факторов (хемоттрактантов) (миграция лейкоцитов из кровяного русла
в очаг воспаления). Ряд провоспалительных цитокинов оказывает на лейкоциты хемотаксическое действие.Слайд 222. Адгезия к объекту (сближение). Обусловлена наличием рецепторов для молекул, представленных на
поверхности объекта. Распознавание осуществляется лектиноподобными рецепторами соответствующей специфичности, в первую
очередь маннозосвязывающим белком и селектинами, присутствующими на поверхности фагоцитов.На поверхности фагоцита имеются рецепторы для хемоатрактантов, в результате чего клетка чувствует градиент хемотаксического сигнала
В эту стадию происходит опсонизация, распознавание и прикрепление фагоцита к объекту фагоцитоза
В сыворотке крови находятся опсонины, соединения, которые способствуют активации фагоцитоза, а именно процесс узнавания чужеродного объекта и прилипание фагоцита к нему.
Слайд 243. Активация мембраны. Подготовка объекта к поглощению путём активации протеинкиназы С и
выхода ионов кальция из внутриклеточных депо.
Слайд 264. Погружение. Обволакивание объекта.
Взаимодействие опсонинов и поверхностных рецепторов фагоцита. Затем происходит
обхват псевдоподиями чужеродной частицы и погружение её в цитоплазму фагоцита.
Слайд 285. Образование фагосомы. Замыкание мембраны, погружение объекта с частью мембраны фагоцита внутрь клетки.
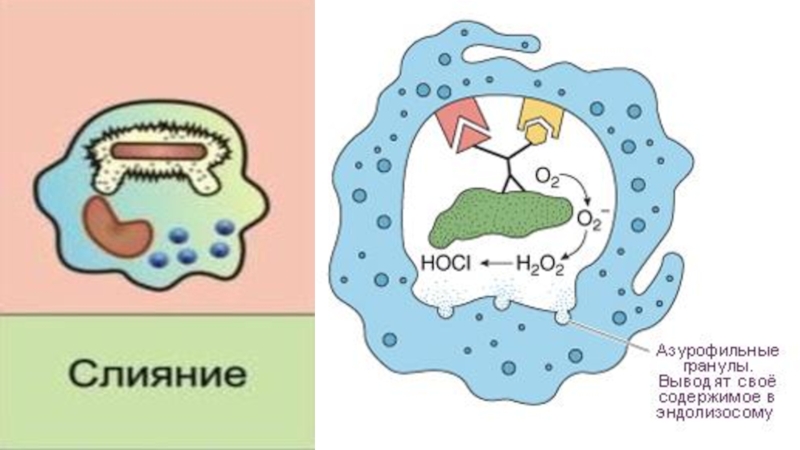
Слайд 306. Образование фаголизосомы. Слияние фагосомы с лизосомами. Содержимое лизосом фиксирует и обездвиживает
патоген, после чего происходит бактериолизис. От негативного действия лизосом макрофаги
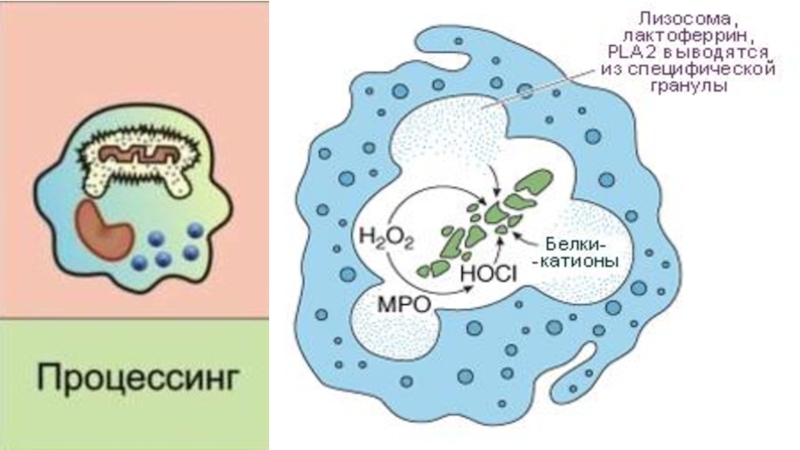
защищаются супероксиддисмутазой.Слайд 327. Киллинг и расщепление. Использование пероксида водорода, лизоцима и др. для разрушения
бактериальных клеток + высокая активность протеаз, нуклеаз, липаз и других ферментов
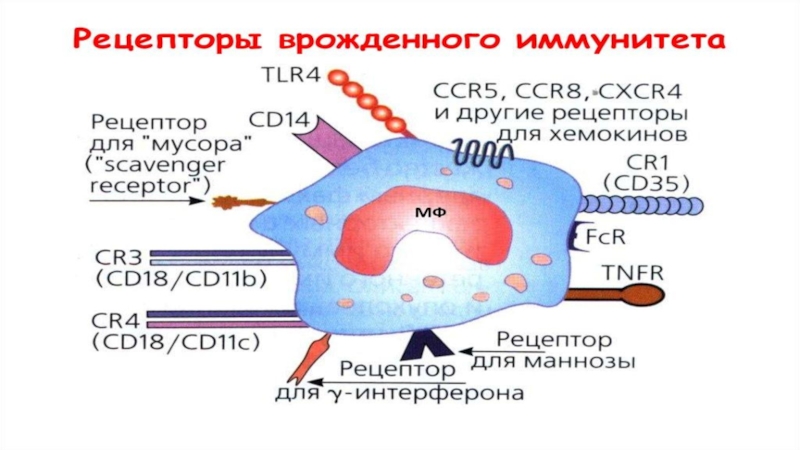
Слайд 37Компоненты: рецепторы фагоцитов
Паттерн-распознающие рецепторы (ПРР)
Лектиновые рецепторы
Фагоцитарные рецепторы
Рецепторы для хемокинов и
хемотрактантов
Гликопротеиновые рецепторы для цитокинов
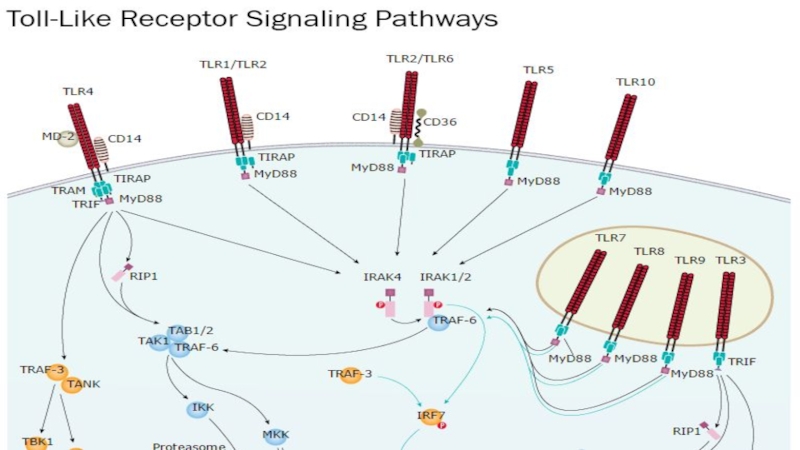
Слайд 38Паттерн-распознающие рецепторы (ПРР) врожденного иммунитета - обеспечивают распознавание большинства патогенов
и молекулярных структур, ассоциированных с опасными для жизни клеток воздействиями.
Ведущими ПРР являются Толл-подобные рецепторы для распознавания чужого (Toll-like receptor – TLR):внеклеточные TLR1, TLR2, TLR4, TLR5, TLR6 и TLR10
внутриклеточные TLR3, TLR7, TLR8, TLR9, а также NOD1 и NOD2-рецепторы.
Слайд 40Лектиновые рецепторы:
маннозно-фукозные рецепторы, распознающие углеводные компоненты поверхностных структур микроорганизмов (бактерии).
Стимулируется витамином Д.
рецепторы для бактериального и клеточного мусора (скавенджер рецепторы
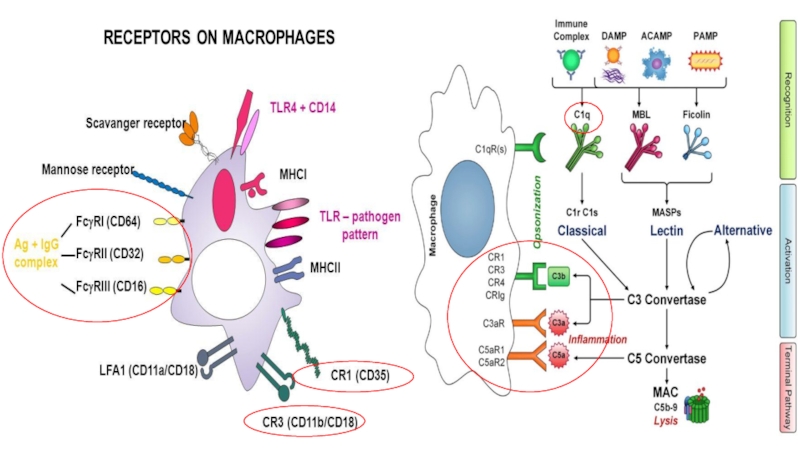
/ SCAR) - связывание фосфолипидных мембран и компонентов собственных разрушенных клеток. Участвуют в фагоцитозе поврежденных, умирающих клеток и патогенов. Делятся на несколько классов: А на макрофагах, В и С (на многих видах клеток). Рецептор класса А имеет 5 типов: SCARA 1-5Слайд 42Фагоцитарные рецепторы - опосредованное распознавание опсонизированных антителами и комплементом патогенов
и других чужеродных частиц и клеток.
Fc-рецепторы и рецепторы для фрагментов активированного
комплемента (CR1, CR3 и CR4 + С3а, С5а, С5b67, вызывающих хемотаксис МН/МФ в очаг воспаления, а также рецепторы для фрагмента C1q) Рецепторы для Fc-фрагментов IgG - связывание иммунных комплексов и фагоцитоз бактерий, меченные иммуноглобулинами и комплементом (эффект опсонизации)
Слайд 43Рецепторы для Fc-фрагментов IgG:
FcγRI (CD64) - характеризуется высокой аффинностью для
IgG и экспрессирован почти исключительно на макрофагах.
FcγRII (CD32) низкоаффинный рецептор,
экспрессирован на моноцитах и макрофагах. FcγRIII (CD16) экспрессирован на моноцитах и макрофагах, отличается низкой аффинностью для IgG и связывает иммунные комплексы или агрегированный IgG.
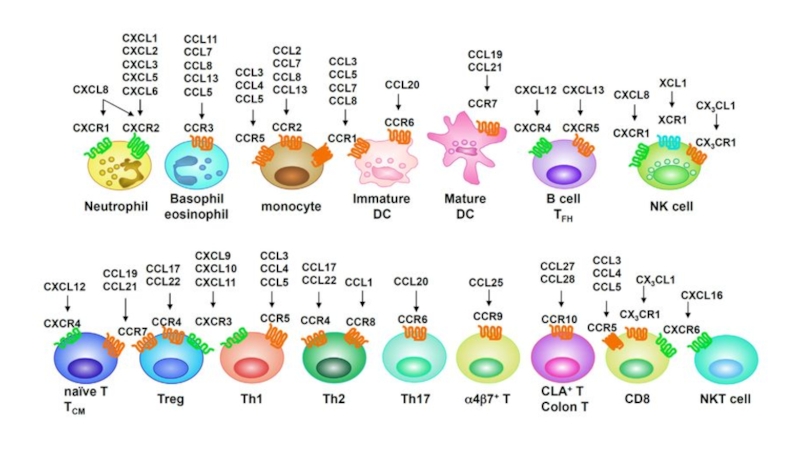
Слайд 45Рецепторы для хемокинов и других хемоаттрактантов. Взаимодействие с лимфоцитами и
реагирование на любые изменения внутренней среды организма. Воспалительные хемокины (CXCR1, CCR1,
CCR2, CCR3, CCR4, CCR5, CCR8 и др.), продуцируемые эпителиальными клетками и эндотелиальными клетками сосудов, а также резидентными МФ стимулируют хемотаксис новых клеток, участвующих в защите. Первыми в очаг воспаления поступают нейтрофилы, позднее начинается моноцитарно-макрофагальная инфильтрация.Слайд 48Гликопротеиновые рецепторы для цитокинов. Служит первым звеном в цепи передачи
активационного сигнала к ядру клетки (ГМ-КСФ или CD115). Позволяет дифференцировать
моноциты и их предшественники от клеток гранулацитарного ряда.Рецепторы для IFN-γ (IFNγRI и IFNγRII), через которые происходит активация многих функций.
Рецепторы для провоспалительных цитокинов (ИЛ-1, ИЛ-6, TNF-α, ИЛ-12, ИЛ-18, ГМ-КСФ) участвующие в воспалительном ответе.
Слайд 49Молекулы адгезии
Молекулы адгезии – молекулы, отвечающие за контакт между клетками и
их перемещением. Взаимодействие и перемещение всех миелодных клеток происходит за
счет:селектинов
интегринов
Кадхеринов
молекул суперсемейства иммуноглобулинов (IgSF).
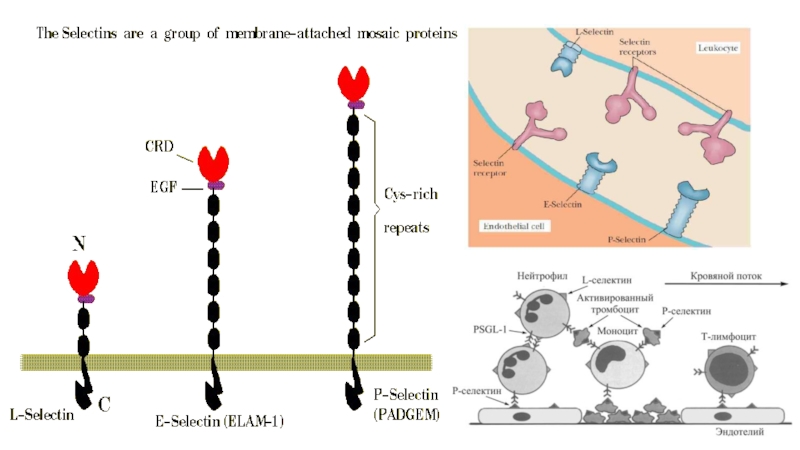
Слайд 50Селектины— поверхностные молекулы, тканевые лектины (трансмембранные белки), экспрессирующиеся на лейкоцитах
и эндотелиальных клетках и вовлекаются в лейкоцитарную адгезию, включая хоминг
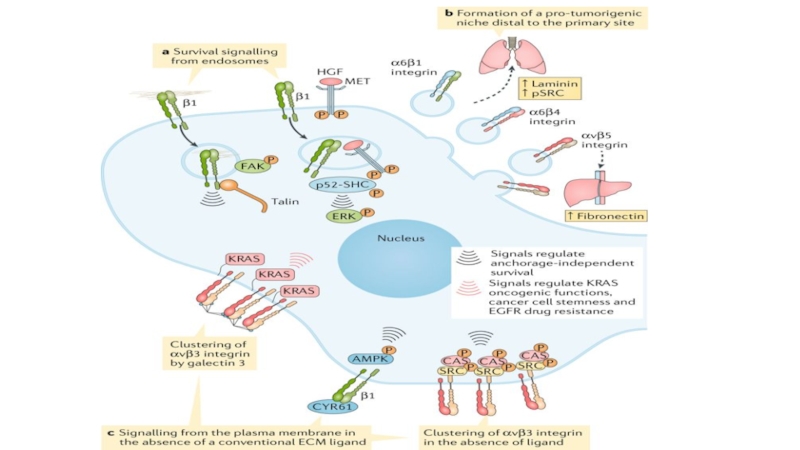
к лимфоидной ткани.Слайд 52Интегрины — многофункциональные молекулы адгезии, которые проводят внутренние и внешние сигналы
клетки. Благодаря им осуществляется эмиграция лейкоцитов из кровотока и поступления
их в очаг воспаления, взаимодействия с клетками-мишенями и др. Выделяют несколько субсемейств:b1 (CD29 или VLA 1-6)
b2 (CD18)
b3 (CD61)
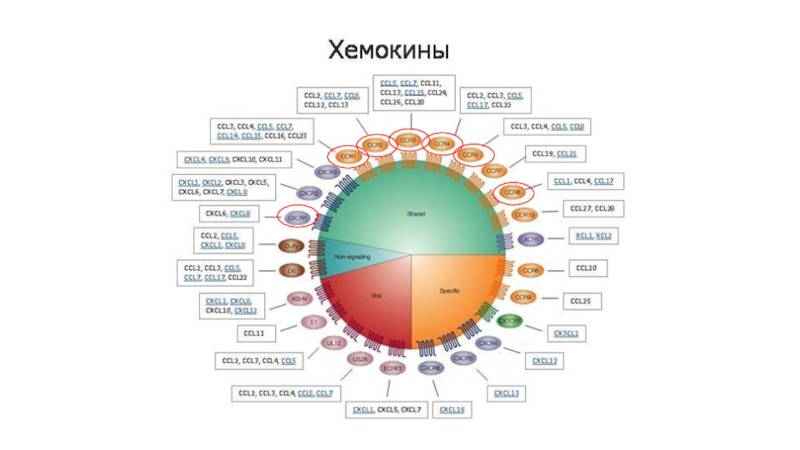
Слайд 53Хемокины - обширная группа цитокинов (полипептиды). На ряду с интегринами и
селектинами могут выступать в роли молекул адгезии. Важны для направленного
движения клеток. По функциональной роли выделяют:гомеостатические хемокины (распределение клеток, а именно лимфоцитов) по лимфоидным органам.
провоспалительные хемокины (активация клеток и привлечение их в очаг воспаления)
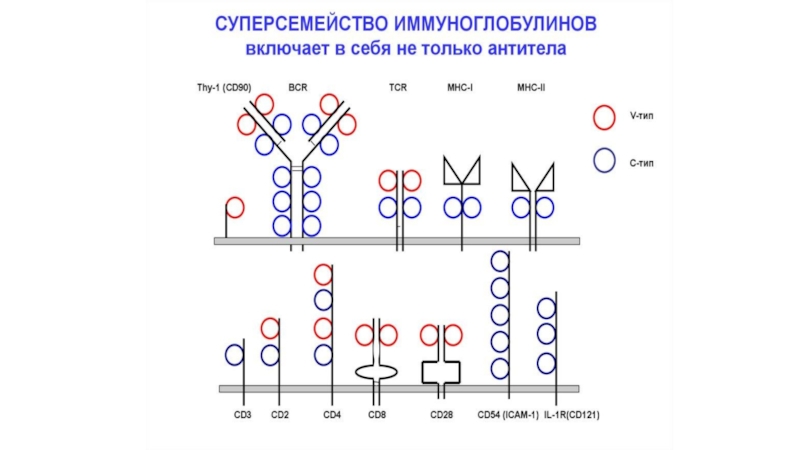
Слайд 55Молекулы суперсемейства иммуноглобулинов (IgSF) – молекулы, связывающие растворимые и поверхностные
клеточные лиганды и играют важную роль в презентации антигенов, клеточной
активации, дифференциации, межклеточной адгезии при различных воспалительных заболеваниях. Выделяют основные молекулы:TCR
BCR
Иммуноглобулины (Ig)
Цитокиновые и Fc рецепторы
HLA
CTLA-4
B7-1, В7-2
ICAM1-ICAM-3 (активированные лимфоциты, моноциты, эозинофилы, фибробласты, эндотелий, эпителиальные клетки) (удержание тесного контакта клеток в процессе распознавания), VCAM-1 и др.