Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Коферменты и простетические группы
Содержание
- 1. Коферменты и простетические группы
- 2. Витамины - кофакторы
- 3. Слайд 3
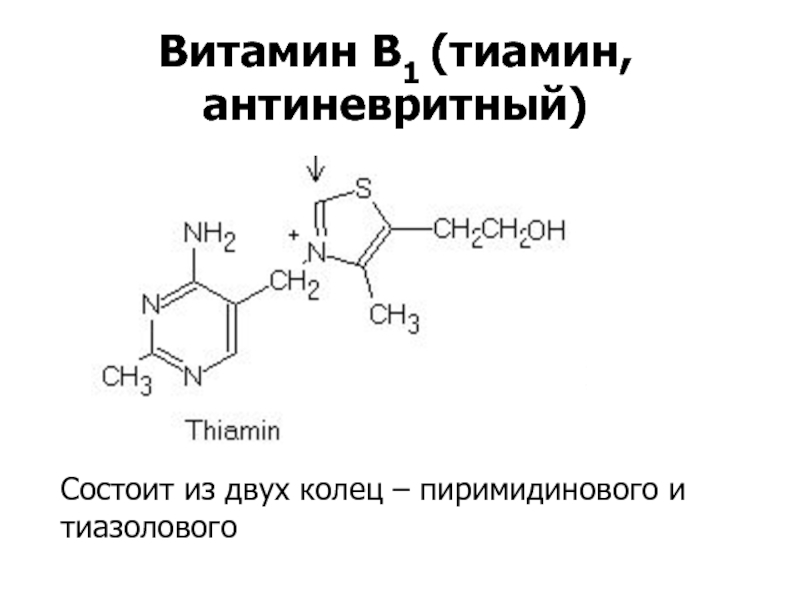
- 4. Витамин В1 (тиамин, антиневритный)Состоит из двух колец – пиримидинового и тиазолового
- 5. В печени фосфорилируется до ТМФ, ТДФ и ТТФТДФ кофермент: пируват- и альфа-кетоглютаратдегидрогеназтранскетолазы
- 6. GlucoseGlucose-6-phosphatePyruvateAcetyl Co AПри недостаточности тимина нагромождаются кетокислоты,
- 7. При угнетении транскетолазы тормозится пентозо-фосфатный цикл, возникает
- 8. Витамин В2 (рибофлавин, витамин роста)Состоит из изоаллоксазина и спирта рибитолаФлавус - жёлтый
- 9. Образует коферменты ФМН и ФАДОбеспечивают деятельность приблизительно
- 10. Флавиновые дегидрогеназы содержат в качестве коферментов FAD
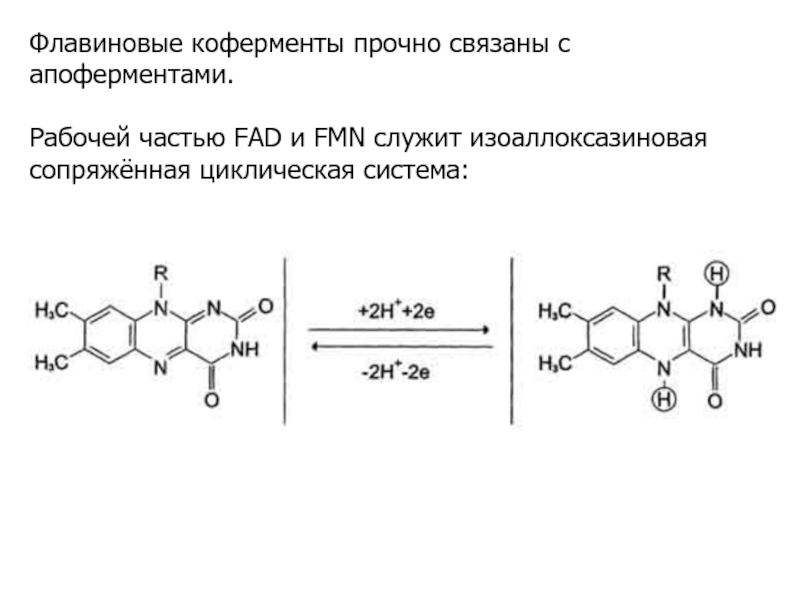
- 11. Флавиновые коферменты прочно связаны с апоферментами.Рабочей частью FAD и FMN служит изоаллоксазиновая сопряжённая циклическая система:
- 12. FAD служит акцептором электронов от многих субстратов
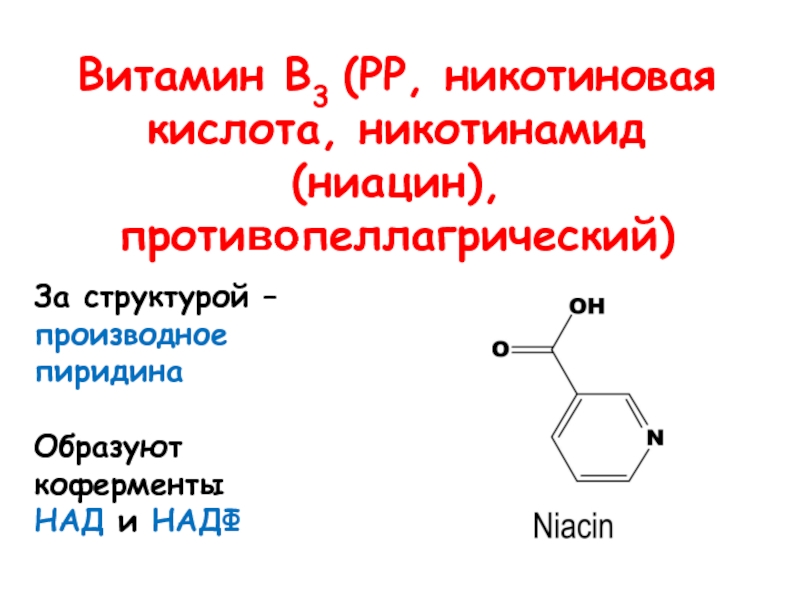
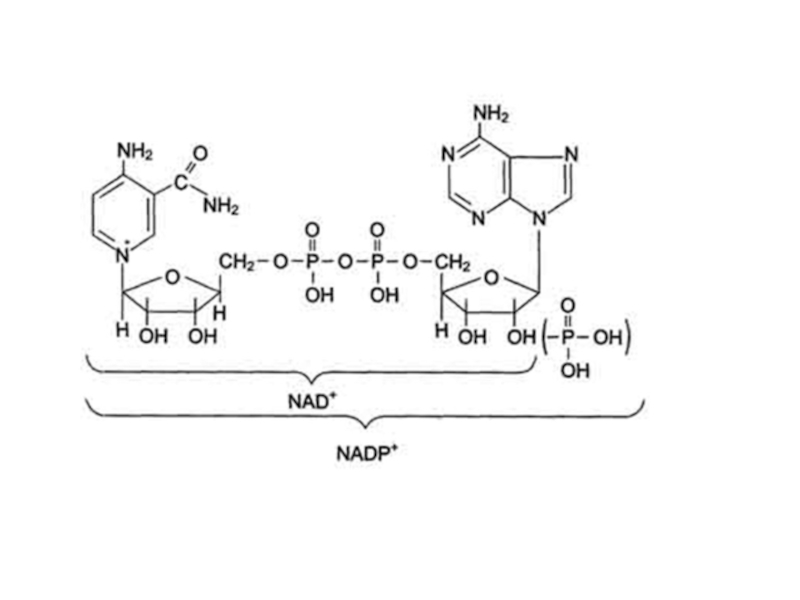
- 13. Витамин В3 (РР, никотиновая кислота, никотинамид (ниацин), противопеллагрический)За структурой – производное пиридинаОбразуют коферменты НАД и НАДФ
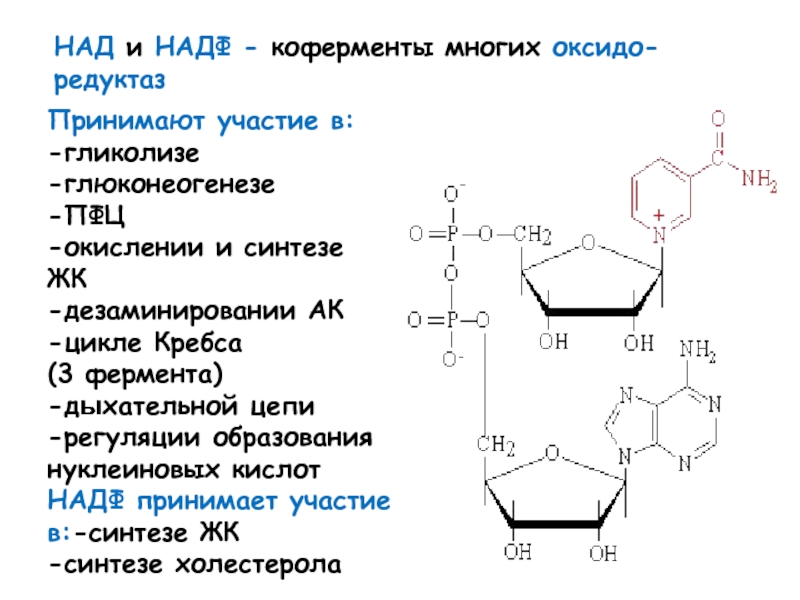
- 14. НАД и НАДФ - коферменты многих оксидо-редуктазПринимают
- 15. Слайд 15
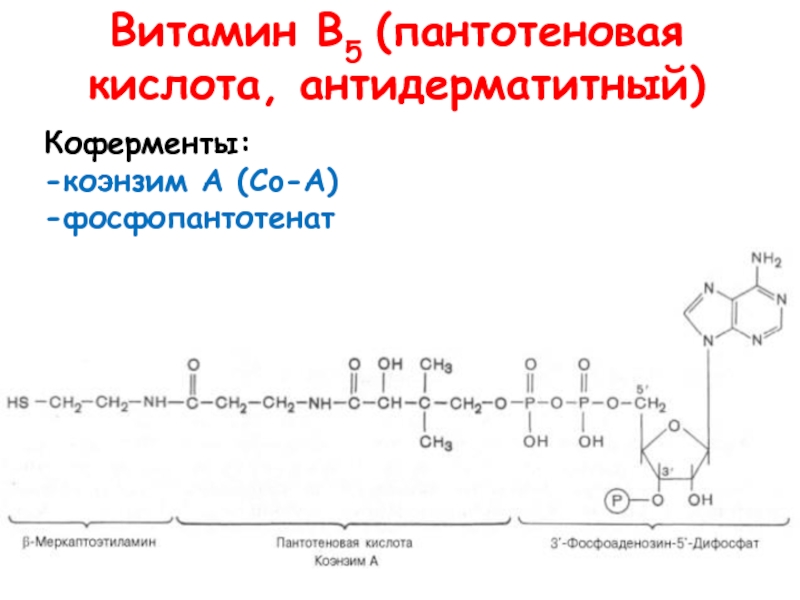
- 16. Витамин В5 (пантотеновая кислота, антидерматитный)Коферменты: -коэнзим А (Co-A)-фосфопантотенат
- 17. Ферментативные процессы при участии витамина B5- окислительное
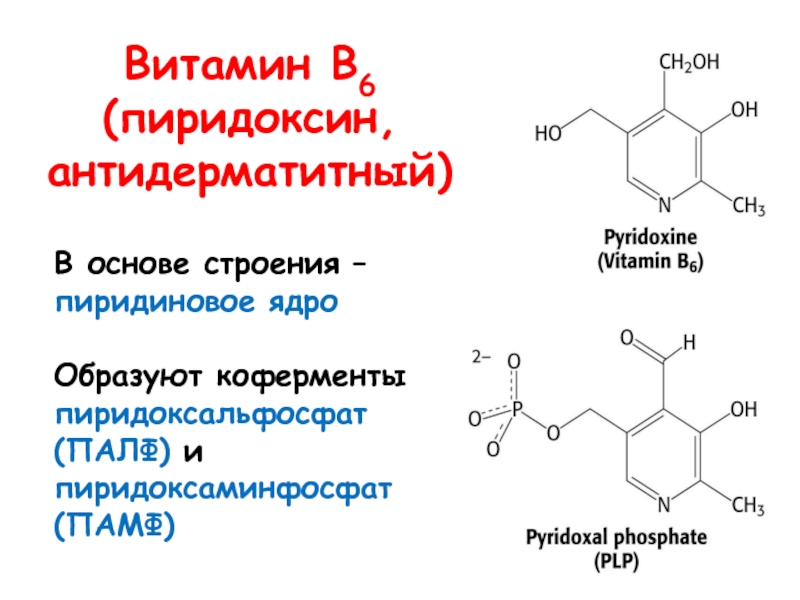
- 18. Витамин В6 (пиридоксин, антидерматитный) В основе строения
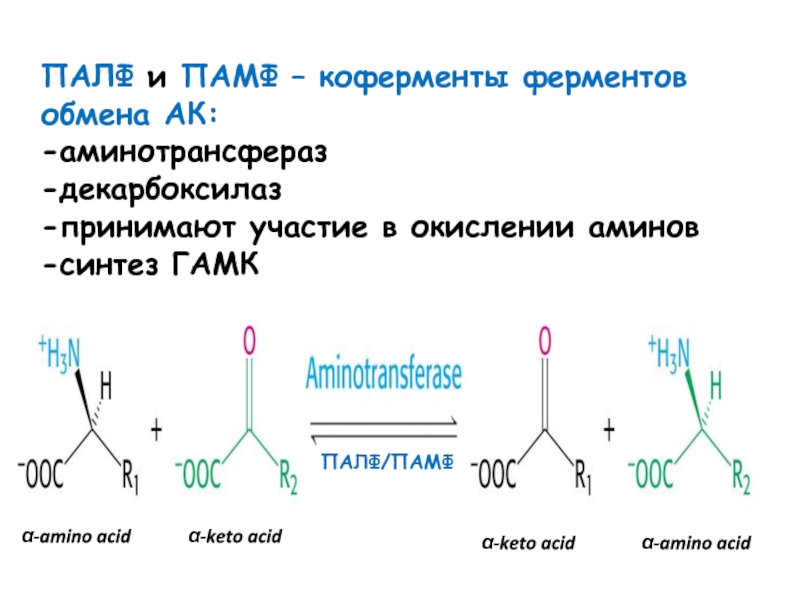
- 19. ПАЛФ и ПАМФ – коферменты ферментов обмена АК:-аминотрансфераз-декарбоксилаз-принимают участие в окислении аминов-синтез ГАМКПАЛФ/ПАМФ
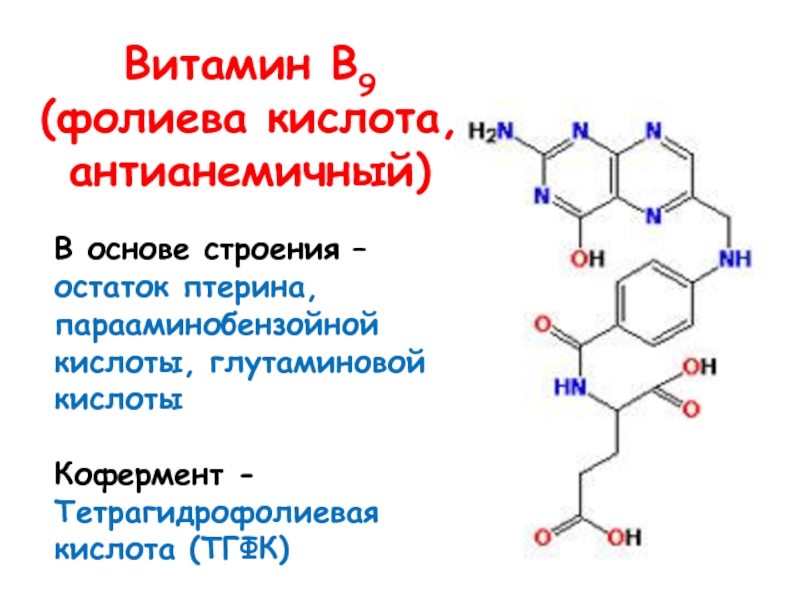
- 20. Витамин В9 (фолиева кислота, антианемичный) В основе
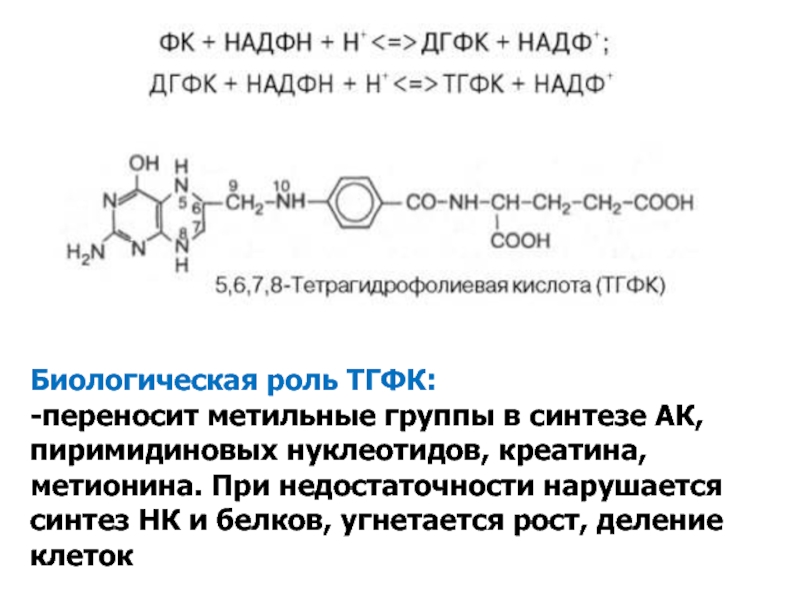
- 21. Биологическая роль ТГФК:-переносит метильные группы в синтезе
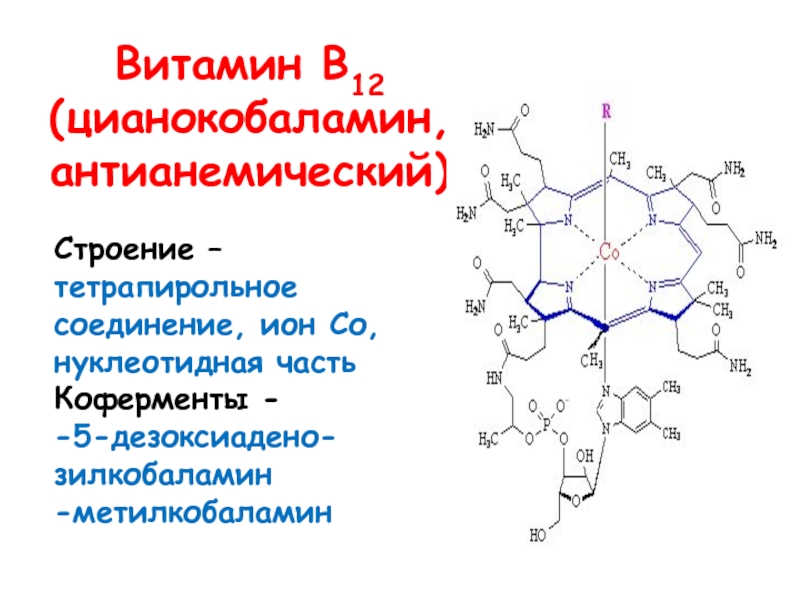
- 22. Витамин В12 (цианокобаламин, антианемический) Строение – тетрапирольное соединение, ион Со, нуклеотидная частьКоферменты - -5-дезоксиадено-зилкобаламин-метилкобаламин
- 23. Биологическая роль:-действие связано с фолиевой кислотой-синтез метионина
- 24. Кофакторы невитаминной природы
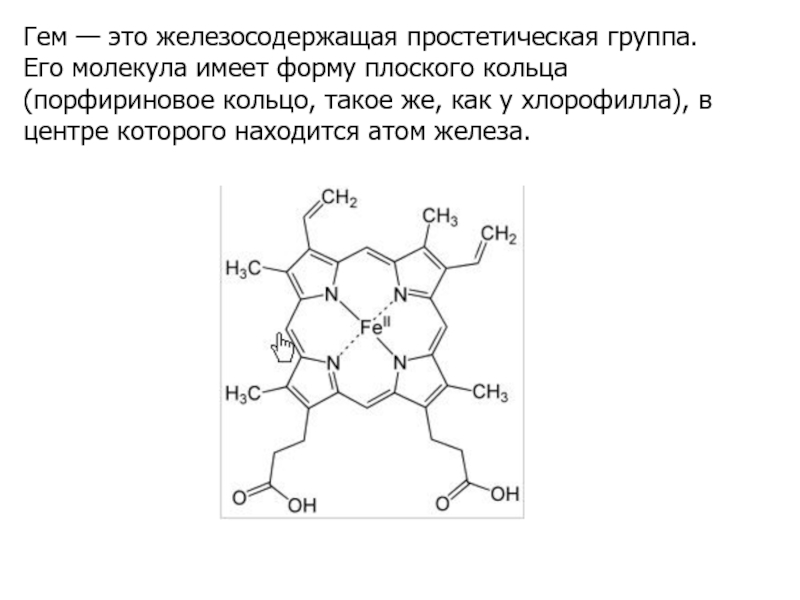
- 25. Гем — это железосодержащая простетическая группа. Его
- 26. Гем выполняет в организме ряд биологически важных
- 27. Перенос кислорода. Гемоглобин и миоглобин — два
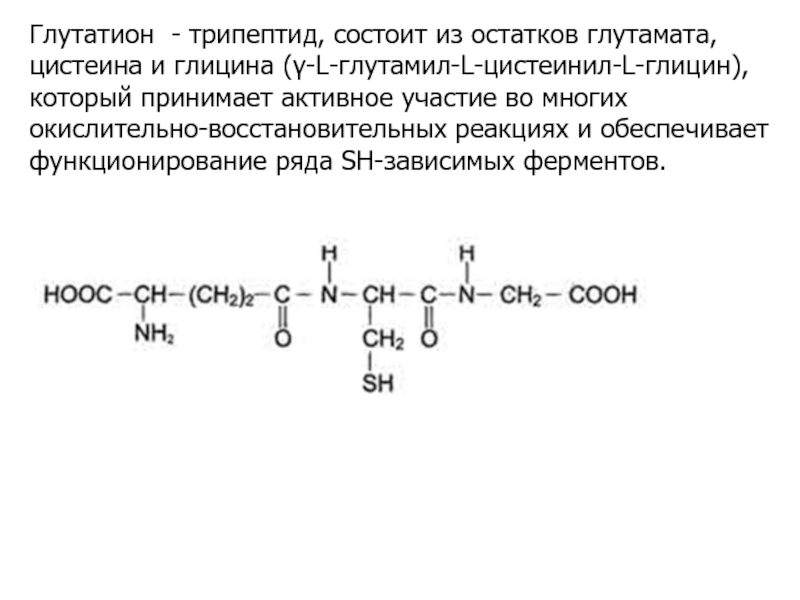
- 28. Глутатион - трипептид, состоит из остатков глутамата,цистеина
- 29. Наиболее важной функциональной группой восстановленной формы глутатиона
- 30. Скачать презентанцию
Витамины - кофакторы
Слайды и текст этой презентации
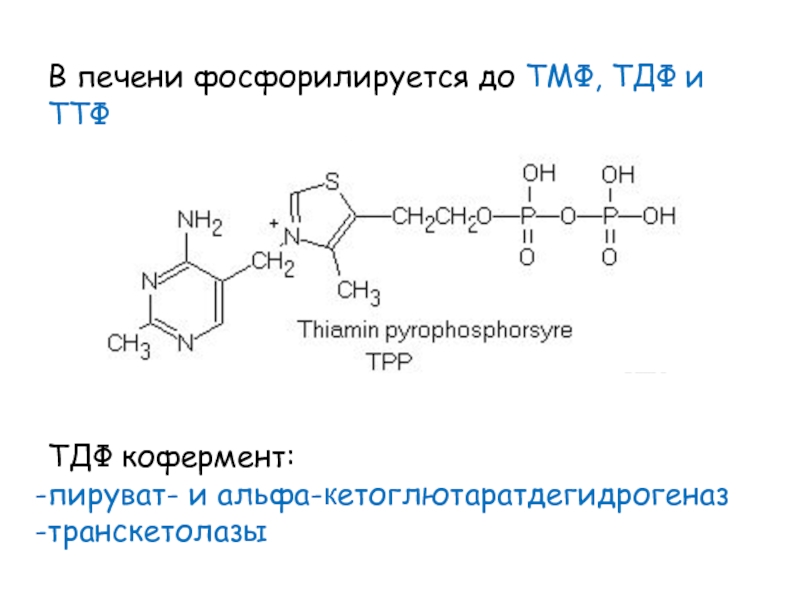
Слайд 5В печени фосфорилируется до ТМФ, ТДФ и ТТФ
ТДФ кофермент:
пируват-
и альфа-кетоглютаратдегидрогеназ
транскетолазы
Слайд 6
Glucose
Glucose-6-phosphate
Pyruvate
Acetyl Co A
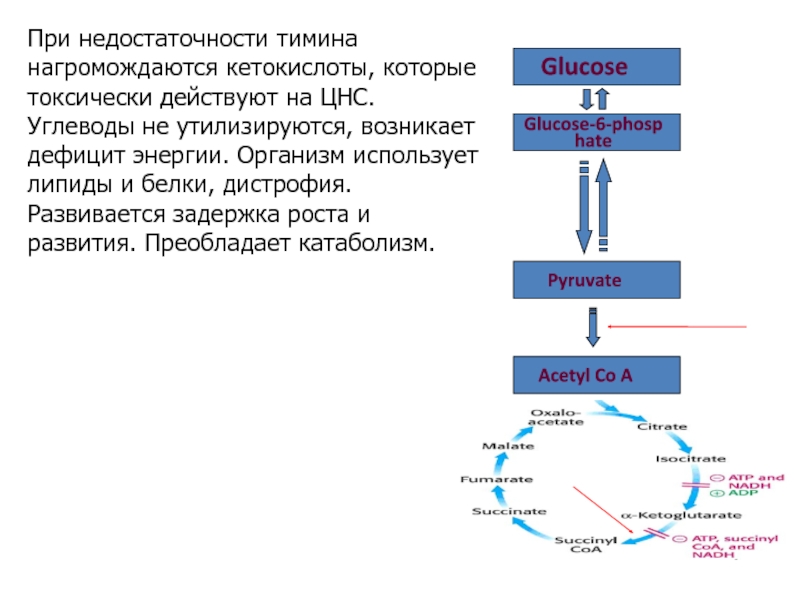
При недостаточности тимина нагромождаются кетокислоты, которые токсически действуют
на ЦНС.
Углеводы не утилизируются, возникает дефицит энергии. Организм использует липиды
и белки, дистрофия. Развивается задержка роста и развития. Преобладает катаболизм.Слайд 7При угнетении транскетолазы тормозится пентозо-фосфатный цикл, возникает дефицит НАДФН и
рибоз, нарушается синтез жирных кислот, стероидных гормонов, холестерола, нуклеиновых кислот.
Слайд 8Витамин В2 (рибофлавин, витамин роста)
Состоит из изоаллоксазина и спирта
рибитола
Флавус - жёлтый
Слайд 9Образует коферменты ФМН и ФАД
Обеспечивают деятельность приблизительно 30 ферментов-оксидоредуктаз (окислительно-восстановительные
реакции)
-дезаминирование АК (оксидазы АК)
-пируватдегидрогеназный и альфа-кетоглутаратдегидрогеназный комплексы
-сукцинатдегидрогеназа (цикл Кребса)
-окисление жирных
кислот (ацил СоА дегидрогеназа)-образование мочевой кислоты (ксантиноксидаза)
-транспорт электронов в дыхательной цепи
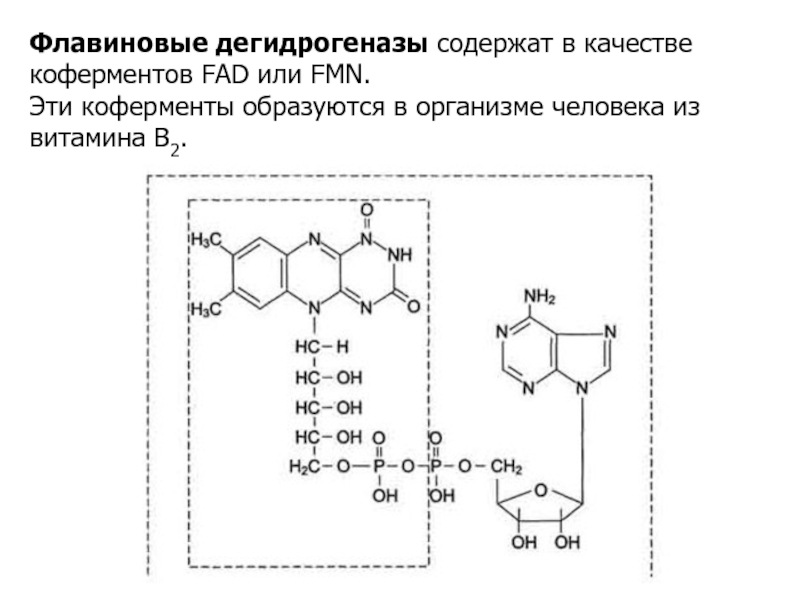
Слайд 10Флавиновые дегидрогеназы содержат в качестве коферментов FAD или FMN.
Эти
коферменты образуются в организме человека из витамина В2.
Слайд 11Флавиновые коферменты прочно связаны с апоферментами.
Рабочей частью FAD и FMN
служит изоаллоксазиновая сопряжённая циклическая система:
Слайд 12FAD служит акцептором электронов от многих субстратов в реакциях типа:
R-CH2-CH2-R1
+ Е (FAD) ↔ R-CH=CH-R1 + Е (FADH2),
где Е -
белковая часть фермента.Большинство FAD-зависимых дегидрогеназ - растворимые белки, локализованные в матриксе митохондрий. Исключение составляет сукцинат-дегидрогеназа, находящаяся во внутренней мембране митохондрий.
К FMN-содержащим ферментам принадлежит NADH-дегидрогеназа, которая также локализована во внутренней мембране митохондрий; она окисляет NADH, образующийся в митохондриальном матриксе.
Реакция протекает по уравнению:
NADH + Н+ + Е (FMN) → NAD+ + Е (FMNH2)
Слайд 13Витамин В3 (РР, никотиновая кислота, никотинамид (ниацин), противопеллагрический)
За структурой –
производное пиридина
Образуют коферменты
НАД и НАДФ
Слайд 14НАД и НАДФ - коферменты многих оксидо-редуктаз
Принимают участие в:
-гликолизе
-глюконеогенезе
-ПФЦ
-окислении и
синтезе ЖК
-дезаминировании АК
-цикле Кребса
(3 фермента)
-дыхательной цепи
-регуляции образования нуклеиновых кислот
НАДФ
принимает участие в:-синтезе ЖК-синтезе холестерола
Слайд 16Витамин В5 (пантотеновая кислота, антидерматитный)
Коферменты:
-коэнзим А (Co-A)
-фосфопантотенат
Слайд 17Ферментативные процессы при участии витамина B5
- окислительное декарбоксилирование пирувата и
альфа-кетоглутарата
- транспорт остатков жирных кислот
- синтез пуриновых нуклеотидов
- активация жирных
кислот- фосфопантотенат – составная часть мультиферментного комплекса – синтазы жирных кислот
- синтез холестерола, кетоновых тел
Слайд 18Витамин В6 (пиридоксин, антидерматитный)
В основе строения – пиридиновое
ядро
Образуют коферменты
пиридоксальфосфат (ПАЛФ) и пиридоксаминфосфат (ПАМФ)
Слайд 19ПАЛФ и ПАМФ – коферменты ферментов обмена АК:
-аминотрансфераз
-декарбоксилаз
-принимают участие в
окислении аминов
-синтез ГАМК
ПАЛФ/ПАМФ
Слайд 20Витамин В9 (фолиева кислота, антианемичный)
В основе строения –
остаток птерина, парааминобензойной кислоты, глутаминовой кислоты
Кофермент -
Тетрагидрофолиевая кислота (ТГФК)
Слайд 21Биологическая роль ТГФК:
-переносит метильные группы в синтезе АК, пиримидиновых нуклеотидов,
креатина, метионина. При недостаточности нарушается синтез НК и белков, угнетается
рост, деление клетокконъюнктивит
Слайд 22Витамин В12 (цианокобаламин, антианемический)
Строение – тетрапирольное соединение, ион Со,
нуклеотидная часть
Коферменты -
-5-дезоксиадено-зилкобаламин
-метилкобаламин
Слайд 23Биологическая роль:
-действие связано с фолиевой кислотой
-синтез метионина из гомоцистеина
-синтез креатина,
холина
-синтез фосфолипидов
-синтез пуриновых и пиримидиновых оснований, НК
Слайд 25Гем — это железосодержащая простетическая группа. Его молекула имеет форму
плоского кольца (порфириновое кольцо, такое же, как у хлорофилла), в
центре которого находится атом железа.Слайд 26Гем выполняет в организме ряд биологически важных функций.
Перенос электронов. В
качестве простетической группы цитохромов - ферментов тканевого дыхания и микросомального
окисления - гем выступает как переносчик электронов. Присоединяя электроны, железо восстанавливается до Fe(II), а отдавая их, окисляется до Fe(III). Гем, следовательно, принимает участие в окислительно-восстановительных реакциях за счет обратимых изменений валентности железа.Слайд 27Перенос кислорода. Гемоглобин и миоглобин — два гемсодержащих белка, осуществляющих
перенос кислорода. Железо находится в них в восстановленной, Fe(II), форме.
Каталитическая функция. Гем входит в состав каталаз и пероксидаз, катализирующих расщепление пероксида водорода до кислорода и воды. Содержится он также и в некоторых других ферментах.
Слайд 28Глутатион - трипептид, состоит из остатков глутамата,цистеина и глицина (γ-L-глутамил-L-цистеинил-L-глицин),
который принимает активное участие во многих окислительно-восстановительных реакциях и обеспечивает
функционирование ряда SH-зависимых ферментов.Слайд 29Наиболее важной функциональной группой восстановленной формы глутатиона является сульфгидрильная (SH-)
группа, которая легко подвергается ферментативному или неферментативному окислению с образованием
дисульфидной (окисленной) формы глутатиона, состоящей из двух молекул восстановленного глутатиона (Г—S— S—Г).Таким образом глутатион функционирует как переносчик водорода.
Глутатион принимает прямое участие в некоторых реакциях цис-транс-изомеризации, является коферментом системы глиоксилазы, формальдегид-дегидрогеназы, глутатионпероксидазы.