пустоту
Энтропия: термодинамическое и статистическое определения. Закон возрастания энтропии.
Энтропия идеального газа.
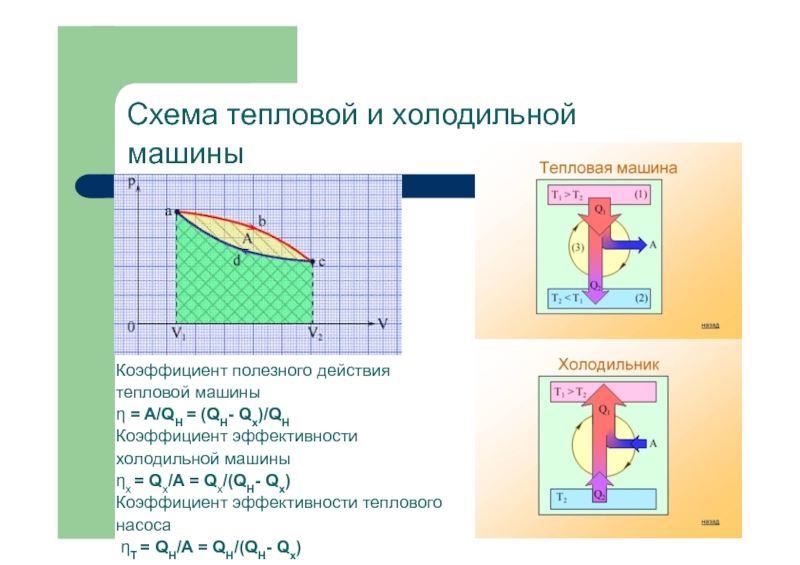
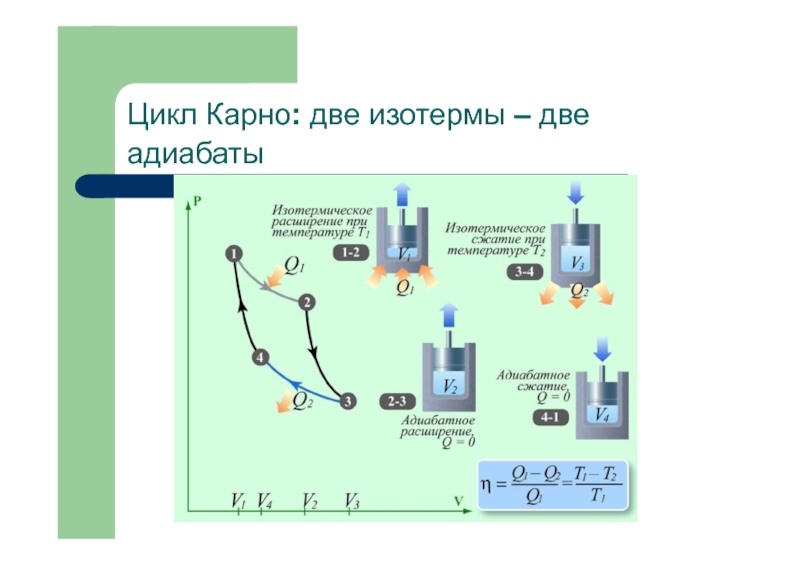
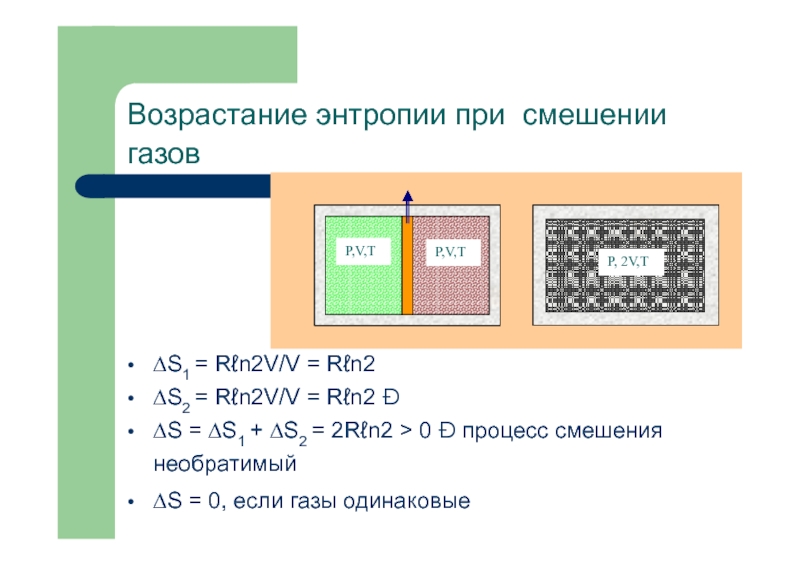
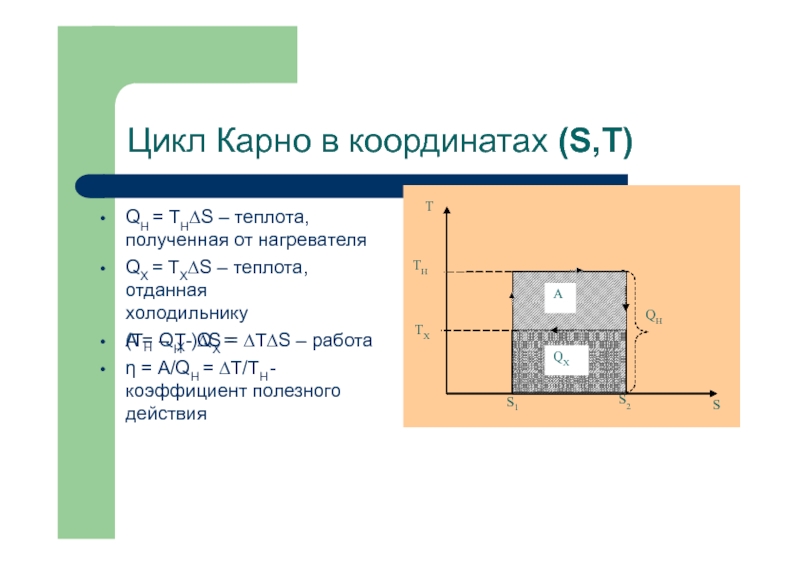
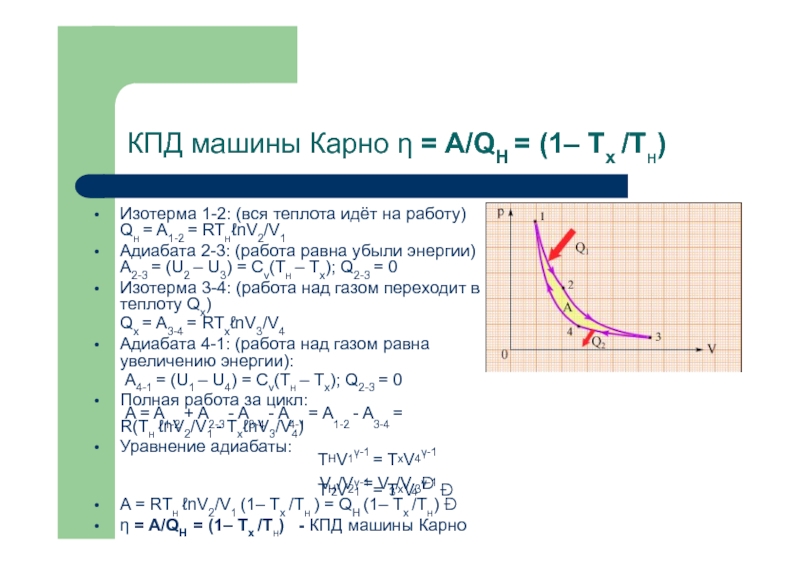
Возрастание энтропии при смешении газов.Тепловые машины. Цикл Карно.