Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Лекция 1 Основы химической термодинамики Основные понятия химической
Содержание
- 1. Лекция 1 Основы химической термодинамики Основные понятия химической
- 2. ЦЕЛИ ЛЕКЦИИ ОБУЧАЮЩАЯ: сформировать
- 3. Термодинамика - это наука, изучающая взаимные превращения
- 4. Основные понятия и термины Термодинамическая
- 5. Основные понятия химической термодинамикиЧасть объектов природы, не
- 6. Если система обменивается с окружающей средой энергией
- 7. Открытая
- 8. Основные понятия химической термодинамики Фаза
- 9. Основные понятия химической термодинамикиВ зависимости от фазового
- 10. Основные понятия химической термодинамики
- 11. Основные понятия химической термодинамики Термодинамические
- 12. Основные понятия химической термодинамики В
- 13. Функции состояния системы В термодинамике для определения
- 14. К термодинамическим функциям системы относятся: 1.
- 15. 1. Внутренняя энергия (U)
- 16. Внутренняя энергия (U): Абсолютное значение
- 17. ΔU=Q V , где Q V -
- 18. Единицы измерения энергии:Джоуль = Дж
- 19. Первый закон термодинамикиПервый закон термодинамики является постулатом:
- 20. Теплота и работа: приращение внутренней работы± Q
- 21. Теплота (Q) - форма передачи
- 22. Первый закон термодинамики Работа (W) -
- 23. Теплота расширения в изобарном процессе:W= p·ΔV, где
- 24. Энтальпия (H): Абсолютное значение энтальпии
- 25. Энтропия (S) характеризует связанную
- 26. Функции состояния системы При протекании изобарно-изотермических
- 27. 1. При ΔН>0 , ΔS>0 , процесс
- 28. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1
Лекция 1
Основы химической термодинамики
Основные понятия химической термодинамики.
Функции состояния системы.
Первый закон
термодинамики.
Слайд 2 ЦЕЛИ ЛЕКЦИИ
ОБУЧАЮЩАЯ: сформировать знания об основах
химической термодинамики, первом законе термодинамики и законе Гесса.
РАЗВИВАЮЩАЯ:
расширить кругозор обучающихся на основе интеграции знаний, развить логическое мышление.ВОСПИТАТЕЛЬНАЯ: содействовать формированию у обучающихся устойчивого интереса к изучению дисциплины.
Слайд 3Термодинамика - это наука, изучающая взаимные превращения различных видов энергии,
связанные с переходом энергии в форме теплоты и работы.
Основные понятия
химической термодинамики
Слайд 4Основные понятия и термины
Термодинамическая система (ТД система)
- это любой объект природы, состоящий из достаточно большого числа
структурных единиц, в частности молекул, отделенных от других объектов природы реальной или воображаемой границей раздела.Слайд 5Основные понятия химической термодинамики
Часть объектов природы, не входящих в систему,
называется средой.
Важными характеристиками системы являются масса вещества (m) и
энергия (Е или U).Слайд 6Если система обменивается с окружающей средой энергией и массой, то
она называется открытой.
Когда система обменивается с окружающей средой энергией, но
не обменивается массой, ее называют закрытой.Система которая не обменивается с окружающей средой массой и энергией в форме теплоты и работы называется изолированной.
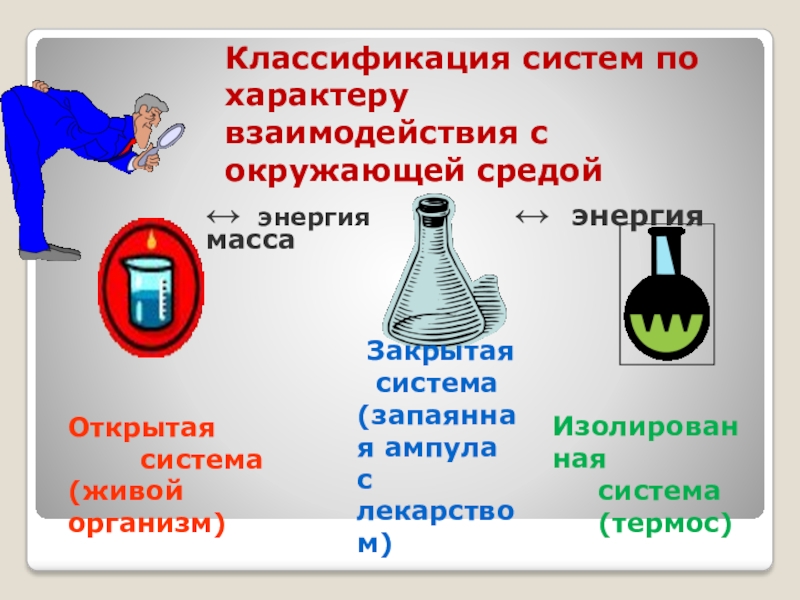
Слайд 7 Открытая
система
(живой
организм)
Закрытая
система
(запаянная ампула с лекарством)
Изолированная
система (термос)
Классификация систем по характеру
взаимодействия с окружающей средой
↔ энергия ↔ энергия масса
Слайд 8Основные понятия химической термодинамики
Фаза - это часть
системы с одинаковыми физическими и химическими свойствами, отделенная от других
частей границей раздела, при переходе через которую свойства резко меняются.Слайд 9Основные понятия химической термодинамики
В зависимости от фазового состояния различают:
1. Гомогенные системы. Это системы, в которых все компоненты
находятся в одной фазе, и в них отсутствуют границы раздела. Пример: растворы глюкозы, солей, кислот.2. Гетерогенные системы. Они состоят из нескольких фаз, отделенных границей раздела. Пример: эритроциты - плазма крови, живой организм.
Слайд 11Основные понятия химической термодинамики
Термодинамические параметры называются стандартными,
если они определяются при стандартных условиях.
К стандартным
условиям относят:t=250С или
Т= (t0С +273) = 298 К
р= 101,3 кПа = 1 атм
С(х) = 1 моль · дм-3
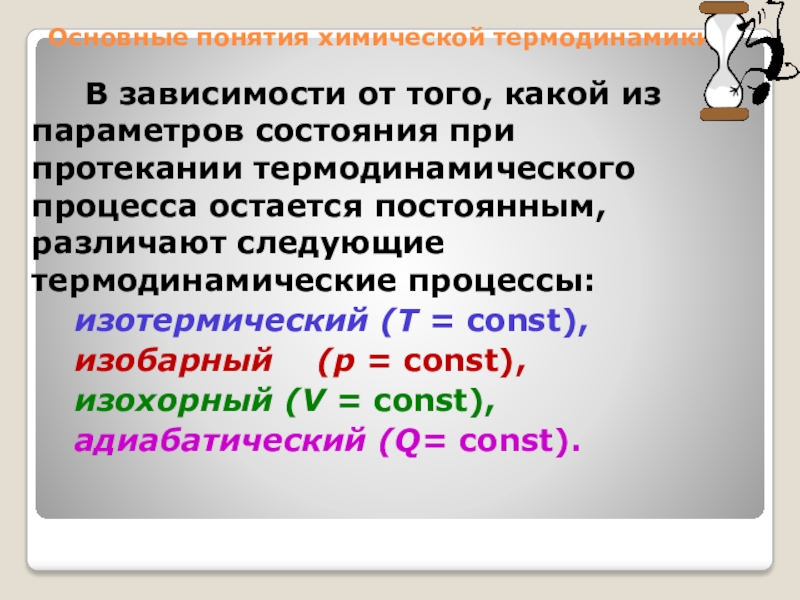
Слайд 12Основные понятия химической термодинамики
В зависимости от того,
какой из параметров состояния при протекании термодинамического процесса остается постоянным,
различают следующие термодинамические процессы:изотермический (Т = const),
изобарный (р = const),
изохорный (V = const),
адиабатический (Q= const).
Слайд 13Функции состояния системы
В термодинамике для определения изменения энергии системы пользуются
различными энергетическими характеристиками, которые называются термодинамическими функциями состояния системы.
Слайд 14К термодинамическим функциям системы относятся:
1. Внутренняя энергия (U).
2. Энтальпия (Н).
3. Энтропия (S).
4.
Энергия Гельмгольца (F).5. Энергия Гиббса (свободная энергия) (G).
6. Химический потенциал (μ).
Слайд 15 1. Внутренняя энергия (U)
Внутренняя энергия системы
складывается из кинетической энергии движения молекул или атомов, образующих систему,
потенциальной энергии их взаимодействия и внутримолекулярной энергии.Слайд 16Внутренняя энергия (U):
Абсолютное значение внутренней энергии измерить
невозможно, поэтому измеряют ее приращение:
Uсистемы = Uкон - Uнач Бесконечно малое изменение U является полным дифференциалом dU.
Слайд 17ΔU=Q V , где Q V - теплота изохорного процесса.
ΔU - кДж/моль или кДж· моль-1
Внутренняя энергия есть функция состояния системы, приращение которой (ΔU) равно теплоте, поступающей в систему при изохорном процессе (ΔV=const). Слайд 18Единицы измерения энергии:
Джоуль = Дж
Так как
Дж очень маленькая величина,
обычно используют кДж.
калория = кал
1 кал = 4.184 Дж 1 кал
4.184 Дж
Коэффициент пересчета!
Слайд 19Первый закон термодинамики
Первый закон термодинамики является постулатом: он не может
быть доказан логическим путем, а вытекает из суммы человеческого опыта.
Большая
роль в обобщении эмпирического опыта при открытии закона принадлежит Г.К. Гессу, Р. Майеру, Джоулю, Гельмгольцу. Слайд 20Теплота и работа: приращение внутренней работы
± Q = U ±
W
Работа, совершаемая системой (+)
или (-) над системой.
Теплота
получаемая (+) или отданная (-) системой.
Внутренняя энергия система
Слайд 21 Теплота (Q) - форма передачи энергии, посредством хаотического
столкновения частиц соприкасающихся систем, системы и среды.
Q = С·ΔT [Дж], где
С - молярная теплоемкость [Дж моль/К].
Слайд 22Первый закон термодинамики
Работа (W) - форма передачи энергии
от системы в окружающую среду или другой системе, посредством упорядоченного
взаимодействия частиц, вызванная преодолением сопротивления.Простейшей работой является работа расширения идеального газа в цилиндре с поршнем (открытая система): W = р ΔV.
Слайд 23Теплота расширения в изобарном процессе:
W= p·ΔV, где
ΔV - изменение
объема системы, ΔV=V2-V1
Энтальпия (от греч. entalpio - нагреваю) -
это часть внутренней энергии системы, которая может совершить полезную работу. 2.Энтальпия (Н)
Слайд 24Энтальпия (H):
Абсолютное значение энтальпии измерить
невозможно, поэтому
измеряют ее приращение: Hсистемы = Hкон - Hнач
ΔН
= Ср ΔТСлайд 25 Энтропия (S) характеризует связанную энергию. В реальных
необратимых системах только часть энергии превращается в работу, другая часть
энергии является как бы связанной. Мера неупорядоченности системы.Энтропия (S)
Слайд 26Функции состояния системы
При протекании изобарно-изотермических процессов:
5. Свободная энергия
Гиббса (G)
Энергия Гиббса (G) - это часть потенциальной энергии реагирующих
веществ, которая может быть использована для осуществления полезной работы. ΔG = ΔH - TΔS
Слайд 271. При ΔН>0 , ΔS>0 , процесс протекает самопроизвольно только
при высоких температурах.
2. При ΔН>0, ΔS
самопроизвольно не протекает ни при каких температурах.3. При ΔН<0, ΔS>0, процесс самопроизвольно протекает при любых температурах.
4. При ΔН<0, ΔS<0, процесс самопроизвольно протекает только при низких температурах.