Слайд 1Лекция 5
● Реальные газы
● Уравнения состояний
● Водяной пар
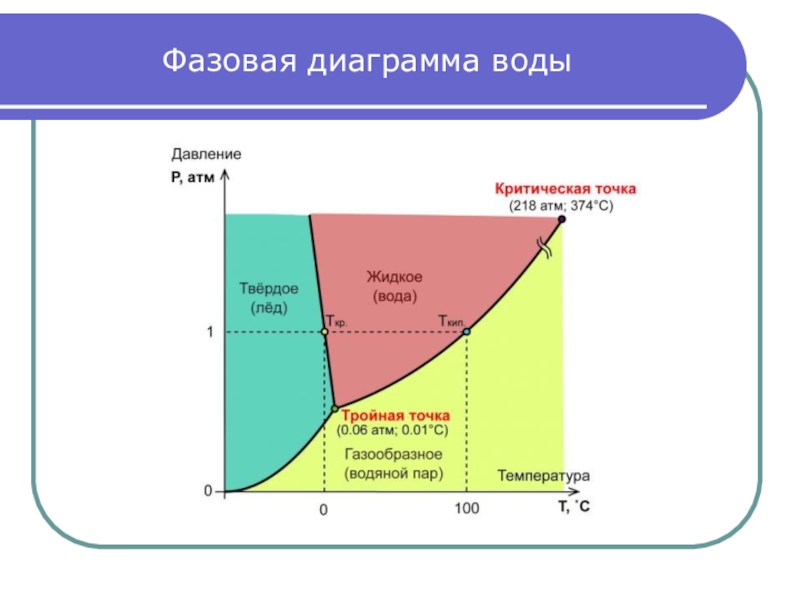
Слайд 2Реальные газы
В реальных газах молекулы представляют собой упругие
тела,
имеют собственный объем и взаимодействуют между
собой.
Из уравнения состояния идеальных газов (Клапейрона)
pv=RT; v=RT/p,
то есть при p=∞: v=0, что не соответствует действительности.
Исторически первое уравнение состояния реальных газов
было получено Ван-Дер-Ваальсом.
Слайд 3Уравнения состояния реальных газов
Уравнение состояния реальных газов Ван-Дер-Ваальса:
.
Ван-Дер-Ваальс учел только два фактора, отличающих
реальные газы
от идеальных, поэтому его уравнение не очень
точное.
Более точным является уравнение Вукаловича-Новикова, в
котором учтены дополнительно ассоциация (объединение в
многомолекулярные комплексы) и диссоциация
(раздробление) комплексов:
.
Слайд 5Водяной пар
Водяной пар является рабочим телом паротурбинных
установок
(ПТУ).
Водяной пар – это реальный газ, состояние которого
можно описать уравнением состояния Вукаловича-Новикова.
Для удобства, состояния пара были просчитаны в большом
диапазоне параметров, а результаты представлены в виде
таблиц термодинамических свойств воды и пара и в форме
pv-, Ts-, hs-диаграмм.
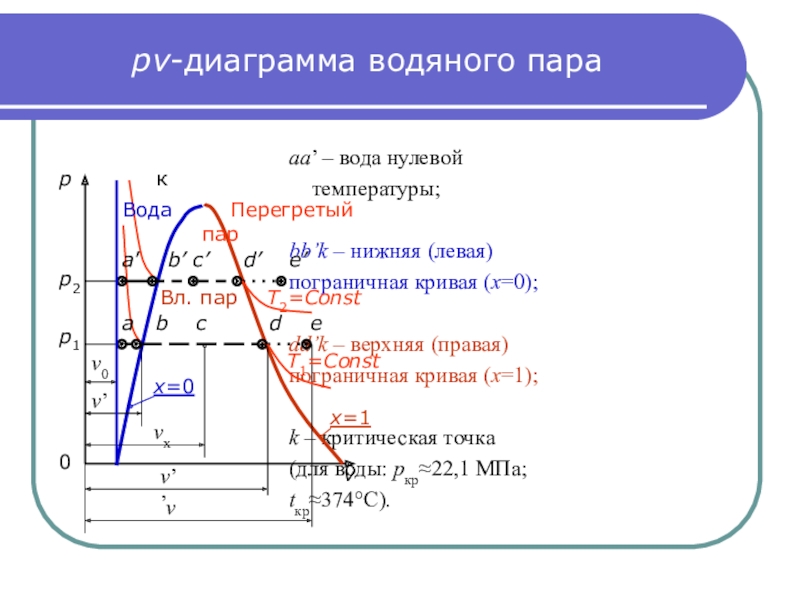
Слайд 6рv-диаграмма водяного пара
aa’ – вода нулевой
температуры;
bb’k – нижняя (левая)
пограничная кривая (х=0);
dd’k – верхняя (правая)
пограничная кривая (х=1);
k – критическая точка
(для воды: pкр≈22,1 МПа;
tкр≈374С).
p к
p2
p1
a’ b’ c’ d’ e’
a b c d e
v0
v’
vx
v’’
v
x=0
x=1
T2=Const
T1=Const
Вода Перегретый
пар
Вл. пар
0
v
Слайд 7К pv-диаграмме
Слева от пограничной кривой – вода;
между
пограничными кривыми – влажный пар;
правее верхней пограничной кривой –
перегретый пар.
На верхней пограничной кривой – сухой, насыщенный пар.
Точка а(v0) – вода нулевой температуры;
процесс ab – изобарный нагрев воды от 0С до температуры
кипения (насыщения) tн;
Слайд 8Процессы и состояния воды и пара
На верхней пограничной кривой
– сухой, насыщенный пар.
Точка а (v0) – вода
нулевой температуры;
процесс ab – изобарный нагрев воды от 0 С до температуры
насыщения tн (кипения);
точка b (v’; х=0) – вода на линии насыщения (закипающая);
процесс bd – изобарно-изотермическое парообразование
(кипение воды) при tн=Const;
точка d (v”; х=1) – сухой, насыщенный пар;
Слайд 9Влажный и перегретый пар
точка c – влажный, насыщенный пар
(х – степень сухости
пара: массовая доля пара во влажном
паре);
процесс de – изобарный перегрев пара;
точка e (v) – перегретый пар.
Начало отсчета внутренней энергии u0=0; энтальпии h0=0
и энтропии s0=0 примем при 0 С (273 К) – точка а.
Слайд 10Ts-диаграмма водяного пара
В тепловой Ts-диаграмме
площади под процессами:
аb
– теплота нагрева воды
от 0 С до температуры
насыщения
q’=h’-h0=h’;
bd – скрытая теплота
парообразования r=h”-h’;
de – теплота перегрева пара q=h-h”;
тогда q’+r+q=h – энтальпия перегретого пара в точке е.
T
273 K
q’
q
r
к v=Const
p=Const
0
s
a
X=Const
b
c
d
e
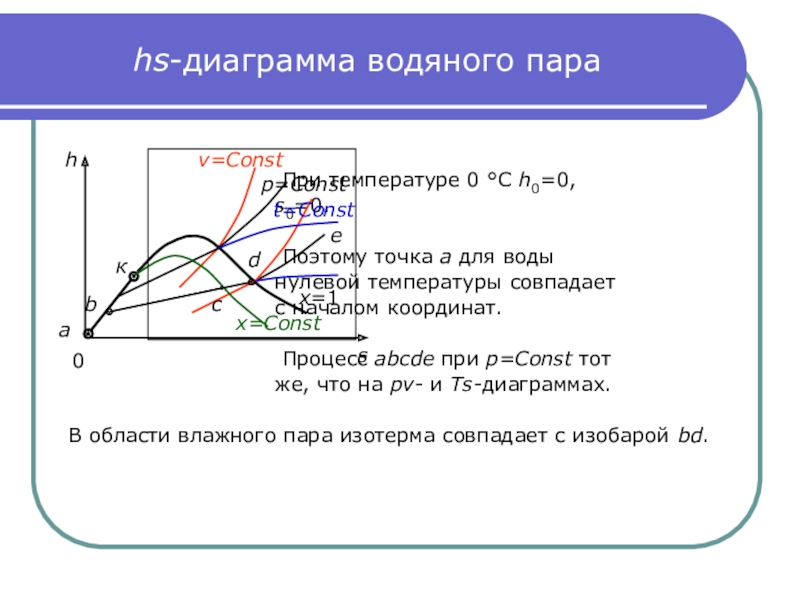
Слайд 11hs-диаграмма водяного пара
При температуре 0
С h0=0,
s0=0.
Поэтому точка а
для воды
нулевой температуры совпадает
с началом координат.
Процесс abcde при p=Const тот
же, что на pv- и Ts-диаграммах.
В области влажного пара изотерма совпадает с изобарой bd.
a
0
s
v=Const
p=Const
t=Const
b
c
d
e
к
h
x=Const
x=1
Слайд 12Расчеты процессов водяного пара
В практических расчетах обычно используются
области
перегретого пара и влажного с высокими степенями сухости.
Поэтому изображается в большем масштабе выделенная
рамкой часть диаграммы.
Более точные расчеты процессов водяного пара выполняется
по таблицам.
Слайд 13Таблицы термодинамических свойств
воды и водяного пара
Бывают таблицы термодинамических
свойств воды
на линии насыщения и сухого, насыщенного пара
(tн,
v’, v”, h’, h”, r, s’, s”)=f(pн)
(pн, v’, v”, h’, h”, r, s’, s”),=f(tн)
где pн, tн – давление и температура насыщения;
v, h, s – удельный объем, энтальпия и энтропия;
индексы ’, ” относятся к воде на линии насыщения и
сухому, насыщенному пару.
Таблицы термодинамических свойств перегретого пара
(v, h, s)=f (p, t).
Слайд 14Внутренняя энергия
В таблицах и диаграммах нет внутренней энергии воды
и пара.
Она находится через энтальпию, Дж/кг:
u’=h’-pv’;
ux=hx-pvx;
u”=h”-pv”;
u=h-pv,
где давление подставляется в Па.
Слайд 15Влажный пар
Параметры состояния влажного пара находятся по смесевым формулам:
vx=v’(1-x)+v”x;
hx=h’(1-x)+h”x;
sx=s’(1-x)+s”x.
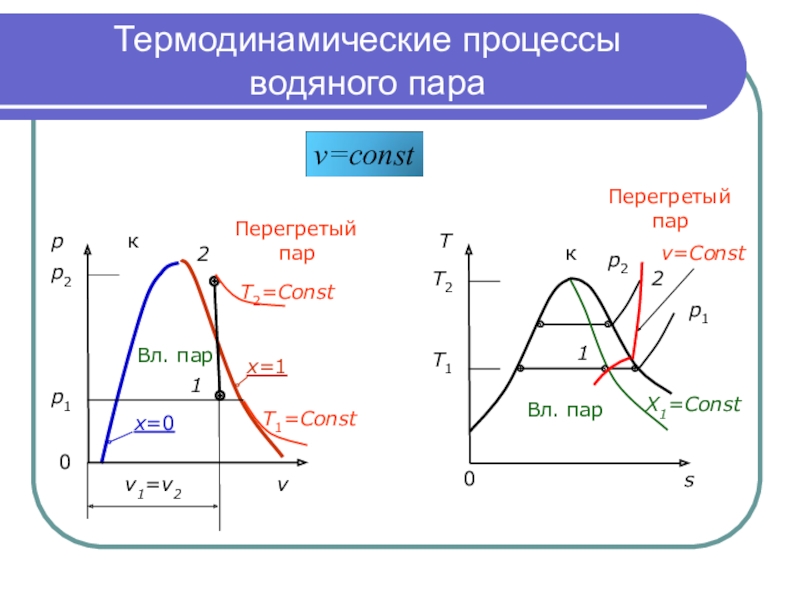
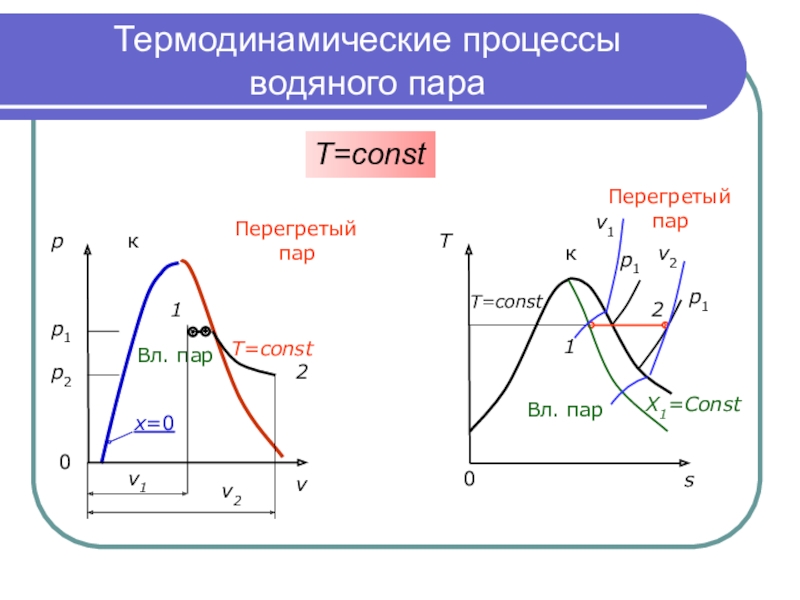
Слайд 16Термодинамические процессы
водяного пара
p к
p2
p1
1
v1=v2
x=0
x=1
Перегретый
пар
Вл. пар
0
v
2
T2=Const
T1=Const
T
к
v=Const
0
s
X1=Const
p1
p2
1
2
T2
T1
Вл. пар
Перегретый
пар
Слайд 17Термодинамические процессы
водяного пара
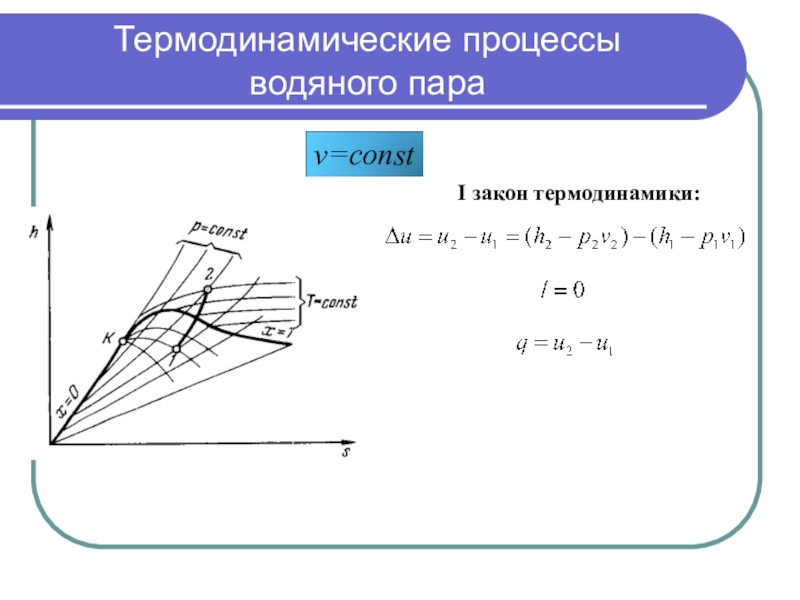
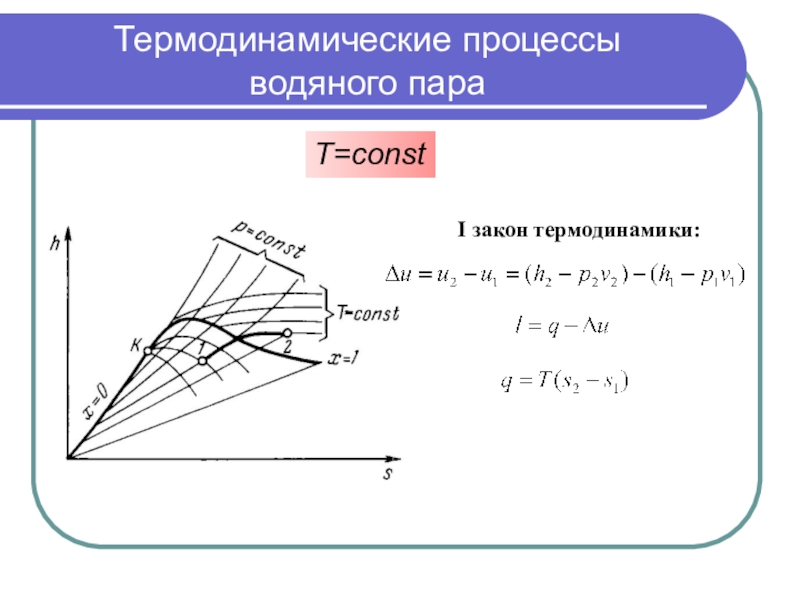
I закон термодинамики:
Слайд 18Термодинамические процессы
водяного пара
1
v1
x=0
x=1
Перегретый
пар
Вл. пар
0
v
2
T2=Const
T1=Const
T
к
0
s
X1=Const
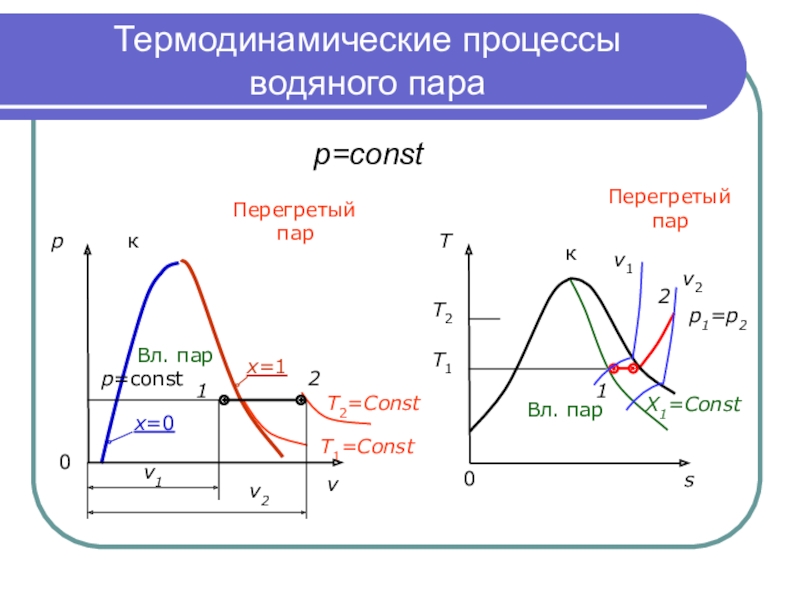
p1=p2
1
2
T2
T1
Вл. пар
Перегретый
пар
p
к
p=const
v2
v1
v2
Слайд 19Термодинамические процессы
водяного пара
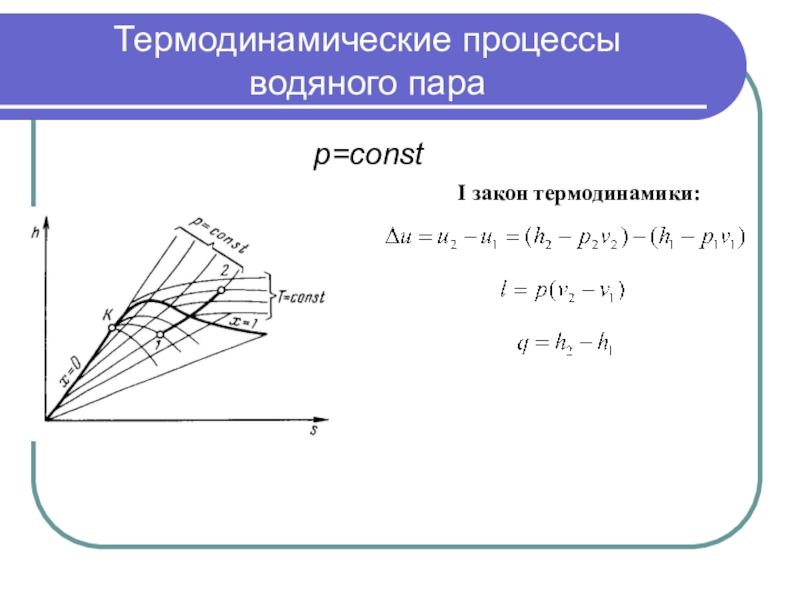
I закон термодинамики:
Слайд 20Термодинамические процессы
водяного пара
p к
p2
p1
1
v2
x=0
Перегретый
пар
Вл. пар
0
v
2
T=const
T
к
0
s
X1=Const
p1
v1
1
2
T=const
T=сonst
Вл.
пар
Перегретый
пар
v1
p1
v2
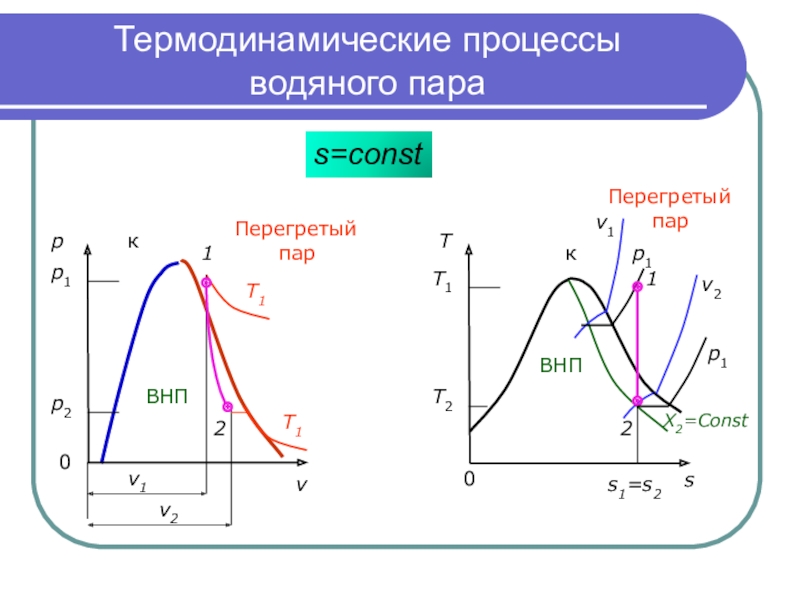
Слайд 21Термодинамические процессы
водяного пара
T=сonst
I закон термодинамики:
Слайд 22Термодинамические процессы
водяного пара
p к
p2
p1
1
v2
Перегретый
пар
ВНП
0
v
2
T1
T
к
0
s
X2=Const
p1
v1
1
2
s=сonst
ВНП
Перегретый
пар
v1
p1
v2
T1
T1
T2
s1=s2
Слайд 23Термодинамические процессы
водяного пара
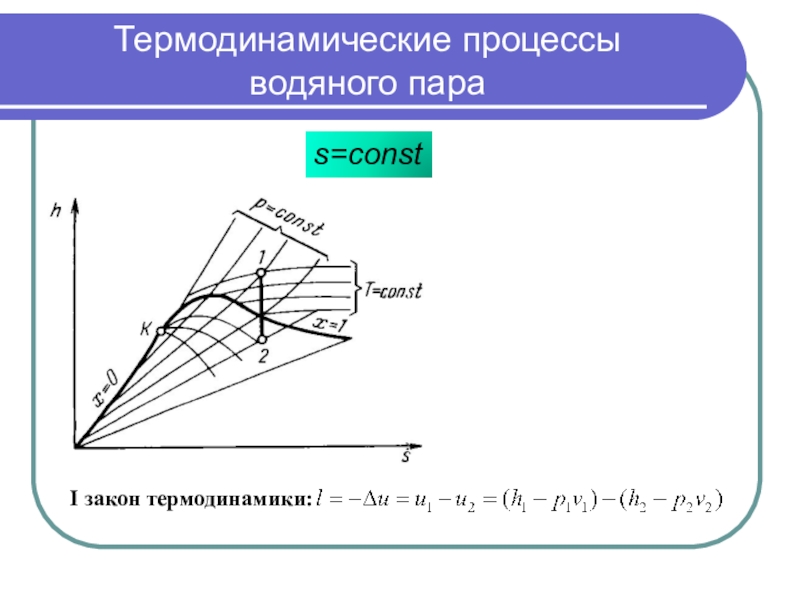
s=сonst
I закон термодинамики:
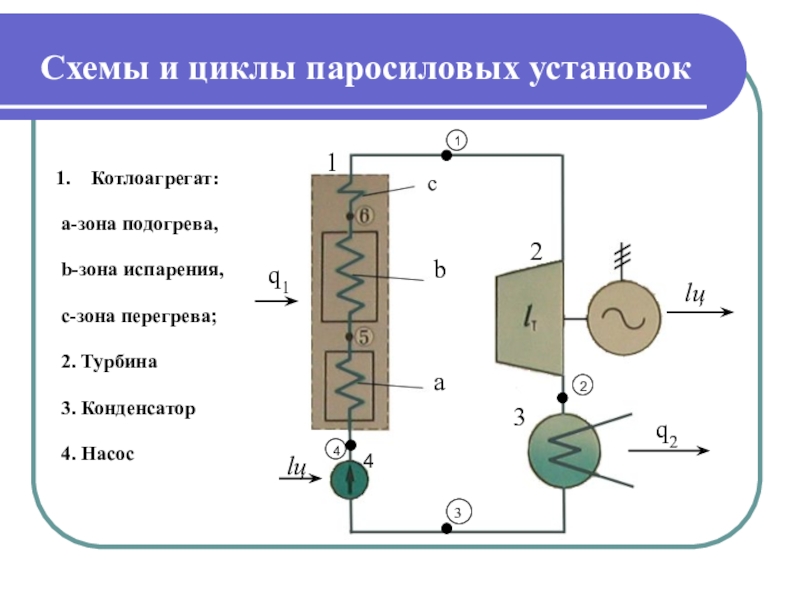
Слайд 24Схемы и циклы паросиловых установок
Котлоагрегат:
a-зона подогрева,
b-зона испарения,
с-зона перегрева;
2. Турбина
3. Конденсатор
4. Насос
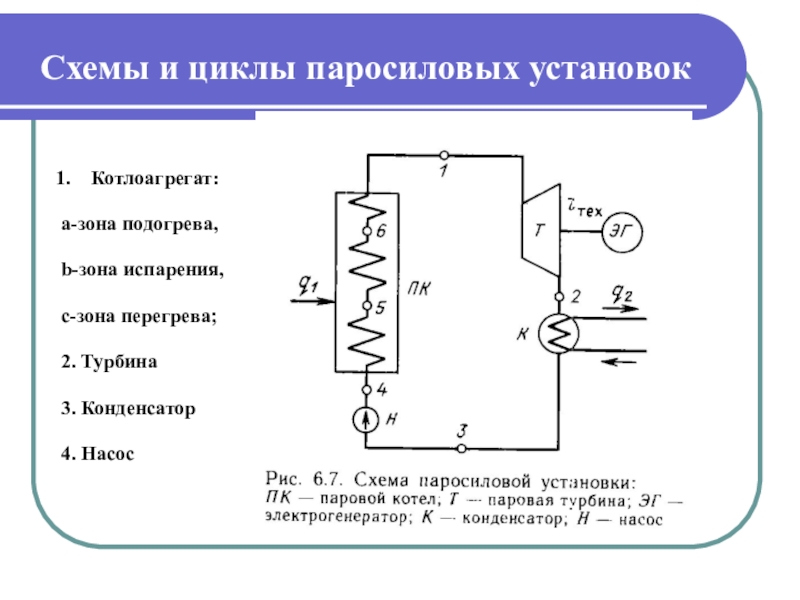
Слайд 25Схемы и циклы паросиловых установок
Котлоагрегат:
a-зона подогрева,
b-зона испарения,
с-зона перегрева;
2. Турбина
3. Конденсатор
4. Насос
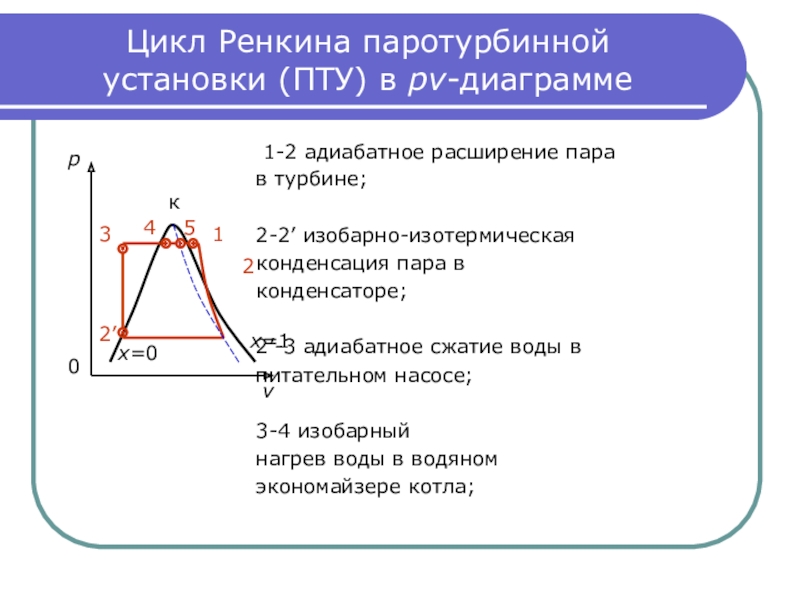
Слайд 26Цикл Ренкина паротурбинной
установки (ПТУ) в pv-диаграмме
1-2
адиабатное расширение пара
в турбине;
2-2’ изобарно-изотермическая
конденсация пара в
конденсаторе;
2’-3 адиабатное сжатие воды в
питательном насосе;
3-4 изобарный
нагрев воды в водяном
экономайзере котла;
x=0
x=1
p
0
v
к
1
2
2’
3
4 5
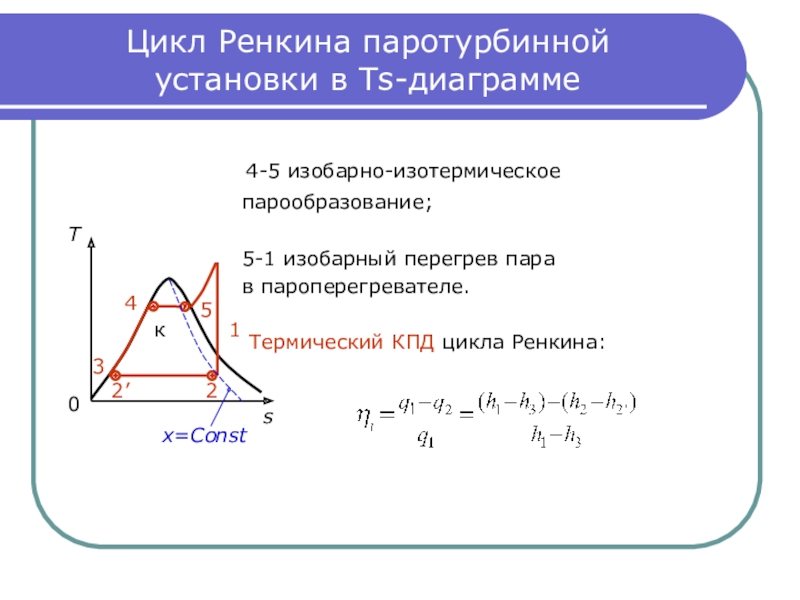
Слайд 27Цикл Ренкина паротурбинной
установки в Ts-диаграмме
4-5 изобарно-изотермическое
парообразование;
5-1 изобарный перегрев пара
в пароперегревателе.
Термический КПД цикла Ренкина:
.
x=Const
T
0
s
к
1
2
2’
3
4
5
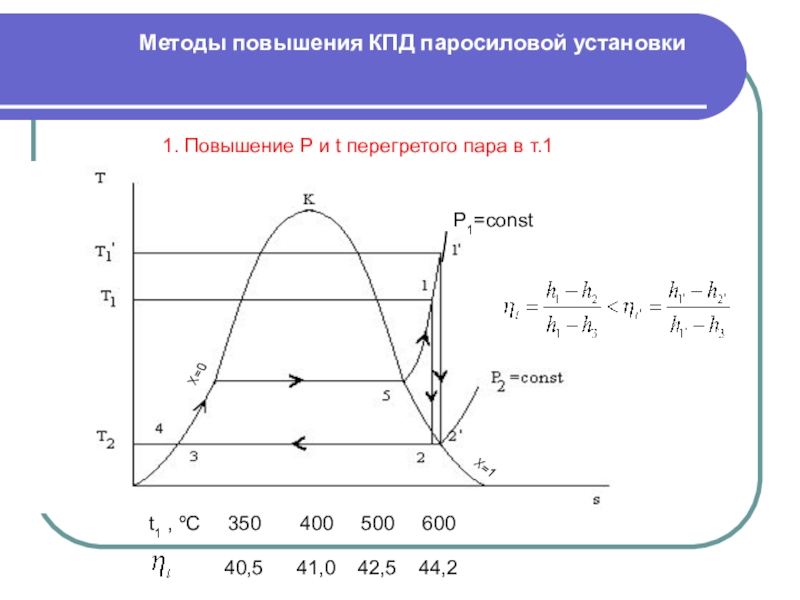
Слайд 28Методы повышения КПД паросиловой установки
1. Повышение Р и t перегретого
пара в т.1
t1 , ºC 350
400 500 600
40,5 41,0 42,5 44,2
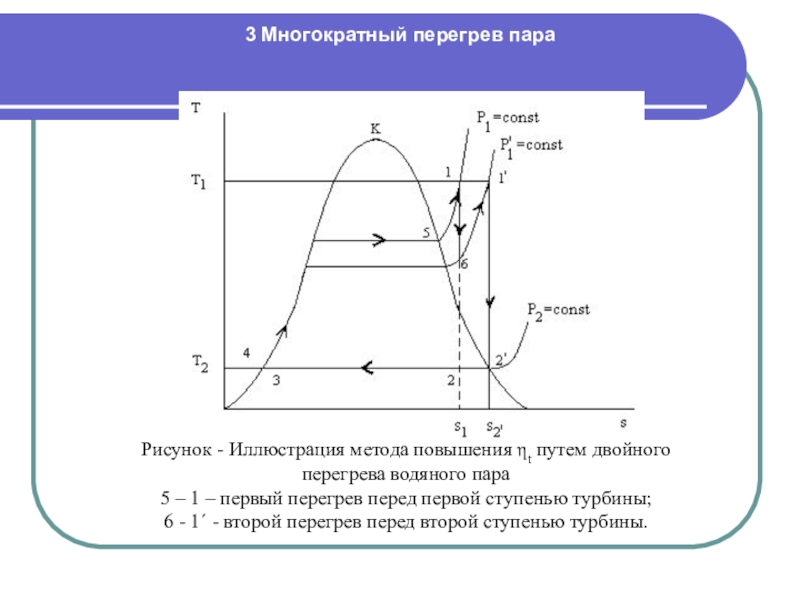
Слайд 293 Многократный перегрев пара
Рисунок - Иллюстрация метода повышения ηt путем
двойного
перегрева водяного пара
5 – 1 – первый перегрев перед первой
ступенью турбины;
6 - 1΄ - второй перегрев перед второй ступенью турбины.