Слайд 1Лекция 5. Функциональная морфология синтетического аппарата.
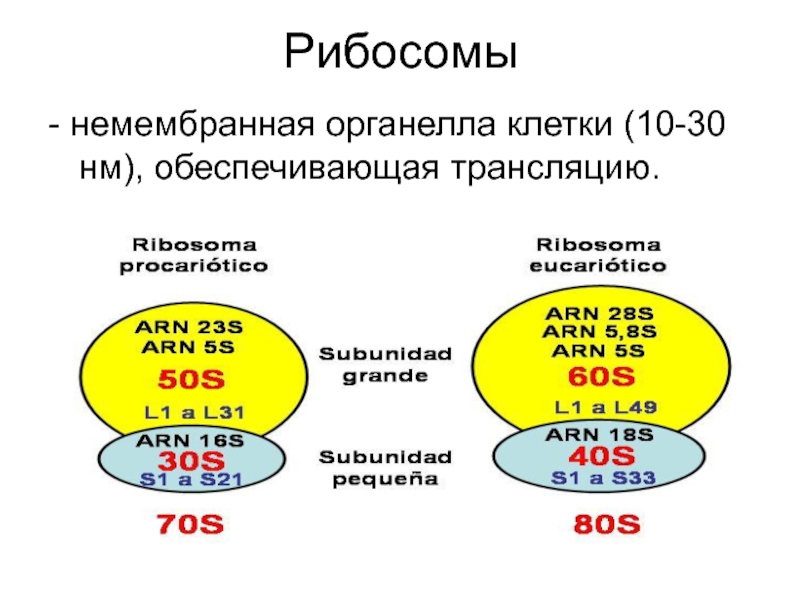
Слайд 2Рибосомы
- немембранная органелла клетки (10-30 нм), обеспечивающая трансляцию.
Слайд 380S рибосома
Неактивные рибосомы диссоциируют и располагаются в цитозоле в виде
отдельных субъединиц.
Рибосомальные белки
рРНК (5S, 18S, 5,8S, 28S)
Малая субъединица содержит 18S
рРНК и 30-40 белков.
Большая субъединица содержит 5,8S, 5S, 28S рРНК
и 50 белков.
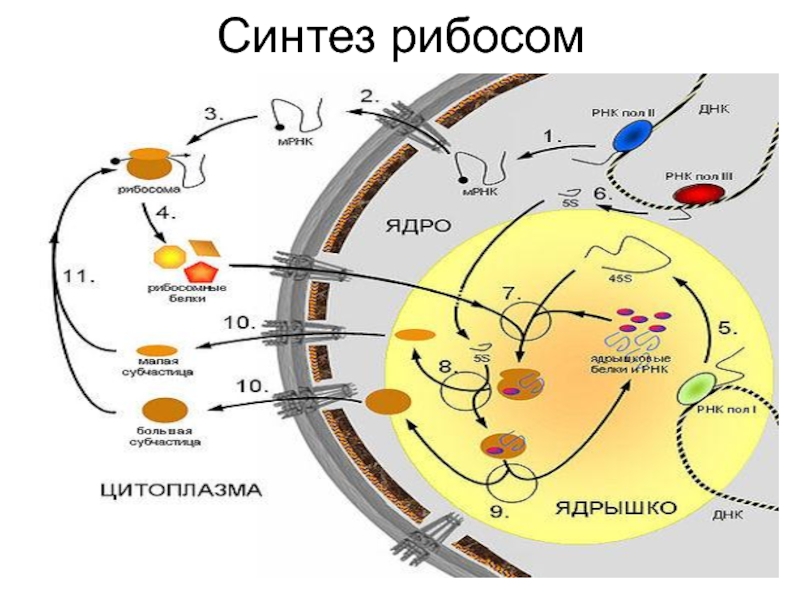
Слайд 6Сборка рибосом в цитоплазме
В присутствии мРНК
малая субъединица
связывается с
её 5‘-
концом, после чего
происходит
взаимодействие с
первой тРНК, затем
присоединение
большой субъединицы и формирование активной рибосомы.
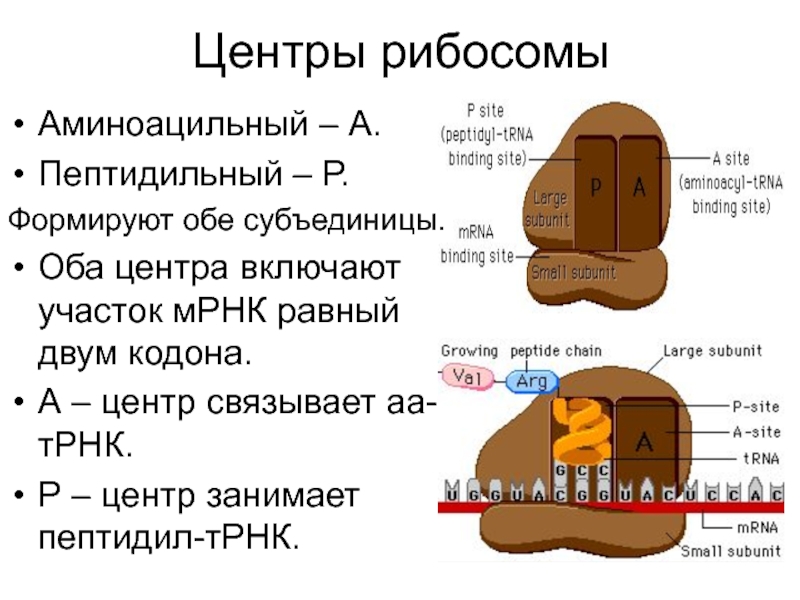
Слайд 7Центры рибосомы
Аминоацильный – А.
Пептидильный – Р.
Формируют обе субъединицы.
Оба центра включают
участок мРНК равный двум кодона.
А – центр связывает аа-тРНК.
Р –
центр занимает пептидил-тРНК.
Слайд 8Полисома (полирибосома)
несколько рибосом, объединенных общей мРНК. Рибосомы в составе полисомы
– транслирующие. Неактивные рибосомы располагаются поодиночке и диссоциированы.
Слайд 9Протеасома
белковый комплекс, осуществляющий разрушение цитоплазматических белков.
В эукариотических клетках
протеасомы содержатся и в ядре
и в цитоплазме клеток.
Протеасомы имеются у
архебактерий и эубактерий.
Слайд 10Синтез 20S протеасом
Коровая частица, 700kDa. Обеспечивает АТФ и убиквитин-независимый протеолиз.
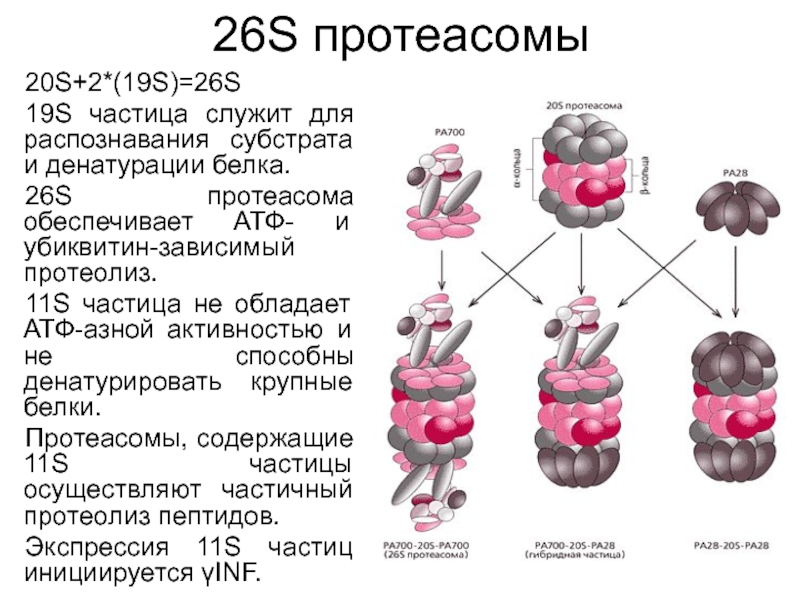
Слайд 1126S протеасомы
20S+2*(19S)=26S
19S частица служит для распознавания субстрата и денатурации белка.
26S
протеасома обеспечивает АТФ- и убиквитин-зависимый протеолиз.
11S частица не обладает АТФ-азной
активностью и не способны денатурировать крупные белки.
Протеасомы, содержащие 11S частицы осуществляют частичный протеолиз пептидов.
Экспрессия 11S частиц инициируется γINF.
Слайд 12Эндоплазматический ретикулум Описан К. Портером в 1945 г.
- постоянная
органелла эукариотической клетки, представляющая собой разветвлённую систему, окружённых мембраной уплощённых
полостей, пузырьков и канальцев.
Граулярный ЭПР.
Агранулярный ЭПР.
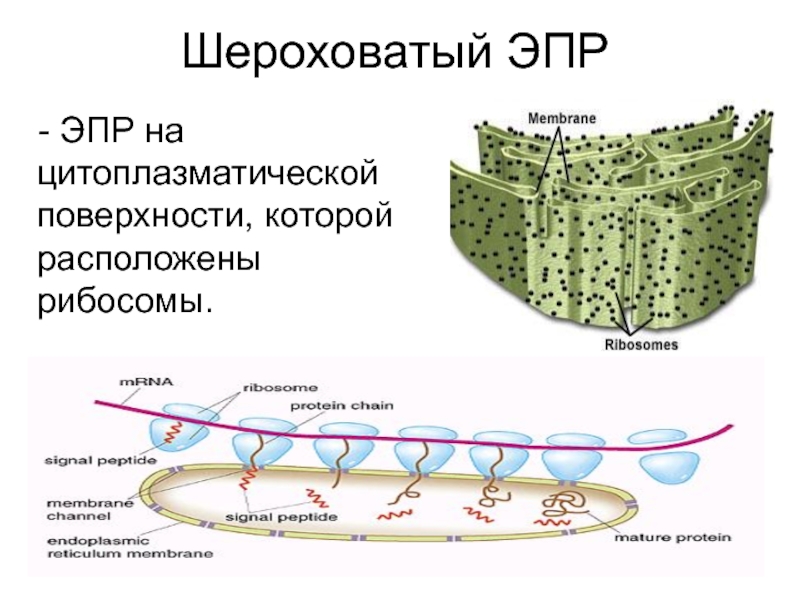
Слайд 13Шероховатый ЭПР
- ЭПР на цитоплазматической поверхности, которой расположены рибосомы.
Слайд 14Функции грЭПР
Биосинтез всех мембранных и экспортных белков.
Посттрансляционные изменения белков (обеспечение
фолдинга, химическая модификация).
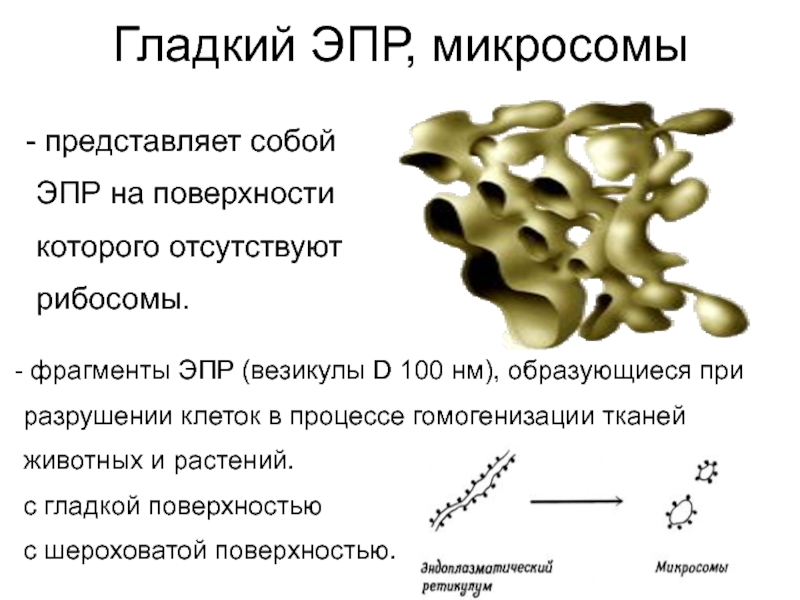
Слайд 15Гладкий ЭПР, микросомы
представляет собой
ЭПР на поверхности
которого отсутствуют
рибосомы.
фрагменты ЭПР (везикулы D 100 нм), образующиеся при
разрушении клеток в
процессе гомогенизации тканей
животных и растений.
с гладкой поверхностью
с шероховатой поверхностью.
Слайд 16Функции аЭПР
Синтез липидов.
Метаболизм углеводов.
Восстановление кариолеммы в
телофазе.
Накопление ионов Са++ (кальретикулин, кальсеквестрин). Концентрация ионов кальция в
ЭПС достигает 10−3 моль, в цитозоле составляет порядка 10−7 моль.
Формирование пероксисом.
Детоксикация (микросомальные оксидазы, внемитохондриальные ЭТЦ: NADPH-цитохром P450 редуктаза-цитохром P450; NADPH-цитохром b5 редуктаза, цитохром b5, стеароил-КоА-десатураза).
Слайд 17Метаболизм липидов и углеводов
Метаболизм липидов:
Синтез холестерола (ГМГ-КоА-редуктаза).
Синтез фосфолипидов.
Ферменты синтеза глико- и сфинголипидов на люменальной стороне
мембраны ЭПР.
Метаболизм гликогена:
глюкоза-6-фосфатаза расположена на цитозольной стороне мембраны аЭПР.
Слайд 18ERGIC
Еndoplasmicum Reticulum - Golgi Intermediate Complex
совокупность везикул, обеспечивающих взаимодействие
между ЭПР и цис- поверхностью комплекса Гольджи.
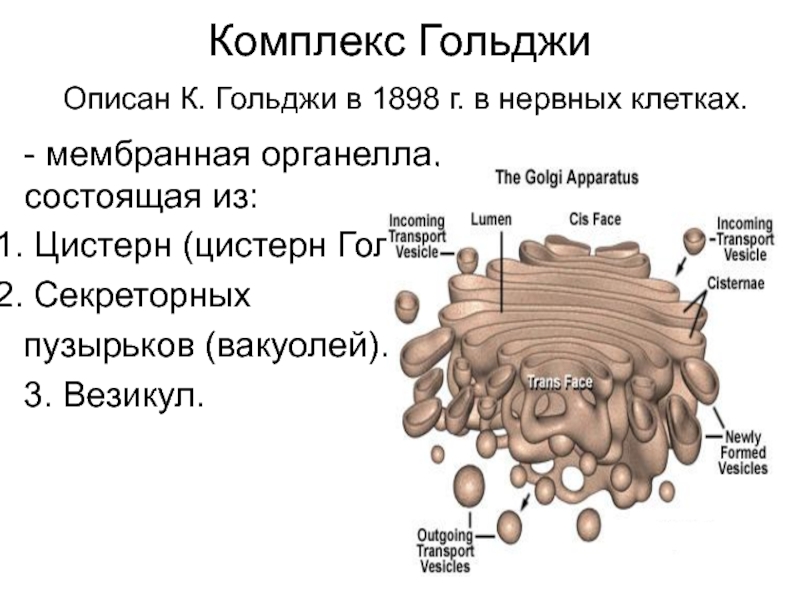
Слайд 19Комплекс Гольджи
Описан К. Гольджи в 1898 г. в нервных
клетках.
- мембранная органелла, состоящая из:
Цистерн (цистерн Гольджи).
Секреторных
пузырьков (вакуолей).
3. Везикул.
Слайд 20Диктиосома (поле Гольджи)
- основная часть комплекса Гольджи, представленная уложенными параллельно
друг другу цистернами Гольджи.
Комплекс Гольджи обычно содержит несколько диктиосом. В
экзокриноцитах диктиосомы собраны в апикальной части клетки. В неполярных
клетках диктиосомы лежат по всей цитоплазме.
Слайд 21Полярность диктиосомы
Цис (незрелая) - выпуклая, обращенная к ЭПР и
связанную с последней системой везикул – ERGIC.
Транс (зрелая) –
вогнутая, обращенная
к плазмолемме и
связанная с последней
секреторными
пузырьками.
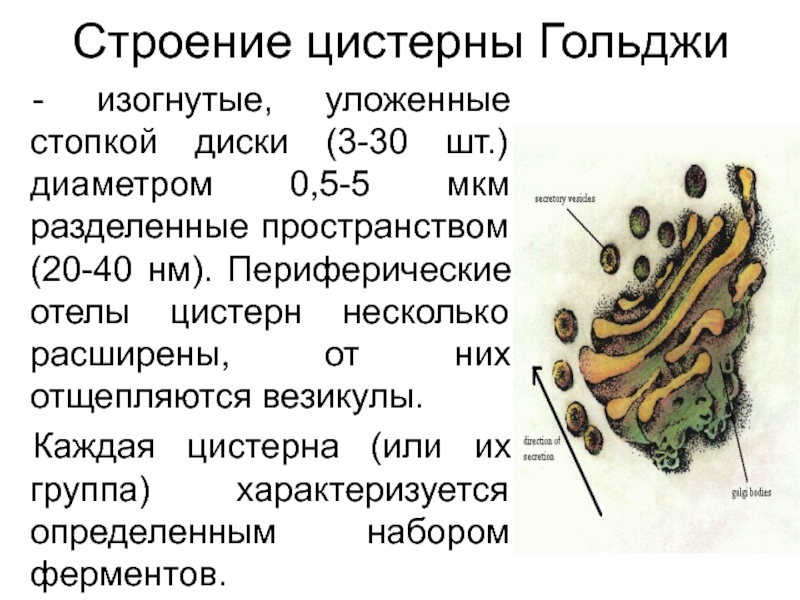
Слайд 22Строение цистерны Гольджи
- изогнутые, уложенные стопкой диски (3-30 шт.) диаметром
0,5-5 мкм разделенные пространством (20-40 нм). Периферические отелы цистерн несколько
расширены, от них отщепляются везикулы.
Каждая цистерна (или их группа) характеризуется определенным набором ферментов.
Слайд 23Везикулы и секреторные пузырьки
Везикулы - сферические элементы (D 40-80 нм),
образующиеся путем отщепления от цистерн. Служат для переноса веществ между
цистернами внутри диктиосомы или комплекса Гольджи.
Вакуоли – крупные сферические образования, формирующиеся на «зрелой» поверхности диктиосомы. Содержат модифицированный продукт, предназначенный для секреции.
Слайд 24Функции комплекса Гольджи
Формирование секреторных гранул.
Обновление плазмолеммы.
Процессинг белков (гликозилирование, фосфорилирование, ацилирование,
сульфатирование, частичный протеолиз).
Синтез полисахаридов.
Сортировка белков (обеспечивается процессингом и рецепторами мембраны
диктиосомы).
Слайд 25Транскрипция. Транскриптон.
Транскрипция - синтез гяРНК по матрице ДНК.
Транскриптон – участок
ДНК, ограниченный промотором и
терминатором,
представляющий
единицу транскрипции.
Матричная
Кодирующая
Слайд 26Инициация-элонгация-терминация транкрипции
ТАТА-фактор, взаимодействует с ТАТА-боксом, после чего происходит присоединение РНК-полимеразы.
Факторы инициации вызывают раскручивание одного витка спирали – транскрипционная вилка.
Синтезируется олигонуклеотид (8-10), присоединяются факторы элонгации. Синтез молекулы идет от 5‘ к 3‘ концу матричной цепи ДНК. Раскручивание двойной спирали в области сайта терминации, вызывает его связывание с факторами терминации. Факторы терминации обеспечивают отделение первичного транскрипта.
Слайд 27Процессинг первичного транскрипта
Сплайсинг.
Кэпирование.
Полиаденилирование.
Модификация азотистых
оснований.
зрелая РНК
Слайд 28Сплайсинг
процесс удаления интронов из гяРНК, с последующим соединением экзонов
и формированием мРНК.
Сплайсосома – нуклеопротеиновый комплекс, обеспечивающий сплайсинг.
Консенсусные последовательности (сайты
сплайсинга):
- 5‘: GUAAGU, AGGU
- 3‘: UCAGG, GAGG.
Слайд 29Варианты сплайсинга
Неферментативный (аутосплайсинг - вид сплайсинга, при котором интроны
являются рибозимами).
Ферментативный:
1. С участием матюраз.
2. С участием сплайсосом:
2.а.
Классический сплайсинг
2.б. Альтернативный сплайсинг
2.в.Транссплайсинг – форма сплайсинга, при которой соединяются РНК разных транскриптов.
Ретросплайсинг – молекулярный эффект вставки интрона (рибозима) в гомологичную ДНК.
Слайд 30Кэпирование пре-мРНК
Присоединение гуанилилтрансферазой к 5’-концу синтезирующейся пре-мРНК (≈ 30
нуклеотидов) 7-метилгуанозина – кэпа.
Биологическая роль:
1. защита пре-мРНК от 5’-экзонуклеаз цитоплазмы;
2.
необходимы для инициации трансляции;
3. Необходимы для сплайсинга.
Слайд 31Полиаденилирование
Присоединение полиаденилатполимеразой к 3’-концу пре-мРНК поли(А)-фрагмента (≈200 адениловых нуклеотидов).
Сигналом к полиаденилированию является – ААUААА.
Биологическая роль:
защита пре-мРНК
от 3’-экзонуклеаз цитоплазмы;
необходимо для транспорта м-РНК из ядра в цитоплазму.
Описанные ферменты активны только в присутствии РНК-полимеразы II.
Слайд 32Ковалентная модификация азотистых оснований РНК
Дезаминирование цитозина (урацил). Редактирование пре-мРНК
апопротеина В в энтероцитах тонкого кишечника. Эта модификация приводит к
возникновению белка апо-В-48, вместо апо-В-100, синтезируемого печенью.
Метилирование рибозы нуклеотидов РНК.
Восстановление уридина (дигидроуридин).
Изомеризация уридина (псевдоуридин).
Метилирование уридина (метилуридин).
Дезаминирование аденозина (инозин).
Метилирование инозина (метилинозин).
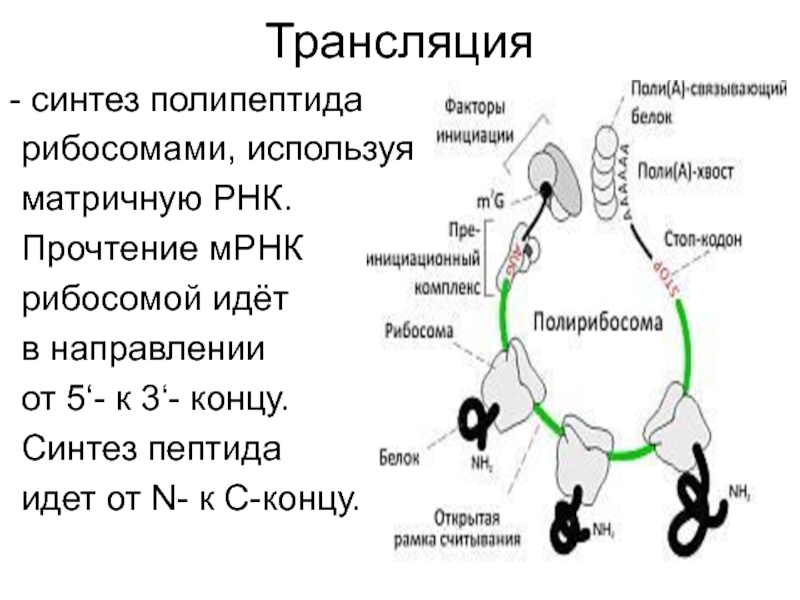
Слайд 33Трансляция
синтез полипептида
рибосомами, используя
матричную РНК.
Прочтение мРНК
рибосомой идёт
в направлении
от 5‘- к 3‘- концу.
Синтез пептида
идет от N-
к С-концу.
Слайд 34Инициация трансляции
Происходит образование комплекса мРНК, рибосомы и инициирующей тРНК (fMet-,
Met-тРНК).
Участвуют eIF (более 10). 40S субъединица связывается с Met-tRNAi, ГТФ
и eIF-2. Далее этот комплекс связывается с 5‘-концом мРНК. Прикрепившись к мРНК 40S перемещается по ней, достигая инициирующего кодона AUG, с затратой АТФ. Затем 40S субъединица соединяется с 60S субъединицей с образованием 80S рибосомы за счет гидролиза ГТФ. Формируются А- и Р-центры. Существуют 2 тРНК, узнающие кодон АUG: Met-tRNAi и Met-tRNA.
Слайд 35Элонгация трансляции
В Р-центре – AUG-кодон, соединенный с Met-tRNAi, в А-центре
– триплет, кодирующий включение первой аминокислоты синтезируемого белка.
Элонгация включает 3
этапа:
связывание аа-тРНК с А-центром рибосомы.
Присоединение пептида пептидил-тРНК Р-центра к NH2-группе аминоацильного остатка аа-тРНК А-центра (транспептидация).
Перемещение удлиненной на один аминокислотный остаток пептидил-тРНК из А-центра в Р-центр (транслокация).
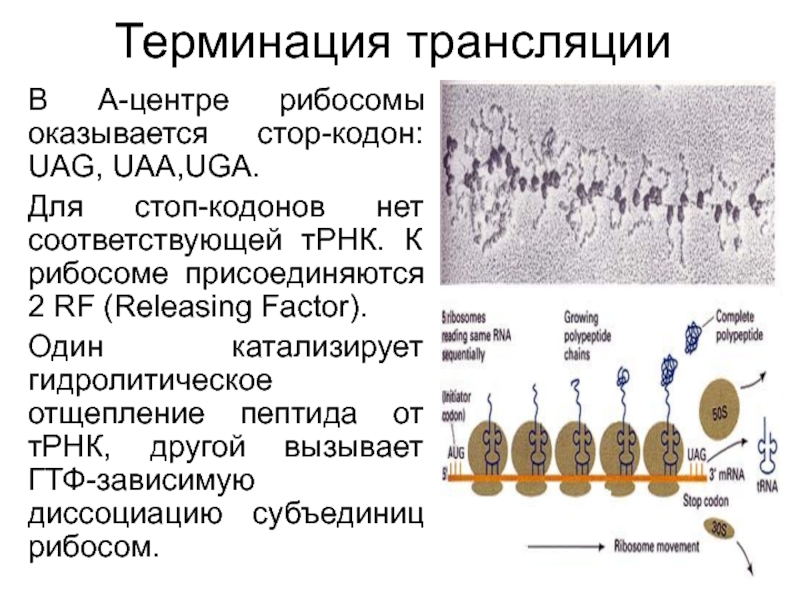
Слайд 36Терминация трансляции
В А-центре рибосомы оказывается стор-кодон: UAG, UAA,UGA.
Для стоп-кодонов нет
соответствующей тРНК. К рибосоме присоединяются 2 RF (Releasing Factor).
Один катализирует
гидролитическое отщепление пептида от тРНК, другой вызывает ГТФ-зависимую диссоциацию субъединиц рибосом.
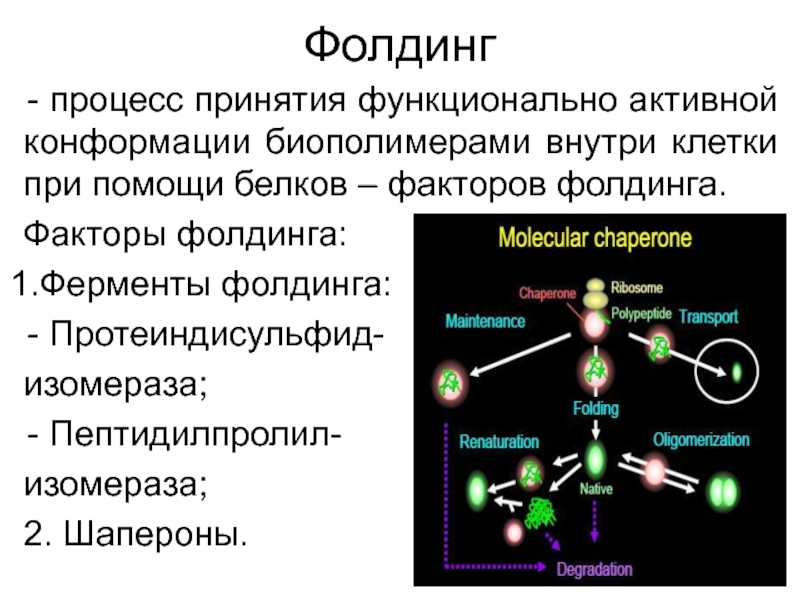
Слайд 37Фолдинг
процесс принятия функционально активной конформации биополимерами внутри клетки при
помощи белков – факторов фолдинга.
Факторы фолдинга:
Ферменты фолдинга:
Протеиндисульфид-
изомераза;
Пептидилпролил-
изомераза;
2. Шапероны.
Слайд 38Шапероны
класс белков, придающих, стабилизирующих и восстанавливающие конформацию других белков.
Конститутивные
Индуцибельные (белки теплового шока, НSP)
Функции шаперонов:
Обеспечение правильного
фолдинга
белков.
Предотвращение агрегации
белковых молекул.
Обеспечение рефолдинга.
Поддержание определенной
конформации белка.
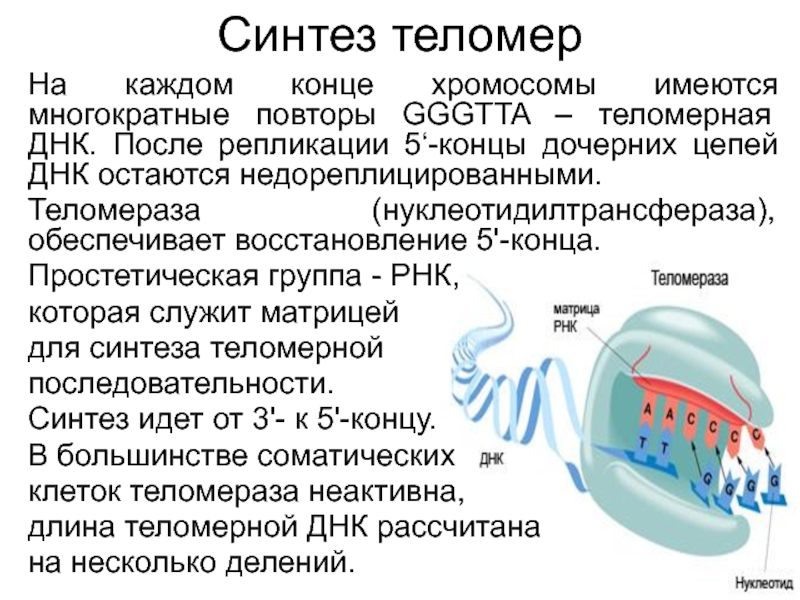
Слайд 39Синтез теломер
На каждом конце хромосомы имеются многократные повторы GGGTTA –
теломерная ДНК. После репликации 5‘-концы дочерних цепей ДНК остаются недореплицированными.
Теломераза (нуклеотидилтрансфераза), обеспечивает восстановление 5'-конца.
Простетическая группа - РНК,
которая служит матрицей
для синтеза теломерной
последовательности.
Синтез идет от 3'- к 5'-концу.
В большинстве соматических
клеток теломераза неактивна,
длина теломерной ДНК рассчитана
на несколько делений.