Слайд 1Лекция №4 для фармацевтического факультета
Крымский федеральный университет
имени В.И. Вернадского
Медицинская академия имени С.И. Георгиевского
Кафедра биологии медицинской
Агеева Елизавета Сергеевна
доктор
медицинских наук,
доцент по кафедре патофизиологии,
Заведующий кафедрой биологии медицинской
Стоматологического факультета
ИЗМЕНЧИВОСТЬ
Слайд 2Изменчивость – фундаментальное свойство живых организмов приобретать новые признаки и
свойства в процессе онтогенеза.
Выделяют модификационную, комбинативную и мутационную изменчивость
Слайд 3Фенотипическая ненаследственная
Признаки для которых характерен этот вид изменчивости: рост,
масса , окраска
Механизм: условия среды воздействуют на реакции и приводят
к их изменению
Факторы:
1. определяются влиянием среды. Имеют направленный характер
2. изменения не наследуются потомками, связаны только с фенотипом
3. изменения появляются массово
4. изменения носят адаптивный характер (приспособительный)
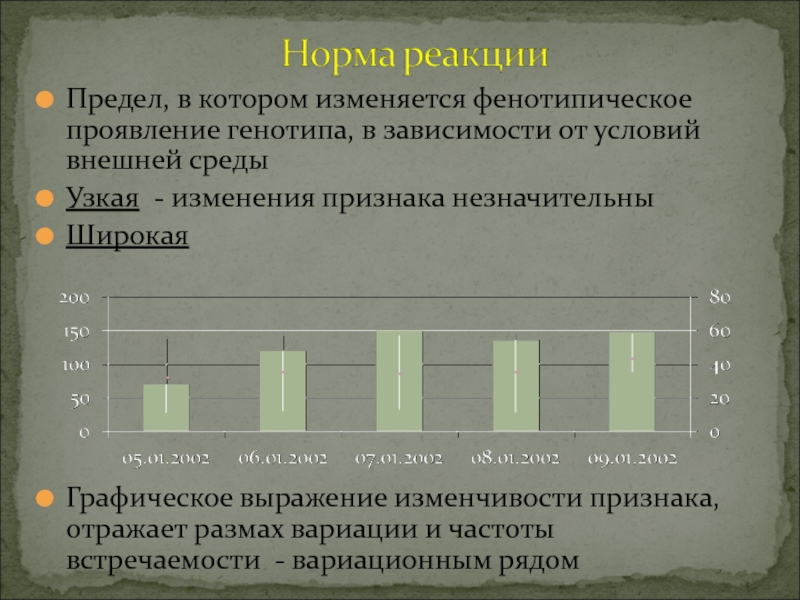
Слайд 4Предел, в котором изменяется фенотипическое проявление генотипа, в зависимости от
условий внешней среды
Узкая - изменения признака незначительны
Широкая
Графическое выражение изменчивости
признака, отражает размах вариации и частоты встречаемости - вариационным рядом
Слайд 5Генотипическая наследственная
Получение новых сочетаний генов в генотипе
Механизм:
1. независимое
расхождение хромосом в анафазе мейоза-1, хроматид в анафазе мейоза-2
2. перекомбинация
генов при кроссинговере
3. случайное сочетание гамет при оплодотворении
Слайд 6Генотипическая наследственная
Мутации генов в генотипе
Свойства мутаций:
1. возникают внезапно
2.
наследуются
3. ненаправлены
4. могут возникать повторно
NB! В ходе репликации и рекомбинации
постоянно возникают различные нарушения в структуре ДНК и хромосом, которые распознаются и исправляются системами репарации. Нарушения во время реализации этого процесса может приводить к мутациям.
Слайд 7Наследственная патология связана с мутациями (т.е. с изменением генетического материала).
Средняя частота мутаций 10-6 на 1 гамету в поколение.
Причины мутаций
- мутагены.
Слайд 8физические - ионизирующее излучение, температурный фактор,
химические – АФК, ароматические углеводороды,
цитостатики, органические растворители, пестициды, препараты ртути,
биологические – вирусы кори, краснухи,
гриппа, антигены некоторых микроорганизмов
Слайд 9Если по происхождению мутагены относятся к факторам окружающей среды, то
они называются экзогенные.
Если они образуются во время жизнедеятельности организма, то
- эндогенные.
Мутагенез - это, соответственно, процесс.
Слайд 10в соматических клетках
злокачественные опухоли
врожденные пороки развития
в половых (генеративные)
наследственные
болезни
болезни с наследственной предрасположенностью ( МФЗ)
врожденные пороки развития (мутации во
время органогенеза)
Слайд 11Спонтанные (самопроизвольные)
Под действием естественных мутагенных факторов внешней среды без вмешательства
человека
Индуцированные
Появляются в результате направленного воздействия определенных мутагенных факторов
Слайд 12Летальные
Вызывают гибель организма
Сублетальные
Снижают жизнедеятельность
Нейтральные
Не влияют жизнедеятельность
Слайд 13Доминантные
Субдоминантные (проявляющиеся частично)
Рецессивные
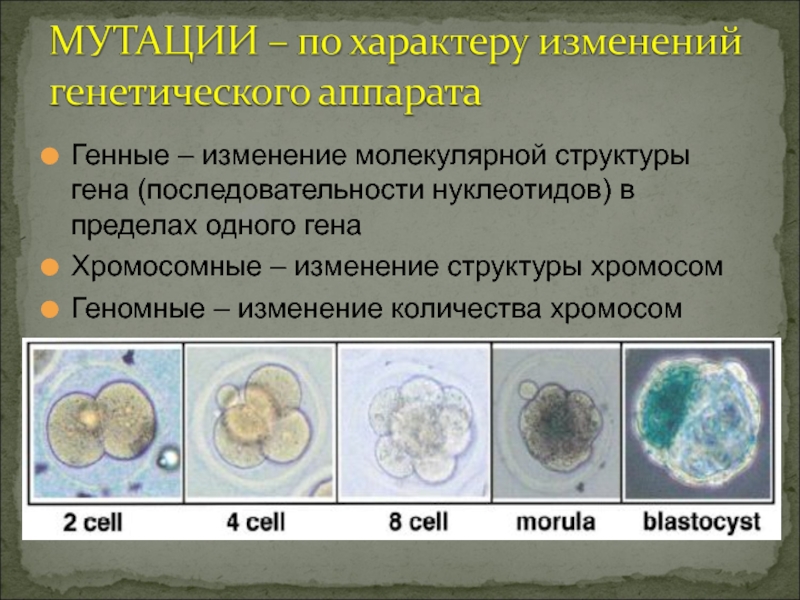
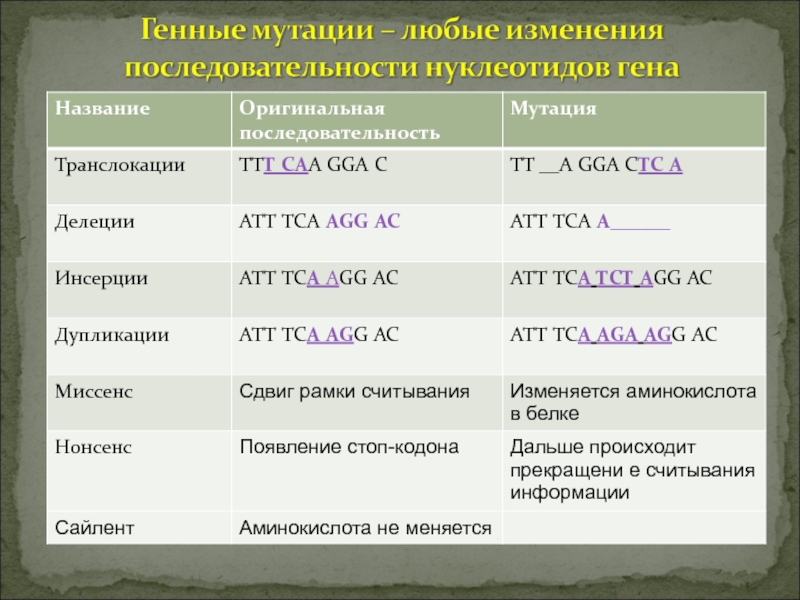
Слайд 14Генные – изменение молекулярной структуры гена (последовательности нуклеотидов) в пределах
одного гена
Хромосомные – изменение структуры хромосом
Геномные – изменение количества
хромосом
Слайд 15Гены
Структурные
Регуляторные
в кодирующей части –может качественно измениться синтез
белка
в регуляторной части – например, в промоторе –количественно измениться
в интронах – ничего не будет – нейтральная (сайлент) мутация
Слайд 17Заболевания связанные с генными мутациями могут быть – моногенными (1
ген – 1 заболевание)
Пример – фенилкетонурия – аутосомно-рецессивное заболевание, обусловленное
нарушением обмена незаменимой аминокислоты фенилаланина, поступающей в организм человека с белковой пищей
ФКУ 1 типа – дефицит фенилаланин-4-гидроксилазы
ФКУ 2 и 3 типа – дефект птеринового кофактора (1-3%)
Слайд 18Эпидемиология фенилкетонурия
Причина – рецессивная мутация
Частота ФКУ составляет 1 на
10 000 новорожденных
(1 : 4370 в Турции, 1 : 80500
в Японии, 1 : 12280 Италия)
(1 : 4735 Курская область, 1 : 18000 Республика Тыва, 1 : 7600 Санкт-Петербург, 1 : 6772 Москва)
Частота носителей гена (гетерозиготы) 1 на 50
Слайд 19Фенилкетонурия
1 тип - дефицит фермента фенилаланингидроксилазы ведет к накоплению
фенилаланина и продуктов его распада в биологических жидкостях – 12q22-q24.1
2
тип – дефицит цитозольной дигидроптеринредуктазы, который приводит к блоку на пути превращения фенилаланина в тирозин, а также предшественников образованиякатехоламинов и серотонина – 4р15.3
3 тип – недостаточность цитозольной 6-пирувоилтетрагидроптеринсинтетазы в печени и эритроцитах, участвующей в процессе синтеза тетрогидробиоптерина из дигидронеоптерина трифосфата – q22.3-23.3
Слайд 20Заболевание
На первом году жизни (2-6 месяцев) – вялость, отсутствие
интереса к окружающему, иногда повышенная раздражительность, беспокойство, срыгивание, гипотония, судороги,
явления дерматита
Задержка мышечного и психического развития
Микроцефалия и гидроцефалия
Гипопигментация кожи
Эпилептические приступы
Течение прогрессирующее, приводящее к смерти на 2-3 году жизни
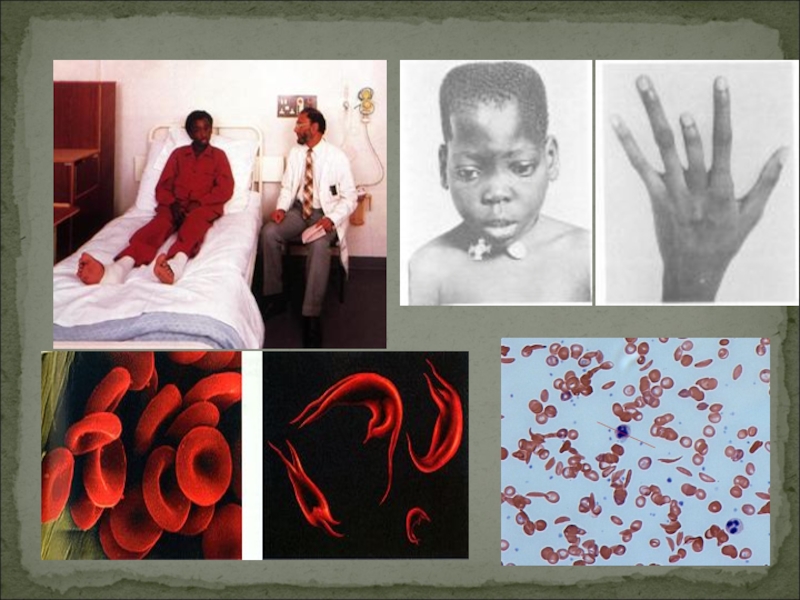
Слайд 21Серповидноклеточная анемия
Мутация в гене β-субъединицы гемоглобина
Дефект гена HBB -
11p15.5.
Дефектный гемоглобин HbS образуется в результате замены валина на
глутаминовую кислоту
Отдавая тканям кислород гемоглобин полимеризуется с образованием волокон, которые деформируют эритроциты с формированием длинных цепей, эритроциты становятся серповидными
Это вызывает увеличение вязкости крови, стаз; создается механическая преграда в мелких артериолах и капиллярах, что приводит к тканевой ишемии (с чем связаны болевые кризы), образуются тромбы, возникает анемия.
Слайд 22ЦТТ в ДНК
ГАА в РНК
ЦАТ в ДНК
ГУА в РНК
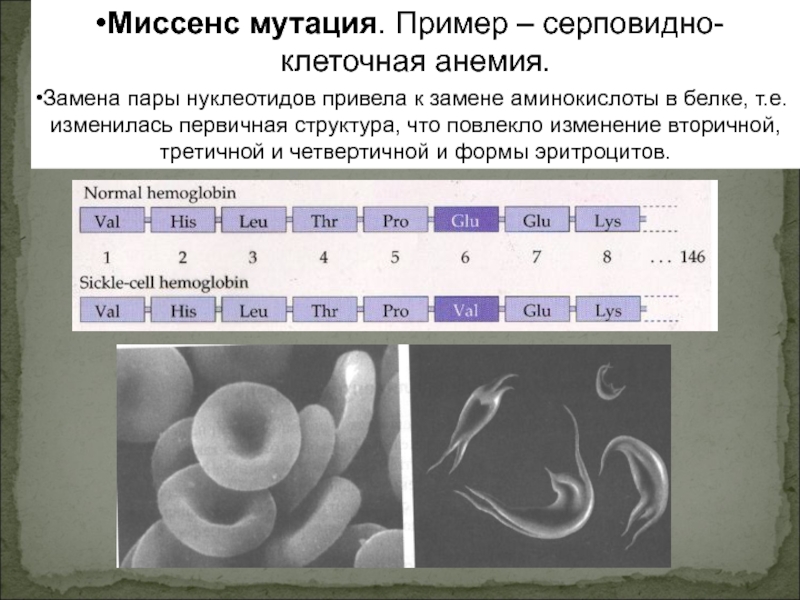
Миссенс мутация.
Пример – серповидно-клеточная анемия.
Замена пары нуклеотидов привела к замене
аминокислоты в белке, т.е.изменилась первичная структура, что повлекло изменение вторичной, третичной и четвертичной и формы эритроцитов.
Слайд 24Нонсенс мутация может возникнуть как в результате замены нуклеотида, так
и при сдвиге рамки считывания. Пример: группа крови 0.
У
людей с данной группой крови в гене произошло выпадение (делеция) одного нуклеотида – в результате возник стоп-кодон. Синтезируется короткий и неактивный белок-фермент.
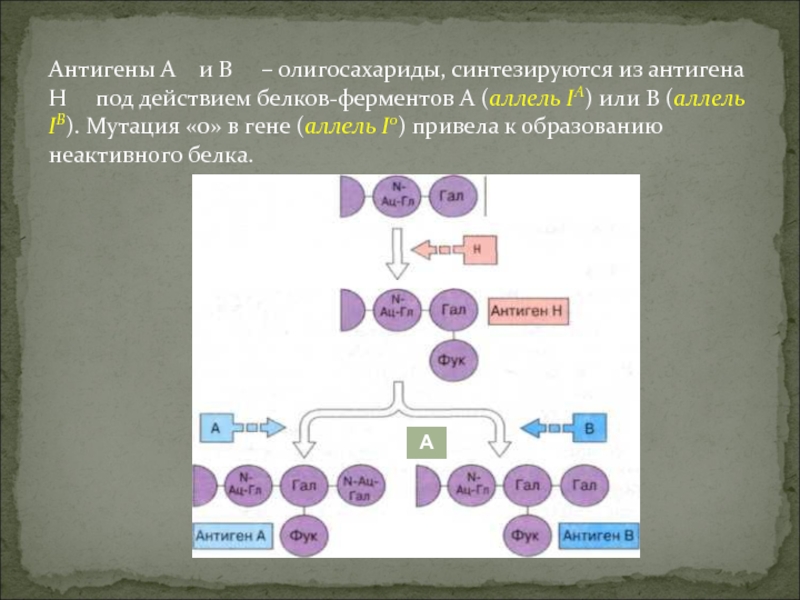
Слайд 25Антигены А и В – олигосахариды, синтезируются
из антигена Н под действием белков-ферментов А (аллель
IA) или В (аллель IВ). Мутация «0» в гене (аллель I0) привела к образованию неактивного белка.
А
Слайд 28Соматические мутации в специфических генах, участвующих в контроле клеточного деления,
дифференцировки, пролиферации, являются причиной развития многих онкологических заболеваний.
Эти гены
делятся на два класса: доминантные и рецессивные онкогены.
Таким образом, рак – это болезнь генов, обусловленная мутациями, чаще всего возникающими de novo в тех соматических клетках и тканях.
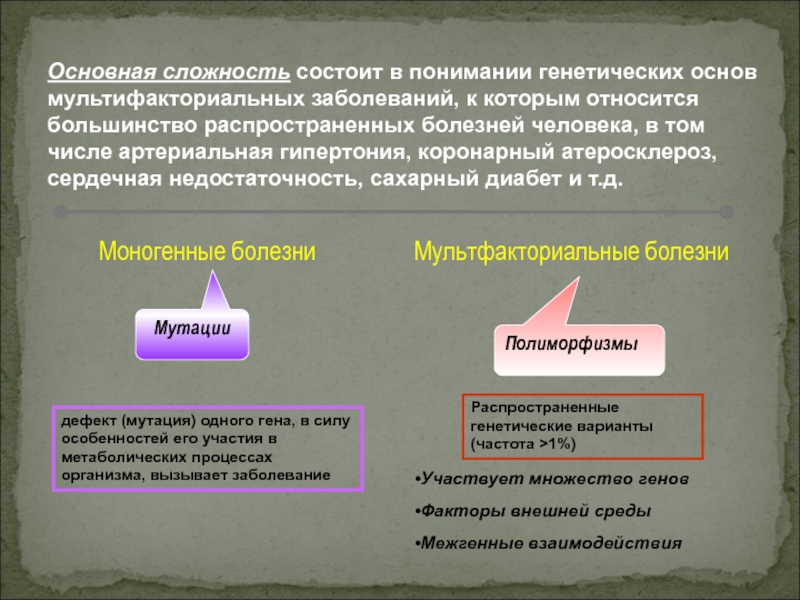
Слайд 29Основная сложность состоит в понимании генетических основ мультифакториальных заболеваний, к
которым относится большинство распространенных болезней человека, в том числе артериальная
гипертония, коронарный атеросклероз, сердечная недостаточность, сахарный диабет и т.д.
дефект (мутация) одного гена, в силу особенностей его участия в метаболических процессах организма, вызывает заболевание
Распространенные генетические варианты (частота >1%)
Участвует множество генов
Факторы внешней среды
Межгенные взаимодействия
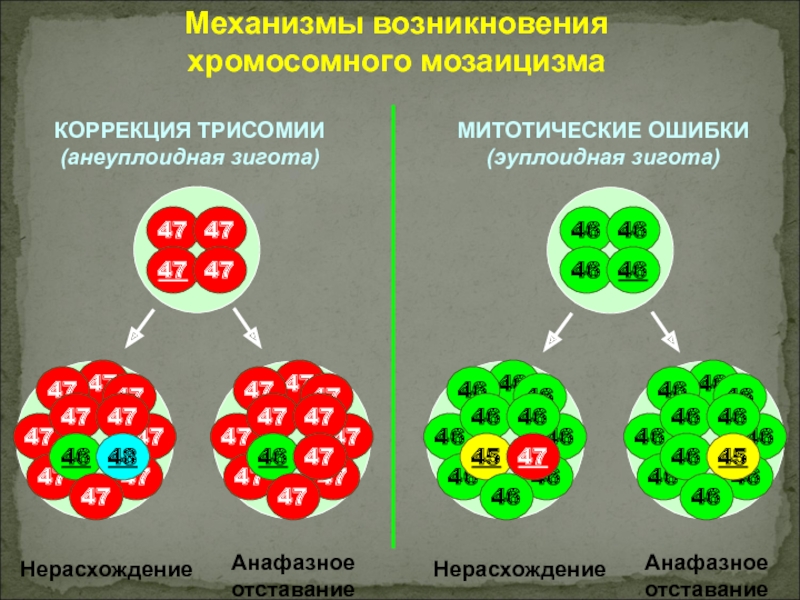
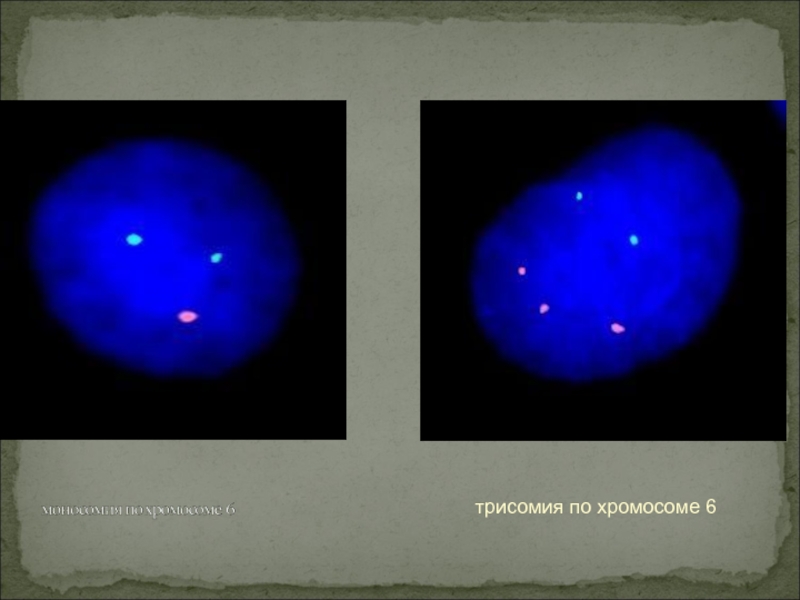
Слайд 30Нарушение структуры хромосомы
межхромосомные, изохромосомные
Слайд 31Большинство мутаций летальны.
Патологический кариотип характерен для всех клеток.
Если мутации
во время органогенеза- мозаицизм
Слайд 33Аутосомные – в аутосомах (неполовых хромосомах)
Сцепленные с Х-хромосомой
Сцепленные с Y-хромосомой
Слайд 34Моносомии, ХО
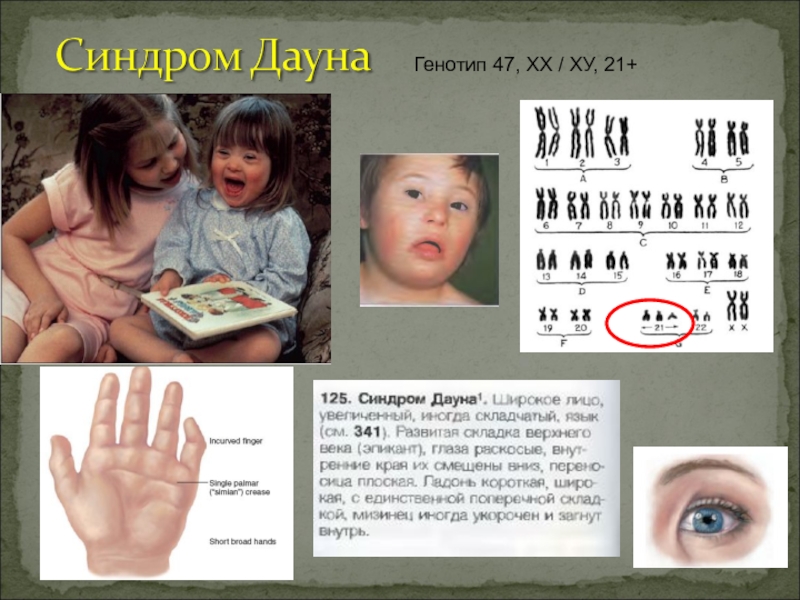
Полисомии , ХХХ, синдром Дауна
Анеуплоидии,
Полиплоидии (1п, 3п,
4п).
Геномные – изменение числа хромосом . Полиплоидии (изменение числа хромосом
в кариотипе кратное гаплоидному набору(1п, 3п, 4п)) и гетероплоиди
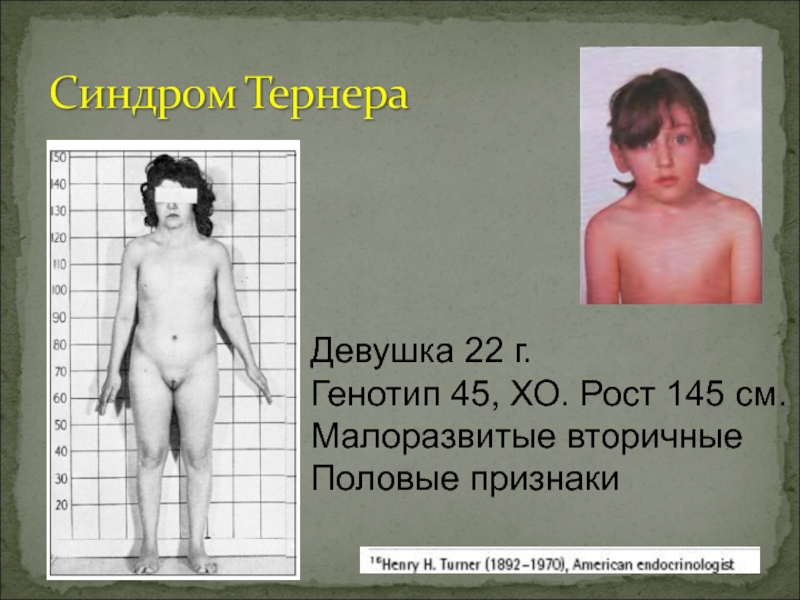
Слайд 36Девушка 22 г.
Генотип 45, ХО. Рост 145 см.
Малоразвитые вторичные
Половые
признаки
Слайд 37Синдром Кляйнефелтера (ХХУ, ХХХУ, ХХХХУ) 2-2,5 случая на 1000.
Трисомия Х
(ХХХ) 1:1000.
Синдром Шерешевского- Тернера (ХО) 1:3000.
Слайд 39Ядерные
Цитоплазматические (немногочисленные, но тяжелые митохондриальные болезни)
Митохондрии имеют свою кольцевую ДНК
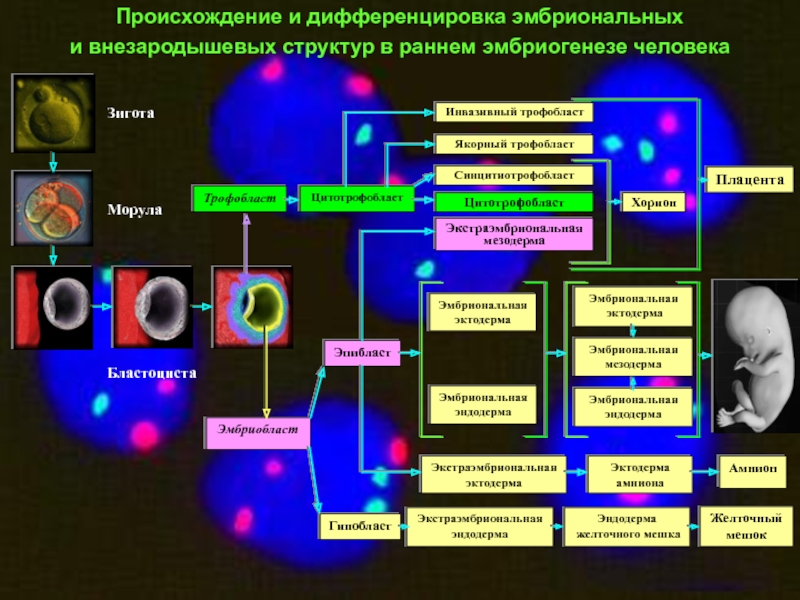
Слайд 40Происхождение и дифференцировка эмбриональных
и внезародышевых структур в раннем эмбриогенезе человека
Слайд 42Формы наследственной патологии Частота на 1000
1. МОНОГЕННЫЕ
4.5 – 15.0
Аутосомно-доминантные 2.0 – 9.5
Аутосомно-рецессивные 2.0 – 3.5
Х-сцепленные 0.5 – 15.0
2. ХРОМОСОМНЫЕ 5.0 – 7.0
3. МУЛЬТИФАКТОРИАЛЬНЫЕ 7.0 – 10.0
4. ВРОЖДЕННЫЕ ПОРОКИ РАЗВИТИЯ 19.0 – 22.0
Слайд 43Уродства – дефекты морфогенеза, наиболее тяжелые проявления ВПР
Дисплазии – деформации,
морфологические врожденные изменения, выходящие за рамки общепринятых норм
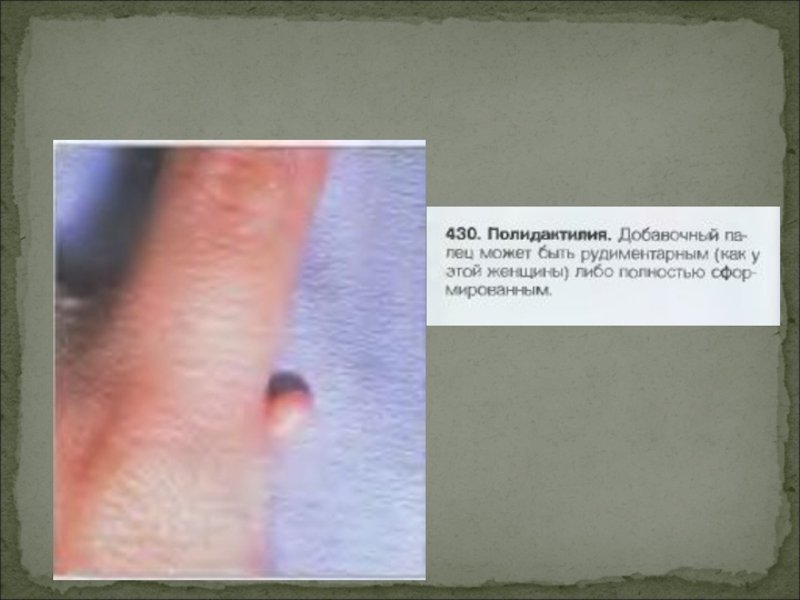
Малые аномалии развития
– стигмы дизэмбриогенеза: синдактилия, ямочки на щеках, искривление мизинца, дефекты, не требующие медицинского вмешательства
Клинически значимые пороки развития – врожденные аномалии требующие медицинского вмешательства
Слайд 44ЛС, алкоголь, марихуана, героин, кокаин, гипертемия, вещества, загрязняющие окружающую среду,
инфекционные заболевания:
Слайд 47Диагностика наследственных болезней
Анализ их распространенности в разных популяциях и этнических
группах
Медико-генетическое консультирование
Профилактика наследственных болезней (пренатальная диагностика)
Изучение молекулярно-генетических основ возникновения
и формирования наследственных заболеваний
Выявление факторов риска мультифакториальных заболеваний
Слайд 48Клинико- синдромологический
морфологические – например, УЗИ
биохимические – дефицит плазменного фактора VIII
Клинико- генеалогический
составление родословной
близнецовый
цитогенетическое - кариотипирование
Молекулярная диагностика
последовательность расположения нуклеотидов в генах
или их фрагментах
Слайд 49Генеалогическое исследование
Метод предложен в 1965 году английским ученым Ф. Гальтоном.
Суть метода - построение родословной и ее анализ. Установление наследственного
характера заболевания и типа наследования, прогнозирование рождения больных детей в семьях с наследственной патологией.
Анализ включает следующие этапы:
1. Установить, является ли заболевание единичным в семье или имеется несколько случаев (семейный характер)? Если признак встречается несколько раз среди поколений, то можно предположить, что он имеет наследственную природу;
2. Определить тип наследования признака. Составление родословной начинают с пробанда. Ведется краткая запись данных о каждом члене рода с указанием его родства по отношению к пробанду.
Генеалогические данные следует получать не менее чем от трех поколений родственников по восходящей и боковой линиям, о всех членах семьи с указанием внуков. Вносят сведения о выкидышах, абортах, мертворожденных детях, бесплодных браках и др., включая рано умерших. Обязательно следует указывать возраст проявления патологии. Чем больше поколений прослежено в родословной, тем она полнее и соответственно тем выше шансы на получение достоверных результатов.

Слайд 50ОСНОВНЫЕ ТЕРМИНЫ
Пробанд – больной или носитель определенного признака, наследование
которого необходимо изучить, то есть лицо, по отношению к которому
строится родословная.
Сибсы - дети одной родительской пары (братья и сестры).
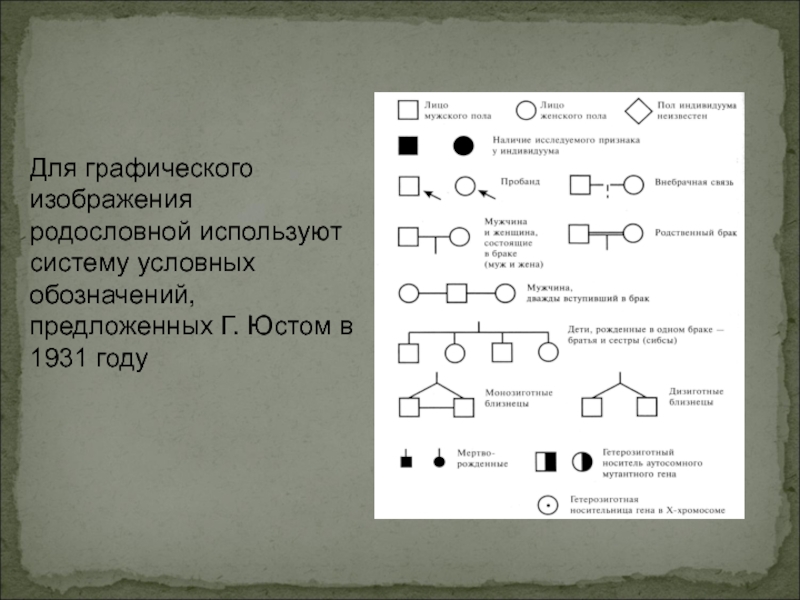
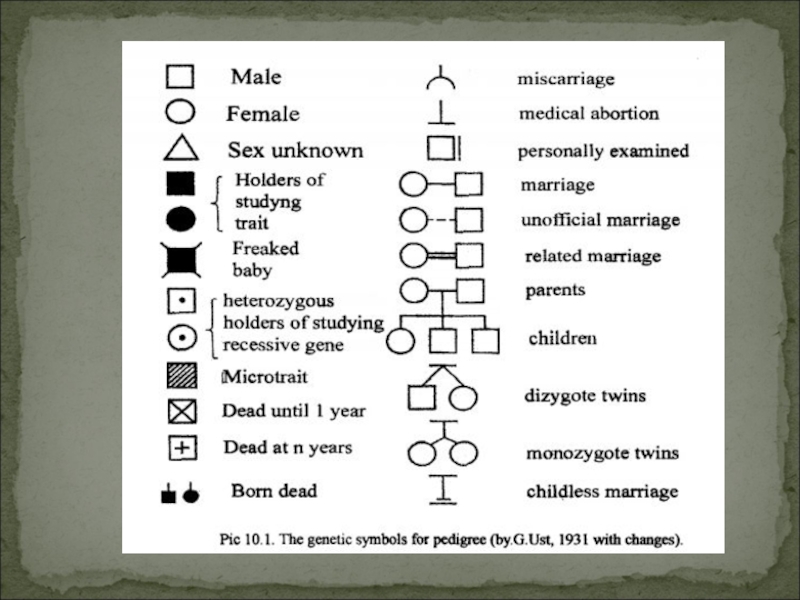
Слайд 51Для графического изображения родословной используют систему условных обозначений, предложенных Г.
Юстом в 1931 году
Слайд 531) болезнь родителей - наличие
2) заболевание у женщин и мужчин
3)
заболеваемость в поколениях (вертикальный характер распределения заболевания)
4) вероятность рождения больного
ребенка
5) заболеваемость среди сибсов (горизонтальный характер распределения заболевания)
Слайд 54Аутосомно-доминантный тип наследования
1. Патологический признак встречается в каждом поколении родословной.
2.
Признак проявляется у гомозиготных и гетерозиготных носителей гена. Если сибсов
в данном поколении много, то соотношение больных и здоровых сибсов приближается к 3:1.
3. Оба пола поражаются в равных пропорциях. Отец и мать одинаково передают мутантный ген дочерям и сыновьям; возможна передача болезни от отца к сыну.
4. Проявления болезней может развиваться не сразу после рождения.
5. Не всегда пенетрантность патологических проявлений 100 % (полная). Это связано с тем, что в поколениях могут встречаться гетерозиготы, но без выраженных признаков болезни. О гетерозиготности свидетельствует появление болезни у части их детей.
6. Различная выраженность клинических проявлений. В зависимости от экспрессивности и пенетрантности мутантного гена клинические проявления болезни могут варьировать. Доминантный ген может обладать разной степенью экспрессивности или степенью выраженности (тяжестью заболевания), что затрудняет установление типа наследования. При высокой экспрессивности гена развивается тяжелая, часто с летальным исходом, форма заболевания, а при низкой – человек внешне может быть здоров. Как правило, многие аутосомно-доминантные заболевания в гомозиготном состоянии протекают в более тяжелой форме, чем в гетерозиготном.
По аутосомно-доминантному типу наследуется полидактилия (шестипалость), брахидактилия (короткопалость), ахондроплазия (карликовость), синдром Марфана и др.

Слайд 55Аутосомно-рецессивный тип наследования
1. Заболевание встречается в родословной редко и не
во всех поколениях.
2. Риск рождения больного ребенка составляет 25 %.
3. Вероятность заболевания у девочек и мальчиков одинакова.
4. Признак может проявиться у детей, родители которых были здоровы, так как являлись гетерозиготными носителями мутантного гена.
5. Мутантный ген проявляет свое действие только в гомозиготном состоянии, в гетерозиготном состоянии он может существовать во многих поколениях, не проявляясь фенотипически.
6. Частота возникновения наследственных рецессивно-аутосомных болезней находится в прямой зависимости от степени распространенности мутантного гена среди населения: повышается в изолированных популяциях и в семьях с высоким процентом близкородственных браков.
7. Возможна различная степень экспрессивности и пенетрантности признака.
К аутосомно-рецессивным заболеваниям относятся: фенилкетонурия, галактоземия, альбинизм и др. Заболевания, как правило, диагностируются в раннем возрасте.
Слайд 56Х-сцепленный доминантный тип наследования
1. Фенотипическое проявление заболевания будут иметь
как гомозиготы, так и гетерозиготы.
2. У здоровых отцов сыновья
и их дети будут здоровыми, так как от отца им может быть передана только Y-хромосома.
3. Дочери гомо- и гетерозиготы будут фенотипически больными.
4. В литературе описаны родословные при некоторых болезнях с этим типом передачи, у которых нет сибсов мужского пола, так как сильная степень поражения вызывает их гибель еще внутриутробно.
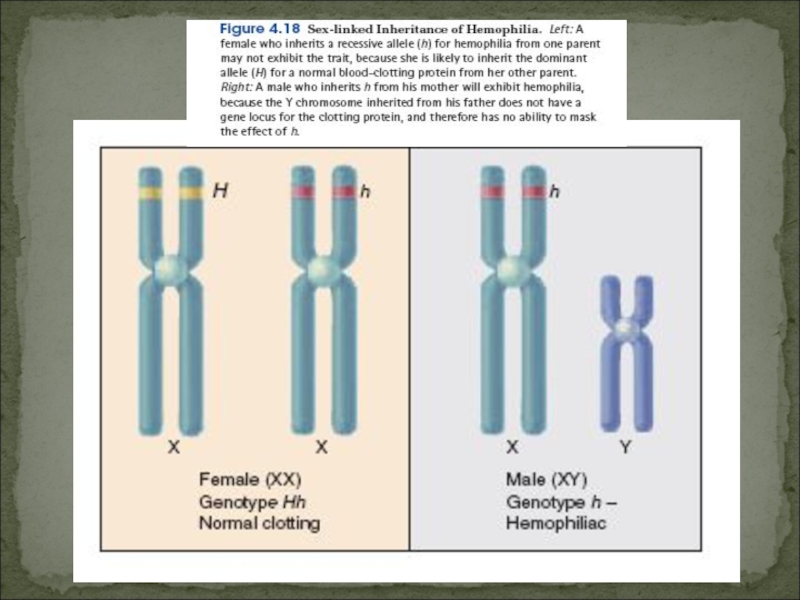
Слайд 57Х-сцепленный рецессивный тип наследования
1. Сыновья будут больными, так как имеют
только одну X-хромосому (гемизиготность).
2тистическое соотношение здоровых и больных мужчин
составляет 1:1.
Гемофилия, миопатия Дюшена, некоторые формы дальтонизма.
Женщины могут болеть такими заболеваниями как гемофилия, дальтонизм. Такие случаи возможны, но они исключительно редки, так как являются результатом встречи гетерозиготной женщины и больного мужчины.
Слайд 58Y-сцепленный тип наследования
1. Передается только сыновьям (голандрическое наследование).
С Y-хромосомой
наследуются такие признаки, как гипертрихоз (наличие волос по краю ушных
раковин), кожные перепонки между пальцами, развитие семенников, интенсивность роста тела, конечностей и зубов.
Слайд 59Цитогенетическое исследование
Осуществляется диагностика хромосомных болезней с помощью цитогенетического анализа.
Материалом
для цитогенетических исследований служат клетки человека, практически любых тканей и
органов, на любой стадии клеточного цикла, в митозе и мейозе, лимфоциты периферической крови, клетки костного мозга, фибробласты, клетки опухолей и эмбриональных тканей и др.
Показания к проведению исследования:
1. Возраст женщины на момент родов 35 лет и более.
2. Подозрение на хромосомные болезни.
3. Множественные врожденные пороки развития у уже родившихся детей.
4. Несколько случаев спонтанных абортов, мертворождений, врожденных пороков развития у детей.
5. Существенная задержка умственного и физического развития у ребенка.
6. Нарушение репродуктивной функции.
Слайд 60Различают прямые и непрямые методы исследования хромосом.
1. Прямые методы применяются
при исследовании тканей, обладающих высокой митотической активностью (костный мозг, клетки
лимфатических узлов, ткани эмбриона на ранних стадиях развития и хорион/плацента на любом сроке беременности) и при исследовании мейотических хромосом.
2. Непрямые методы включают получение препаратов хромосом из любой ткани после стимулирования пролиферации клеток в культуральных условиях в течение времени — от нескольких часов (кратковременные культуры) до нескольких лет (перевиваемые культуры).
В клинической цитогенетике широко применяются методы анализа буккального эпителия и лимфоцитов периферической крови.
Слайд 62БЛИЗНЕЦОВЫЙ МЕТОД
Предложил Ф. Гальтон в 1875 году для разграничения роли
наследственности и среды в развитии различных признаков у человека.
Суть
метода - сравнение проявления признака в разных группах близнецов. Учитывают частоту встречаемости признаков и различия их генотипов.
Различают две группы близнецов – монозиготные и дизиготные.
Монозиготные близнецы развиваются из одной оплодотворенной яйцеклетки в результате нарушения ее дробления (расхождение зародышевых клеток обычно на стадии двух бластомеров). Они однополые, генетически идентичны, так как имеют 100 % общих генов.
Дизиготные близнецы появляются в результате одновременного оплодотворения двух отличных яйцеклеток двумя разными сперматозоидами. Дизиготные близнецы имеют в среднем около 50 % общих генов и могут быть как однополыми, так и разнополыми.
Результатом сравнения этих двух групп близнецов является расчет показателей соответствия (конкордантности) и несоответствия (дискордантности), а также вычисление частоты возникновения признака в каждой группе близнецов.
Слайд 63Конкордантность (С) – показатель идентичности пары близнецов по определенному признаку;
соответствует доле (%) сходных (конкордантных) по изучаемому признаку пар среди
обследованных пар близнецов для каждой группы:
СMZ = (n MZ /NMZ) х100 %, СDZ = (n DZ /NDZ) х100 %,
где MZ – монозиготная группа близнецов, DZ – дизиготная группа близнецов, n – число пар соответствующей группы, у которых признак отмечен у обоих близнецов, N – общее число обследованных близнецовых пар этой же группы.
Дискордантность (D) – показатель, который рассчитывается для дизиготных близнецов как доля дискордантных (т. е. признак выявлен только у одного близнеца из пары) по изучаемому признаку среди всех обследованных дизиготных пар близнецов:
DDZ = 100 % – СDZ
где DZ – дизиготная группа близнецов, СDZ – показатель идентичности пары близнецов по определенному признаку.
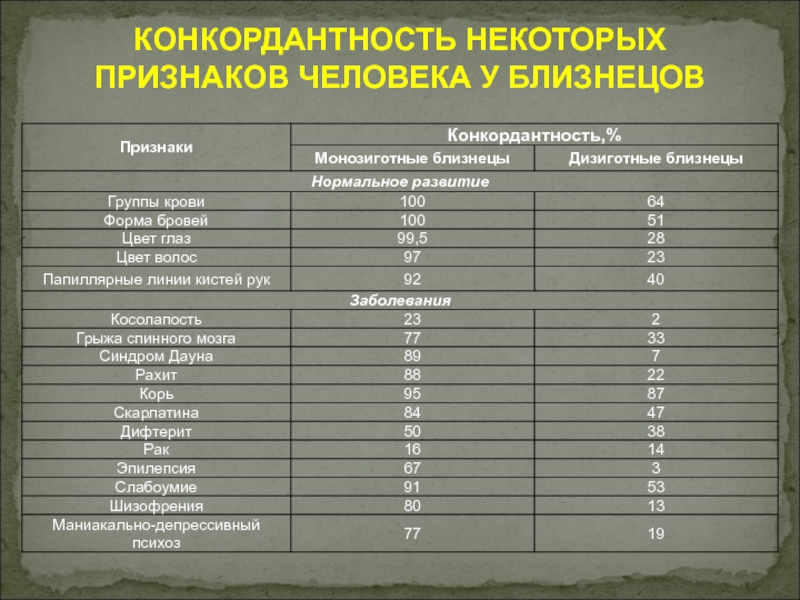
Слайд 64КОНКОРДАНТНОСТЬ НЕКОТОРЫХ ПРИЗНАКОВ ЧЕЛОВЕКА У БЛИЗНЕЦОВ
Слайд 65ПОПУЛЯЦИОННО-СТАТИСТИЧЕСКИЙ МЕТОД
Изучают наследственные признаки в больших группах населения в одном
или нескольких поколениях. С использованием статистической обработки получаемых данных.
Методом
можно рассчитать частоту встречаемости в популяции аллелей гена и соответствующих генотипов по этим аллелям, выяснить распространение в ней различных наследственных признаков, в том числе заболеваний.
Изучить мутационный процесс, роль наследственности и среды в формировании фенотипического полиморфизма человека по нормальным признакам, а также в возникновении болезней, особенно с наследственной предрасположенностью.
Основой для выяснения генетической структуры популяции является закон генетического paвновесия Харди-Вайнберга. Отражает закономерность, в соответствии с которой при определенных условиях соотношение аллелей генов и генотипов в генофонде популяции сохраняется неизменным в ряду поколений.
Математическим выражением закона Харди-Вайнберга служит формула:
(pA + ga)2 = 1,
где р и g – частоты встречаемости аллелей А и а соответствующего гена. Анализ частот встречаемости разных признаков в популяции в случае их соответствия закону Харди-Вайнберга позволяет утверждать, что признаки обусловлены разными аллелями одного гена.

Слайд 66БИОХИМИЧЕСКОЕ ИССЛЕДОВАНИЕ
Основано на том, что при мутациях ферментов и транспортных
белков, их можно выявлять по накоплению патологических метаболитов.
Субстраты ферментных
реакций или транспортируемые через мембрану вещества (аминокислоты, сахара, глюкозаминоглюканы, кетокислоты) накапливаются в моче и сыворотке крови.
Например, при недостатке фенилаланингидроксилазы в крови и тканях накапливается фенилаланин и продукты его переаминирования – фенилпировиноградная и фенилуксусная кислота. Обе кислоты токсически воздействует на мозг ребенка.
Слайд 67Показаниями к биохимическим исследованиям служат:
1. Неясные и затяжные формы желтух
у детей в период новорожденности и первого года жизни.
2. Хроническое
расстройство пищеварения неинфекционной природы (диарея, рвота, гепатомегалия, трудности с кормлением).
3. Аномалии развития скелета не рахитической природы.
4. Нарушение речи, органов зрения, слуха.
5. Дефекты поведения, двигательная расторможенность, мышечная гипотония.
6. Гиперрефлексия, судорожный синдром.
7. Умственная отсталость.
8. Необычные волосы, ногти, лицо.
9. Стойкие изменения в моче – протеинурия, гематурия, лейкоцитурия, фосфатурия, глюклзурия.
Данные методы применяют при подозрении на наследственные болезни обмена веществ. Они могут быть многоэтапными (скрининговые) или сразу строго направленными на определенную патологию.
В практике здравоохранения Российской Федерации используется двухэтапная программа:
1. Просеивающая программа (массовый и селективный скрининг).
2. Методы, подтверждающие диагноз.
В нашей стране осуществляется диагностика фенилкетонурии, врожденного гипотиреоза, адреногенитального синдрома, врожденных аномалий развития нервной трубки и болезни Дауна.

Слайд 68МОЛЕКУЛЯРНО-ГЕНЕТИЧЕСКОЕ ИССЛЕДОВАНИЕ
Позволяет диагностировать наследственные болезни на уровне генетических дефектов.
Прямая
диагностика мутаций включает несколько методов:
определение нуклеотидной последовательности (секвенирование)
в генах или их фрагментах;
выявление нарушения места рестрикции; аллельспецифическую гибридизацию с синтетическими олигонуклеотидными зондами;
химическое и ферментативное расщепление ДНК в местах неправильного сшивания оснований;
регистрацию изменения электрофоретической подвижности мутантных молекул ДНК;
трансляцию белкового продукта in vitro,
метод нуклеотидной последовательности
Слайд 69Спектр наследственных болезней, выявляемых с помощью методов ДНК-диагностики в Российской
Федерации (по данным П. В. Новикова и О. В. Евграфова)
Слайд 71ИММУНОГЕНЕТИЧЕСКОЕ ИССЛЕДОВАНИЕ
Методы позволяют выявлять наследственные (первичные) иммунодефициты, оценить совместимость матери
и плода, определить прогноз при болезнях с наследственным предрасположением. Показаниями
к проведению могут служить следующие так называемые «настораживающие признаки»:
1. Частые заболевания отитом (не менее 6-8 раз в течение одного года).
2. Несколько подтвржденных серьезных синуситов (не менее 4-6 раз в течение одного года).
3. Более двух подтвержденных пневмоний в течение одного года.
4. Повторные глубокие абсцессы кожи или внутренних органов.
5. Потребность в длительной терапии антибиотиками для купирования инфекции (до 2 мес. и более).
6. Потребность во внтуривенном введении антибиотика для купирования инфекции.
7. Не менее двух глубоких инфекций, таких как менингит, остеомиелит, сепсис.
8. Отставание грудного ребенка в росте и массе.
9. Наличие в семье первичных иммунодефицитов, факты ранних смертей от тяжелых инфекций или наличие одного из перечисленных симптомов.
10. Персистирующая молочница или грибковое поражение кожи в возрасте старше 1 года.
Изучение иммунного статуса при иммунодефицитах должно включать изучение количества и функциональной активности основных компонентов иммунной системы (фагоцитарная система, система комплемента, Т- и В-системы иммунитета). Методы, применяемые для оценки функционирования этих систем, условно разделены на тесты 1-го и 2-го уровней. Тесты 1-го уровня являются ориентировочными и направлены на выявление грубых дефектов в иммунной системе. Тесты 2-го уровня являются функциональными и направлены на обнаружение конкретной «поломки» в иммунной системе

Слайд 72Диагностика наследственных болезней бывает первичной и вторичной, суть которой не
допустить рождения больного ребенка. Направления первичной диагностики включают:
1) планирование
семьи: проспективное (до рождения ребенка) и ретроспективное консультирование (после рождения больного ребенка);
2) пренатальная диагностика с элиминацией патологических эмбрионов и плодов.
Вторичная диагностика предусматривает коррекцию болезни после рождения (нормокопирование) - формирование здорового фенотипа при патологическом генотипе.
Слайд 73Показаниями к пренатальной диагностике являются:
1. Возраст женщины старше 35-37 лет,
мужчины старше 45 лет.
2. Рождение ребенка с хромосомной или генной
болезнью.
3. Наличие в семье точно установленного наследственного заболевания.
4. Носительство матерью гена Х-сцепленного рецессивного заболевания.
5. Наличие в анамнезе у беременных спонтанных абортов в ранние сроки беременности, мертворождений, рождение детей с пороками развития и хромосомной патологией.
6. Беременные из зоны повышенного радиационного фона.
7. Наличием кровно-родственных браков.
8. Наличие сходных случаев заболевания в семье и среди отдаленных кровных родственников.
9. Рецидивирующее, хроническое, длительно неподдающееся лечению течение заболевания.
10. Наличие редко встречающихся специфических симптомов или их сочетание.
11. Множественное поражение органов и систем органов.
12. Наличие более 5 врожденных морфогенетических вариантов, называемых также микроаномалиями развития.
13. Врожденный характер заболевания.
Слайд 74В настоящее время применяют непрямые и прямые методы пренатальной диагностики.
При непрямых методах исследуют беременную женщину (например, исследование сыворотки крови
на альфа-фетопротеин).
При прямых методах исследуют плод.
Методы пренатальной диагностики бывают инвазивные и неинвазивные.
К инвазивным относятся - преимплантационная диагностика, которая осуществляется на 1-2 клетках, взытых на ранних стадиях дробления (8-18 клеток) от оплодотворенной in vitro яйцеклетки; хорионбиопсия (взятие эпителия ворсинок хориона); плацентобиопсия; амниоцентез (получение амниотической жидкости и клеток плода); кордоцентез (забор крови из пуповины); биопсия кожи, печени, мышц плода; везикоцентез (прокол стенки мочевого пузыря плода для получения его мочи); фетоскопия (осмотр плода фиброоптическим эндоскопом, введенным в амниотическую полость через брюшную стенку матки, метод позволяет осмотреть плод, пуповину, плаценту, произвести биопсию).
К неинвазивным относятся – ультразвуковое исследование (УЗИ), скрининговое исследование сыворотки крови беременной женщины (определение альфа-фетопротеина (АФП), хорионического гонадотропина, неконъюгированного эстриола, ацетилхолинэстеразы)

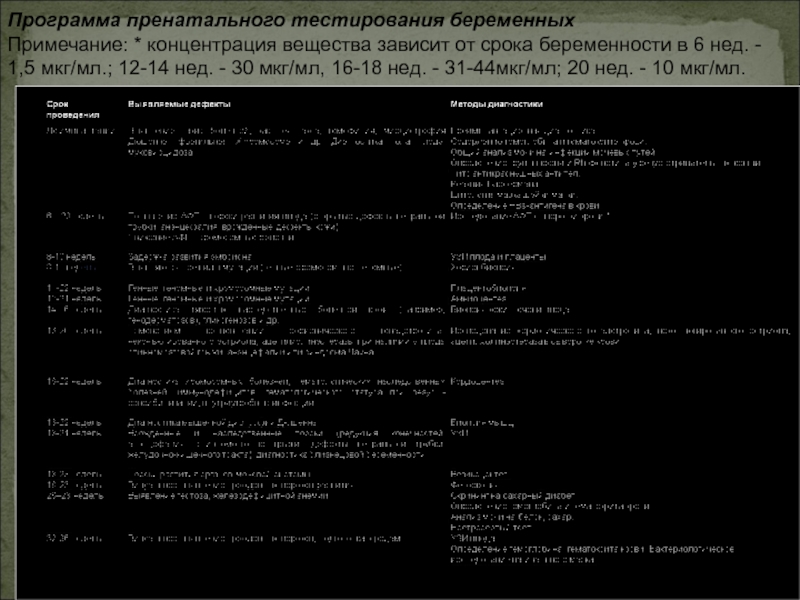
Слайд 75Программа пренатального тестирования беременных
Примечание: * концентрация вещества зависит от срока
беременности в 6 нед. - 1,5 мкг/мл.; 12-14 нед. -
30 мкг/мл, 16-18 нед. - 31-44мкг/мл; 20 нед. - 10 мкг/мл.