Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Микробиология иерсиниозы
Содержание
- 1. Микробиология иерсиниозы
- 2. Особо опасные инфекции (ООИ) — условная
- 3. В настоящее время понятия «ООИ» в
- 4. Список таких заболеваний сейчас значительно расширен.
- 5. 2 -«болезни, любое событие с которыми
- 6. В настоящее время сфера применения новых
- 7. Чума возникла на Земле раньше, чем
- 8. Эпидемии чумы известны с III века
- 9. вторая пандемия чумы в XIV-XV веках
- 10. остров Лазаретто (15-16 вв)Остров Лаззаретто-Веккьо - первая
- 11. Слайд 11
- 12. «Thetriumph of death» («Триумф смерти»), 1562Питер Брейгель Старший
- 13. Возбудитель чумы обнаружили Г.Н. Минх (1878)
- 14. Большой вклад в изучение эпидемиологии чумы
- 15. В 2004-2009 г.г. по данным ВОЗ
- 16. Сегодня распространение чумы в мире совпадает
- 17. В России с 2001 по 2006
- 18. На территории Российской Федерации в 2011 году
- 19. Прогноз эпизоотической активности природных очагов чумы Российской
- 20. ПрогнозВ условиях современной терапии смертность при
- 21. электронная микроскопия блохи, переносчика чумы xenopsylla
- 22. Чума́ (лат. pestis) — острое природно-очаговое
- 23. Возбудитель чумы Возбудитель чумы в гное из бубона EnterobacteriaceaeYersinia Yersinia pestis Y. рseudotuberculosisY. enterocolitica
- 24. Yersinia pestis scanning electron micrograph
- 25. Y. pestis (палочка Китазато) — овоидная
- 26. Аэроб или факультативный анаэроб гетеротроф (не
- 27. на жидких питательных средах - поверхностная
- 28. обладает слабо выраженной биохимической активностью, ферментирует
- 29. 16 антигенов: 11 – общих с
- 30. Активатор плазминогена чумы — протеаза, активирующая
- 31. Факторы патогенностиАдгезии (yadA)гиалуронидазаФибринолизинПлазмокоагулазаТоксическая субстанция со свойствами
- 32. Биологические св-ва МКО, облегчающие формирование инфекционного
- 33. РезистентностьВ мокроте сохраняется до 10 сут,
- 34. Пути передачи трансмиссивный (переносчик - блохи) контактный (снятие шкурки, разделка туши) пероральный воздушно-капельный
- 35. Чума — антропозооноз, поражающий грызунов (основной
- 36. Механизм развития чумы включает три стадии:Проникшие
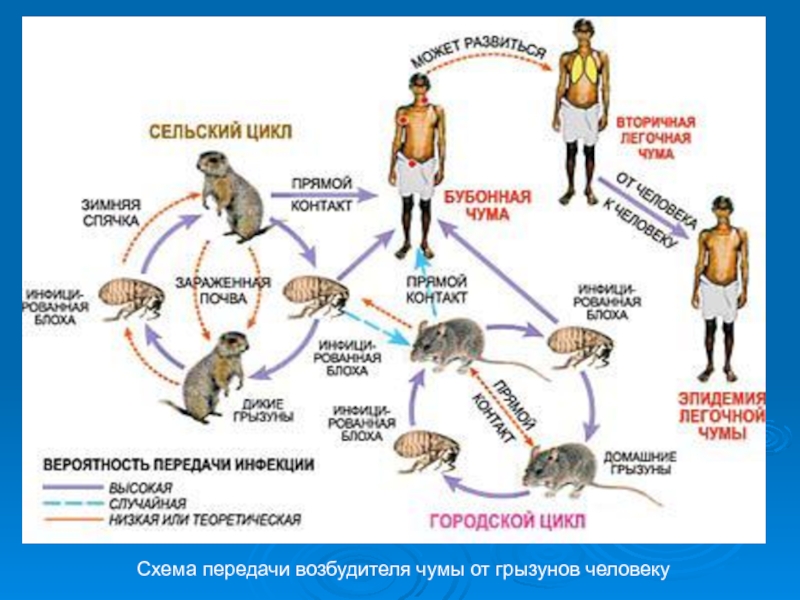
- 37. Схема передачи возбудителя чумы от грызунов человеку
- 38. инкубационный период - 1-2 - 3-6
- 39. Патогенетически различают первичные (всегда связаны с
- 40. Клинические формы Контакт, укус блохи –
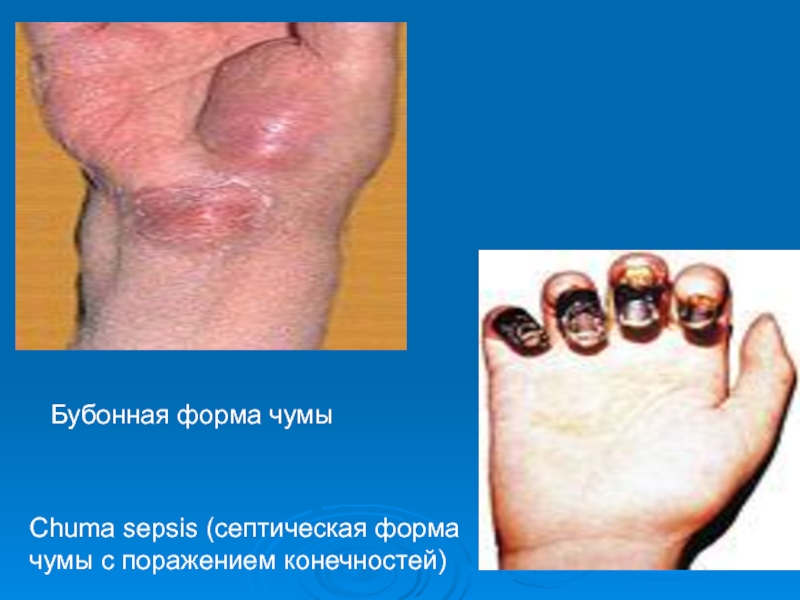
- 41. Бубонная форма чумыChuma sepsis (септическая форма чумы с поражением конечностей)
- 42. Клиническое течение чумы отличается разнообразием форм.
- 43. Характерным признаком бубонной формы является резко
- 44. Вторично-септическая форма чумы - следствие бубонной
- 45. Появляется кашель вначале сухой, чуть позднее
- 46. Материал для исследований отделяемое бубонов содержимое
- 47. Методы исследования бактериоскопический бактериологический серологический аллергический биологический
- 48. Биохимическую идентификацию возбудителя чумы проводят в
- 49. Антигены чумной палочки идентифицируют в РА,
- 50. Биологическая проба проводят при сильной контаминации
- 51. Аллергическая проба при чумеДля ретроспективной диагностики
- 52. Иммунитет- Стойкий антимикробный- Клеточный АТ вырабатываются
- 53. ПрофилактикаДля надзора за эндемичными очагами чумы
- 54. специфическая иммунопрофилактика живая аттенуированная вакцина из
- 55. ЛечениеПри диссеминированных и системных заболеваниях необходимо
- 56. Слайд 56
- 57. Слайд 57
- 58. подвижные овоидные Гр-палочки, в молодых культурах
- 59. На твёрдых питательных средах формируют мутные
- 60. Возбудитель псевдотуберкулёза по структуре О-антигена разделяют
- 61. клиника Энтероколиты воспаление брыжеечных лимфатических узлов
- 62. Материал для исследованийИспражненияЖелчьСуставная жидкостьКровьпродукты питания вода
- 63. Материал засевают на среду Эндо (Y.
- 64. Иерсиниоз — инфекционное заболевание, сопровождающееся диареей,
- 65. Возбудитель иерсиниоза (Yersinia enterocolitica) широко распространён
- 66. Инфицирование человека происходит фекально-оральным путём. Точные
- 67. Yersinia enterocolitica - полиморфные, чаще овоидные
- 68. Температурный оптимум 28-30 °С; оптимум рН
- 69. О-антиген (эндотоксин), похожий на антигены многих
- 70. Факторы вирулентности - адгезины и инвазины,
- 71. Бактерии проникают в слизистую оболочку тонкой
- 72. доминирует симптоматика гастроэнтерита (энтероколит с диареей,
- 73. материал для исследований кровь, испражнения,
- 74. Для выявления AT в сыворотке
- 75. Слайд 75
- 76. Защитный костюм
- 77. Защитный костюм
- 78. antibiotic treatment
- 79. Определение чувствительности к антибиотикам
- 80. вакцина
- 81. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1
ГБОУ ВПО «ТИХООКЕАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ» МЗ РФ
Кафедра микробиологии
и вирусологии
д.м.н., проф. Шаркова В. А.Слайд 2
Особо опасные инфекции (ООИ) — условная группа инфекционных заболеваний,
представляющих исключительную эпидемическую опасность
Перечень и меры профилактики распространения ООИ
закреплены в Международных медико-санитарных правилах (ММСП), принятых 22-й сессией Всемирной ассамблеи здравоохранения ВОЗ 26 июля 1969 г.Слайд 3
В настоящее время понятия «ООИ» в мировой медицине не
существует
Этот термин продолжает быть только в странах СНГ
В мировой
практике ООИ — это «инфекционные заболевания, которые вошли в перечень событий, что могут являть собой чрезвычайную ситуацию в системе охраны здоровья в международном масштабе»
Слайд 4
Список таких заболеваний сейчас значительно расширен. Согласно приложению №
2 ММСП-2005 он разделен на две группы
«болезни, которые являются необычными
и могут оказать серьёзное влияние на здоровье населения»: оспа, полиомиелит, вызванный диким полиовирусом, человеческий грипп, вызванный новым подтипом, тяжелый острый респираторный синдром (ТОРС) или (SARS)
Слайд 5
2 -«болезни, любое событие с которыми всегда оценивается как
опасное, поскольку эти инфекции обнаружили способность оказывать серьёзное влияние на
здоровье населения и быстро распространяться в международных масштабах»: холера, легочная форма чумы, желтая лихорадка, геморрагические лихорадки — лихорадка Ласса, Марбург, Эбола, лихорадка Западного НилаСюда же ММСП-2005 относят инфекционные болезни, «которые представляют особую национальную и региональную проблему», например лихорадку Денге (для стран тропического пояса), лихорадку Рифт-Валли, менингококковую инфекцию (в странах Центральной Африки)
В России к ООИ также причисляются сибирская язва и туляремия
Слайд 6
В настоящее время сфера применения новых ММСП-2005 г. больше
не ограничивается инфекционными болезнями, а охватывает «болезнь или медицинское состояние,
независимо от происхождения или источника, которое представляет или может представлять риск нанесения людям значительного вреда»
Слайд 7
Чума возникла на Земле раньше, чем появился человек, и
ее истоки в далеких геологических эпохах, когда начали появляться прапращуры
современных грызунов,— около 50 млн лет назад. Тогда уже существовали роды блох, сходные с ныне живущими, как подтверждают остатки ископаемых насекомых в янтареПрародина чумы — бескрайние степи и пустыни Центральной Азии, среднеафриканские саванны и североафриканские пустыни и полупустыни, где эта болезнь развивалась и поддерживалась среди местных видов песчанок, сурков и сусликов
Слайд 8
Эпидемии чумы известны с III века до н.э., иногда
они приобретали характер пандемий
Первая достоверная пандемия 527-565 гг. («юстинианова чума»),
начавшаяся в Египте и Эфиопии, привела к огромным потерям среди населения Восточной Римской империиСлайд 9
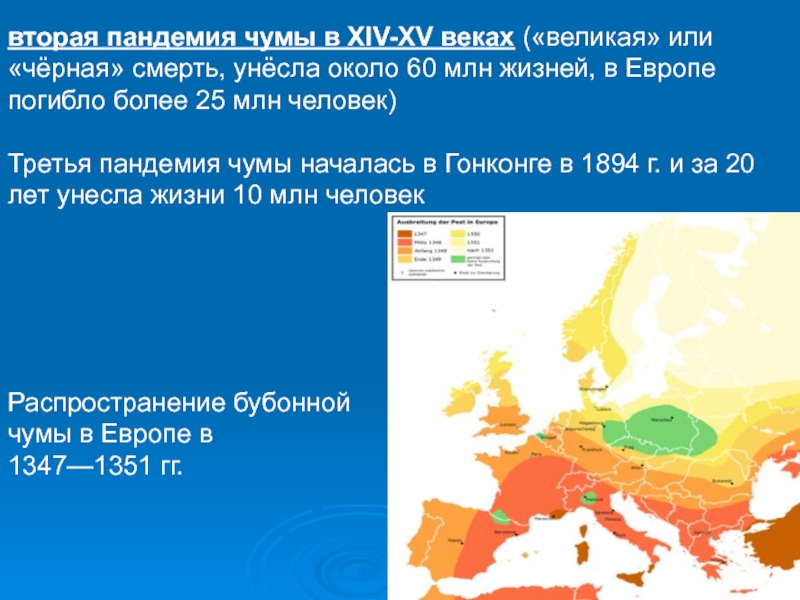
вторая пандемия чумы в XIV-XV веках («великая» или «чёрная»
смерть, унёсла около 60 млн жизней, в Европе погибло более
25 млн человек)Третья пандемия чумы началась в Гонконге в 1894 г. и за 20 лет унесла жизни 10 млн человек
Распространение бубонной чумы в Европе в 1347—1351 гг.
Слайд 10остров Лазаретто (15-16 вв)
Остров Лаззаретто-Веккьо - первая в мире лечебница
для карантина. Венецианский лазарет начал работу во время вспышки чумы
1485 года (жертвами инфекции оказалось множество людей, среди них глава Венецианской республики, 72-й дож Джованни Мочениго (1408 - 14 сентября 1485 гг.).Слайд 13
Возбудитель чумы обнаружили Г.Н. Минх (1878) и независимо А.
Иерсен и Ш. Китазато (1894)
описали морфологию
выделили чистую культуру
воспроизвели инфекционный процессСлайд 14
Большой вклад в изучение эпидемиологии чумы внесли исследования
Д.С. Самойлович (первые в Европе)
В.И. Исаев и Н.Н. Клодницкий
И.И. Мечников, руководившего работой противочумных отрядов в Астраханской губернии (1911) (впервые дал сводную характеристику чумы – 1897г.)И.А. Лебединский,
Н.Ф. Гамалея, Заболотный
Владимир Хавкин - создатель первой
вакцины против чумы и холеры
Слайд 15
В 2004-2009 г.г. по данным ВОЗ в 16
странах мира зарегистрировано 12548 случаев заболевания чумой, включая 845 летальных
из 16 стран Африки, Азии и АмерикиНаиболее интенсивные вспышки были зарегистрированы в странах Африканского континента, в Демократической Республике Конго и Мадагаскаре
В течение 2010 г. о случаях заболевания чумой сообщали из Китая, Мьянмы, Перу, Боливии и США
В 2011 году на севере Мадагаскара отмечена крупная вспышка легочной формы чумы, в результате которой умерло 16 человек, точное число больных неизвестно
Слайд 16
Сегодня распространение чумы в мире совпадает с географическим распределением
ее природных очагов
В Российской Федерации наиболее активные природные очаги расположены
на территориях Республик Алтай, Дагестан, Кабардино-Балкарской, Калмыкия, Карачаево-Черкесской, Тыва. При этом на территории России случаи заболевания чумой не зафиксированы с 1979 года, хотя ежегодно на территории природных очагов (общей площадью более 253 тыс. кв. км) в риске заражения находятся свыше 20 тыс. человек.
В то же время в 2001—2003 годах в Республике Казахстан зарегистрированы 7 случаев заболевания чумой (с одним летальным исходом), в Монголии — 23 (3 летальных исхода), в Китае в 2001—2002 годах заболело 109 человек (9 летальных исходов).
Слайд 17
В России с 2001 по 2006 год зафиксировано 752
штамма возбудителя чумы
Особую тревогу вызывает отсутствие систематического наблюдения за активностью
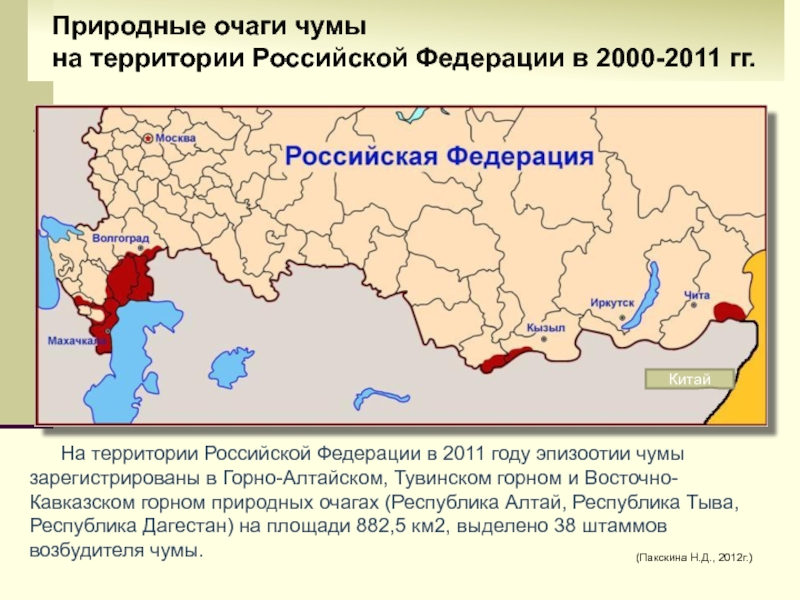
очагов, расположенных в Ингушской и Чеченской РеспубликахСлайд 18На территории Российской Федерации в 2011 году эпизоотии чумы зарегистрированы
в Горно-Алтайском, Тувинском горном и Восточно-Кавказском горном природных очагах (Республика
Алтай, Республика Тыва, Республика Дагестан) на площади 882,5 км2, выделено 38 штаммов возбудителя чумы.Природные очаги чумы
на территории Российской Федерации в 2000-2011 гг.
(Пакскина Н.Д., 2012г.)
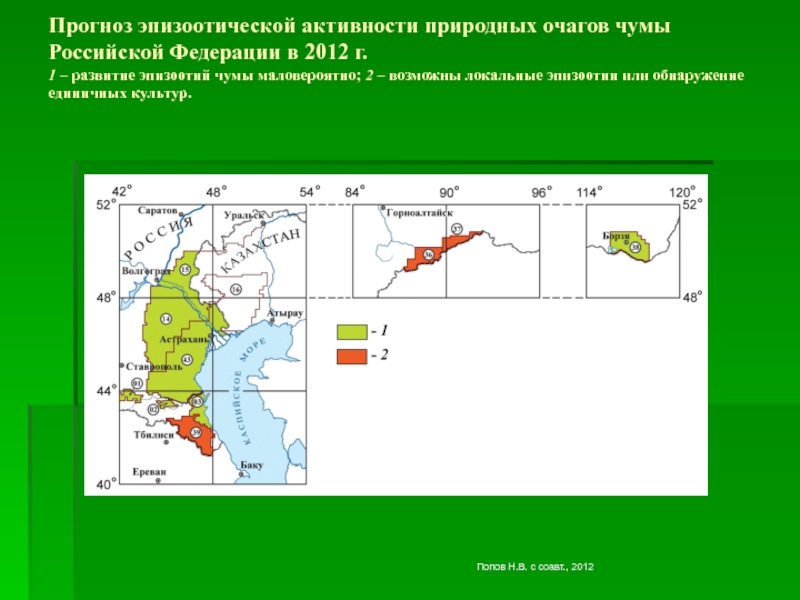
Слайд 19Прогноз эпизоотической активности природных очагов чумы Российской Федерации в 2012
г. 1 – развитие эпизоотий чумы маловероятно; 2 – возможны локальные
эпизоотии или обнаружение единичных культур.Попов Н.В. с соавт., 2012
Слайд 20
Прогноз
В условиях современной терапии смертность при бубонной форме не
превышает 5-10 %, но и при других формах процент выздоровлений
достаточно высок, если лечение начато рано. В ряде случаев возможна быстротечная септическая форма заболевания, слабо поддающаяся прижизненной диагностике и лечению («молниеносная форма чумы»)Слайд 21 электронная микроскопия
блохи, переносчика чумы
xenopsylla cheopis –
основной
переносчик чумы
Керамическая бомба с колонией блох, зараженных Y.pestis
Слайд 22
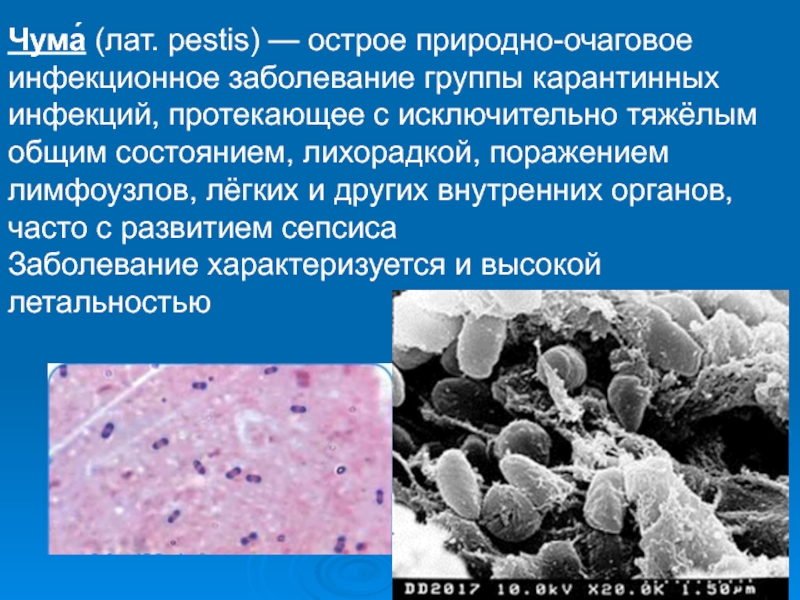
Чума́ (лат. pestis) — острое природно-очаговое инфекционное заболевание группы
карантинных инфекций, протекающее с исключительно тяжёлым общим состоянием, лихорадкой, поражением
лимфоузлов, лёгких и других внутренних органов, часто с развитием сепсисаЗаболевание характеризуется и высокой летальностью
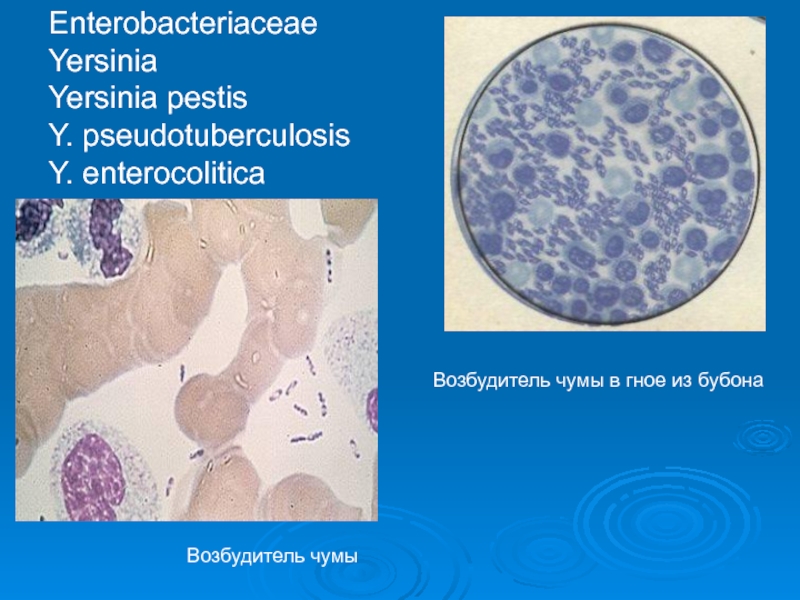
Слайд 23Возбудитель чумы
Возбудитель чумы в гное из бубона
Enterobacteriaceae
Yersinia
Yersinia
pestis
Y. рseudotuberculosis
Y. enterocolitica
Слайд 25
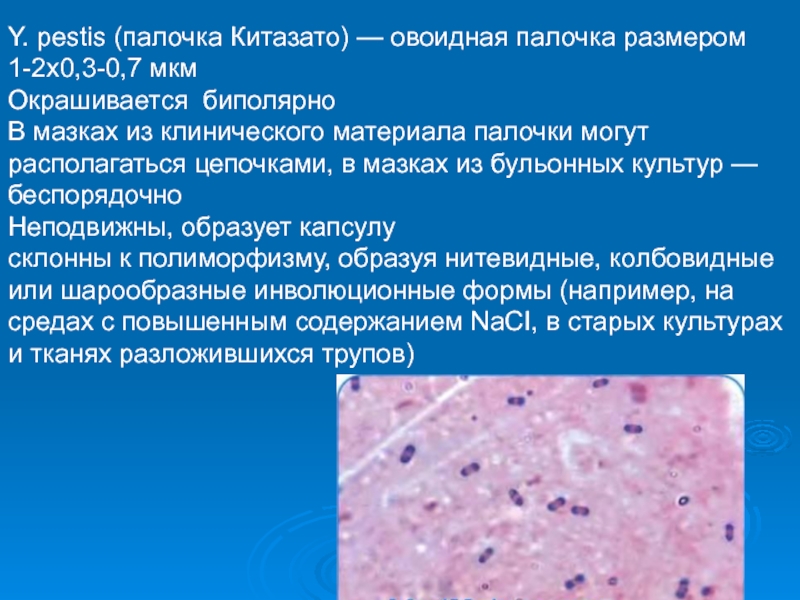
Y. pestis (палочка Китазато) — овоидная палочка размером 1-2x0,3-0,7
мкм
Окрашивается биполярно
В мазках из клинического материала палочки могут располагаться цепочками,
в мазках из бульонных культур — беспорядочноНеподвижны, образует капсулу
склонны к полиморфизму, образуя нитевидные, колбовидные или шарообразные инволюционные формы (например, на средах с повышенным содержанием NaCI, в старых культурах и тканях разложившихся трупов)
Слайд 26
Аэроб или факультативный анаэроб
гетеротроф (не требователен к
питат средам)
стимуляторы роста: сульфит натрия, гемолизированная кровь, экстракты бактерий
(сарцины), антифаговая сывороткаПсихрофил (28-30град С – 0-45)
8-10-20 час
R-форма вирулентна
диссоциируют в S-форму (бактериофаг)
способны образовывать тёмный пигмент и обесцвечивать красители (например, метиленовый синий)
Слайд 27
на жидких питательных средах - поверхностная пленка, придонный
осадок, оставляя среду прозрачной, «сталактитовый рост»
сероватые слизистые колонии
На
твердых питательных средах первоначальный рост чумного микроба имеет вид прозрачных мелких «кружевных платочков», в центре которых в последующем появляется уплотнение постоянно разрастающееся и образующее выпуклый зернистый центр колонииэлективные среды – казеиновые и гидролизаты кровяных сгустков
Слайд 28
обладает слабо выраженной биохимической активностью,
ферментирует маннит,
глюкозу, мальтозу с образованием кислоты без газа
разлагающие глицерин –
континентальная чуманеразлагающие глицерин – океаническая (портовая) чума
не разжижают желатин
Не выделяют индол
не свертывают молоко
продуцируют сероводород
Слайд 29
16 антигенов:
11 – общих с Y. pseudotuberculosis
общие гетерогенные с Er O(I) группы крови чел.
общие гетерогенные
с эшерихиями, шигелламиО-антиген (эндотоксин) (Липополисахаридно-белковые комплексы О-антигена классифицируют на основе химических и антигенных характеристик на S и R, последние — общие для Y pseudotuberculosis и Y. pestis.
Фракция 1 (F1-антиген чумы) представлена поверхностным пликопротеиновым антигеном (капсульным антигеном) - предохраняет бактерии от поглощения фагоцитами и, не оказывая токсического действия, проявляет иммуногенные свойства
Слайд 30
Активатор плазминогена чумы — протеаза, активирующая лизис фибриновых
сгустков, препятствующих диссеминированию возбудителя, и инактивирующая С3b и С5а компоненты
комплементаV/W (Vi)-антиген чумы состоит из белка (V-фракции) и липопротеина (W-фракции) - проявляет антифагоцитарные свойства и способствует внутриклеточному размножению бактерий (штаммы, содержащие только V/W-Ar, вирулентны для мышей)
Мышиный токсин чумы — антагонист адренергических рецепторов (белок, локализован внутриклеточно; LD50 для мышей менее 1 мг (также токсичен для крыс), вызывает шок и смерть лабораторных животных)
Слайд 31
Факторы патогенности
Адгезии (yadA)
гиалуронидаза
Фибринолизин
Плазмокоагулаза
Токсическая субстанция со свойствами эндо-экзотоксина (выражена гемолитическая
активность)
аггрессиноподобная субстанция – цитотоксичность, ингибиция миграции и активности фагоцитов
(yop)выделяет бактериоцины (пестинины), обладающие иммуногенными свойствами)
Слайд 32
Биологические св-ва МКО, облегчающие формирование инфекционного процесса
способность к
аэробному и анаэробному дыханию
нетребовательность к питательным средам
Слайд 33
Резистентность
В мокроте сохраняется до 10 сут, на одежде и
белье — несколько недель, в трупах при низкой температуре окружающей
среды — неопределённо долгое времяВозбудитель быстро погибает под воздействием солнца, высыхания и высоких температур, при 60 °С погибает за 1 ч, при кипячении — за несколько минут
- чувствительны к действию дезинфектантов
Слайд 34
Пути передачи
трансмиссивный (переносчик - блохи)
контактный (снятие шкурки,
разделка туши)
пероральный
воздушно-капельный
Слайд 35
Чума — антропозооноз, поражающий грызунов (основной природный резервуар) и
проявляющийся спорадическими вспышками или эпидемиями (эпизоотиями). Человеку передаётся через блох,
а также контактным, алиментарным и аспирационным путями; опасны вторично загрязнённые объекты и трупыинфицирование блохи происходит при её питании кровью грызунов в период бактериемии, предшествующей гибели животных
Чумная палочка внедряется в организм в месте укуса блохи
Ни один Аг или токсин, синтезируемый Y. pestis, в отдельности не в состоянии вызвать заболевание
Слайд 36
Механизм развития чумы включает три стадии:
Проникшие бактерии чумы активно
поглощаются фагоцитами, однако, фагоцитарные реакции носят незавершённый характер и способствуют
дальнейшему распространению возбудителя. Одновременно1. Лимфогенный перенос возбудителя чумы от места проникновения до лимфатических барьеров (лимфаденит)
2. Распространение возбудителя из лимфатических узлов в кровоток (бактериемия)
3. Распространение чумы до забарьерных клеточных систем (генерализованная септицемия).
Слайд 38
инкубационный период - 1-2 - 3-6 сут
внезапный подъём температуры
тела, головная боль и чувство разбитости, налёт на языке («натёртый
мелом язык»), его отёк, в результате чего речь становится невнятной. Тяжелая интоксикация. В тяжёлых случаях возникают галлюцинацииЧумная палочка не вызывает воспалительных изменений кожи и мигрирует в ближайший лимфатический узел, где развивается серозно-геморрагическое воспаление, формируется резко болезненный бубон
Слайд 39
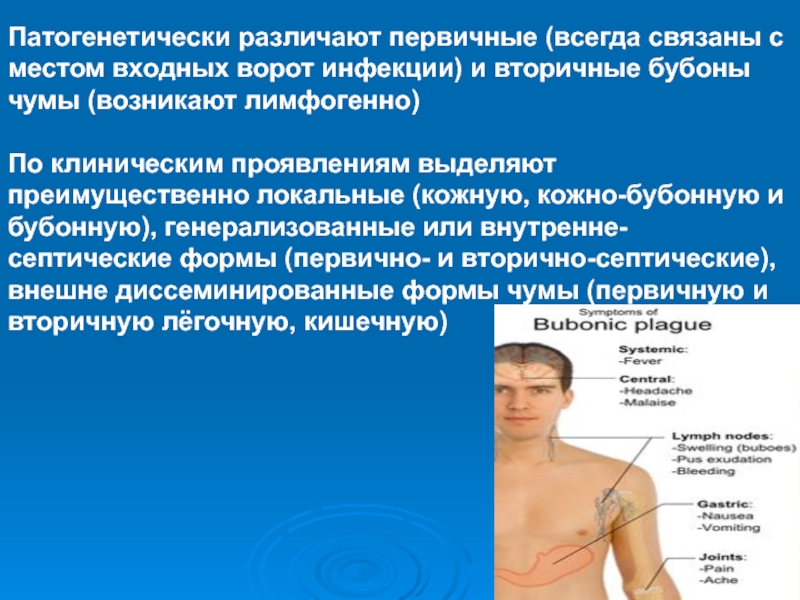
Патогенетически различают первичные (всегда связаны с местом входных ворот
инфекции) и вторичные бубоны чумы (возникают лимфогенно)
По клиническим проявлениям выделяют
преимущественно локальные (кожную, кожно-бубонную и бубонную), генерализованные или внутренне-септические формы (первично- и вторично-септические), внешне диссеминированные формы чумы (первичную и вторичную лёгочную, кишечную)Слайд 40
Клинические формы
Контакт, укус блохи – кожная, бубонная
ч/з
рот – кишечная форма
Воздушно-капельно – первично-легочная
Слайд 42
Клиническое течение чумы отличается разнообразием форм. Помимо общетоксического синдрома,
вскоре на первый план выходят те или иные ее проявления.
----Общепринятой классификацией чумы является предложенная Г.П. Рудневым, большим знатоком этой инфекции. Он рассматривает клинику чумы с патогенетических и эпидемиологических позиций, что важно для практики ведения больных чумой и проведения противоэпидемических мероприятий.Различают локальные формы-кожную, кожно-бубонную, бубонную и генерализованные: внутренне диссеминированные (первично-септическая) и внешне диссеминированные (первично-легочная, вторично-легочная, кишечная).
При кожной форме чумы местные изменения проходят стадии пятна, папулы, везикулы, пустулы, язвы. Язва отличается болезненностью, медленным заживлением с образованием рубца.
Слайд 43
Характерным признаком бубонной формы является резко болезненный, -----увеличенный лимфоузел.
Наиболее часто при чуме увеличиваются паховые, подмышечные и шейные лимфоузлы;
они болезненны, локальная боль появляется в месте будущего бубона гораздо раньше, чем сам бубон. Над бубоном появляется отечность, увеличенные лимфоузлы сливаются в единый конгломерат, резко болезненный. Изменения окраски кожи, приобретающей красный лоснящийся цвет, появляются позднее самого бубона. Бубоны раньше, как правило, самостоятельно вскрывались с образованием втянутого рубца или склерозировались.При современном лечении они могут рассасываться. В прошлом летальность даже при бубонной форме чумы достигала 40-90%. В настоящее время при антибиотикотерапии все больные выздоравливают.
Первично-септическая форма чумы встречается редко (1-3% случаев). Изменений на коже при этой форме болезни не наблюдается. Болезнь сразу приобретает картину остроразвивающегося сепсиса с быстрым нарастанием токсикоза, возможным появлением менингоэн-цефалита, развитием ТГС и скоротечным течением (1-3 дня). Заканчивается летальным исходом при явлениях ИТШ и комы.
Слайд 44
Вторично-септическая форма чумы - следствие бубонной формы, которая быстро
переходит в сепсис с прогрессирующей бактериемией и интоксикацией. ----- Для
нее характерны вторичные очаги инфекции с выраженными проявлениями геморрагической септицемии. Эта форма отличается большой тяжестью течения и частыми летальными исходами.Первично-легочная форма чумы возникает при общении с больным вторично-легочной чумой. Новые заражения первично-легочной чумой возникают при неосуществлении профилактических мер (запоздалая изоляция всех подозрительных на чуму больных). При этой форме инкубационный период сокращается до 1-3 дней, т.к. происходит вдыхание «облака чумной заразы» и массивное попадание микробов в легкие Болезнь начинается внезапно, с резкого озноба и крутого подъема температуры до высоких цифр; больных беспокоят сильная головная боль, рвота.
В первые сутки, иногда с захватом половины вторых суток, болезнь развивается без четких проявлений пневмонии. И только позже возникают характерная «режущая» боль в груди, сердцебиение, учащение пульса, одышка, боязнь глубокого вдоха, бред.
Слайд 45
Появляется кашель вначале сухой, чуть позднее с обильной мокротой,
----которая приобретает пенистый вид, становится жидкой, ржавой, иногда с примесью
крови (в отличие от мокроты сибиреязвенных септических больных, кровь в которой легко свертывается). Физикальные данные скудные: дыхание ослаблено, редкие влажные хрипы, крепитация. Боль в груди усиливается с каждым часом, т.к. в воспалительный процесс вовлекается плевра Смерть при отсутствии этиотропного лечения обычно наступает на 3-5-й день при явлениях нарастающей дыхательной недостаточности и отека легких.Клиника вторичной легочной чумы напоминает описанную картину поражения легких при первичной легочной чуме с той разницей, что ей предшествует развитие прогрессирующей бубонной формы, когда возникает гематогенная генерализация инфекции.
Слайд 46
Материал для исследований
отделяемое бубонов
содержимое язв или других
кожных поражений
мокрота и слизь из зева
кровь
фекалии
СМЖУпаковка материала в контейнер
Слайд 47
Методы исследования
бактериоскопический
бактериологический
серологический
аллергический
биологический
Слайд 48
Биохимическую идентификацию возбудителя чумы проводят в соответствии с принципами,
применяемыми в отношении прочих энтеробактерий
В соответствии со способностью ферментировать глицерин
и углевод мелибиозу выделяют биовары antigua (+, -) выделяют в Центральной Азии и Центральной Африке,
medievalis (+, +) - в Средней Азии и Иране
orientalis (-, -) — повсеместно
Отечественная классификация выделяет подвиды
pestis (основной подвид)
altaica (алтайский подвид)
caucasica (кавказский подвид)
hissarica (гиссарский подвид)
udegeica (удэгейский подвид)
Слайд 49
Антигены чумной палочки идентифицируют в РА, РНГА, РП в
стандартных агаровых пластинках, ИФА и др
ускоренная диагностика
высокая специфичность
и вирулентность чумного бактериофага для чумной палочки позволяют применять его для идентификации чумы путём внесения в исследуемый материал — о положительном результате свидетельствует образование негативных колоний бактериофага либо увеличение титра бактериофага в средеСлайд 50
Биологическая проба
проводят при сильной контаминации материала посторонней
микрофлорой
морских свинок заражают накожно, подкожно или внутрибрюшинно
Выявление Аг
возбудителя в тканях погибших животных проводят при помощи РИГА, ИФА или с использованием AT, меченных флюоресцеинами. При снижении вирулентности или применении малой заражающей дозы перед заражением животным вводят глюкокортикоиды, что позволяет ослабить защитные силы и ускорить получение результатаСлайд 51
Аллергическая проба при чуме
Для ретроспективной диагностики чумы ставят кожные
пробы с пестином (белковый аллерген из культур возбудителя чумы)
Слайд 52
Иммунитет
- Стойкий антимикробный
- Клеточный АТ вырабатываются к поверхностному Vi
и капсульному АГ (наделены выраженной антифагоцитарной активностью)
Слайд 53
Профилактика
Для надзора за эндемичными очагами чумы и организации мероприятий
по предупреждению эпидемий создана специальная противочумная служба (включает сеть противочумных
институтов и станций)- контроль за эпизоотиями
- госпитализация подозрительных на заболевание
Госпитализация контактных на 10 дн.
дератизация, дезинсекция
карантин
Слайд 54
специфическая иммунопрофилактика
живая аттенуированная вакцина из штамма EV
Поствакцинальная
невосприимчивость сохраняется до года
Активную иммунизацию проводят в эндемических очагах,
а также охотникам и лицам, занимающимся отловом грызунов и работающим с возбудителемДля определения
напряжённости иммунитета
применяют кожные пробы с
пестином
Слайд 55
Лечение
При диссеминированных и системных
заболеваниях необходимо немедленное
применение антибактериальных
средств
При своевременно начатом лечении чумы антибиотики (стрептомицин, тетрациклин и др.)
снижают смертность при бубонной форме чумы почти на 100%, при лёгочной — на 5-10% При бубонной форме чумы антимикробную терапию можно дополнять введением антисыворотки, получаемой гипериммунизацией лошадей убитыми, а затем и живыми бактериями
Слайд 56
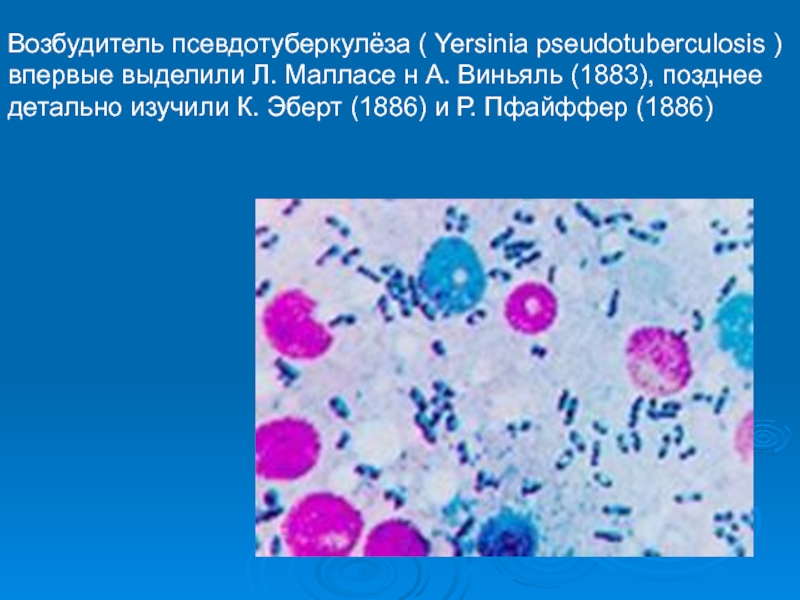
Возбудитель псевдотуберкулёза ( Yersinia pseudotuberculosis ) впервые выделили Л.
Малласе н А. Виньяль (1883), позднее детально изучили К. Эберт (1886) и Р. Пфайффер (1886)
Слайд 57
У человека микроорганизм вызывает острый брыжеечный аденит, или аппендицитоподобный
синдром, с патологоанатомическими изменениями, сходными с таковыми при туберкулёзе. У диких и домашних животных заболевание протекает с системными поражениями. Природный резервуар возбудителя псевдотуберкулёза — грызуны, олени, домашние животные и птицы. Псевдотуберкулез у человека наблюдают сравнительно редко.
Эпидемиология псевдотуберкулеза поражений аналогична таковой у прочих кишечных инфекций. Наиболее часто заражение происходит при употреблении продуктов, долго хранящихся в холодильнике.
Слайд 58
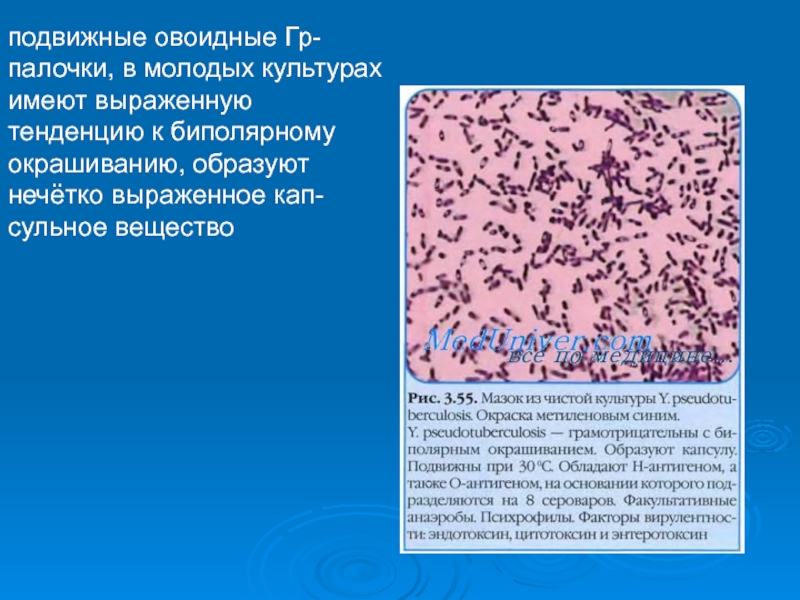
подвижные овоидные Гр-палочки, в молодых культурах имеют выраженную тенденцию
к биполярному окрашиванию, образуют нечётко выраженное кап-сульное вещество
Слайд 59
На твёрдых питательных средах формируют мутные колонии с серовато-желтоватым
оттенком в проходящем свете
При культивировании на среде Эндо (48 ч
при 37 °С) колонии остаются бесцветнымиЧасто образуются R-колонии — выпуклые, бугристые, с фестончатой зоной (или без неё), напоминающие колонии Y, pestis
При старении колонии увеличиваются в размере и полностью теряют прозрачность
На бульоне из R-колоний растут в виде хлопьевидного осадка, оставляя среду прозрачной
бактерии из S-колоний вызывают её равномерное помутнение
Температурный режим и оптимум рН аналогичны таковым у прочих иерсиний
Слайд 60
Возбудитель псевдотуберкулёза
по структуре О-антигена разделяют на 8 групп
(I-V1II) с 20 факторными антигенами (1-20)
по структуре Н-антигена —
на 5 групп (а-е)По соотношению О- и Н-антигена выделяют 13 сероваров и подсероваров (Ia, Ib, IIа, IIb, IIe, III, IVa, IVb, Va, Vb, VI. VII. VIII)
Слайд 61
клиника
Энтероколиты
воспаление брыжеечных лимфатических узлов в подвздошно-слепокишечной области,
часто не отличимое от аппендицита
Диссеминирование по кровеносным или лимфатическим
сосудам возникает редкоСлайд 62
Материал для исследований
Испражнения
Желчь
Суставная жидкость
Кровь
продукты питания
вода
Методы исследования
бактериоскопический
бактериологический
серологический – РПГА, РА, ИФА
Слайд 63
Материал засевают на среду Эндо (Y. pseudotuberculosis практически не
растёт на среде Плоскирева) и жидкую среду обогащения
После выделения чистой
культуры проводят определение основных биохимических свойствДополнительным признаком служит реакция Фогеса-Проскауэра, отрицательная при любых температурных режимах культивирования
Окончательное типирование возбудителя псевдотуберкулеза осуществляют
с помощью агглютинирующих
О- и Н-антисывороток
Слайд 64
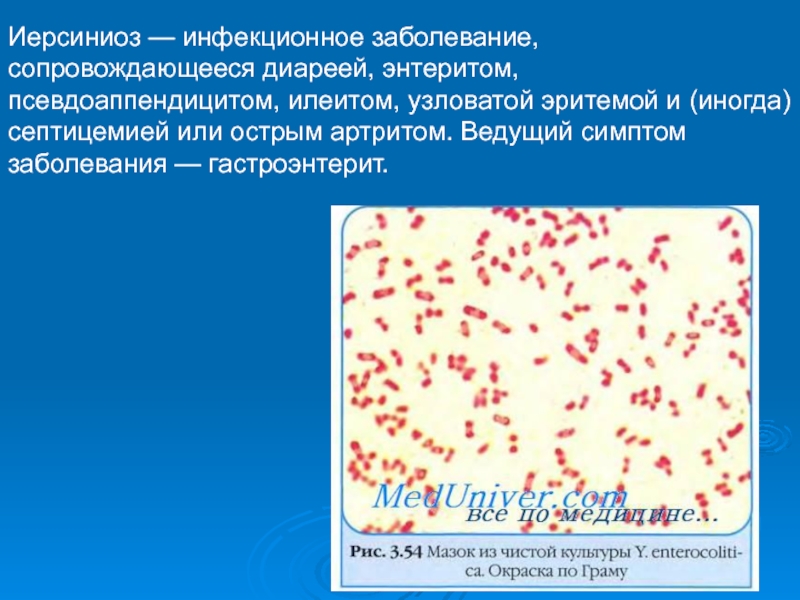
Иерсиниоз — инфекционное заболевание, сопровождающееся диареей, энтеритом, псевдоаппендицитом, илеитом,
узловатой эритемой и (иногда) септицемией или острым артритом. Ведущий симптом
заболевания — гастроэнтерит.Слайд 65
Возбудитель иерсиниоза (Yersinia enterocolitica) широко распространён в природе, его
выделяют от насекомых, моллюсков, ракообразных, птиц, грызунов, собак, кошек, домашних
сельскохозяйственных животных (основные хозяева).Возбудитель иерсиниоза (Yersinia enterocolitica) также обнаруживают в пресной воде.
В Европе основной резервуар возбудителя иерсиниоза — свиньи, поэтому большинство достоверных случаев заражения связано с употреблением плохо термически обработанной свинины.
Слайд 66
Инфицирование человека происходит фекально-оральным путём. Точные значения распространённости иерсиниоза
до сих пор не установлены, так как высеваемость возбудителя из
фекалий при гастроэнтеритах не превышает 3%.Подъём заболеваемости отмечают в осенне-зимний период.
Слайд 67
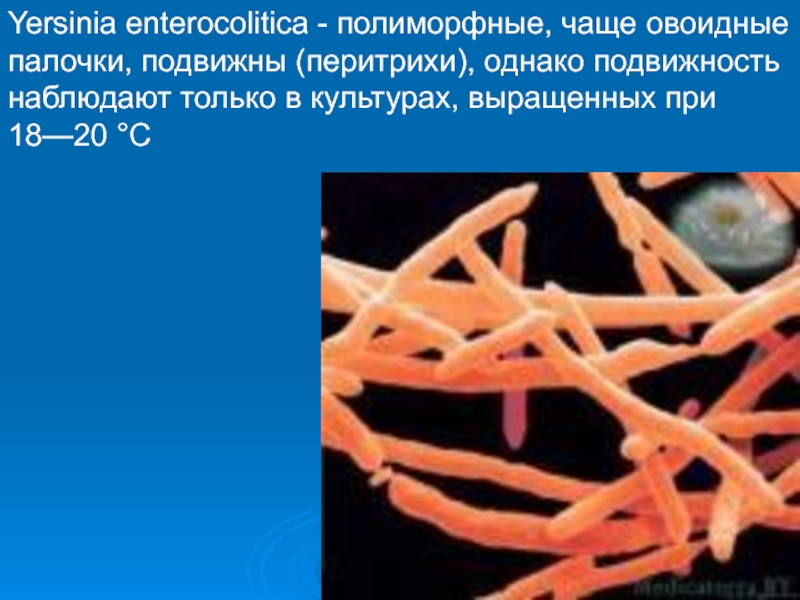
Yersinia enterocolitica - полиморфные, чаще овоидные палочки, подвижны (перитрихи),
однако подвижность наблюдают только в культурах, выращенных при 18—20 °С
Слайд 68
Температурный оптимум 28-30 °С; оптимум рН 6,9-7,2.
хорошо растут
на простых питательных средах
на плотных средах образуют мелкие блестящие, часто
выпуклые S-колонии с голубоватым оттенком в проходящем светеОбразование R-колоний для бактерий возбудителя иерсиниоза нехарактерно
При культивировании на среде Эндо (48 ч при 37 "С) колонии розоватого оттенка
проявляют пектиназную активность, на пектиновом агаре колонии окружены зоной разжижения
При культивировании в жидких питательных средах микроорганизм вызывает их помутнение
Слайд 69
О-антиген (эндотоксин), похожий на антигены многих грамотрицательных бактерий и
токсичный для животных и человека
По структуре О-антигена выделяют 34 серовара
Подавляющее большинство поражений вызывают серовары 03 и 09, реже — 05-08Слайд 70
Факторы вирулентности
- адгезины и инвазины, облегчающие взаимодействие с
кишечньш эпителием;
- низкомолекулярные белки, ингибирующие активность бактерицидных факторов, - энтеротоксин,
аналогичный термостабильным токсинам Е. соlliСлайд 71
Бактерии проникают в слизистую оболочку тонкой кишки, размножаются
в пёйеровых бляшках и мигрируют в брыжеечные лимфатические узлы.
Патогенез
суставной патологии связан со способностью компонентов клеточной стенки взаимодействовать с молекулами II класса HLA с образованием суперантигенов, активирующих Т-клетки и стимулирующих их пролиферацию.Слайд 72
доминирует симптоматика гастроэнтерита (энтероколит с диареей, лихорадкой и болями
в животе)
Сопутствующая регионарная лимфаденопатия при иерсиниозе имитирует острый аппендицит.
Диарея
при иерсиниозе обусловлена действием термостабильного энтеротоксина, стимулирующего синтез гуанилатциклазы. . Кишечная инфекция может привести к септицемии с поражением внутренних органов и тяжёлыми артритами; поражения обычно возникают через 7-14 сут от начала болезни.
Анкилозирующий спондилит при иерсиниозе. В связи со способностью вызывать реактивные артриты многие авторы рассматривают У. enterocolitica как причину некоторых форм анкилозирующего спондилита
Слайд 73
материал для исследований
кровь, испражнения, продукты питания и
вода.
Материал засевают на среды Эндо, Плоскирева и жидкую среду
обогащения. Наиболее благоприятная температура для выделения возбудителя иерсиниоза 22-29 С. На средах для изучения подвижности (например, содержащих индол и орнитин) Y. enterocoiltica неподвижны или малоподвижны при 35 "С и подвижны при 25 °С.
После выделения чистой культуры возбудителя иерсиниоза проводят определение основных биохимических свойств
Дополнительным признаком служит реакция Фогеса-Проскауэра, положительная при 22-28"С.
Окончательное типирование возбудителя иерсиниоза осуществляют с помощью агглютинирующих О-антисывороток.