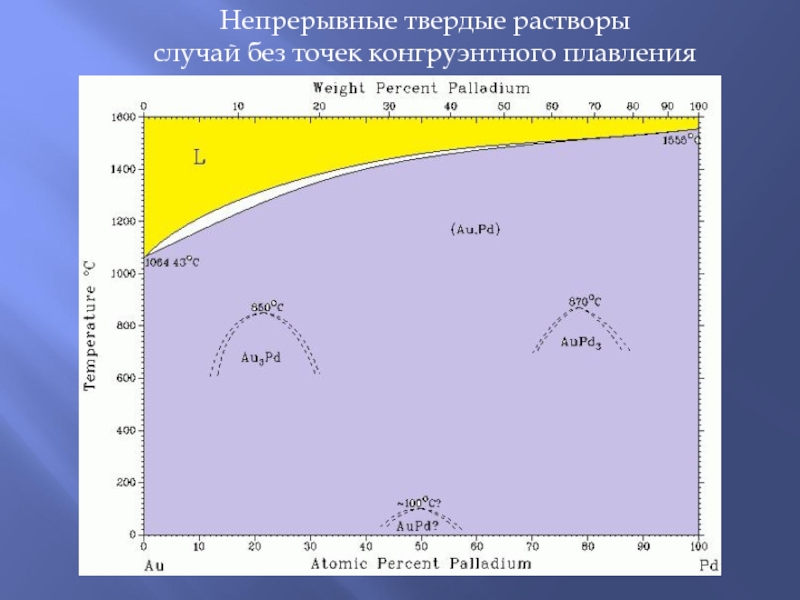
Слайд 1Непрерывные твердые растворы
случай без точек конгруэнтного плавления
Слайд 2Требования к компонентам, при соблюдении которых возможно образование НТР:
- близость
в характере химических связей в твердых фазах A и B;
если компоненты – простые вещества, – то близость электронного строения атомов A и B;
- размерный фактор: разница в параметрах кристаллической решетки фаз A и B – не должна превышать 8-12% (иногда – до 15%); если A и B простые вещества, то можно говорить о необходимости соответствия атомных радиусов элементов в пределах 8-12 %;
- кристаллические решетки фаз A и B должны быть одинакового типа (возможны некоторые редкие исключения.).
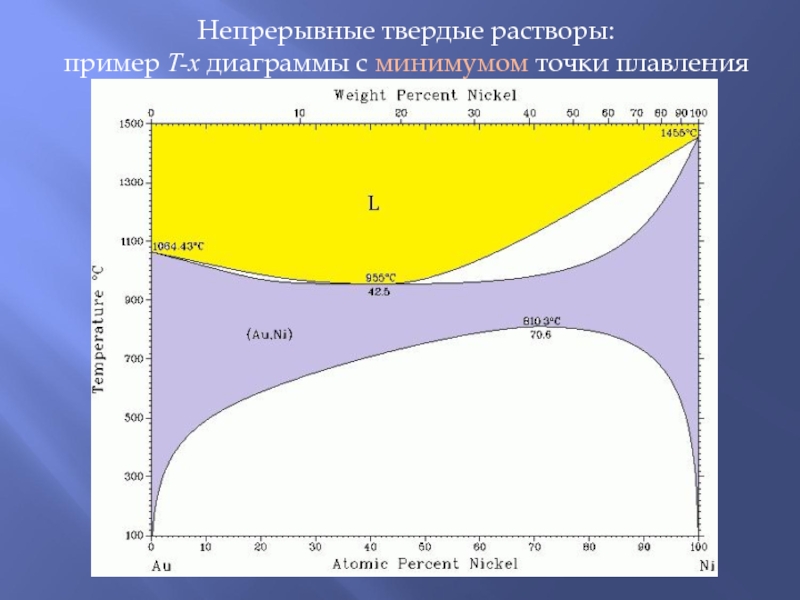
Слайд 3Непрерывные твердые растворы:
пример T-x диаграммы с минимумом точки плавления
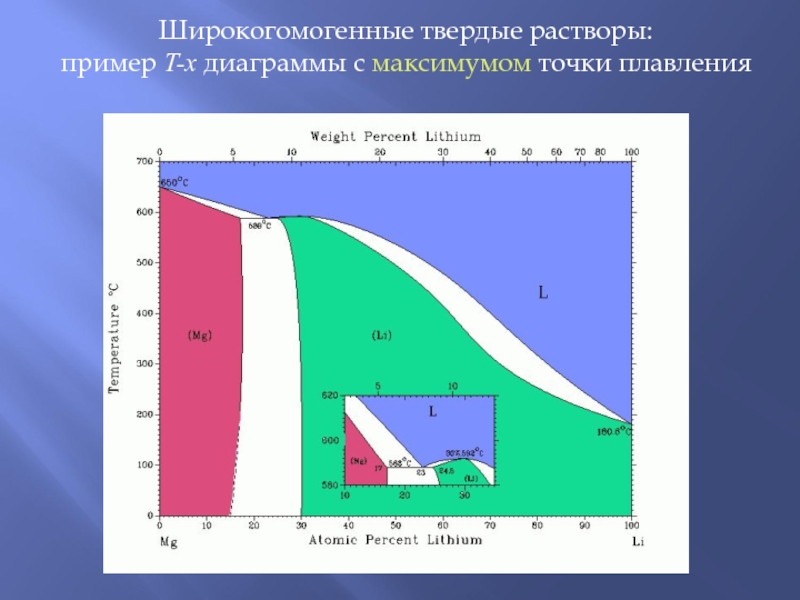
Слайд 4Широкогомогенные твердые растворы:
пример T-x диаграммы с максимумом точки плавления
Слайд 5Генезис ФД от полной нерастворимости (во всех агрегатных состояниях) к
полной растворимости (или наоборот – с какого края рассматривать)
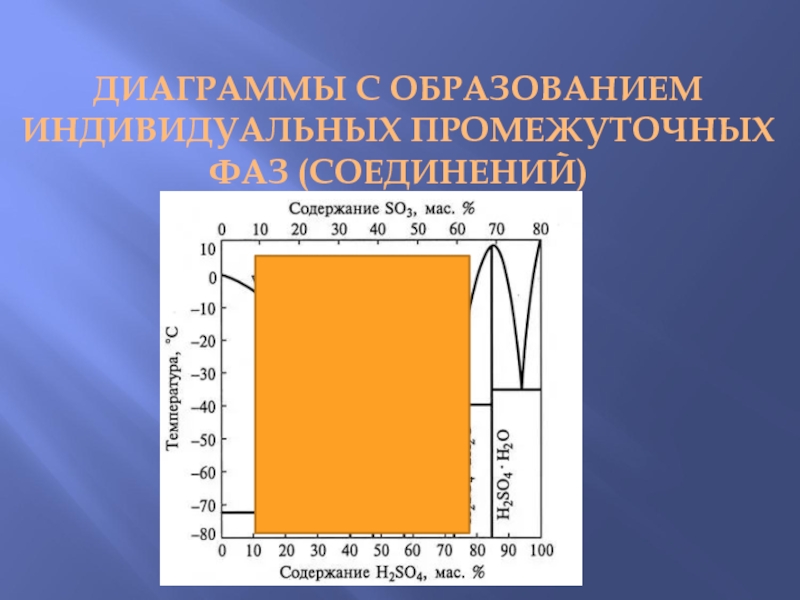
Слайд 6Диаграммы с образованием индивидуальных промежуточных фаз (соединений)
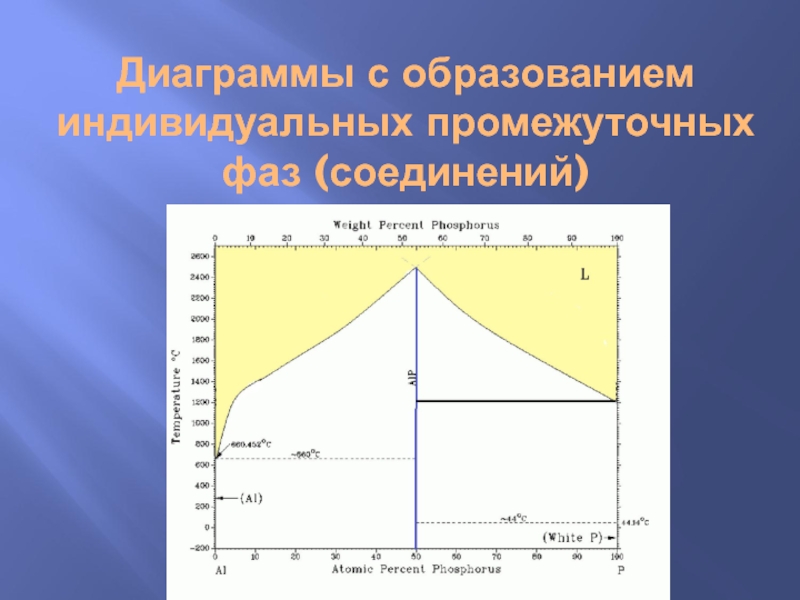
Слайд 7Диаграммы с образованием индивидуальных промежуточных фаз (соединений)
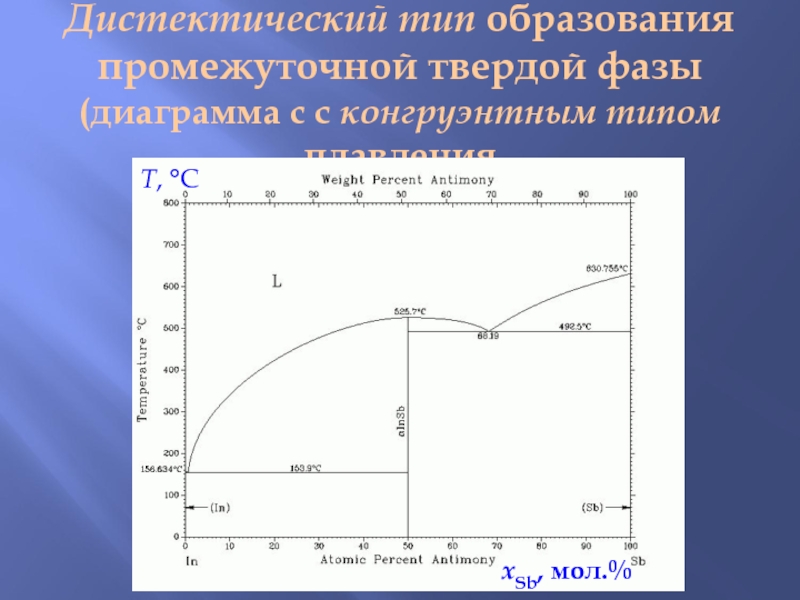
Слайд 8Дистектический тип образования промежуточной твердой фазы
(диаграмма с с конгруэнтным типом
плавления
T, C
xSb, мол.%
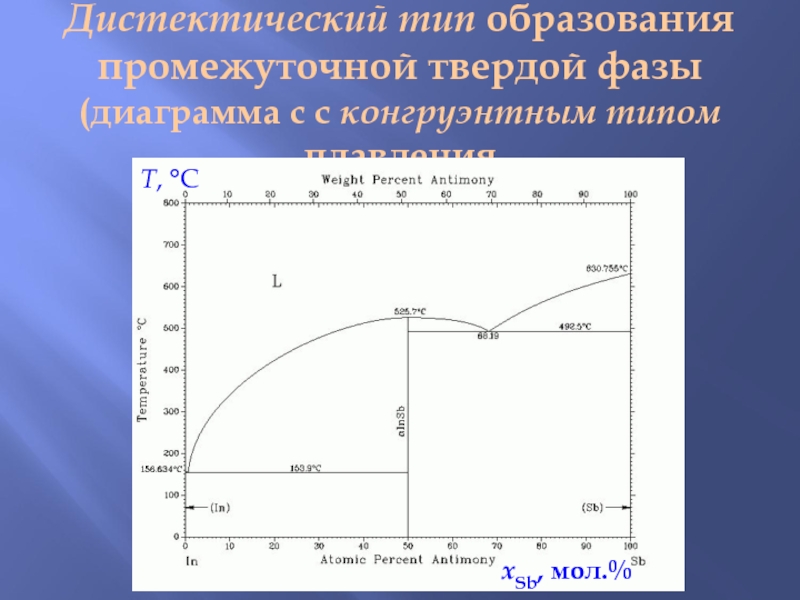
Слайд 9Дистектический тип образования промежуточной твердой фазы
(диаграмма с с конгруэнтным типом
плавления
T, C
xSb, мол.%
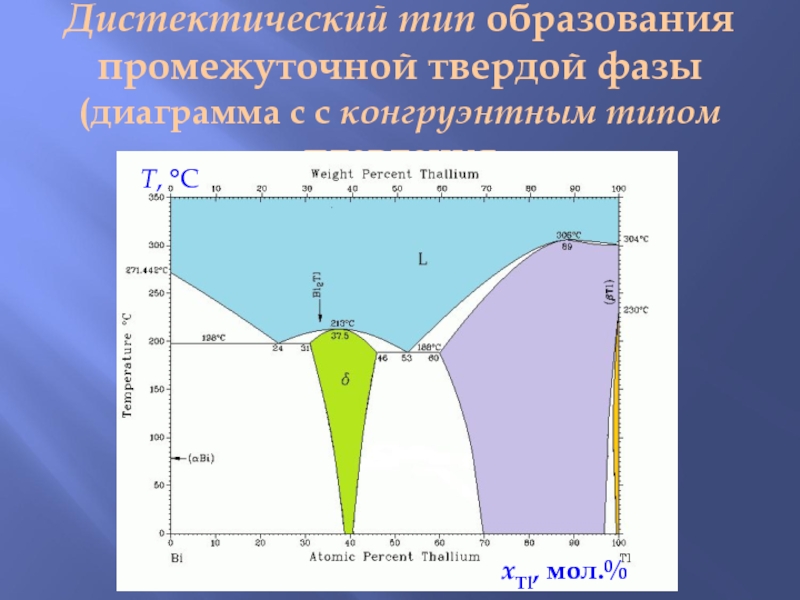
Слайд 10Дистектический тип образования промежуточной твердой фазы
(диаграмма с с конгруэнтным типом
плавления
T, C
xTl, мол.%
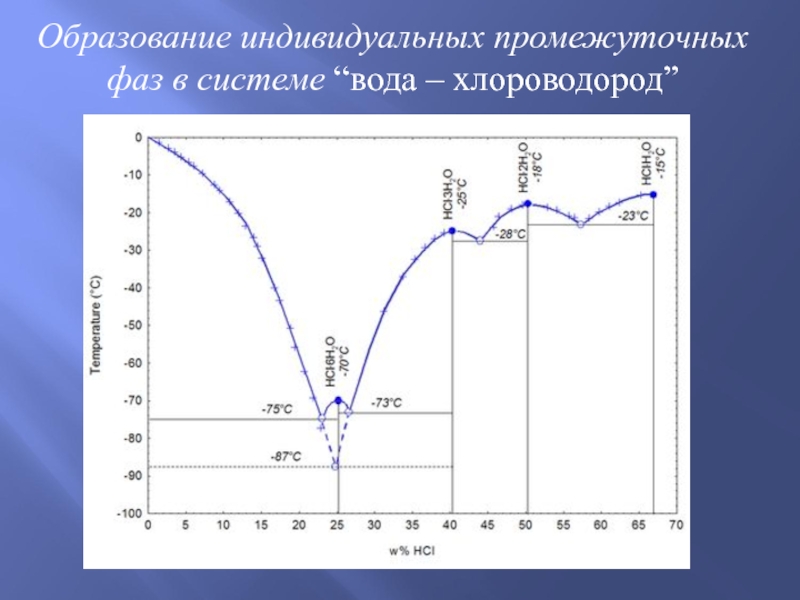
Слайд 11Образование индивидуальных промежуточных фаз в системе “вода – хлороводород”
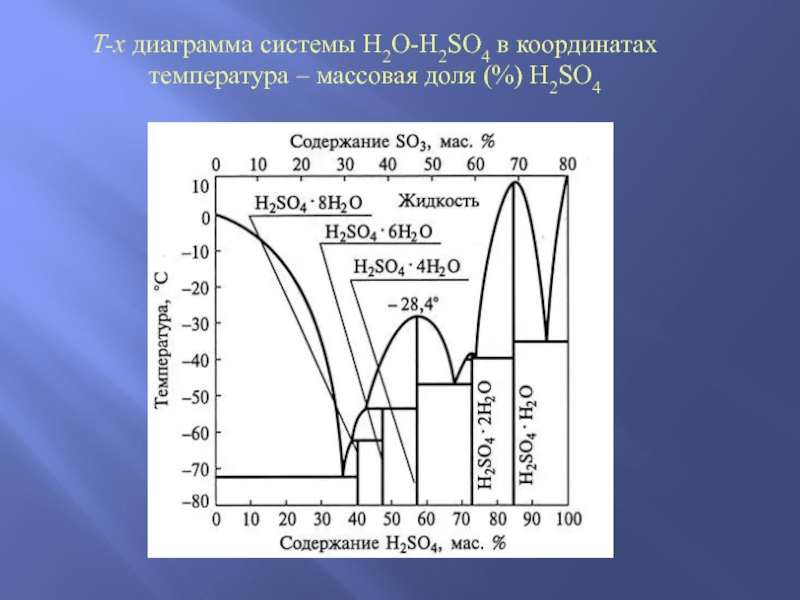
Слайд 12T-x диаграмма системы H2O-H2SO4 в координатах
температура – массовая доля
(%) H2SO4
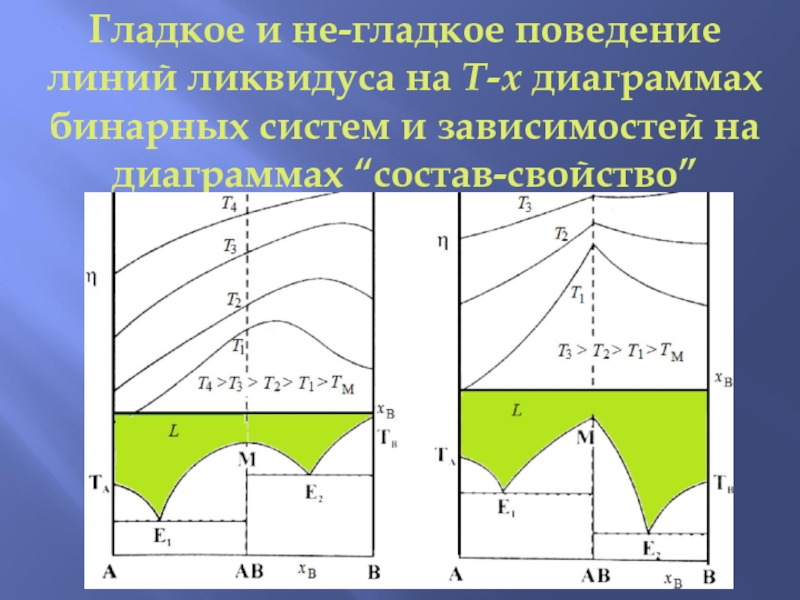
Слайд 13Гладкое и не-гладкое поведение линий ликвидуса на T-x диаграммах бинарных
систем и зависимостей на диаграммах “состав-свойство”
Слайд 14Диаграммы “Состав – свойство”
Закономерности Курнакова:
1. При расслоении в твердой фазе
(образование гетерогенной смеси) свойства сплава изменяются по линейному закону (аддитивно). Величины, характеризующие
свойства сплава находятся в интервале между свойствами чистых компонентов.
Слайд 15Закономерности Курнакова:
2. При образовании твердых растворов свойства изменяются по криволинейной зависимости, причем
некоторые свойства, в первую очередь электро-сопротивление, могут значительно отличаться от компонентов.
При образовании механической смеси электросопротивление повышается незначительно, при образовании твердого раствора — весьма сильно.
Для интерметаллидных систем твердость непрерывных твердых растворов как правило, достигает максимума при равных мольных концентрациях компонентов (т.е. около
50 мол.%) . Это происходит за счет максимального искажения кристаллической структуры при составах, близких 50 мол %. По той же причине электропроводность также достигает максимума вблизи 50 мол %. Выделенная выше цветом закономерность иногда называется законами Курнакова.
Слайд 16Закономерности Курнакова:
3. При образовании ограниченных твердых растворов свойства в интервале концентраций,
отвечающем однофазным твердым растворам, изменяются по криволинейному, а в двухфазной
области диаграммы — по прямолинейному закону, причем крайние точки на прямой являются свойствами чистых фаз, предельно насыщенных твердых растворов, образующих данную смесь.
Слайд 17
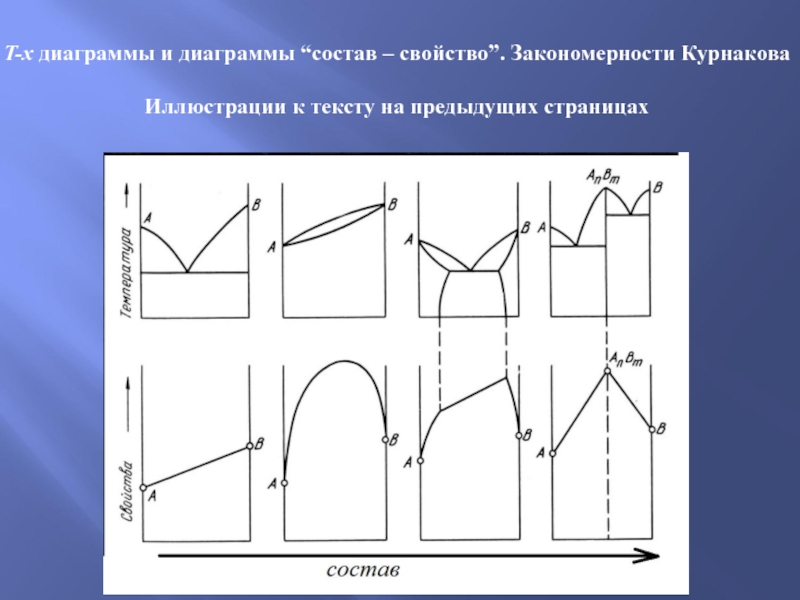
T-x диаграммы и диаграммы “состав – свойство”. Закономерности Курнакова
Иллюстрации к
тексту на предыдущих страницах
Слайд 18Законы Курнакова
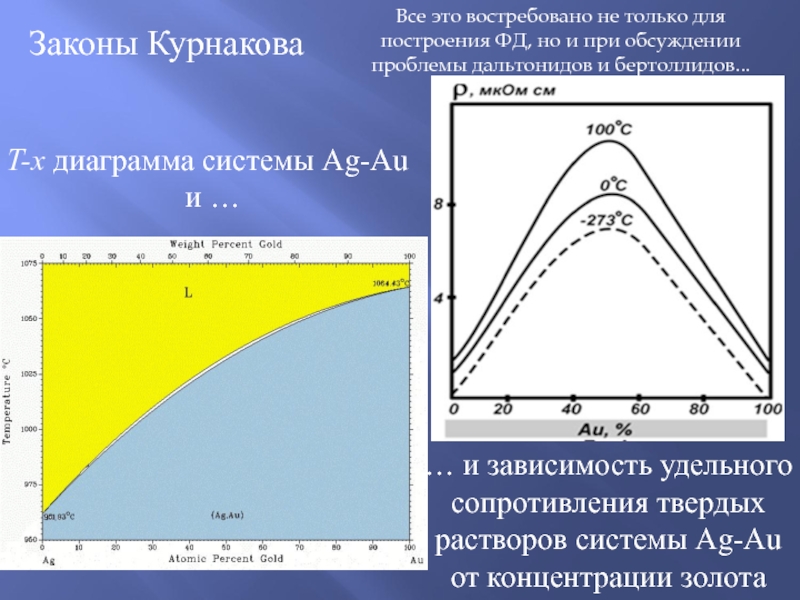
… и зависимость удельного сопротивления твердых растворов системы Ag-Au
от концентрации золота
T-x диаграмма системы Ag-Au
и …
Все это востребовано не
только для построения ФД, но и при обсуждении проблемы дальтонидов и бертоллидов...
Слайд 19Бывают и другие виды T-x диаграмм, в которых реализуются промежуточные
фазы...
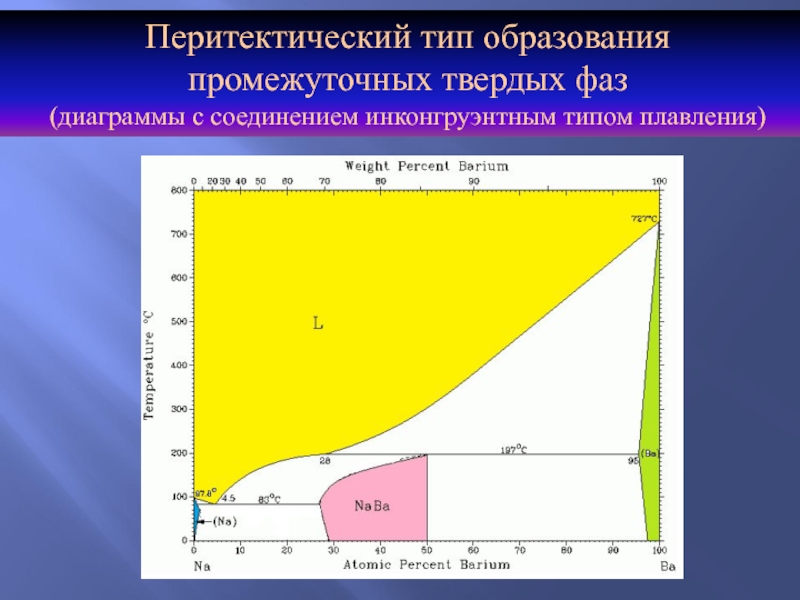
Перитектический тип образования
промежуточных твердых фаз
(диаграммы с соединением инконгруэнтным
типом плавления)
Слайд 20Бывают и другие виды T-x диаграмм, в которых реализуются промежуточные
фазы...
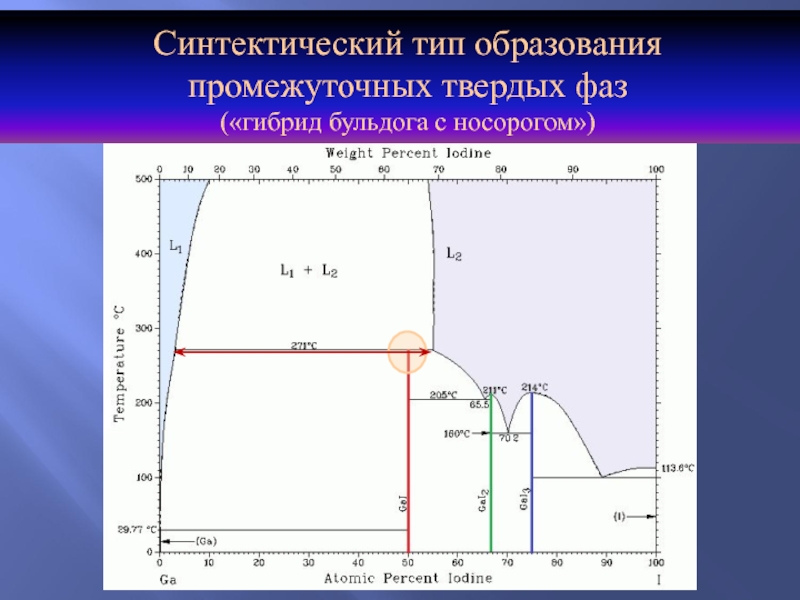
Синтектический тип образования
промежуточных твердых фаз
(«гибрид бульдога с носорогом»)
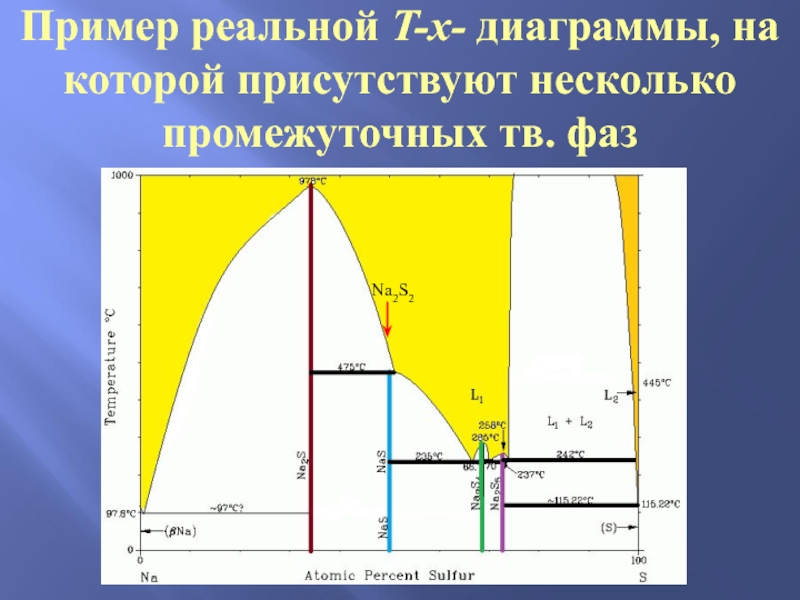
Слайд 21Пример реальной T-x- диаграммы, на которой присутствуют несколько промежуточных тв.
фаз
Na2S2
Слайд 22Взаимодействия с участием только твердых фаз в бинарных системах:
эвтектоидный,
перитектоидный и дистектоидный
типы взаимодействия
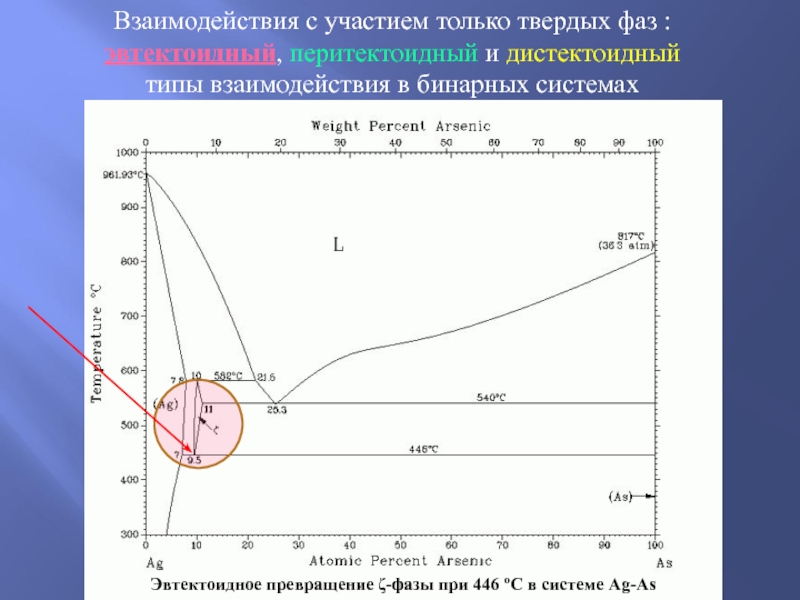
Слайд 23Взаимодействия с участием только твердых фаз :
эвтектоидный, перитектоидный и
дистектоидный
типы взаимодействия в бинарных системах
Эвтектоидное превращение -фазы при 446
oС в системе Ag-As
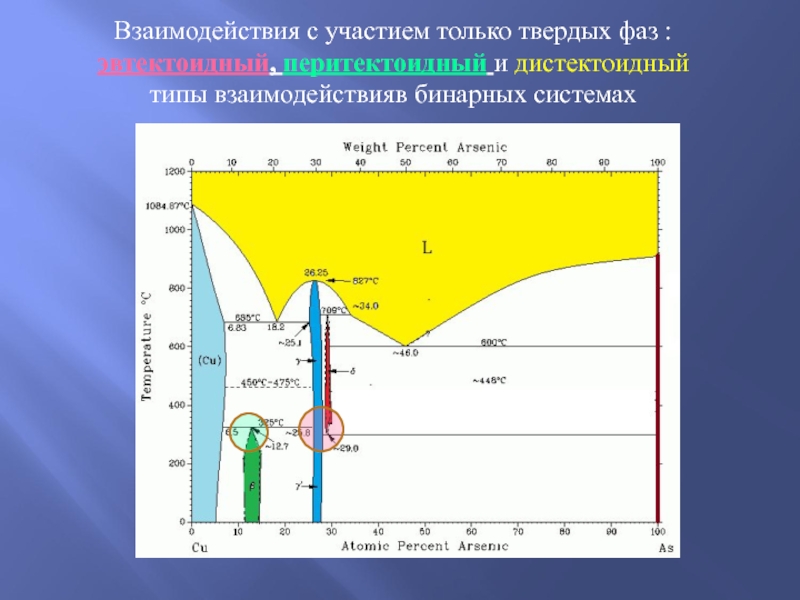
Слайд 24Взаимодействия с участием только твердых фаз :
эвтектоидный, перитектоидный и
дистектоидный
типы взаимодействияв бинарных системах
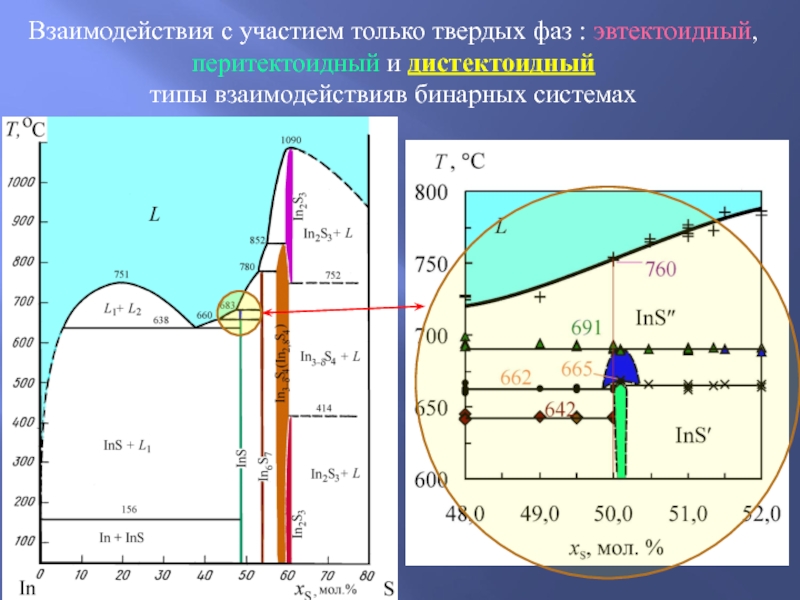
Слайд 25Взаимодействия с участием только твердых фаз : эвтектоидный, перитектоидный и
дистектоидный
типы взаимодействияв бинарных системах
Слайд 26Природная эвтектика:
SiO2-K[AlSi3O8]; скол еврейского гранита
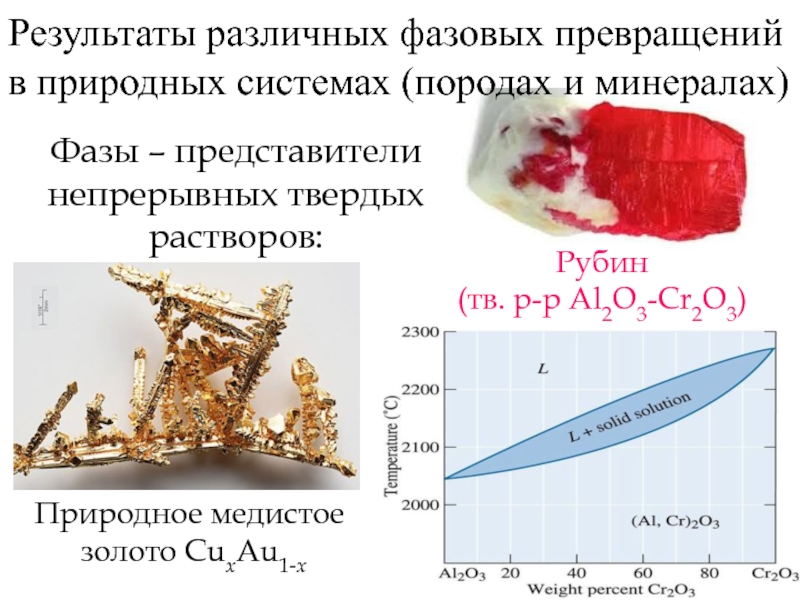
Результаты различных фазовых превращений в
природных системах (породах и минералах)
Слайд 27Природное медистое
золото CuxAu1-x
Фазы – представители
непрерывных твердых растворов:
Рубин
(тв.
р-р Al2O3-Cr2O3)
Результаты различных фазовых превращений в природных системах (породах и
минералах)
Слайд 28Результаты различных фазовых превращений в природных системах (породах и минералах)
Промежуточные
(индивидуальные) фазы:
аурипигмент (желт.) As2S3 и реальгар As4S4 (красн.)
As4S4 As2S3
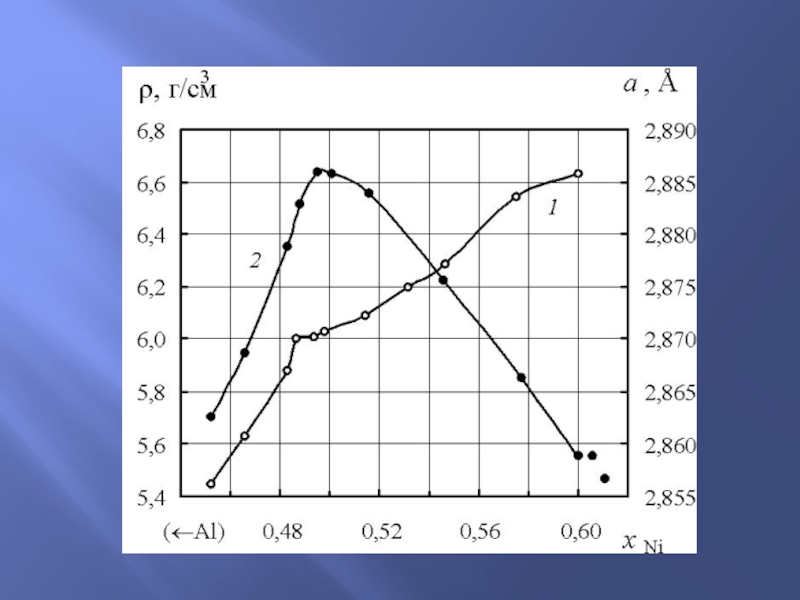
Слайд 29Проблема поиска преимущественного состава в промежуточных твердых фазах: проблема дальтонидов
и бертоллидов
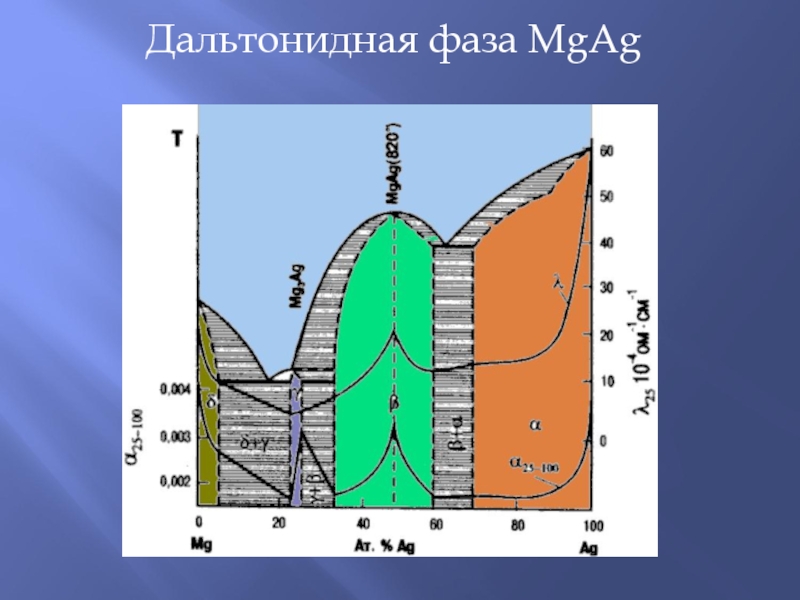
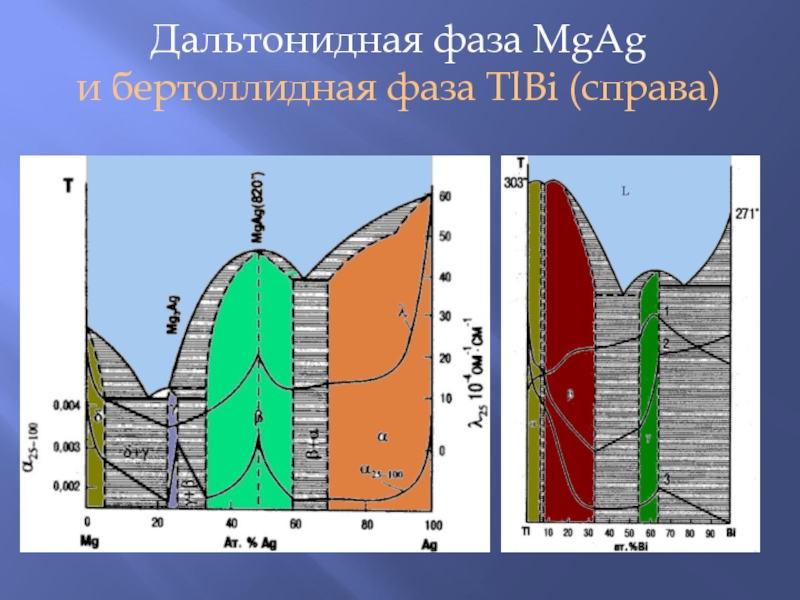
Слайд 31Дальтонидная фаза MgAg
и бертоллидная фаза TlBi (справа)
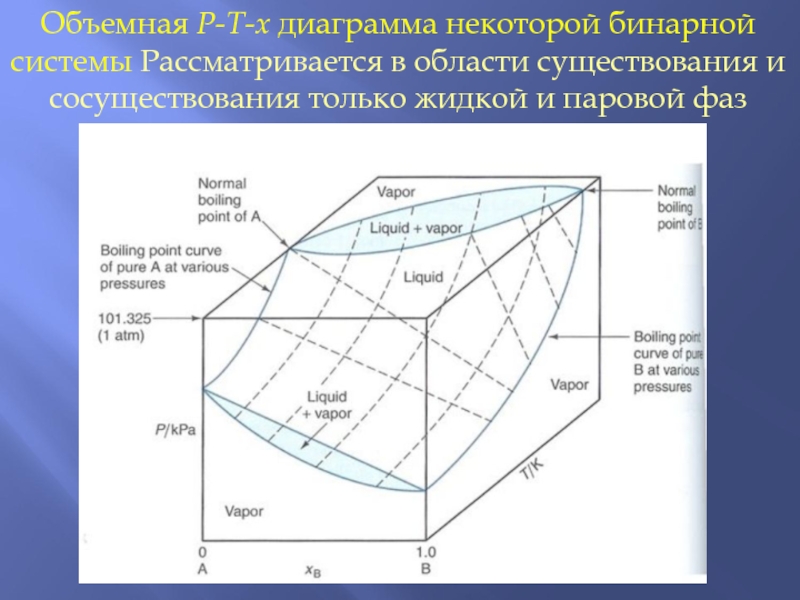
Слайд 33Объемная P-T-x диаграмма некоторой бинарной системы Рассматривается в области существования
и сосуществования только жидкой и паровой фаз
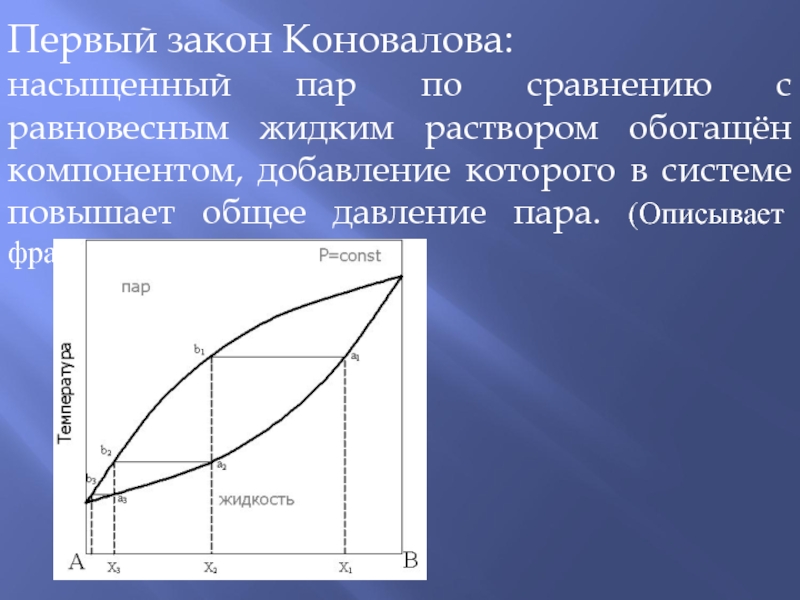
Слайд 34Первый закон Коновалова:
насыщенный пар по сравнению с равновесным жидким раствором
обогащён компонентом, добавление которого в системе повышает общее давление пара.
(Описывает фракционную перегонку)
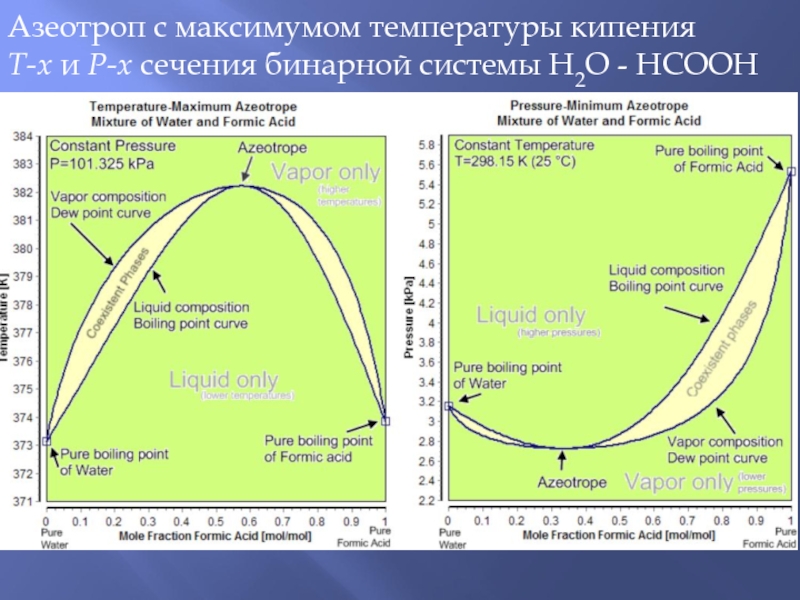
Слайд 35Азеотроп с максимумом температуры кипения
T-x и P-x сечения бинарной системы
H2O - HCOOH
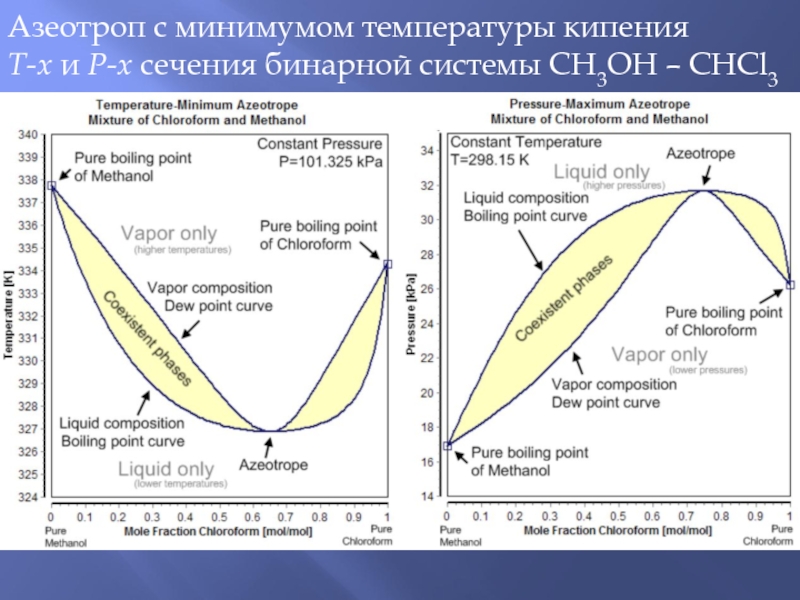
Слайд 36Азеотроп с минимумом температуры кипения
T-x и P-x сечения бинарной системы
СH3OH – CHCl3
Слайд 37Второй закон Коновалова описывает растворы с отклонениями от свойств идеальных
растворов и объясняет существование азеотропных растворов, состав которых при перегонке
не изменяется:
Экстремумы на T-x- и P-x-сечениях отвечают такому равновесию раствора и насыщенного пара, при котором состав обеих фаз одинаков
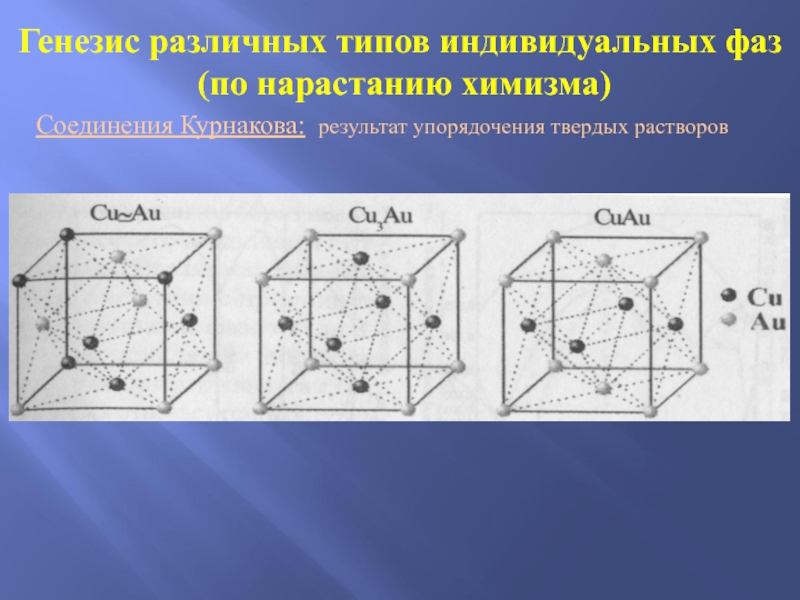
Слайд 39Генезис различных типов индивидуальных фаз
(по нарастанию химизма)
Соединения Курнакова:
результат упорядочения твердых растворов
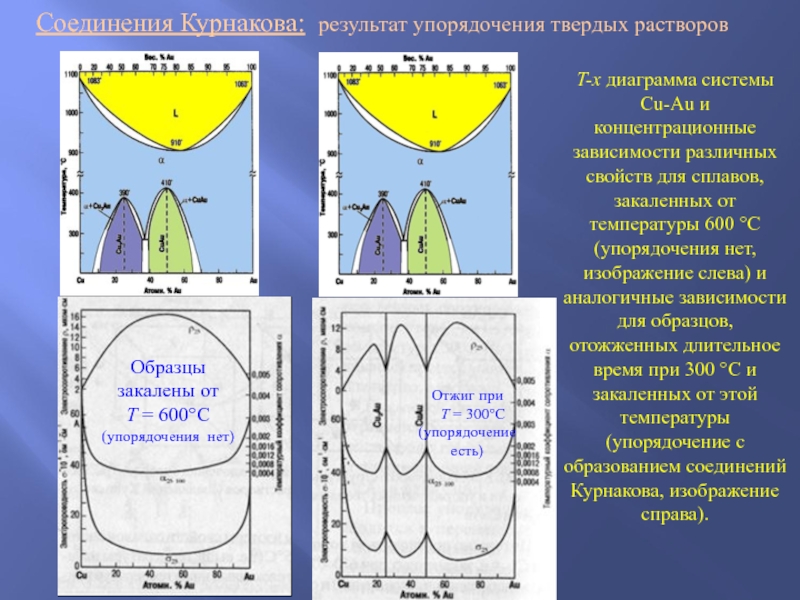
Слайд 40Соединения Курнакова: результат упорядочения твердых растворов
Образцы закалены от
T =
600C (упорядочения нет)
Отжиг при
T = 300C (упорядочение
есть)
T-x диаграмма системы Cu-Au и концентрационные зависимости различных свойств для сплавов, закаленных от температуры 600 С (упорядочения нет, изображение слева) и аналогичные зависимости для образцов, отожженных длительное время при 300 С и закаленных от этой температуры (упорядочение с образованием соединений Курнакова, изображение справа).
Слайд 41Генезис различных типов индивидуальных фаз
(по нарастанию химизма)
Фазы Лавеса
Фазы
Лавеса образуются атомами двух сортов A и B, причем атом
сорта A всегда имеет больший атомный радиус, чем атом сорта B, причем существует идеальное соотношение радиусов компонентов RA:RB=1.225 (VA:VB = 2:1). К фазам Лавеса относятся соединения, кристаллизующиеся в несколько родственных структурных типов, из которых наиболее многочисленными являются три следующих: - гексагональный тип MgZn2, кубический тип MgCu2, гексагональный тип MgNi2.Все фазы Лавеса имеют разный порядок укладки одинаковых структурных единиц, в качестве которой в данном случае выступает многослойный «сэндвич». Так кубическая фаза Лавеса MgCu2 представляет собой трёхслойную укладку элементарных структурных единиц в порядке …XYZXYZ…, фаза MgZn2 является двухслойной …XYXY…, а фаза MgNi2 — четырёхслойной …XYXZXYXZ… . Возможны и другие последовательности укладки слоёв.
Основная особенность фаз Лавеса – наличие кластеров из атомов B (атомы меньшего размера).
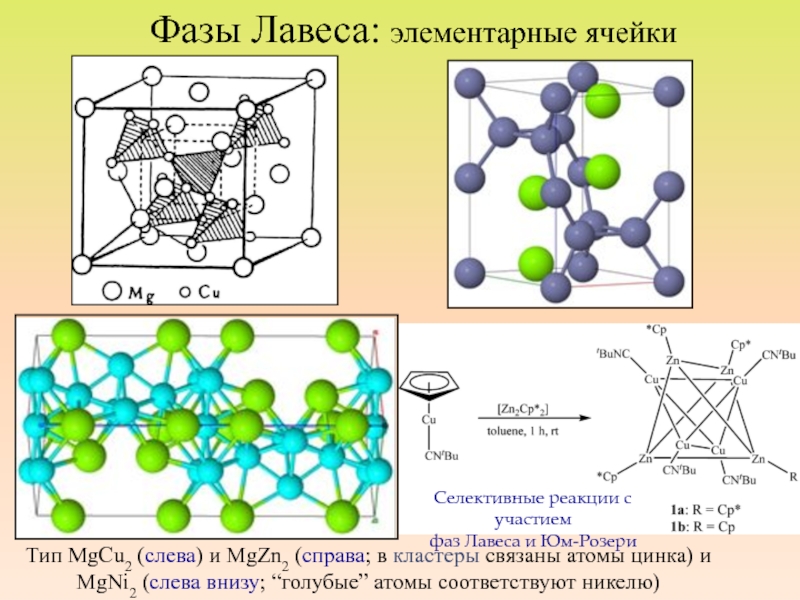
Слайд 42Фазы Лавеса: элементарные ячейки
Тип MgCu2 (слева) и MgZn2 (справа; в
кластеры связаны атомы цинка) и MgNi2 (слева внизу; “голубые” атомы
соответствуют никелю)
Селективные реакции с участием
фаз Лавеса и Юм-Розери
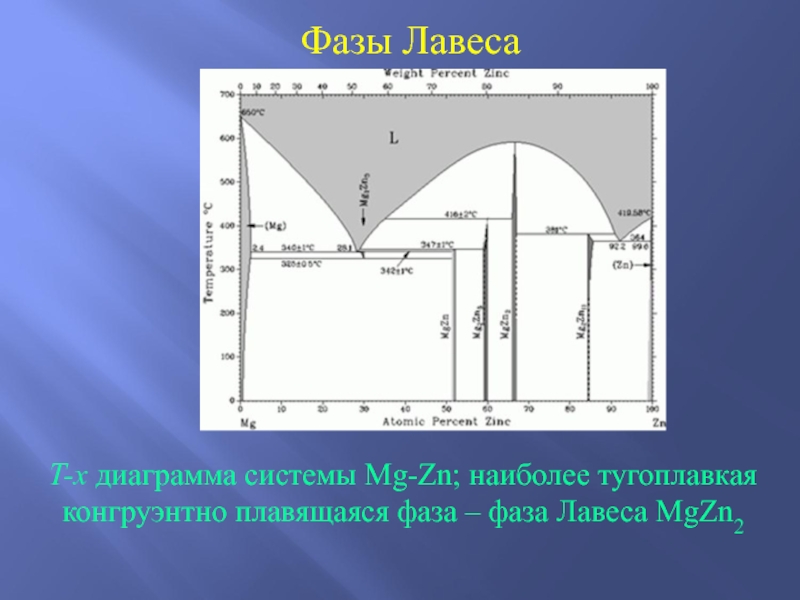
Слайд 43Фазы Лавеса
T-x диаграмма системы Mg-Zn; наиболее тугоплавкая конгруэнтно плавящаяся фаза
– фаза Лавеса MgZn2
Слайд 44Генезис различных типов индивидуальных фаз
(по нарастанию химизма)
Фазы внедрения
(фазы Хэгга). Структура состоит из атомов металла, расположенных так же,
как и в характерных для металлов плотных упаковках (гексагoнальная., гранецентрированный. или объемноцентрированный. куб), а атомы неметаллов (Н, N, С, В, Р, О) расположены в тетраэдрических и октаэдрических пустотах этой плотной упаковки. Число тетраэдрических пустот в плотнейшей упаковке (рис “a” внизу) в два раза больше числа октаэдрических (рис “б” внизу). Фазы внедрения могут образовываться, если отношение радиусов атомов RMe/Rx 0,59 (правило Хэгга). В фазах внедрения подрешетка атомов металла отличается от структуры исходного металла. Так, у карбидов Ti и V типа MX гранецентрированная кубическая решетка (хотя Ti и V не кристаллизуются в ней). Для фаз внедрения характерны заметные области гомогенности, границами которых со стороны неметалла является стехиометрический состав.
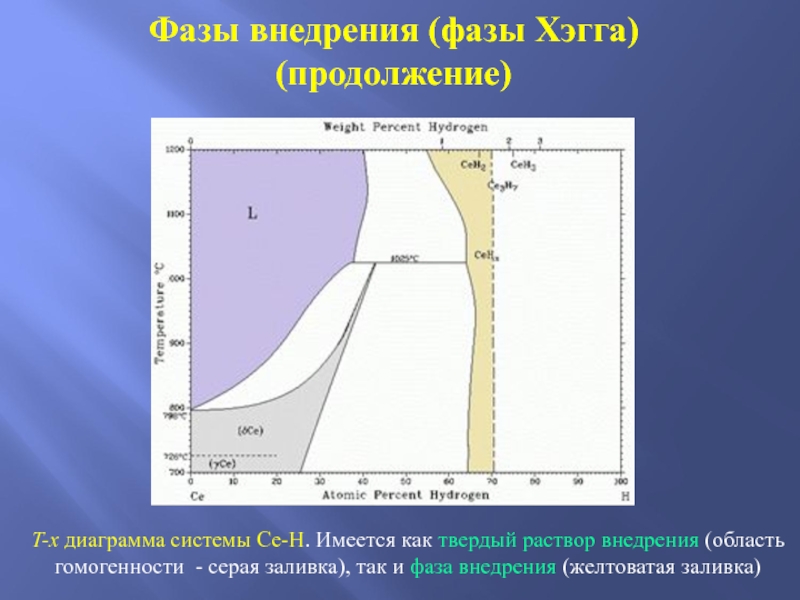
Слайд 45Фазы внедрения (фазы Хэгга)
(продолжение)
T-x диаграмма системы Ce-H. Имеется как твердый
раствор внедрения (область гомогенности - серая заливка), так и фаза
внедрения (желтоватая заливка)
Слайд 46T-x диаграмма системы Cu-Zn с образованием многочисленных соединений Юм-Розери (CuZn,
Cu5Zn8, CuZn3)
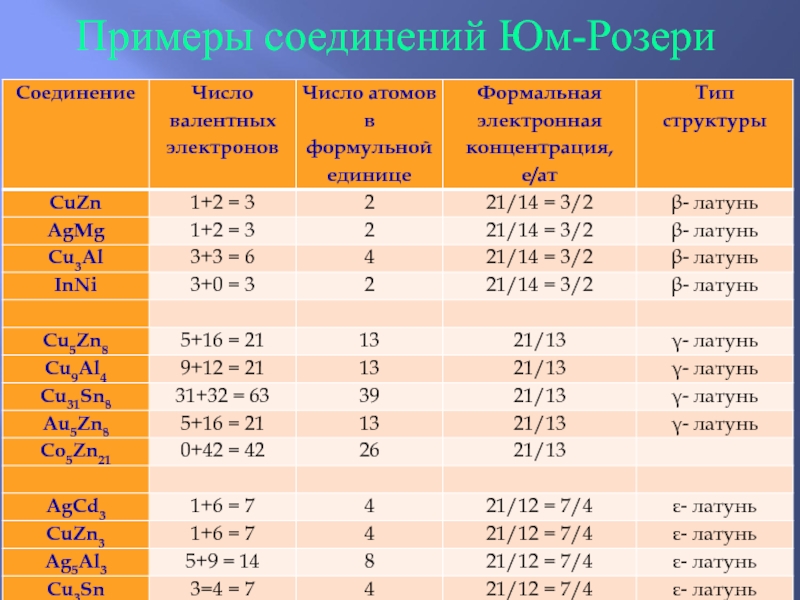
Электронные соединения Юм-Розери
Стехиометрию определяет формальная электронная концентрация:
Ne/Nat = 21/12;
Ne/Nat = 21/13; Ne/Nat =21/14
Расположение атомов в структуре g-латуни
Слайд 48Генезис различных типов индивидуальных фаз
Интеркалированные слоистые соединения (аналогия между
твердыми растворами внедрения и фазами внедрения)
Реакция вхождения атомов или даже
молекул или ионов между слоями структуры – матрицы (“хозяина”) называется интеркалированием, а сами продукты – интеркалатами.
Структуры типичного “хозяина” графита - слева и графена (монослой графита) - справа
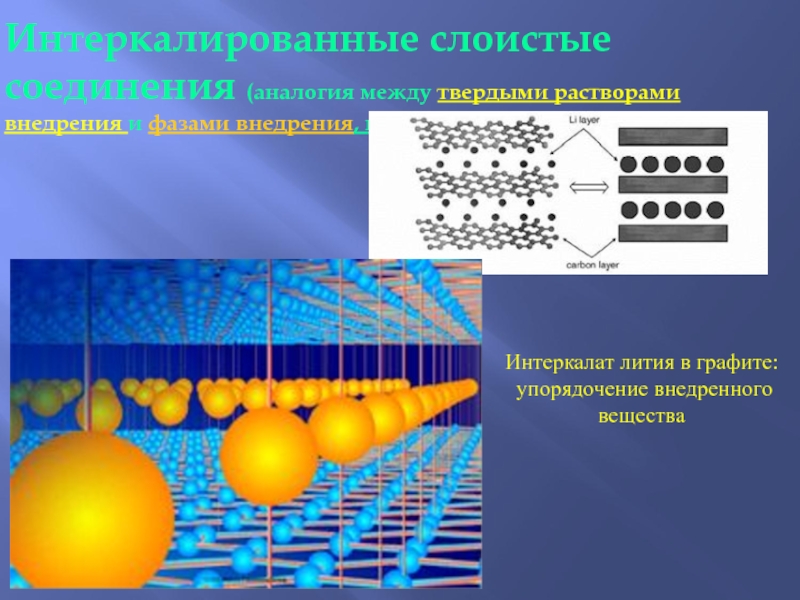
Слайд 49Интеркалированные слоистые соединения (аналогия между твердыми растворами внедрения и фазами
внедрения, продолжение)
Интеркалат лития в графите:
упорядочение внедренного вещества
Слайд 50Интеркалированные слоистые соединения (аналогия между твердыми растворами внедрения и фазами
внедрения, продолжение)
Интеркалированные соединения:
(C60)xC (слева), LaC8 (показан один слой, рис.
справа)
Слайд 51Соединения внедрения графита (СВГ) – частный случай интеркалатов.
СВГ делятся на
два широких класса: донорные и акцепторые. Перераспределение электронной плотности между
молекулами интеркалята и атомами углерода в СВГ акцепторного типа приводит к появлению дополнительного количества делокализованных дырок в графитовых слоях. В донорных соединениях внедренные вещества отдают свои валентные электроны, и проводимость осуществляется избыточными электронами в углеродных слоях. Акцепторные соединения образуются при внедрении таких веществ, как галогены, галогениды металлов, кислоты. Донорные соединения образуются при внедрении щелочных или щелочноземельных металлов в графитовую матрицу. Примерами соединений донорного типа являются С4К, C8Li, C8Ca. Акцепторые соединения имеют более сложный состав, например C16Br2, C20FeCl3, C16ICl, (C24)+HSO4‑ и т.д..
Кроме того, известны СВГ, в которых межслоевые пространства попеременно заняты двумя интеркалирующими агентами. Это так называемые гетеросоединения, типичным примером которых является СВГ с СuС12 и ICl.
Они еще более расширяют возможности получения новых материалов с уникальным набором свойств. При интеркалировании всегда происходит значительное (в 2-3 раза) увеличение расстояния между графитовыми слоями и может нарушиться порядок чередования слоев, характерный для монокристаллического графита. Отличительной особенностью СВГ является наличие целого спектра соединений одного и того же интеркалята, различающихся составом и строением. Они называются ступенями. Номер ступени N равен числу графитовых сеток между ближайшими слоями внедренного вещества.

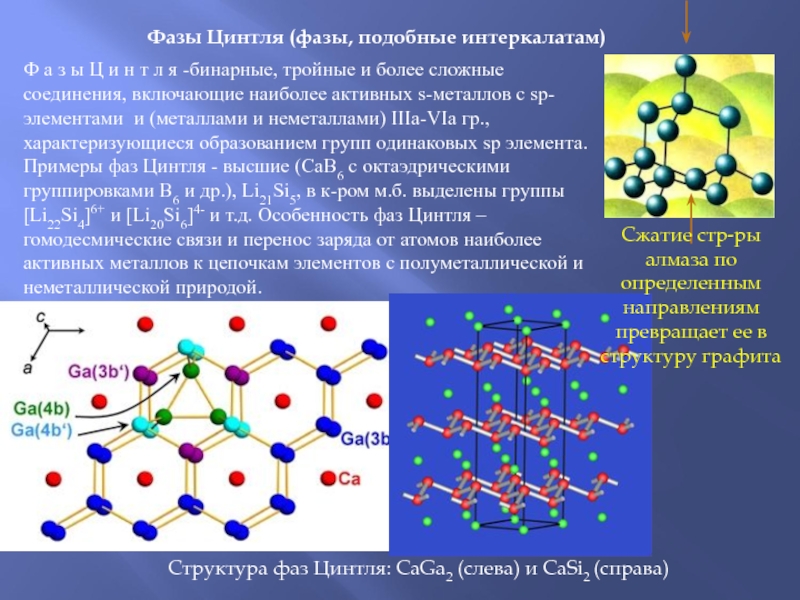
Слайд 52Фазы Цинтля (фазы, подобные интеркалатам)
Ф а з ы Ц и
н т л я -бинарные, тройные и более сложные соединения,
включающие наиболее активных s-металлов с sp- элементами и (металлами и неметаллами) IIIa-VIa гр., характеризующиеся образованием групп одинаковых sp элемента. Примеры фаз Цинтля - высшие (СаВ6 с октаэдрическими группировками В6 и др.), Li21Si5, в к-ром м.б. выделены группы [Li22Si4]6+ и [Li20Si6]4- и т.д. Особенность фаз Цинтля – гомодесмические связи и перенос заряда от атомов наиболее активных металлов к цепочкам элементов с полуметаллической и неметаллической природой.
Структура фаз Цинтля: CaGa2 (слева) и CaSi2 (справа)
Сжатие стр-ры алмаза по определенным направлениям превращает ее в структуру графита
Слайд 53Валентные соединения
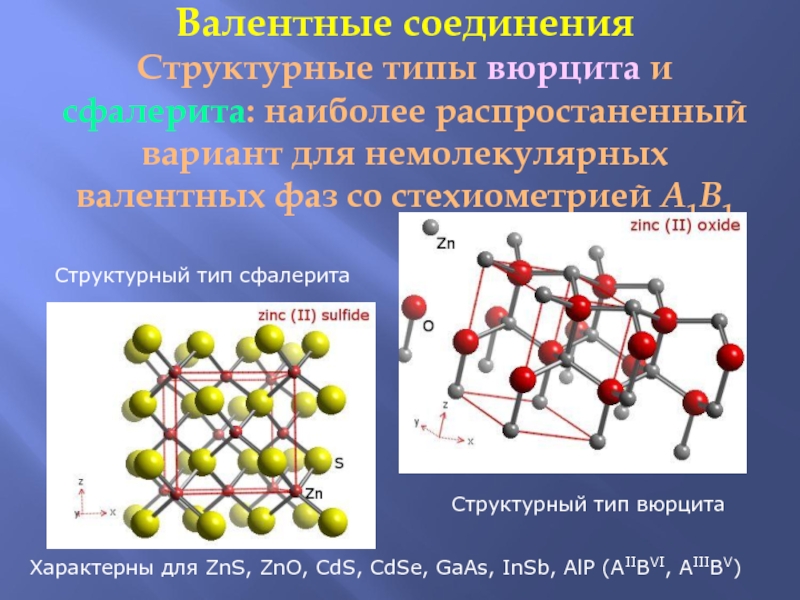
Структурные типы вюрцита и сфалерита: наиболее распростаненный вариант для
немолекулярных валентных фаз со стехиометрией A1B1
Cтруктурный тип сфалерита
Cтруктурный тип
вюрцита
Характерны для ZnS, ZnO, CdS, CdSe, GaAs, InSb, AlP (AIIBVI, AIIIBV)
Слайд 54Классические валентные соединения
в немолекулярных структурах
Примитивные правила устойчивости структурного типа для
ионно-ковалентных структур
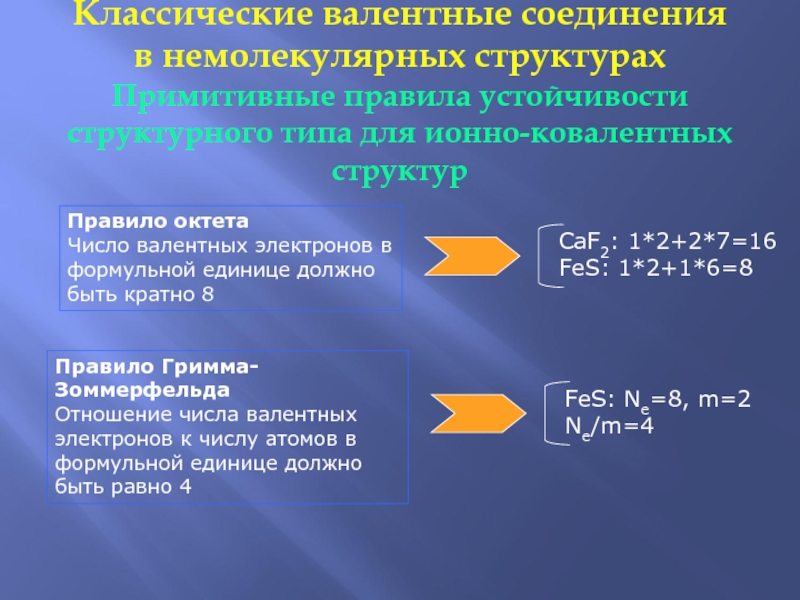
Правило октета
Число валентных электронов в формульной единице должно быть
кратно 8
CaF2: 1*2+2*7=16
FeS: 1*2+1*6=8
Правило Гримма-Зоммерфельда
Отношение числа валентных электронов к числу атомов в формульной единице должно быть равно 4
FeS: Ne=8, m=2
Ne/m=4
Слайд 55Более универсальное правило устойчивости структурного типа для ионно-ковалентных структур
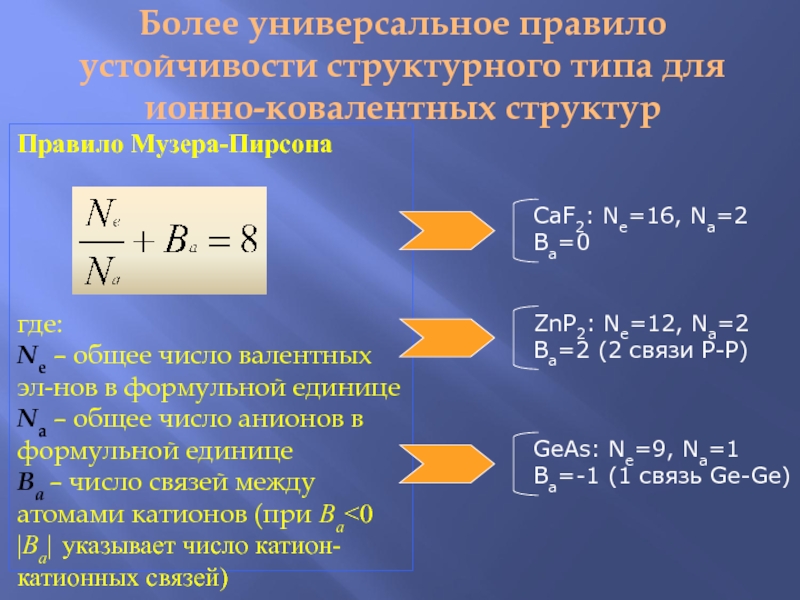
Правило Музера-Пирсона
где:
Ne
– общее число валентных эл-нов в формульной единице
Nа – общее
число анионов в формульной единице
Ва – число связей между атомами катионов (при Ва<0 |Ва| указывает число катион-катионных связей)
CaF2: Ne=16, Na=2
Ba=0
ZnP2: Ne=12, Na=2
Ba=2 (2 связи Р-Р)
GeAs: Ne=9, Na=1
Ba=-1 (1 связь Ge-Ge)
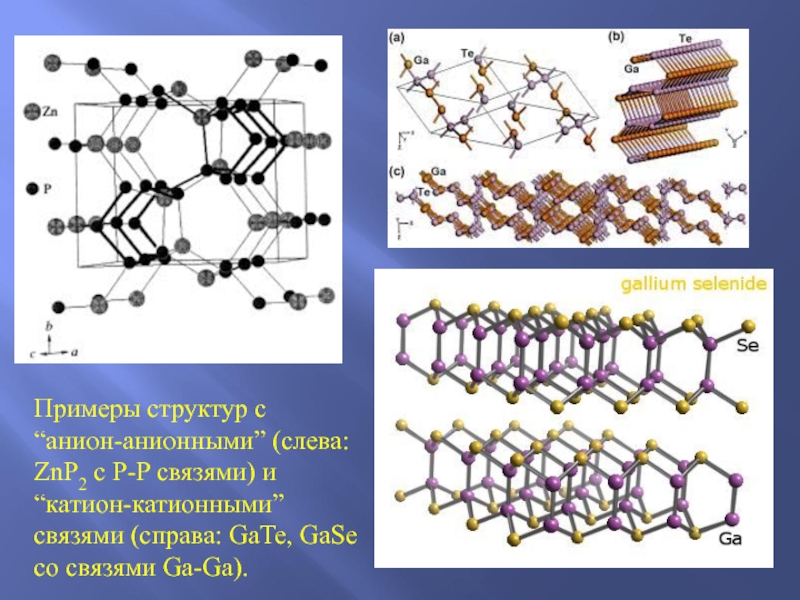
Слайд 56Примеры структур с “анион-анионными” (слева: ZnP2 с P-P связями) и
“катион-катионными” связями (справа: GaTe, GaSe со связями Ga-Ga).
Слайд 57Генезис различных фаз по типу усложнения химического взаимодействия:
РасслоениеЭвтектикаОграниченные тв. р-ры
неограниченный ряд твердых растворов
Соединенрия КурнаковаФазы Лавеса
Фазы внедрения (Хэгга)
Соединения Юм-РозериИнтеркалированные
соединенияФазы ЦинтляВалентные соединения Соединения высших порядков (комплексные соединения)






![Непрерывные твердые растворы
случай без точек конгруэнтного плавления Природная эвтектика:SiO2-K[AlSi3O8]; скол еврейского гранита Результаты различных фазовых превращений в природных системах (породах и минералах) Природная эвтектика:SiO2-K[AlSi3O8]; скол еврейского гранита Результаты различных фазовых превращений в природных системах (породах и минералах)](/img/thumbs/412a66e99be5f43532f90846bee9ea90-800x.jpg)