Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Обмен нуклеотидов
Содержание
- 1. Обмен нуклеотидов
- 2. Лекция 16. Обмен нуклеотидов
- 3. Актуальность темыНуклеотиды и их производные выполняют многообразные
- 4. План лекцииОбразование фосфорибозилдифосфата (ФРДФ) – ключевой момент
- 5. Цель лекцииЗнать:Основные метаболические пути превращения пуриновых и
- 6. Вспомните самостоятельно из курса химииПуриновые и пиримидиновые
- 7. Структура нуклеотидаКомпоненты нуклеотида:АЗОТИСТОЕ ОСНОВАНИЕ (АО) (циклические соединения,
- 8. Азотистые основания
- 9. Пентозы
- 10. Образование фосфорибозилдифосфата (ФРДФ)Почти все клетки способны к
- 11. Синтез пуриновых нуклеотидов (см. схему синтеза на
- 12. Слайд 12
- 13. Происхождение атомов С и N в пуриновом основании
- 14. Образование АМФ и ГМФ из ИМФ Образование
- 15. Слайд 15
- 16. Ферменты синтеза АМФ И ГМФ: подписи к
- 17. Регуляция синтеза пуриновых нуклеотидовАллостерические ферменты:ФРДФ-синтазаАмидофосфорибозилтрансферазаИМФ-дегидрогеназаАденилосукцинатсинтетазаОтрицательные эффекторы: АМФ, ГМФ
- 18. Запасные пути синтеза пуриновых нуклеотидов :
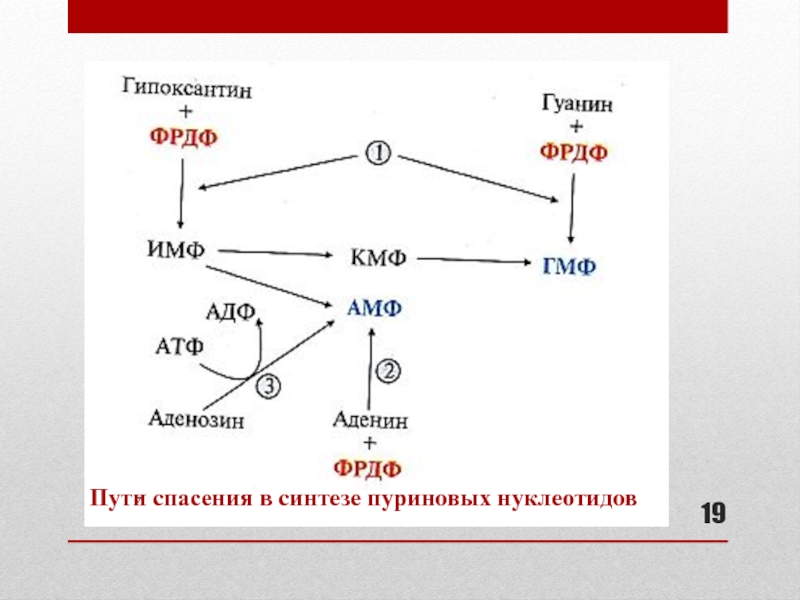
- 19. Пути спасения в синтезе пуриновых нуклеотидов
- 20. Ферменты «пути спасения» в синтезе пуриновых нуклеотидов К слайду 19:1 – гипоксантин-гуанинфосфорибозилтрансфераза2 – аденинфосфорибозилтрансфераза3 - аденозинкиназа
- 21. Катаболизм пуриновых нуклеотидовСхема реакций катаболизма представлена на
- 22. Схема реакций катаболизма пуриновых нуклеотидов
- 23. Ферменты катаболизма пуриновых нуклеотидовК слайду 22:1 –
- 24. Нарушения обмена пуриновых нуклеотидовПричина: дефект генов ферментовгиперактивация,
- 25. Синтез пиримидиновых нуклеотидовОсновные этапы синтеза:Формирование пиримидинового кольца
- 26. Образование оротата и УМФглутамин + СО2 +
- 27. Нарушения образования оротатаМутация в гене УМФ-синтазы приводит
- 28. Фосфорилирование УМФ и образование ЦТФФосфорилирование УМФ: образование
- 29. Регуляция синтеза пиримидиновых нуклеотидовАллостерическая регуляция по механизму
- 30. Запасные пути синтеза пиримидиновых нуклеотидовЗапасные пути синтеза
- 31. Катаболизм пиримидиновых нуклеотидовОтщепление остатков фосфорной кислоты и
- 32. Образование дезоксирибонуклеотидовВнутриклеточная концентрация дезоксирибонуклеотидов низкая Активность процесса
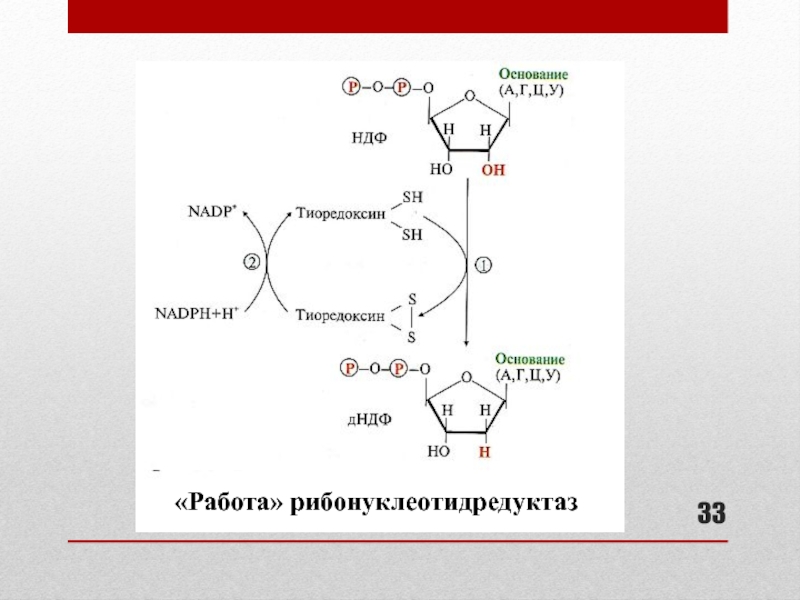
- 33. «Работа» рибонуклеотидредуктаз
- 34. Регуляция активности рибонуклеотидредуктазного комлпексаКоличество ферментов комплекса зависит
- 35. ИммунодефицитыВозникают при ингибировании работы РНР-комплекса вследствие:1) недостаточности
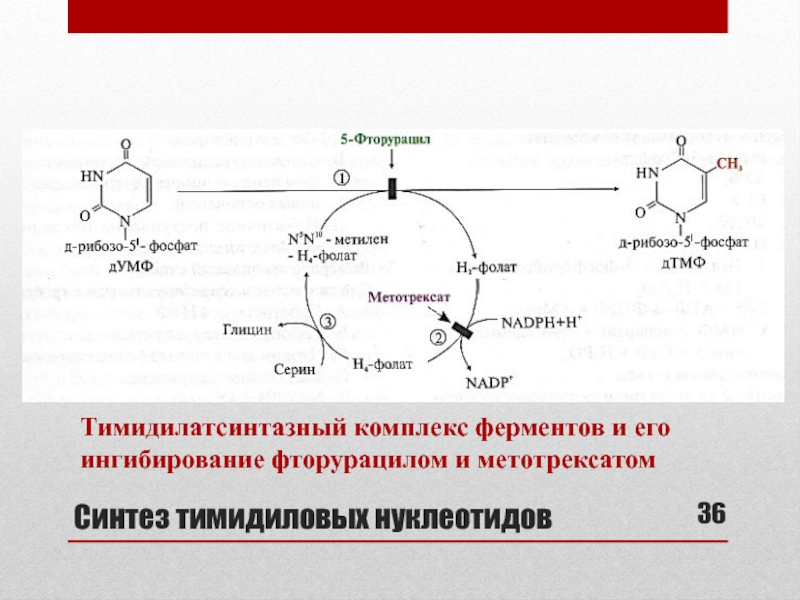
- 36. Синтез тимидиловых нуклеотидовТимидилатсинтазный комплекс ферментов и его ингибирование фторурацилом и метотрексатом
- 37. Тимидилсинтаза и запасные пути синтезаТимидилатсинтаза (включение одноуглеродного
- 38. Задание для самостоятельной работыИзучить информацию по теме:
- 39. ЗаключениеБольшая часть используемых в клетках нуклеотидов синтезируется
- 40. ЛитератураБиохимия: учебник для ВУЗов / Е. С.
- 41. Скачать презентанцию
Лекция 16. Обмен нуклеотидов
Слайды и текст этой презентации
Слайд 1
Обмен нуклеотидов
Дисциплина: биохимия (Б1.Б.15)
Специальность: 31.05.02 педиатрия
НГМУ, кафедра медицинской химии
Д.б.н.,
доцент Суменкова Дина Валерьевна
Слайд 3Актуальность темы
Нуклеотиды и их производные выполняют многообразные функции в организме
человека: участвуют в синтезе нуклеиновых кислот, нуклеотидных коферментов (NAD, NADP,
FAD, FMN), участвуют в образовании активных форм углеводов (УДФ-глюкоза), аминокислот (SAM), «энергетических молекул» (АТФ, ГТФ), участвуют в передаче сигнала гормонов в клетку (цАМФ, цГМФ).Нарушение процессов обмена нуклеотидов лежит в основе патогенеза некоторых заболеваний человека (подагра, мегалобластная анемия, иммунодефицитные состояния).
В основе механизма действия ряда противовирусных и противоопухолевых препаратов лежит ингибирование процессов синтеза нуклеотидов.
Слайд 4План лекции
Образование фосфорибозилдифосфата (ФРДФ) – ключевой момент в синтезе нуклеотидов
Синтез
и катаболизм пуриновых нуклеотидов: ход процесса, регуляция, «запасные» пути синтеза.
Нарушения обмена пуриновых нуклеотидовСинтез и катаболизм пиримидиновых нуклеотидов: ход процесса, регуляция, «запасные» пути синтеза. Нарушения обмена пиримидиновых нуклеотидов
Образование дезоксирибонуклеотидов
Синтез нуклеотидов – мишень действия лекарственных препаратов (задание для самостоятельной работы, см. слайд 38)
Слайд 5Цель лекции
Знать:
Основные метаболические пути превращения пуриновых и пиримидиновых нуклеотидов
Знания об
обмене нуклеотидов необходимы для понимания:
механизмов возникновения заболеваний у детей и
подростков, связанных с нарушением синтеза и катаболизма нуклеотидовмеханизма действия противоопухолевых и противовирусных лекарственных препаратов – ингибиторов синтеза нуклеотидов
Слайд 6Вспомните самостоятельно
из курса химии
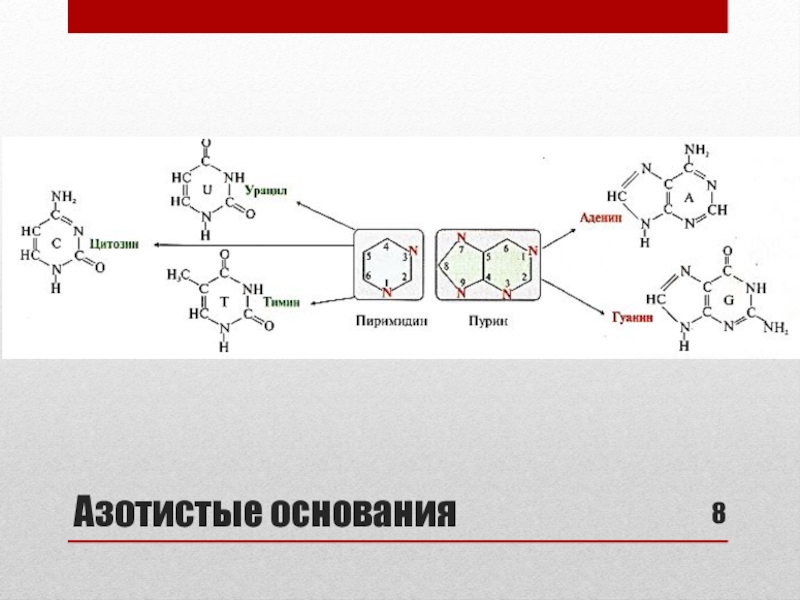
Пуриновые и пиримидиновые азотистые основания
Структура пуриновых и
пиримидиновых рибо- и дезоксирибонуклеотидов нуклеотидов
Виды химических связей в нуклеотидах
Роль нуклеотидов
в организме человекаСлайд 7Структура нуклеотида
Компоненты нуклеотида:
АЗОТИСТОЕ ОСНОВАНИЕ (АО) (циклические соединения, производные пурина или
пиримидина)
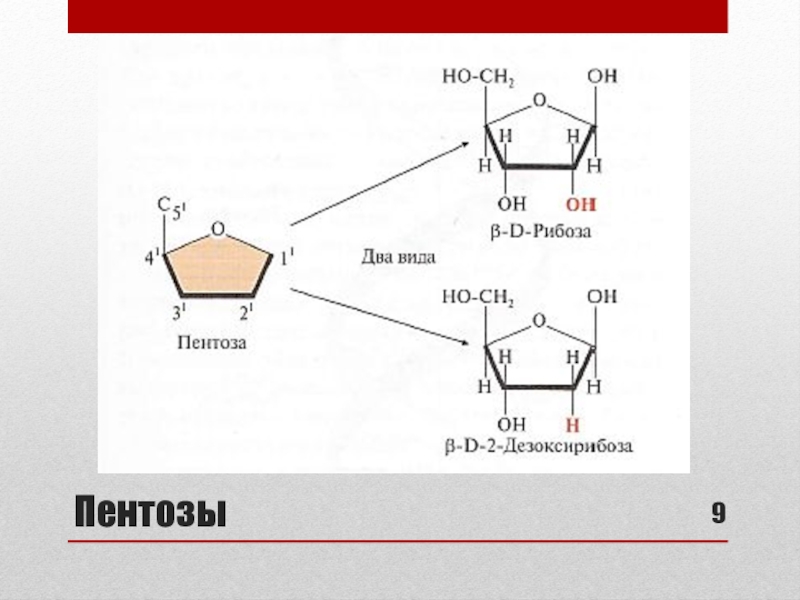
ПЕНТОЗА (рибоза или дезоксирибоза)
ОСТАТОК ФОСФОРНОЙ КИСЛОТЫ (нуклеотид моно-, ди- или
трифосфаты)Виды химических связей между компонентами нуклеотида:
N-гликозидная связь между АО (N9 у пуриновых и N1 у пиримидиновых) и пентозой (1᾽)
5᾽ -фосфоэфирная связь между пентозой и фосфорной кислотой
Слайд 10Образование фосфорибозилдифосфата (ФРДФ)
Почти все клетки способны к синтезу нуклеотидов.
Продукты расщепления
нуклеиновых кислот тканей и пищи используются повторно в незначительной степени.
Образование
ФРДФ – центральное место в синтезе пуриновых и пиримидиновых нуклеотидовИсточник образования ФРДФ: рибозо-5-фосфат
(продукт ПФП окисления глюкозы)
рибозо-5-фосфат + АТФ → 5-фосфорибозил-1-дифосфат + АМФ (ФРДФ синтаза)
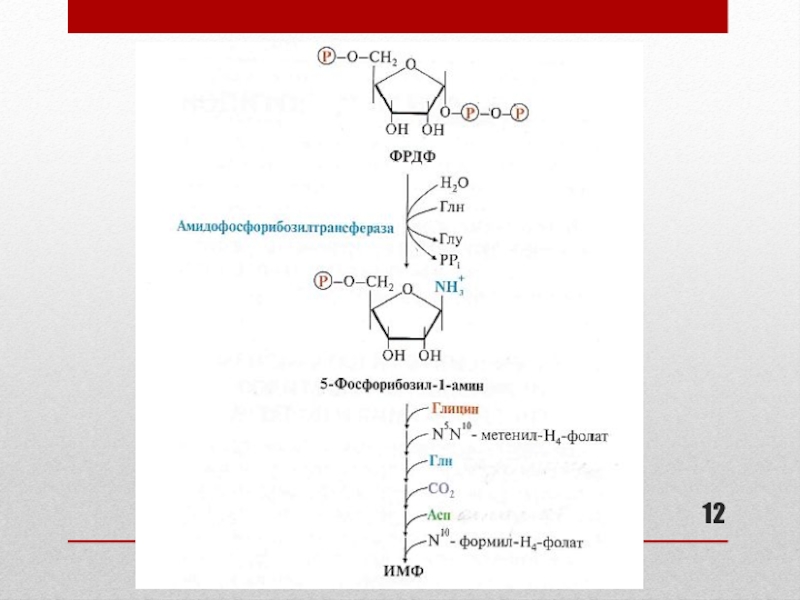
Слайд 11Синтез пуриновых нуклеотидов
(см. схему синтеза на след. слайде)
Сборка пуринового гетероциклического
основания осуществляется на ФРДФ при участии глицина, глутамина, аспартата, СО2
и одноуглеродных производных Н4-фолата в цитозоле:формирование 5-членного кольца
формирование 6-членного кольца
образование первого пуринового нуклеотида – инозинмонофосфата (ИМФ: гипоксантин – рибоза – фосфат)
Синтез ИМФ включает 10 стадий и требует затрат 6 АТФ
образование АМФ и ГМФ из ИМФ путем присоединения аминогруппы к 6С с образованием аденина (источник аминогруппы – аспартат) или к 2С с образованием гуанина (источник аминогруппы – глутамин)
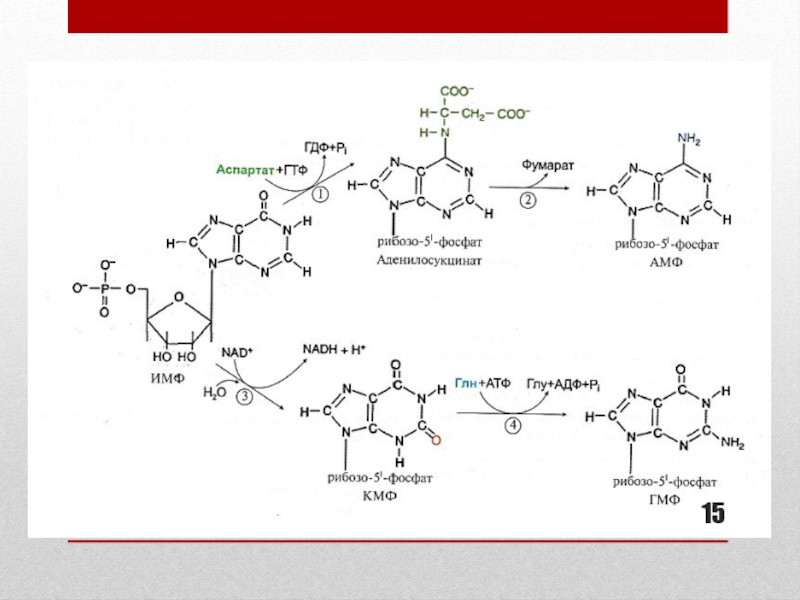
Слайд 14Образование АМФ и ГМФ из ИМФ
Образование АДФ, ГДФ, ГТФ
В образовании
АМФ из ИМФ участвует аспартат
В образовании ГМФ из ИМФ
участвует глутаминСхема реакций представлена на след. слайде.
Нуклеозидди- и трифосфаты синтезируются при участии АТФ и киназ:
АМФ + АТФ ↔ 2АДФ (аденилаткиназа)
ГМФ + АТФ → ГДФ + АДФ (гуанилаткиназа)
ГДФ + АТФ → ГТФ + АДФ
Внимание! Образование АТФ происходит путем субстратного (в процессе гликолиза, цикла Кребса)
и окислительного (в процессе тканевого дыхания) фосфорилирования АДФ
Слайд 16Ферменты синтеза АМФ И ГМФ:
подписи к схеме слайда 15.
В синтезе
АМФ из ИМФ участвуют ферменты:
1 – аденилосукцинатсинтетаза
2 – аденилосукциназа
В синтезе
ГМФ из ИМФ участвуют ферменты:3 – ИМФ-дегидрогеназа
4 – ГМФ-синтетаза
КМФ – ксантозин-5-монофосфат
Слайд 17Регуляция синтеза пуриновых нуклеотидов
Аллостерические ферменты:
ФРДФ-синтаза
Амидофосфорибозилтрансфераза
ИМФ-дегидрогеназа
Аденилосукцинатсинтетаза
Отрицательные эффекторы: АМФ, ГМФ
Слайд 18Запасные пути синтеза пуриновых нуклеотидов : «пути спасения»
В период
активного роста тканей синтез пуриновых нуклеотидов из простых предшественников не
способен полностью обеспечить нуклеиновые кислоты субстратами, поэтому в этих условиях важную роль играют запасные пути, или «пути спасения»Для синтеза нуклеотидов по «пути спасения» используются азотистые основания и нуклеозиды, образующиеся в процессе катаболизма нуклеиновых кислот
Слайд 20Ферменты «пути спасения» в синтезе пуриновых нуклеотидов
К слайду 19:
1
– гипоксантин-гуанинфосфорибозилтрансфераза
2 – аденинфосфорибозилтрансфераза
3 - аденозинкиназа
Слайд 21Катаболизм пуриновых нуклеотидов
Схема реакций катаболизма представлена на следующих слайдах
Терминальный фермент
катаболизма: ксантиноксидаза (аэробная дегидрогеназа); кофакторы: Fe 3+, Мо 2+, FAD
Конечный
продукт: мочевая кислотаобразуется в основном в печени и кишечнике
выводится с мочой и через кишечник
слабая кислота: в биологических жидкостях находится в комплексе с белками или в виде натриевой соли (ураты)
в крови: 0,15 – 0,47 ммоль/л (3-7 мг/дл)
выводится в сутки: 0,4 – 0,6 г мочевой кислоты и уратов
Слайд 23Ферменты катаболизма пуриновых нуклеотидов
К слайду 22:
1 – фосфатаза (нуклеотидаза)
2 –
аденозиндезаминаза
3 – пуриннуклеозидфосфорилаза
4 – гуаназа
5 - ксантиноксидаза
Слайд 24Нарушения обмена пуриновых нуклеотидов
Причина: дефект генов ферментов
гиперактивация, или устойчивость ФРДФ-синтазы
к аллостерическим ингибиторам
снижение активности гипоксантин-гуанинфосфорибозилтрансферазы (отсутствие активности вызывает тяжелое заболевание
синдром Леша-Нихена, сопровождающееся психическими отклонениями)Проявления: гиперурикемия
Длительная гиперурикемия вызывает подагру (отложение мочевой кислоты в суставах)
Аллопуринол (лекарственный препарат) – структурный аналог гипоксантина - используется в лечении подагры.
Каков механизм действия препарата?
Катаболизм пуринов останавливается на стадии гипоксантина, который лучше растворяется в жидкостях организма, чем мочевая кислота.
Слайд 25Синтез пиримидиновых нуклеотидов
Основные этапы синтеза:
Формирование пиримидинового кольца (оротата) из глутамина,
аспартата, СО2
Образование нуклеотида ОМФ путем переноса фосфорибозила с ФРДФ на
оротат (ОМФ: оротат – рибоза – фосфат)Образование нуклеотида УМФ путем декарбоксилирования оротата в составе ОМФ (при декарбоксилировании оротата образуется урацил)
Фосфорилирование УМФ с образованием УТФ (источник фосфата – АТФ)
Образование ЦТФ из УТФ путем присоединения аминогруппы к урацилу (источник аминогруппы – глутамин)
Слайд 26Образование оротата и УМФ
глутамин + СО2 + 2 АТФ +
Н2О → карбамоилфосфат + 2 АДФ + Рi (карбамоилфосфатсинтетаза II)
присоединение
аспартата (образование карбамоиласпартата), отщепление воды (образование циклического дигидрооротата)Данные реакции катализирует мультиферментный комплекс КАД-фермент:
карбамоилфосфатсинтетаза
аспартаттранскарбамоилаза
дигидрооротаза
окисление дигидрооротата при участии дигидрооротатдегидрогеназы (NAD-дегидрогеназа) с образованием оротата
перенос фосфорибозила с ФРДФ на оротат с образованием ОМФ и декарбоксилирование оротидинфосфата с образованием УМФ (УМФ-синтаза: трансфераза и декарбоксилаза)
Слайд 27Нарушения образования оротата
Мутация в гене УМФ-синтазы приводит к нарушению образования
УМФ из оротата и вызывает наследственное заболевание, которое сопровождается оратацидурией
Клинические
проявления: мегалобластная анемия, нарушение работы ЖКТ, сердца, интеллектуальной и двигательной активностиПричина проявлений: «пиримидиновый голод», нарушение синтеза нуклеиновых кислот и деления клеток
Для лечения применяют уридин или цитидин (нуклеозиды: азотистое основание + рибоза), которые используются в «запасных» путях синтеза УМФ и ЦМФ путем фосфорилирования при участии АТФ
Слайд 28Фосфорилирование УМФ и
образование ЦТФ
Фосфорилирование УМФ: образование УТФ
УМФ + АТФ →
УДФ + АДФ
УДФ + АТФ → УТФ + АДФ
Реакции
катализируют киназыОбразование ЦТФ:
УТФ + глутамин + АТФ → ЦТФ + глутамат + АДФ +H3PO4
(ЦТФ синтетаза)
Слайд 29Регуляция синтеза пиримидиновых нуклеотидов
Аллостерическая регуляция по механизму отрицательной обратной связи:
УТФ
ингибирует КФС II в составе КАД-фермента
УМФ и ЦМФ ингибируют УМФ-синтазу
ЦТФ
ингибирует ЦТФ-синтетазуСлайд 30Запасные пути синтеза пиримидиновых нуклеотидов
Запасные пути синтеза пиримидиновых нуклеотидов не
играют существенной роли:
Урацил или Цитозин + ФРДФ → УМФ или
ЦМФ + РРi (пиримидинфосфорибозилтрансфераза)Урацил + рибозо-1-фосфат → уридин + H3PO4 (уридинфосфорилаза)
Уридин + АТФ → УМФ + АДФ (уридинкиназа)
Слайд 31Катаболизм пиримидиновых нуклеотидов
Отщепление остатков фосфорной кислоты и рибозы (аналогично катаболизму
пуриновых нуклеотидов)
Пиримидиновые основания разрушаются ферментными системами: например
Цитозин → СО2 +
NH3 + бета-аланинКонечные продукты – растворимы в воде
Бета-аланин включается в состав карнозина и ансерина (мышечные пептиды, антиоксиданты)
Слайд 32Образование дезоксирибонуклеотидов
Внутриклеточная концентрация дезоксирибонуклеотидов низкая
Активность процесса их образования повышается
перед делением клеток во время репликации (дезоксирибонуклеотиды необходимы только для
репликации)Образование дНДФ (А, Г, Ц, У) из НДФ
Образование дТМФ из дУМФ
2 ферментных комплекса:
Рибонуклеотидредуктаза (РНР) (восстановление рибонуклеотидов АДФ, ГДФ, ЦДФ, УДФ с образованием дезоксипроизводных) включает:
рибонуклеотидредуктаза (разные формы для определенных нуклеотидов)
белок-восстановитель тиоредоксин
тиоредоксинредуктаза
Тимидилатсинтаза (для образования дТМФ)
Слайд 34Регуляция активности рибонуклеотидредуктазного комлпекса
Количество ферментов комплекса зависит от скорости синтеза
ДНК (регуляция по механизму индукции)
Аллостерическая регуляция:
Отрицательные эффекторы: дНТФ
дАТФ – ингибитор
восстановления всех рибонуклеотидовдГТФ – ингибитор восстановления пиримидиновых НДФ
Слайд 35Иммунодефициты
Возникают при ингибировании работы РНР-комплекса вследствие:
1) недостаточности аденозиндезаминазы (см. катаболизм
АМФ)
В этом случае, накопление дАТФ приводит к ингибированию РНР
и лишает клетки-предшественники В и Т-лимфоцитов образования дезоксирибонуклеотидов (пуриновых и пиримидиновых). Нарушается синтез ДНК, деление клеток. Возникают тяжелые формы клеточного и гуморального иммунодефицита. Дети погибают от частых инфекций.2) недостаточность пуриннуклеозидфосфорилазы (см. катаболизм ГМФ)
В этом случае, накопление дГТФ приводит к ингибированию РНР и нарушению синтеза пиримидиновых дезоксирибонуклеотидов. Снижается клеточный иммунитет. Больные страдают частыми инфекционными заболеваниями.
Слайд 36Синтез тимидиловых нуклеотидов
Тимидилатсинтазный комплекс ферментов и его ингибирование фторурацилом и
метотрексатом
Слайд 37Тимидилсинтаза и запасные пути синтеза
Тимидилатсинтаза (включение одноуглеродного радикала в дУМФ
путем переноса СН2 с метилен-Н4-фолата)
Дигидрофолатредуктаза
Сериноксиметилтрансфераза (перенос оксиметильной группы с серина
на Н4-фолат с образованием метилен-Н4-фолата)Запасные пути синтеза:
Тимидин + АТФ → дТМФ + АДФ (тимидинкиназа)
Слайд 38Задание для самостоятельной работы
Изучить информацию по теме: «Ферменты синтеза нуклеотидов
– мишени действия противоопухолевых и противовирусных препаратов» (см. литературу)
Составить таблицу
(препарат – механизм действия – область применения) и охарактеризовать препараты: фторурацил, метотрексат, ацикловир, азидотимидинСлайд 39Заключение
Большая часть используемых в клетках нуклеотидов синтезируется de novo из
простых предшественников (с участием аминокислот, производных фолиевой кислоты). Центральное место
в синтезе нуклеотидов занимает образование фосфорибозилдифосфата.«Запасные» пути синтеза (из имеющихся в клетке азотистых оснований и нуклеозидов) играют важную роль в образовании пуриновых нуклеотидов.
Нарушение метаболизма пуриновых нуклеотидов лежит в основе патогенеза подагры, синдрома Леша-Нихена. Нарушение синтеза пиримидиновых нуклеотидов лежит в основе патогенеза мегалобластной анемии.
Механизм действия ряда противовирусных и противоопухолевых лекарственных препаратов связан с нарушением синтеза нуклеотидов.
Слайд 40Литература
Биохимия: учебник для ВУЗов / Е. С. Северин -М.: ГЭОТАР-Медиа,
2014. -768 с. (раздел 10)
Биологическая химия с упражнениями и задачами: учебник
/ ред. С. Е. Северин. - М. : ГЭОТАР-Медиа, 2013. - 624 с. (С. 476 – 495, для выполнения самостоятельной работы «Лекарственные препараты-ингибиторы синтеза нуклеотидов» см. С. 487)Биологическая химия: учебник для студентов медицинских вузов / А.Я. Николаев. – М.: Мед. информ. агенство, 2007. – 568 с.