Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ОБЩИЕ СВОЙСТВА МЕТАЛЛОВ. СПЛАВЫ. ПЛАН 1. Введение. Классификация металлов. 2
Содержание
- 1. ОБЩИЕ СВОЙСТВА МЕТАЛЛОВ. СПЛАВЫ. ПЛАН 1. Введение. Классификация металлов. 2
- 2. характерные признаки:металлы тяжелее воды
- 3. GaCsHgБольшинство - твердые вещества при комнатной температуре, но есть и жидкие:
- 4. Большинство имеют металлический блеск, серые или белыеCs кристаллыCu самородокAu самородок
- 5. КЛАССИФИКАЦИЯ МЕТАЛЛОВ1. Черные и цветные2. Тяжелые (ƍ≥5
- 6. ЧерныеПолучено электро-лизом, чистота 99,97%Fe
- 7. ЦветныеAgBiRbSnTi
- 8. ТяжелыеFeHgPbBi
- 9. ТяжелыеCoSbNi99,99%Медленный электролиз
- 10. ЛегкиеLi, K, Na, Rb, Cs, Fr, Be, Mg, Ca, Sr, Ba, Al, Sn AlCaRbMg«осч»
- 11. ДРАГОЦЕННЫЕAgAu
- 12. Платиновые металлыOsRhPt
- 13. РедкоземельныеLa
- 14. EuYSc
- 15. Металлы: s-, d-, f- элементы, а также
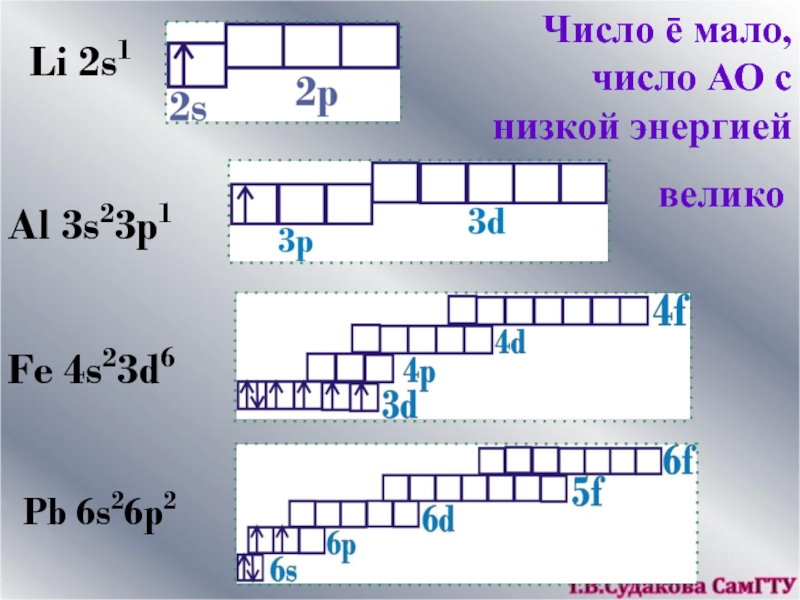
- 16. Li 2s1Al 3s23p1Fe 4s23d6Pb 6s26p2
- 17. В кристаллах металлов АО перекрывают-ся Единая 3-мерная АО, в пределах которой движутся вален-тные ē
- 18. Слайд 18
- 19. КЧ = 812Металлическая связь ненаправленная, поэтому большие значения координационных чисел объемно-центрирован-наякубические:гране-центрирован-наягексагональная плотная упаковкаКЧ=8КЧ=12КЧ=12
- 20. ХИМИЧЕСКИЕ СВОЙСТВАОбщие:1. Малая электроотрицательность (ЭО).2. Ме в
- 21. Металлы p- и d-элементы:Низшая СО +1, +2
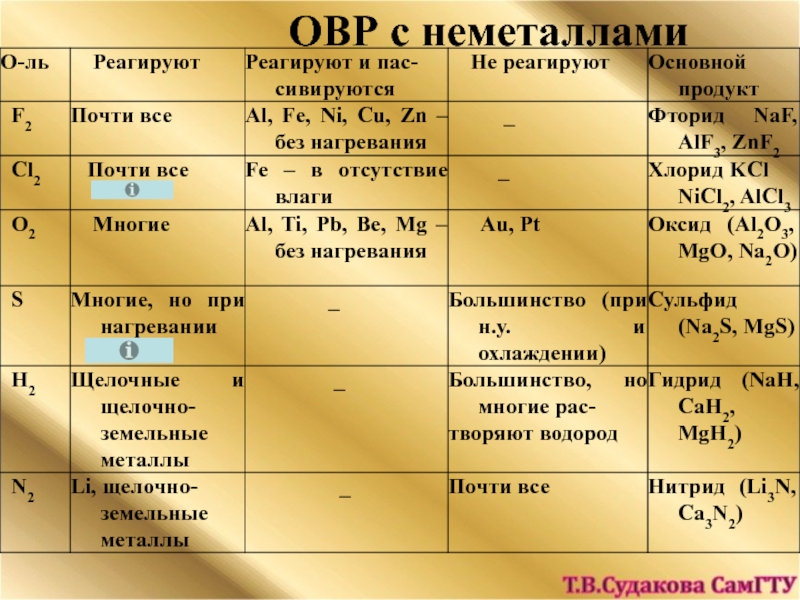
- 22. ОВР с неметаллами
- 23. Отношение металлов к воде и водным растворам
- 24. взаимодействие с водой -это ОВР, где окислитель
- 25. Ме0 + ОН– → МеО2– + Н2 Ме0
- 26. Наиболее типичная реакция:Ме0 + 2Н+ → Ме2+
- 27. Оксидные: Fe2O3 - гематит, Fe2O3•H2O – гетит,
- 28. гематит Fe2O3боксит Al2O3касситерит SnO2
- 29. пирит FeS2 халькопирит Cu2S•FeS2
- 30. Общие методы получения: Вытеснение металла более активным
- 31. 3V2O5 (к) + 10Al(к) →5Al2O3(к) + 6V(к)TiCl4
- 32. Восстановление неметаллами -пирометаллургия -только при высоких температурахMgO
- 33. электролиз водных растворов или расплавов: NaCl
- 34. макрогомогенная система, обладающая металлическими свойствами и состоящая
- 35. однородное (гомогенное) кристал-лическое вещество переменного состава, в
- 36. типы твердых раствороврастворы замещениярастворы внедренияупорядоченные растворыCu -
- 37. Очень сильное взаимодействие между атомами металловИнтерметаллические соединения
- 38. Манганин – сплав 11% Mn, 2,5-3,5% Ni
- 39. Слайд 39
- 40. сплав Fe с С (3,5-5,5%) и Mn
- 41. Обычная углеродистаянержавеющаяКровля, до 25 лет
- 42. литьеСталь 35ГПовышенная твердость и износостойкостьщеки дробилокбашня танка
- 43. высокое электрическое сопротивление, самые «тихие» сплавы:
- 44. Бронза: оловянная – Cu-Snалюминиевая – Cu-Alбериллиевая – Cu-Be и т.п.Самая древняя !
- 45. Нейзильбер:
- 46. Слайд 46
- 47. Поверхность супер-сплава под микроскопом:упорядоченная -фазахаотичная
- 48. скалывающая силадислокацияstopНарушение порядка требует дополнительной энергии!!!Неупорядоченный кристаллУпорядоченный кристалл
- 49. Сверхпластичностьзерна < 5 мкм, под нагрузкой скользят
- 50. Чем больше S поверхности частиц (наноразмеры), тем
- 51. аморфные металлыСверхбыстрое охлаждениеТолько ближний порядок в структуре
- 52. 1976г. - лента аморфного магнитного сплава Ni-Fe-P-B
- 53. тарелки с нагревательным контуром из тонких металлических
- 54. Источники информации:Фролов В.В. Химия. М.: Высшая школа.
- 55. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1ОБЩИЕ СВОЙСТВА МЕТАЛЛОВ. СПЛАВЫ.
ПЛАН
1. Введение. Классификация металлов.
2. Металлическая связь.
3. Химические
свойства.
Слайд 5КЛАССИФИКАЦИЯ МЕТАЛЛОВ
1. Черные и цветные
2. Тяжелые (ƍ≥5 г\см3) и легкие
(ƍ≤5г\см3)
3. Драгоценные
4. Платиновые
5. Редкоземельные
Благородные
металлы
Y, Sc, La и лантаноиды
Слайд 15Металлы: s-, d-, f- элементы, а также небольшое количество p-
элементов – Al, Ga, In, Tl, Sn, Pb, Bi.
Металлическая связьХИМИЧЕСКИЕ И ФИЗИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ
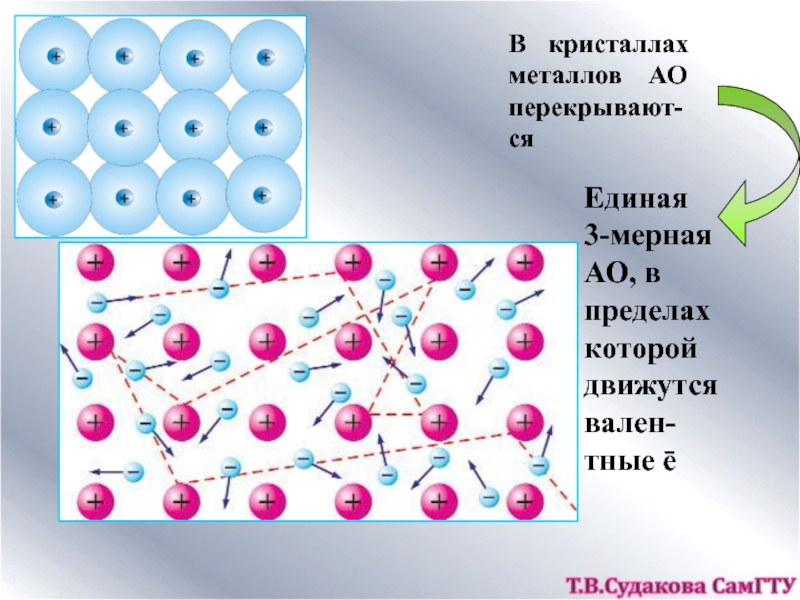
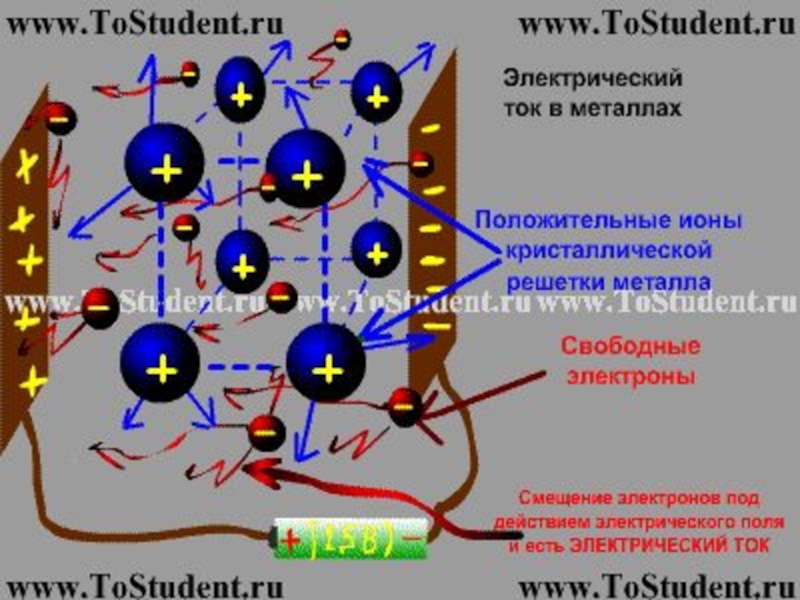
Слайд 17В кристаллах металлов АО перекрывают-ся
Единая 3-мерная АО, в пределах
которой движутся вален-тные ē
Слайд 19КЧ = 812
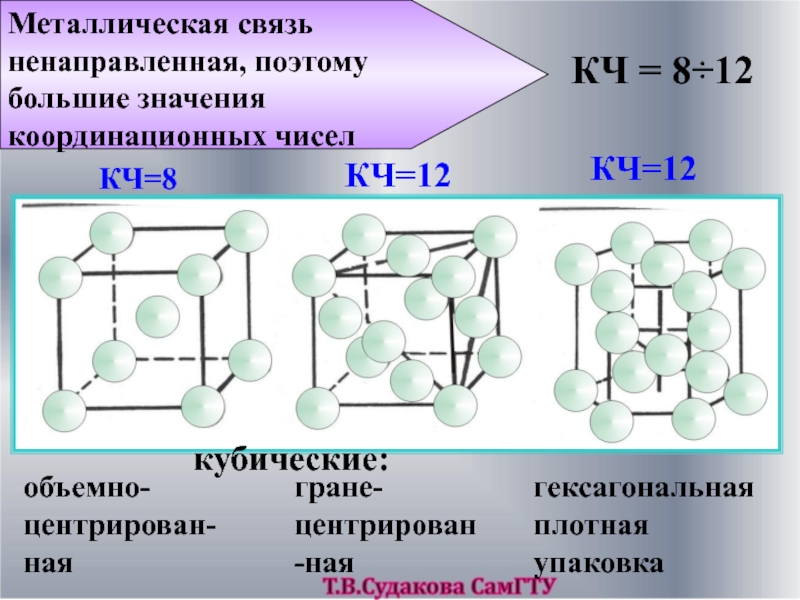
Металлическая связь ненаправленная, поэтому большие значения координационных чисел
объемно-центрирован-ная
кубические:
гране-центрирован-ная
гексагональная плотная упаковка
КЧ=8
КЧ=12
КЧ=12
Слайд 20ХИМИЧЕСКИЕ СВОЙСТВА
Общие:
1. Малая электроотрицательность (ЭО).
2. Ме в реакциях образуют только
катионы:
Me0 ─ nē → Men+
Металлы – s-элементы:
СО = +1
и +2Образуют основные оксиды и гидроксиды
Li2O, LiOH, K2O, KOH, CaO, Ca(OH)2, SrO, Sr(OH)2
Слайд 21Металлы p- и d-элементы:
Низшая СО +1, +2
Основные оксиды и
гидроксиды
Промежуточ-ная СО +3, +4
Высшая СО +4, +5, +6, +7, +8
Амфотер-ные
Кислотные
оксиды и гидроксидыPbO, Pb(OH)2, CuO, Cu(OH)2, CrO, Cr(OH)2, MnO, Mn(OH)2
Al2O3, Al(OH)3, Cr2O3, Cr(OH)3, Mn2O3, Mn(OH)3, MnO2, Mn(OH)4
OsO4, Mn2O7, HMnO4, H2MnO4, MnO3, Mn2O5, HMnO3, CrO3, H2CrO4
Слайд 23Отношение металлов к воде и водным растворам окислителей
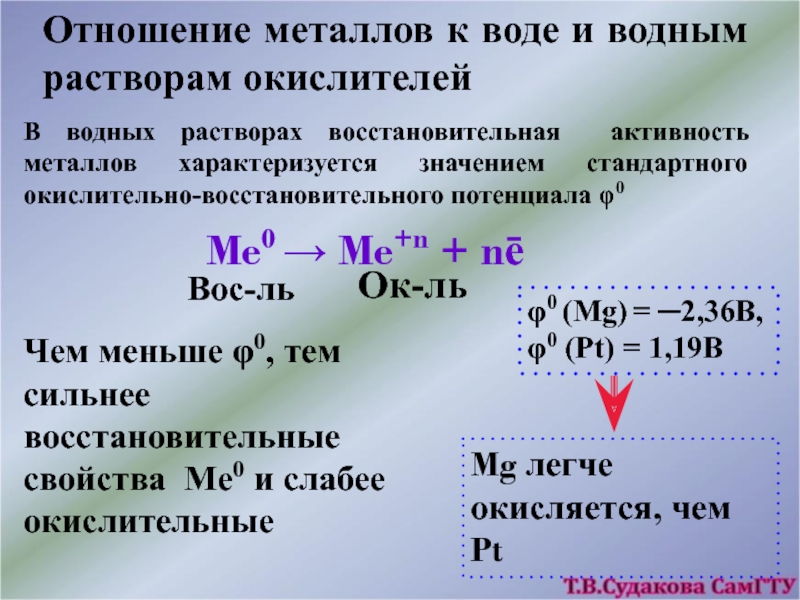
В водных растворах
восстановительная активность металлов характеризуется значением стандартного окислительно-восстановительного потенциала φ0
Me0 →
Me+n + nēВос-ль
Ок-ль
Чем меньше φ0, тем сильнее восстановительные свойства Ме0 и слабее окислительные
φ0 (Mg) = ─2,36B, φ0 (Pt) = 1,19В
Mg легче окисляется, чем Pt
Слайд 24взаимодействие с водой -
это ОВР, где окислитель Н+
φ(2Н+/Н2) = -
0,059•рН = 0,059•7 = -0,413В
2Н2О + 2ē = 2ОН─
+ Н2─0,413<0
Легче идет реакция 2ОН─ +Н2 ─ 2ē = 2Н2О
Слайд 25Ме0 + ОН– → МеО2– + Н2
Ме0 + Н2О +
ОН– → [Ме(ОН)4]– + Н2
Взаимодействие со щелочами:
Реагируют только металлы, образующие
амфотерные оксиды:Be + 2NaOH + 2H2O = Na2[Be(OH)4] + H2
2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2
Sn + 2NaOH = Na2SnO2 + H2
Ок-ль Н+: 2Н2О + 2ē = 2ОН─ + Н2
При рН=14 φ(2Н2О/Н2) = -0,059•14 = -0,83 В
φ0(Be) = -1,85B, φ0(Al) = -1,62B, φ0(Sn) = -0,14B
сплавление
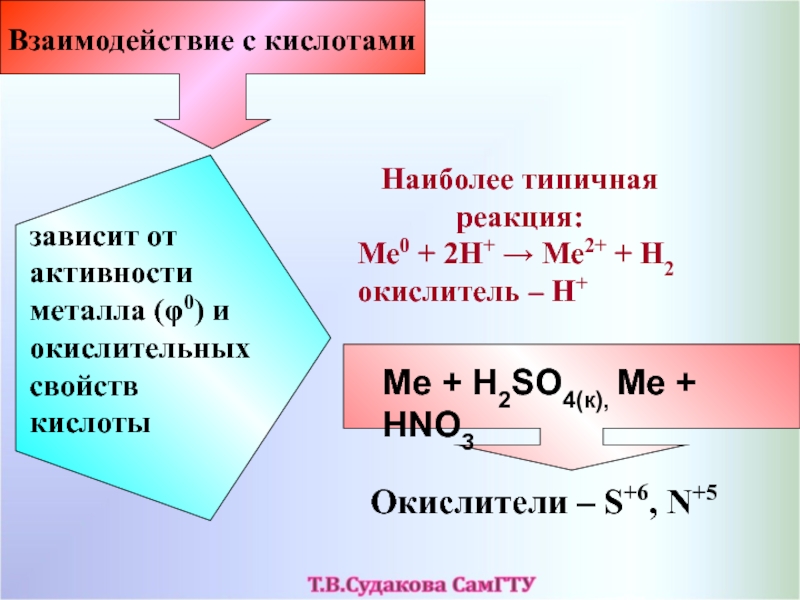
Слайд 26Наиболее типичная реакция:
Ме0 + 2Н+ → Ме2+ + Н2
окислитель – Н+
Взаимодействие с кислотами
зависит от активности металла (φ0) и
окислительных свойств кислотыMe + H2SO4(к), Me + HNO3
Окислители – S+6, N+5
Слайд 27Оксидные: Fe2O3 - гематит, Fe2O3•H2O – гетит, Al2O3 – боксит,
TiO2 – рутил, SnO2 – касситерит;
Карбонатные: CaCO3 - мрамор, мел,
известняк; MgCO3 - магнезит, CuCO3•Cu(OH)2 – малахит; Сульфидные: FeS2 – железный колчедан (пирит), Cu2S•FeS2 – медный колчедан (халькопирит), PbS – свинцовый блеск, ZnS – цинковая обманка
Силикатные и алюмосиликатные: полевой шпат K2O•Al2O3•6SiO2, каолинит Al2O3•2SiO2•2H2O, берилл 3BeO•Al2O3•6SiO2;
Галидные: NaCl - каменная или поваренная соль, KCl - сильвин, KCl•MgCl2•6H2O – карналлит.
Руды – природные соединения металлов
Слайд 30Общие методы получения:
Вытеснение металла более активным металлом.
Восстановление металлов
неметаллами - газообразными СО и Н2 или твердым углеродом С.
Электрометаллургия - электролиз либо водных растворов либо расплавов.
Слайд 313V2O5 (к) + 10Al(к) →5Al2O3(к) + 6V(к)
TiCl4 (к) + 4Na
(к) → Ti (к) + 4NaCl (к)
Вытеснение металлами:
гидрометаллургия
металлотермия
водный р-р
2[Au(CN)2]– +
Zn → [Zn(CN)4]2– + 2Auпри нагревании
700-900оС
Слайд 32Восстановление неметаллами -
пирометаллургия -только при высоких температурах
MgO + C =
CO + Mg
Sb2O4 + 4C = 2Sb + 4CO
SnO2 + 2C = Sn + 2CO
PbO + CO = Pb + CO2
Fe2O3 + 3H2 = 2Fe + 3H2O
MoO3 + 3H2 = Mo + 3H2O
2000oC
280-700oC
950oC
Слайд 33электролиз водных растворов или расплавов:
NaCl → Na+
+ Cl─
катод─:
анод+: Na+ + ē = Na 2Cl─ - 2ē = Cl2
ZnSO4 → Zn 2+ + SO4 2─
катод─: анод+:
Zn+2 + 2ē =Zn
2H2O - 4ē = 4H+ + 2O2
расплав
раствор
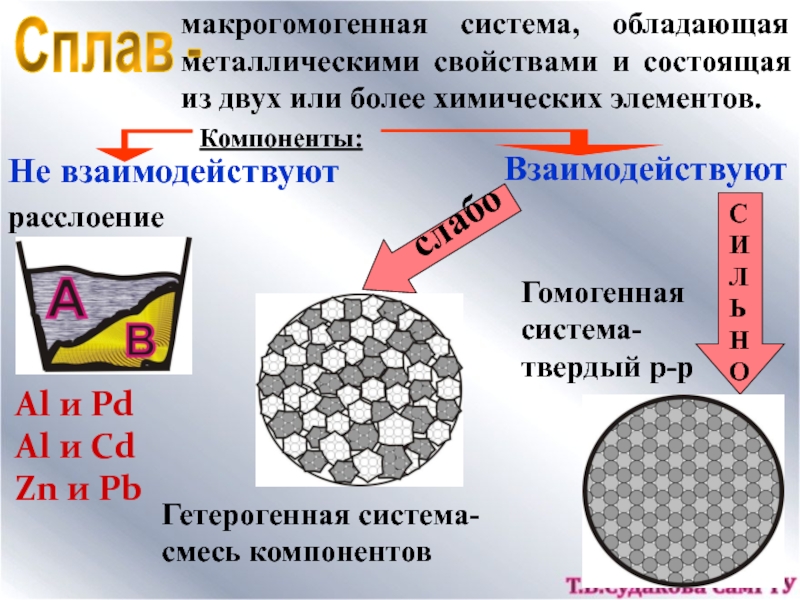
Слайд 34макрогомогенная система, обладающая металлическими свойствами и состоящая из двух или
более химических элементов.
Сплав -
Компоненты:
Не взаимодействуют
Взаимодействуют
расслоение
Al и Pd
Al и Cd
Zn
и Pbслабо
С
И
Л
Ь
Н
О
Гетерогенная система- смесь компонентов
Гомогенная система- твердый р-р
Слайд 35однородное (гомогенное) кристал-лическое вещество переменного состава, в кристаллическую решетку которого
входят атомы или ионы нескольких компонентов.
Твердые
растворы
Непрерывные:
с постепенно
меняющейся концентрацией компонентов от 0 до 100% существует предел растворимости одного металла в другом.
Ограниченные:
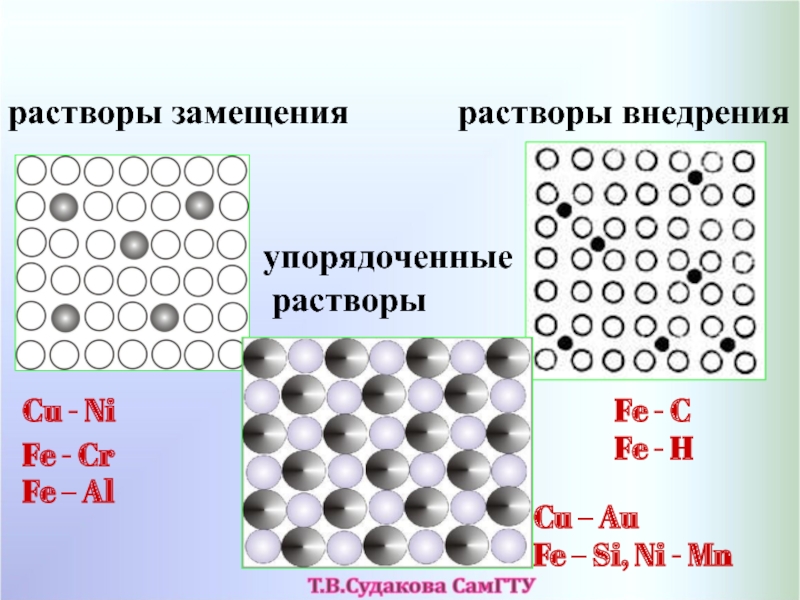
Слайд 36типы твердых растворов
растворы замещения
растворы внедрения
упорядоченные
растворы
Cu - Ni
Fe - C
Fe
- H
Cu – Au
Fe – Si, Ni - Mn
Fe -
CrFe – Al
Слайд 37Очень сильное взаимодействие между атомами металлов
Интерметаллические соединения (интерметаллиды)-
Соединения металлов между
собой и с неметаллами (Н, В, С, N и др.);
связь металлическая.ScMn2, Sc3Fe, ScFe3, TiCr3, CrMn3, Mg2Si, Mg2Ge, Mg2Sn, Mg3P2, Mg3As2, Ag3Sn
Слайд 38Манганин – сплав 11% Mn, 2,5-3,5% Ni и 86% Cu;
Примеры сплавов:
Чугун – сплав Fe с С, содержание С >
2% масс.;Зеркальный чугун
Сталь – сплав Fe с С, содержание С менее 2% масс.;
Марганцовистая сталь – сталь, содержащая марганец не менее 1%;
Нейзильбер, фехраль.
Бронза – сплавы на основе Cu (Sn, Al, Be, As, Pb, Cr);
Слайд 40сплав Fe с С (3,5-5,5%) и Mn (5-20%);
На изломе –
зеркальный блеск
используется в произ-водстве стали для раскисления и наугле-роживания:
Mn
+ S = MnS2Mn + O2 = 2MnO
Слайд 43высокое электрическое сопротивление,
самые «тихие» сплавы: 70% Mn и
30% Cu
демпфирование - поглощение энергии механических колебаний - при ударе
по сплаву звук не звучит громко. Слайд 46
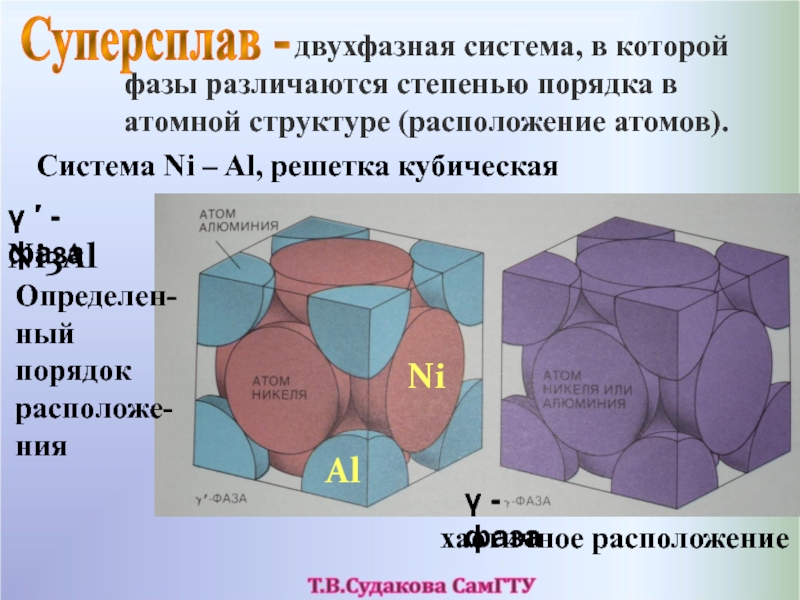
двухфазная система, в которой фазы различаются степенью порядка в
атомной структуре (расположение атомов).Суперсплав -
Система Ni – Al, решетка кубическая
Ni
Al
- фаза
- фаза
Ni3Al
Определен-ный порядок расположе-ния
хаотичное расположение
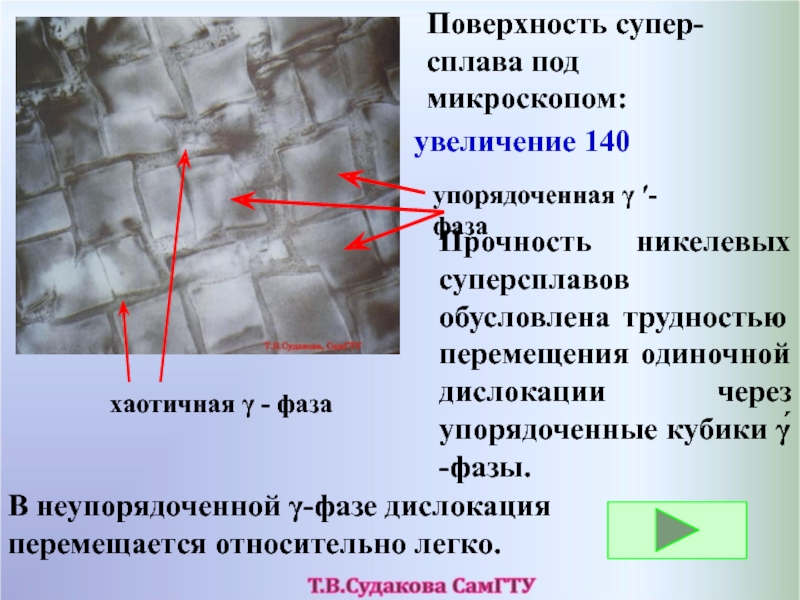
Слайд 47Поверхность супер-сплава под микроскопом:
упорядоченная -фаза
хаотичная - фаза
Прочность никелевых
суперсплавов обусловлена трудностью перемещения одиночной дислокации через упорядоченные кубики γ́
-фазы.В неупорядоченной γ-фазе дислокация перемещается относительно легко.
увеличение 140
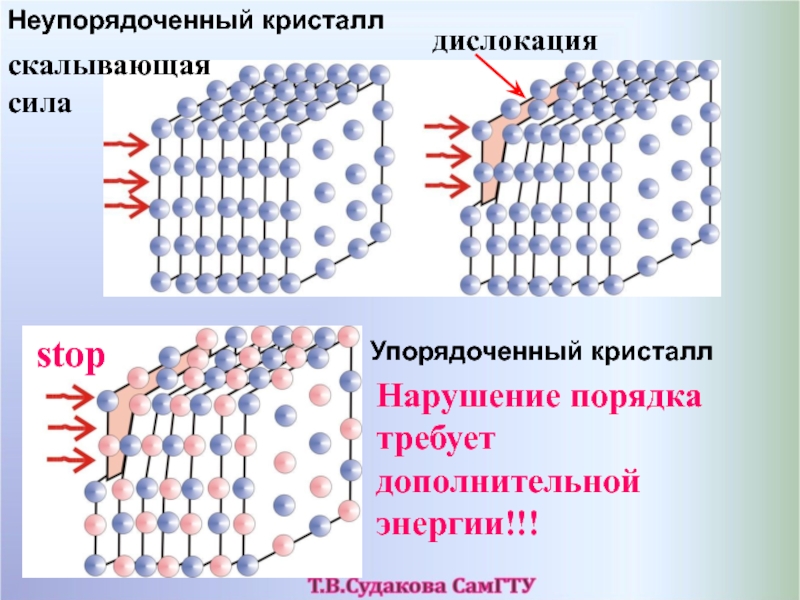
Слайд 48скалывающая сила
дислокация
stop
Нарушение порядка требует дополнительной энергии!!!
Неупорядоченный кристалл
Упорядоченный кристалл
Слайд 49Сверхпластичность
зерна < 5 мкм, под нагрузкой скользят (текут) друг по
другу без разрушения: относительное растя-жение Δl/l0=10, то есть длина образца
увели-чивается на 1000% от первоначальной.Чем мельче зерно, тем выше скорость деформации. Причина - деформация металлических связей в контактах зерен, то есть большое количество поверхностных дефектов.
сплав Al-Mg-Li после испытаний на сверхпластичность
1900%
Сверхбыстрое охлаждение
Слайд 50Чем больше S поверхности частиц (наноразмеры), тем больше поверхностная G
Сплав не устойчив! При Т зерна укрупняются!
Сверхпластическое формование детали
нагрев
быстрое
охлаждениетвердая прочная деталь
конец 1990-х, американская компания Superform: в режиме сверхпластической формовки из листа обычного алюминиевого сплава можно изготовить кузов «Феррари» за одну операцию втечение 16 часов.
Слайд 521976г. - лента аморфного магнитного сплава Ni-Fe-P-B
1960г. -первый аморфный
сплав Au75Si25
свойства:
нет кристаллической решетки
нет дефектов
нет напряжений
Высокая прочность
нет кристаллитов (зерен)
нет границ
между нимивысокая химическая однородность
Высокая коррозионная стойкость
НО! Материал пока получается довольно дорогой!
Слайд 53тарелки с нагревательным контуром из тонких металлических лент: подогрев пищи
прямо в тарелке. Металл для нагреватель-ного элемента - Au и
аморфный металл.Корейский ресурс Korea IT News пустил слух о применении аморфоного метала фирмы Liquidmetal в новых iPhone 6го поколения. Впервые аморфный металл применялся в иголках для слота SIM в ограниченных партиях iPhone 3GS и iPad. Новый iPhone будет представлен в июне на WWDC 2012.
Слайд 54Источники информации:
Фролов В.В. Химия. М.: Высшая школа. 1986.
Глинка Н.А.
Общая химия. М.: «Интеграл-Пресс». 2009. 727с.
http://www.avglob.org/fehralevaya-lenta.html
http://www.nanonewsnet.ru/
http://chemistry-chemists.com/index.html
Popgun.ru,
Azocm.ua, ToStudent,ru
Nuclearfusion.narod.ru
Expert.ru
http://itrecord.ru/gadzhety/korpus-iphone-5-budet-sdelan-iz-liquidmetal/
Hrenovina.net
Radelan.com.ua,
periodictable.ru,


















![ОБЩИЕ СВОЙСТВА МЕТАЛЛОВ. СПЛАВЫ.
ПЛАН
1. Введение. Классификация металлов.
2 Ме0 + ОН– → МеО2– + Н2 Ме0 + Н2О + ОН– Ме0 + ОН– → МеО2– + Н2 Ме0 + Н2О + ОН– → [Ме(ОН)4]– + Н2Взаимодействие со щелочами:Реагируют](/img/tmb/3/256227/3abf1445a91f42396624d168c0850bad-800x.jpg)