Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
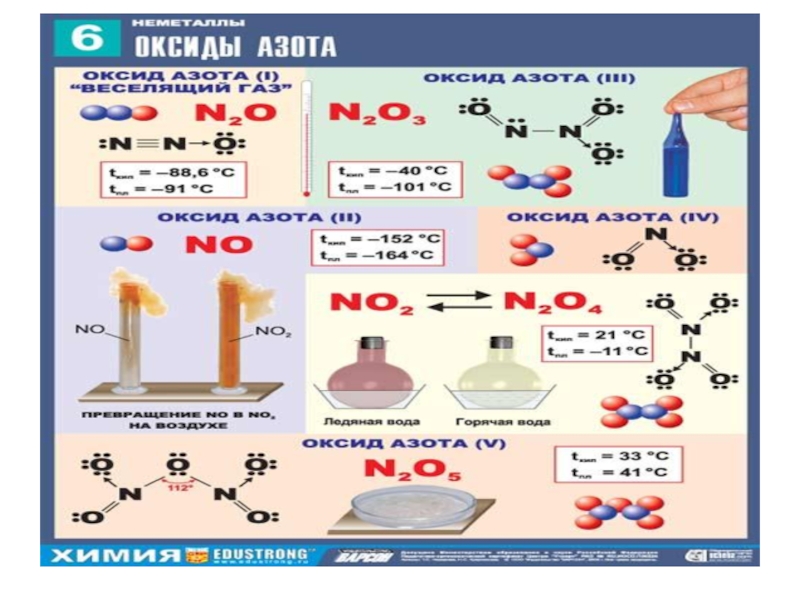
Оксиды - соединения элементов с кислородом
Содержание
- 1. Оксиды - соединения элементов с кислородом
- 2. Образцы оксидов в стекле
- 3. Формула оксидов: ЭхОуОксиды – сложные вещества, состоящие из атомов двух химических элементов, один из которых кислород.
- 4. Слайд 4
- 5. СuО - оксид меди - твердое вещество
- 6. Слайд 6
- 7. Название оксидовОксид + название химического элементаОксид магния
- 8. Применение оксидовИз руд, состоящих из Fe2О3, получают
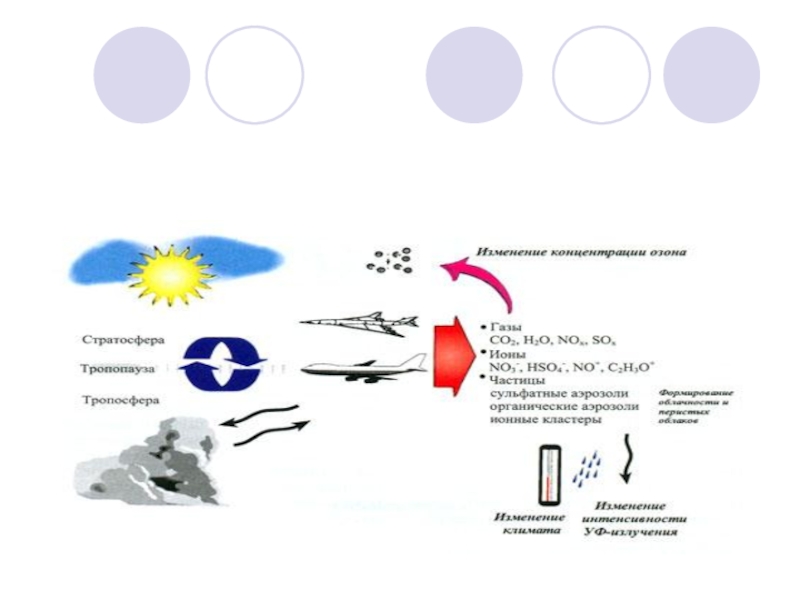
- 9. Выделение СО и СО2
- 10. Спасибо за внимание
- 11. Скачать презентанцию
Образцы оксидов в стекле
Слайды и текст этой презентации
Слайд 3Формула оксидов: ЭхОу
Оксиды – сложные вещества, состоящие из атомов двух
химических элементов, один из которых кислород.
Слайд 5
СuО - оксид меди - твердое вещество черного цвета;
СаО
– оксид кальция – твердое вещество белого цвета;
SО3 – оксид
серы (VІ) – бесцветная летучая жидкость;СО2 – оксид углерода (ІV) – бесцветный газ.
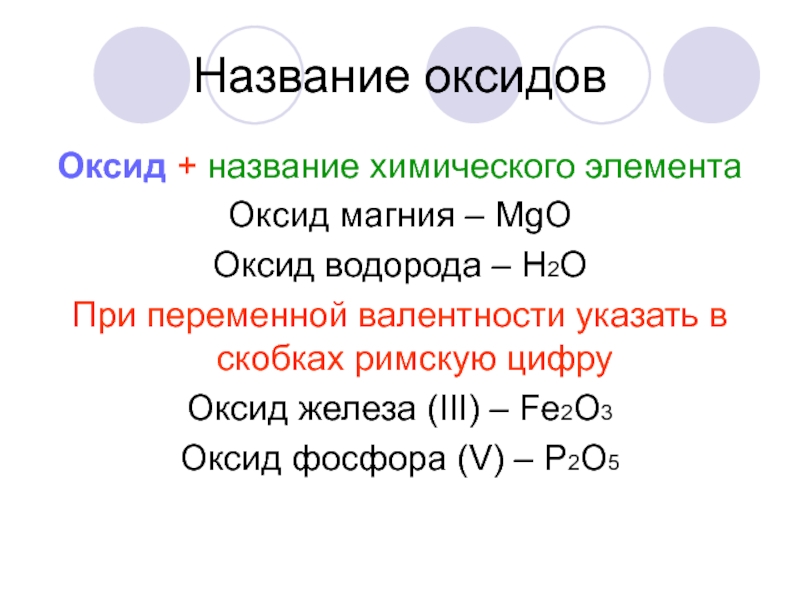
Слайд 7Название оксидов
Оксид + название химического элемента
Оксид магния – МgО
Оксид водорода
– Н2О
При переменной валентности указать в скобках римскую цифру
Оксид железа
(ІІІ) – Fe2О3 Оксид фосфора (V) – Р2О5