заряженный положительным зарядом шар радиуса порядка 10-10м, внутри которого около
своих положений равновесия колеблются электроны.Недостатки модели:
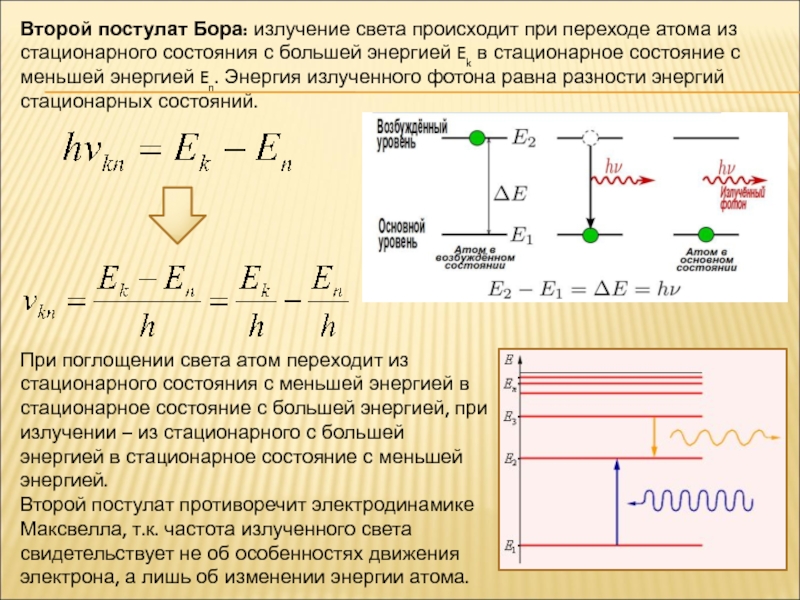
не объясняла дискретный характер излучения атома и его устойчивость;
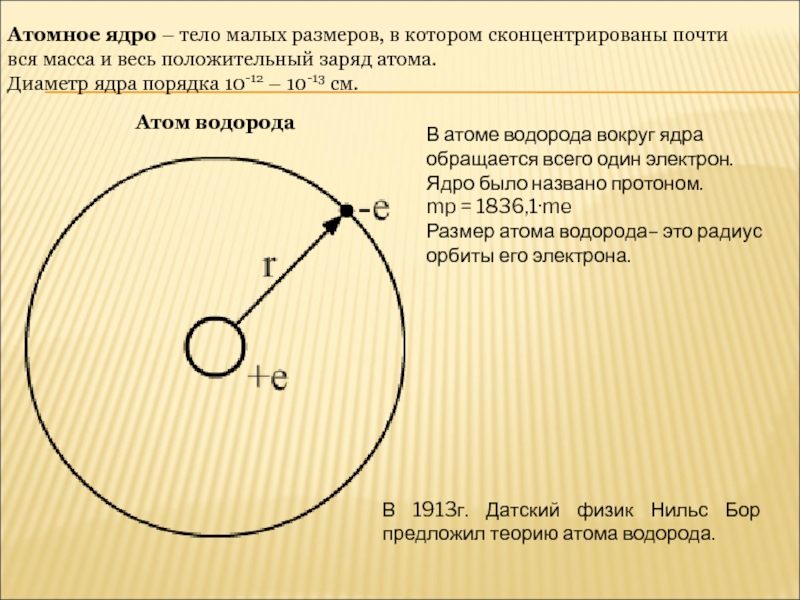
не дает возможности понять, чем определяются размеры атомов;
оказалась в полном противоречии с опытами по исследованию распределения положительного заряда в атоме (опыты, проводимые Эрнестом Резерфордом).