Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Острый лимфобластный лейкоз
Содержание
- 1. Острый лимфобластный лейкоз
- 2. Острый лимфобластный лейкоз (ОЛЛ) – гетерогенная группа
- 3. История Alfred-Armand-Louis-Marie Velpeau (1795 – 1867)Французский анатом и хирург1827 - Предоставление первого точного описания лейкемии
- 4. История Он сообщил о случае 63-летней женщины,
- 5. История Virchow, Rudolf. Weißes Blut , 1845Рудольф Людвиг Карл Вирхов (1821 - 1902)1845 – вводит понятие «лейкемия»
- 6. История 1877 Описал нормальные и изменённые лейкоцитыПауль
- 7. История Emil "Tom" Frei III 1900Лейкемия – семейство
- 8. РФ 2018 год1840 случаев (0,29% от всех
- 9. Структура заболеваемости детского населения злокачественными заболеваниямиРФ 2018
- 10. США 20206,150 случаев (0,34% от всех впервые
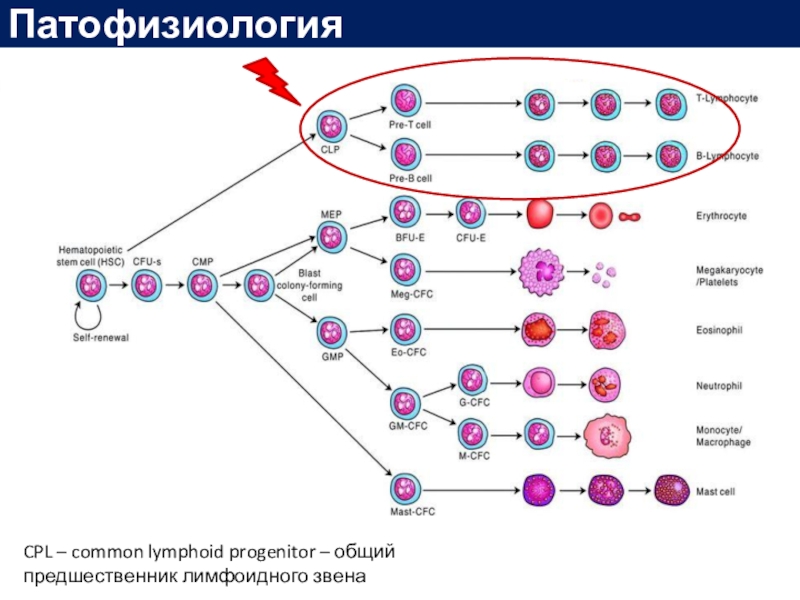
- 11. ПатофизиологияCPL – common lymphoid progenitor – общий предшественник лимфоидного звена
- 12. ПатофизиологияA. Emadi, J. E. Karp «Acute Leukemia. An Illustrated Guide to Diagnosis and Treatment», 2018
- 13. Синдром ДаунаЭтиологияВрожденные генетические синдромы Анемия ФанкониСиндром Блума Синдром Луи-Бар NBS
- 14. Этиология• Воздействие ионизирующего излучения • Вирусы (EBV, HTLV-1)• Пестициды, химиотерапия и другие токсичные химические вещества
- 15. Клинические проявления1. НЕЙТРОПЕНИЯ •Повышение температуры •Тяжелые, затяжные
- 16. Классификация ВОЗ 2016 Arber, D. A., Orazi,
- 17. Диагностика МорфологияИммунофенотипировение Цитогенетика/молекулярная генетика
- 18. Диагностика Цитохимическое исследованиеCпецифичных тестов для диагностики ОЛЛ
- 19. Диагностика - морфологияFAB-классификация
- 20. Диагностика- морфология (А) - FAB L1(В) -
- 21. Иммунологическая классификацияEuropean Group for the Immunological Characterization
- 22. Ключевые маркеры бластных клеток при T- ОЛЛ
- 23. Диагностика - иммунофенотипирование (F) Типичный иммунофенотип B-ОЛЛ
- 24. Jacob M. Rowe. Prognostic factors in adult
- 25. Диагностика – генетический анализ Williams Hematology 9thEdition
- 26. Диагностика – генетический анализ Дети VS Взрослые
- 27. Диагностика – генетический анализ Распределение цитогенетических аномалий
- 28. Диагностика – генетический анализ A. Emadi, J.
- 29. (1) Дети(2) Взрослые Bahoush G, Nojoomi M «Frequency
- 30. ДиагностикаПроведение СМ-пункции В результате анализа ликвора возможны следующие варианты:• CNS1 – пункция не травматичная (
- 31. Диагностика• Клинический анализ крови • Биохимический анализ
- 32. Прогнозирование D. Hoelzer, R. Bassan, H. Dombret,
- 33. Факторы высокого риска ОЛЛ у детейHunger, S.
- 34. ЛечениеЦели лечения:• Эрадикация лейкемического клона• Восстановление нормального
- 35. Критерии ответа на терапию у пациентов с
- 36. Минимальная остаточная болезнь (МОБ; minimal residual disease
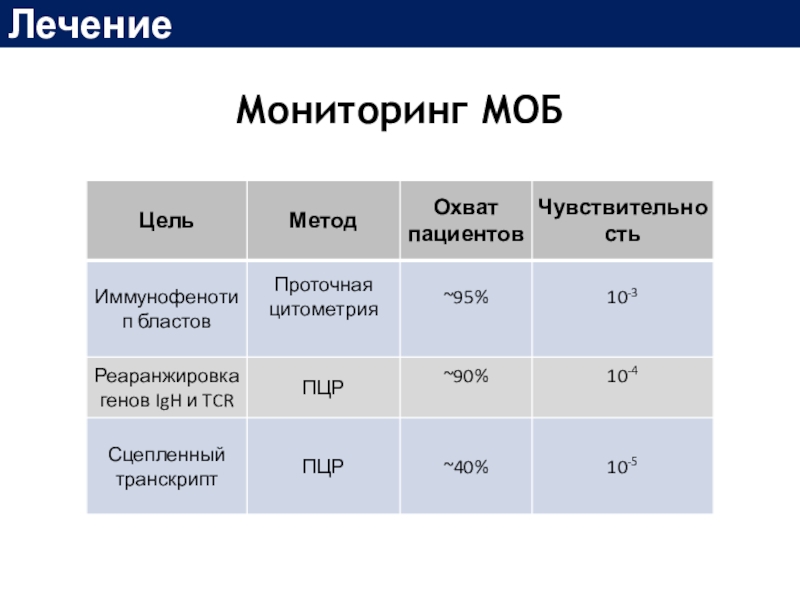
- 37. Мониторинг МОБЛечение
- 38. Лечение ALL-MB-2015SRG – группа стандартного рика; ImR
- 39. Лечение ALL-MB-2015T-SRT-IRT-HRCD1a+, TCR‒Инициальный лейкоцитоз
- 40. Лечение ALL-MB-2015Этапы лечения острого лейкоза1. Индукция ремиссии
- 41. 29381522136ДэксПЭГ-АСПВКРДРЦТРИПЛЕТИТБ*Дэкс – дексаметазон; ПЭГ-АСП – пэгаспаргиназа; ВКР
- 42. Лечение ALL-MB-2015Консолидация – 1 7
- 43. Лечение ALL-MB-2015Вторая фаза индукции (для группы T-IR)
- 44. Лечение ALL-MB-2015Терапия пациентов высокого риска Блок HR-1Протокол
- 45. Лечение ALL-MB-2015Меркаптопурин – ежедневно Метотрексат – 1
- 46. ЛечениеАлло-ТГСК1. Высокая группа риска в первой ремиссии
- 47. ЛечениеСергей Н. Бондаренко, Иван С. Моисеев, Ольга А. Слесарчук, et
- 48. ЛечениеCR1, n2500 CR1, n804 CR2, n817 CR2,
- 49. ЛечениеСергей Н. Бондаренко, Иван С. Моисеев, Ольга А. Слесарчук, et
- 50. Общая выживаемость группы высокого риска АллоТГСК, n248Без
- 51. ОЛЛ стандартного риска Возраст 15-55 летМОБ+ на
- 52. ЛечениеИммунотерапия Блинатумомаб - BiTE АТ анти-CD19/CD3Franquiz, M.
- 53. ЛечениеKantarjian, H., Stein, A., Gökbuget, N., Fielding,
- 54. ЛечениеБлинатумомаб в сравнении с историческим стандартным лечением
- 55. ОВ, 53% (95% CI 36-70%)БРВ, 38% (95%
- 56. Безрецидивная выживаемость пациентов ОЛЛ после терапии блинатумомабом
- 57. Частота рецидивов при ОЛЛ после терапии блинатумомабом
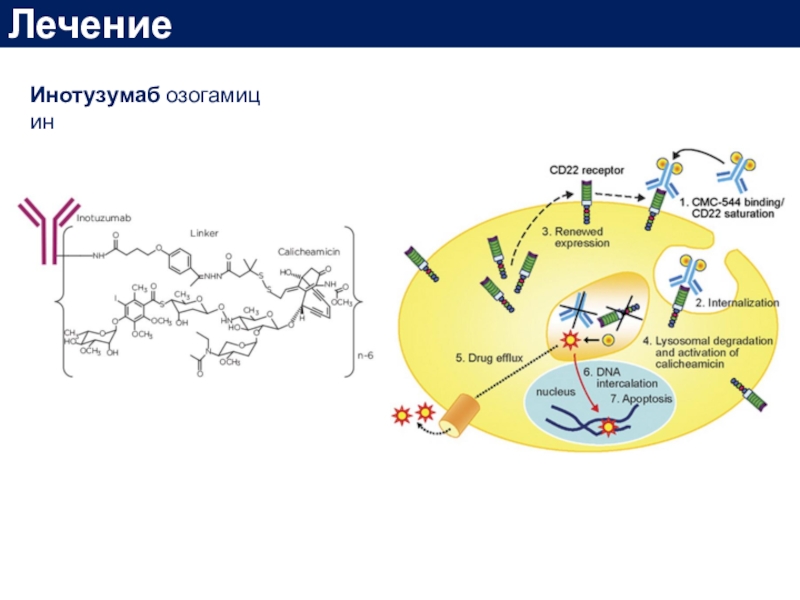
- 58. ЛечениеИнотузумаб озогамицин
- 59. ЛечениеKantarjian, H. M., DeAngelo, D. J., Stelljes,
- 60. ЛечениеKantarjian, H. M., DeAngelo, D. J., Stelljes,
- 61. ЛечениеCAR-T клеточная терапия Kymriah – анти CD 19 CAR-TEmily Whitehead – первый педиатрический CAR-T пациент
- 62. ЛечениеCAR-T клеточная терапия
- 63. Лечение«На данный момент мы находимся на стадии
- 64. ЛечениеNovartis Oncology for Health Care Professionals, KYMRIAH®
- 65. ЛечениеXian Zhang, Jing-Jing Li, Pei-Hua Lu «Advances
- 66. ЛечениеПобочные эффекты : • Синдром выброса цитокинов •
- 67. Проблема : высокодозная химиотерапия повреждает лимфоциты пациента,
- 68. ЛечениеCAR T – анти CD 19 (CD
- 69. Лечение34 пациента Р/Р В-ОЛЛ (24 с предшествующей
- 70. Динамика общей выживаемости детей с ОЛЛ в
- 71. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Острый лимфобластный лейкоз
СНО НИИ детской онкологии, гематологии и
трансплантологии
им. Р.М.Горбачевой
Слайд 2Острый лимфобластный лейкоз (ОЛЛ) – гетерогенная группа злокачественных клональных заболеваний
системы крови, происходящих из клеток-предшественниц гемопоэза преимущественно лимфоидной направленности дифференцировки
и характеризующиеся чаще всего исходным поражением костного мозга, вытеснением нормального кроветворения и вовлечением различных органов и систем организма (ЦНС, яички, лимфатическая ткань любой локализации), а также возможностью исходного поражения органов лимфатической ткани без вовлечения костного мозгаНАЦИОНАЛЬНОЕ ГЕМАТОЛОГИЧЕСКОЕ ОБЩЕСТВО, «КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ДИАГНОСТИКЕ И ЛЕЧЕНИЮ ОСТРЫХ ЛИМФОБЛАСТНЫХ ЛЕЙКОЗОВ ВЗРОСЛЫХ» , 2018
Слайд 3История
Alfred-Armand-Louis-Marie Velpeau
(1795 – 1867)
Французский анатом и хирург
1827 - Предоставление
первого точного описания лейкемии
Слайд 4История
Он сообщил о случае 63-летней женщины, которая умерла от
лихорадки, опухшего желудка и общей слабости. При вскрытии у нее
была обнаружена огромная селезенка (в двадцать раз больше нормальной), в которой кровь была «такой же густой, как каша, что можно было задуматься, а не является ли это большим количеством гноя, а не кровью»Слайд 5История
Virchow, Rudolf. Weißes Blut , 1845
Рудольф Людвиг Карл Вирхов
(1821 - 1902)
1845 – вводит
понятие «лейкемия»
Слайд 6История
1877
Описал нормальные и изменённые лейкоциты
Пауль Эрлих
(1854 –
1915)
Вильгельм Эбштейн
(1836 – 1912)
1889
Вводит понятие «острого»
лейкозаФранц Эрнст Кристиан Нейман (1834 – 1918)
1869
Охарактеризовал лейкемию как
заболевание костного мозга
Слайд 7История
Emil "Tom" Frei III
1900
Лейкемия – семейство заболеваний
1913
Классификация лейкемий
ХЛЛ,
ХМЛ, ОЛЛ, Эритролейкемия
Сидни Фарбер (1903- 1973)
1947
Аминоптерин – антифолат
– блокирует деление лейкоцитов при ОЛЛЭмиль Фрэйрих
(1927)
Эмиль Фрэй III
(1924-2013)
1962
Комбинированная химиотерапия ОЛЛ
Разработка протокола VAMP
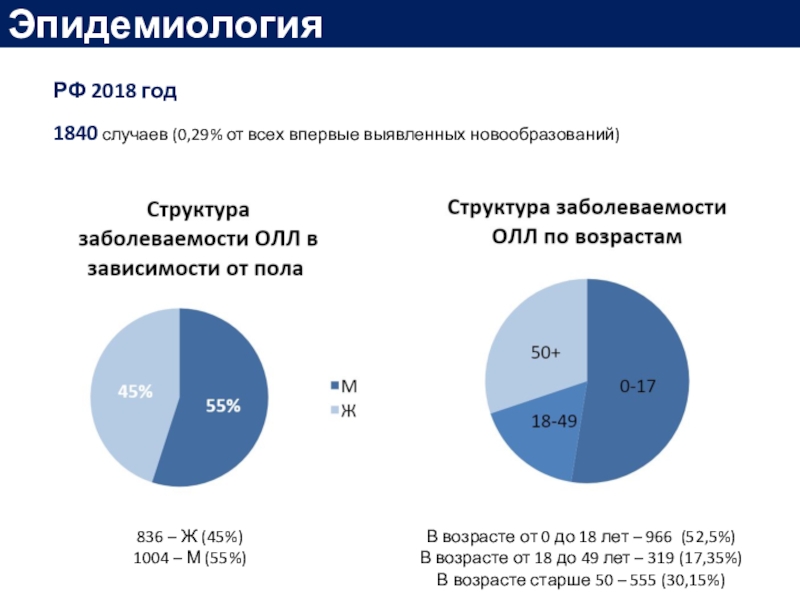
Слайд 8РФ 2018 год
1840 случаев (0,29% от всех впервые выявленных новообразований)
836
– Ж (45%)
1004 – М (55%)
В возрасте от 0 до
18 лет – 966 (52,5%)В возрасте от 18 до 49 лет – 319 (17,35%)
В возрасте старше 50 – 555 (30,15%)
Эпидемиология
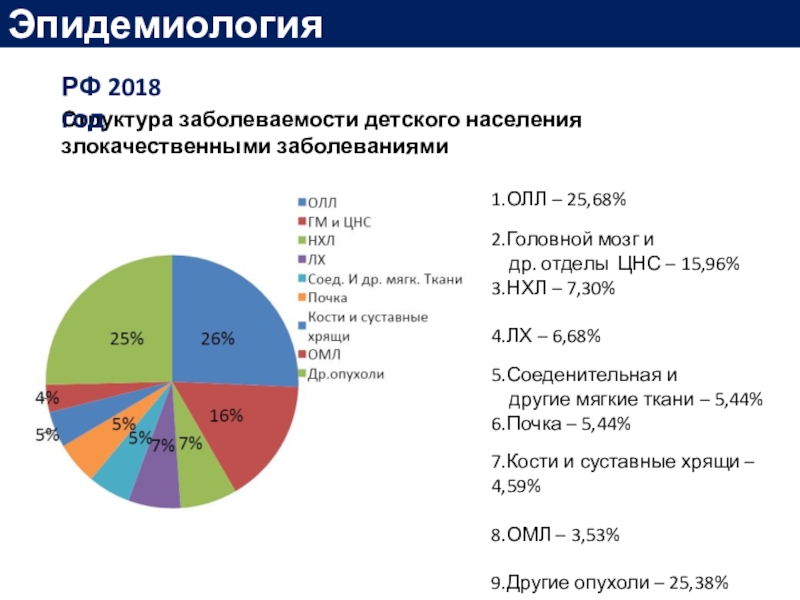
Слайд 9Структура заболеваемости детского населения злокачественными заболеваниями
РФ 2018 год
1.ОЛЛ – 25,68%
2.Головной
мозг и
др. отделы ЦНС – 15,96%
3.НХЛ –
7,30%4.ЛХ – 6,68%
5.Соеденительная и
другие мягкие ткани – 5,44%
6.Почка – 5,44%
7.Кости и суставные хрящи – 4,59%
8.ОМЛ – 3,53%
9.Другие опухоли – 25,38%
Эпидемиология
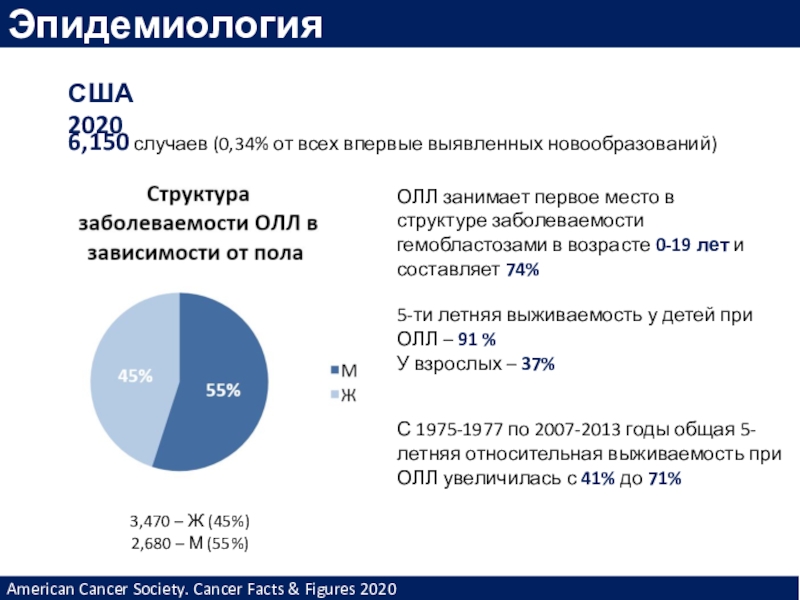
Слайд 10США 2020
6,150 случаев (0,34% от всех впервые выявленных новообразований)
3,470 –
Ж (45%)
2,680 – М (55%)
ОЛЛ занимает первое место в структуре
заболеваемости гемобластозами в возрасте 0-19 лет и составляет 74%5-ти летняя выживаемость у детей при ОЛЛ – 91 %
У взрослых – 37%
С 1975-1977 по 2007-2013 годы общая 5-летняя относительная выживаемость при ОЛЛ увеличилась с 41% до 71%
American Cancer Society. Cancer Facts & Figures 2020
Эпидемиология
Слайд 12Патофизиология
A. Emadi, J. E. Karp «Acute Leukemia. An Illustrated Guide
to Diagnosis and Treatment», 2018
Слайд 13Синдром Дауна
Этиология
Врожденные генетические синдромы
Анемия Фанкони
Синдром Блума
Синдром Луи-Бар
NBS
Слайд 14Этиология
• Воздействие ионизирующего излучения
• Вирусы (EBV, HTLV-1)
• Пестициды, химиотерапия
и другие токсичные
химические вещества
Слайд 15Клинические проявления
1. НЕЙТРОПЕНИЯ
•Повышение температуры
•Тяжелые, затяжные инфекции
2. АНЕМИЯ
•Тахикардия
• Бледность
кожных покровов и слизистых
• Слабость
• Одышка
3. ТРОМБОЦИТОПЕНИЯ
• Кровоизлияния
в кожу и слизистые 4. ИНФИЛЬТРАЦИЯ ОРГАНОВ
•Гепато-/Сплнеомегалия
•Лимфаденопатия
•Гиперпластические гингивиты
•Лейкемиды
5. ОПУХОЛЕВАЯ ИНТОКСИКАЦИЯ
•Слабость
•Ночные поты
•Похудание
6. ЛЕЙКОСТАЗ
•Нарушения зрения
•Неврологические нарушения
•Головная боль
•Дистресс синдром легких
•Приапизм
Слайд 16Классификация
ВОЗ 2016
Arber, D. A., Orazi, A., Hasserjian, R.,
Thiele, J., Borowitz, M. J., Le Beau, M. M., …
Vardiman, J. W. (2016). The 2016 revision to the World Health Organization classification of myeloid neoplasms and acute leukemia. Blood, 127(20), 2391–2405.NOS – not otherwise specified - Без специфических характеристик
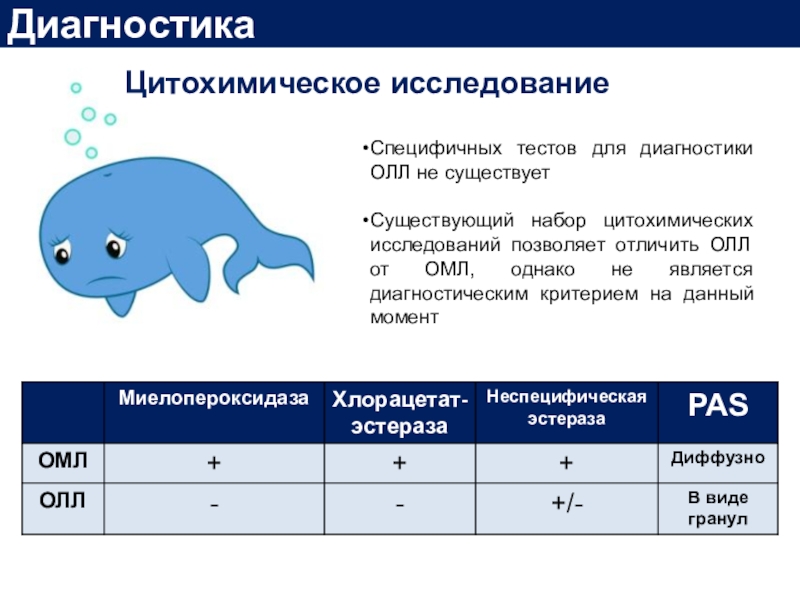
Слайд 18Диагностика
Цитохимическое исследование
Cпецифичных тестов для диагностики ОЛЛ не существует
Существующий набор
цитохимических исследований позволяет отличить ОЛЛ от ОМЛ, однако не является
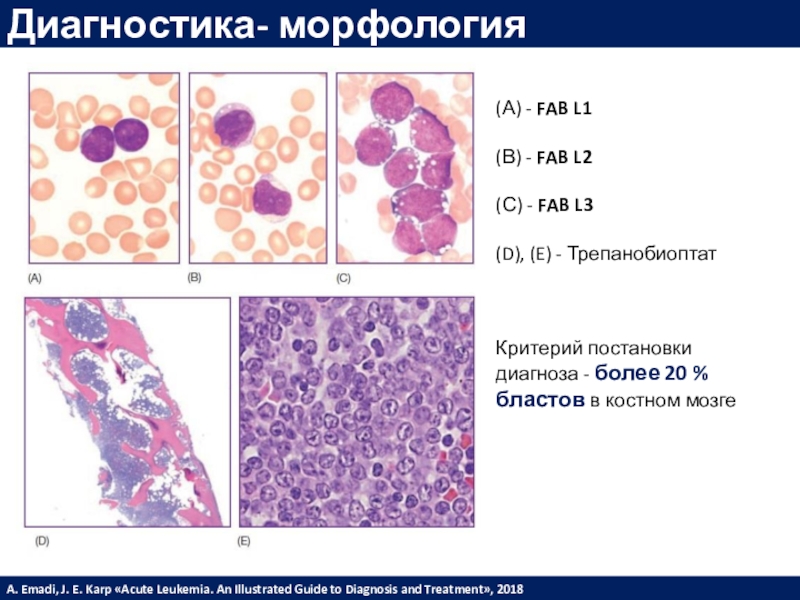
диагностическим критерием на данный моментСлайд 20Диагностика- морфология
(А) - FAB L1
(В) - FAB L2
(С) -
FAB L3
(D), (E) - Трепанобиоптат
Критерий постановки диагноза - более 20
% бластов в костном мозге A. Emadi, J. E. Karp «Acute Leukemia. An Illustrated Guide to Diagnosis and Treatment», 2018
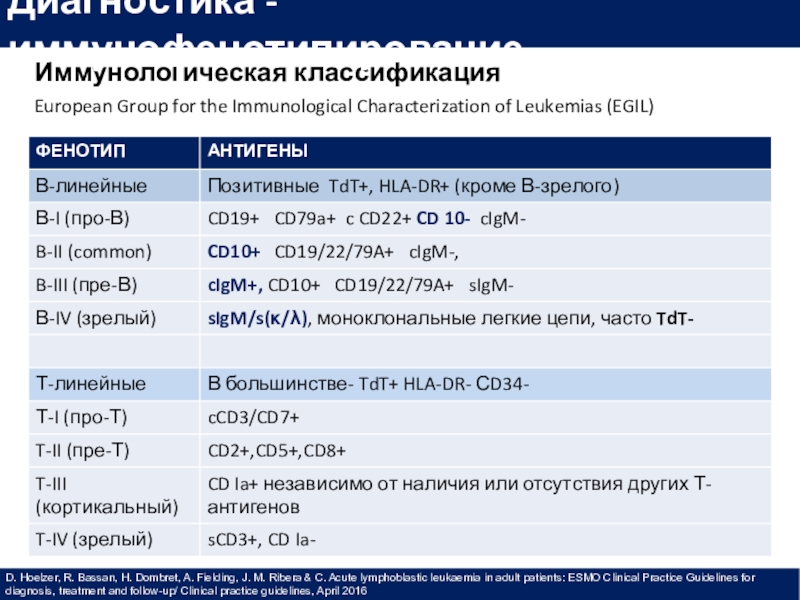
Слайд 21Иммунологическая классификация
European Group for the Immunological Characterization of Leukemias (EGIL)
Диагностика - иммунофенотипирование
D. Hoelzer, R. Bassan, H. Dombret, A. Fielding,
J. M. Ribera & C. Acute lymphoblastic leukaemia in adult patients: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up/ Clinical practice guidelines, April 2016Слайд 22Ключевые маркеры бластных клеток при T- ОЛЛ (EGIL)
Диагностика -
иммунофенотипирование
Про-Т (T I)
CD7+, cCD3+
Пре-Т (T II)
CD7+, сCD3+,
CD2+ and/or CD5+Ранний Т-ОЛЛ
Common-Т (T III)
CD7+, cCD3+, CD5+, CD2+, CD1a+
Тимический Т-ОЛЛ
Т (T IV)
CD7+,CD5+, sCD3+, CD1a-
Зрелый Т-ОЛЛ
Тимус
Слайд 23Диагностика - иммунофенотипирование
(F) Типичный иммунофенотип B-ОЛЛ (CD19+ CD79a+ CD10+
TdT+)
(G) Типичный иммунофенотип T-ОЛЛ (цитоплазматический CD3+ CD2+ CD5+ TdT+)
A. Emadi,
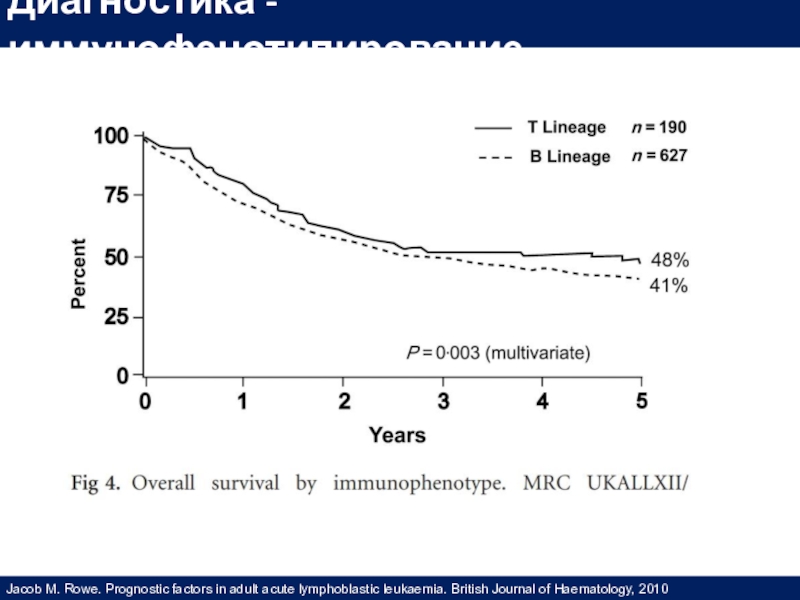
J. E. Karp «Acute Leukemia. An Illustrated Guide to Diagnosis and Treatment», 2018Слайд 24Jacob M. Rowe. Prognostic factors in adult acute lymphoblastic leukaemia.
British Journal of Haematology, 2010
Диагностика - иммунофенотипирование
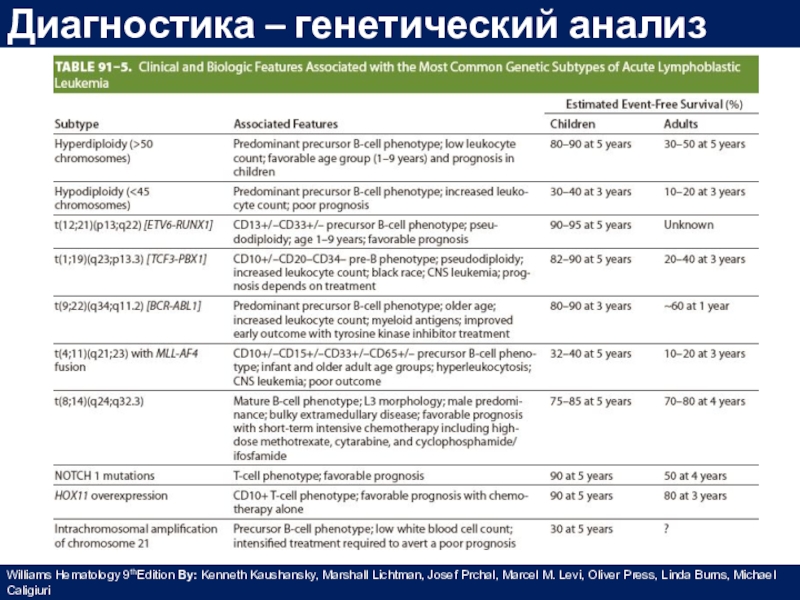
Слайд 25Диагностика – генетический анализ
Williams Hematology 9thEdition By: Kenneth Kaushansky, Marshall
Lichtman, Josef Prchal, Marcel M. Levi, Oliver Press, Linda Burns, Michael Caligiuri
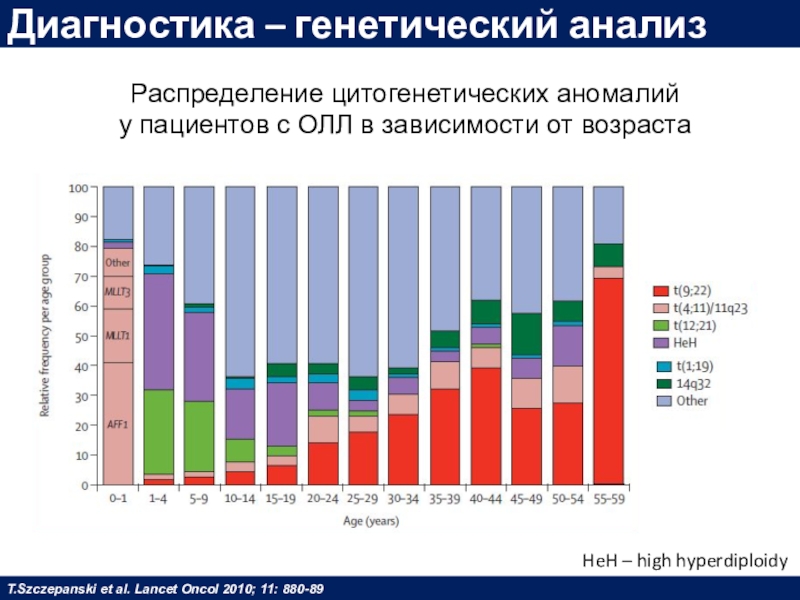
Слайд 27Диагностика – генетический анализ
Распределение цитогенетических аномалий
у пациентов с
ОЛЛ в зависимости от возраста
T.Szczepanski et al. Lancet Oncol
2010; 11: 880-89HeH – high hyperdiploidy
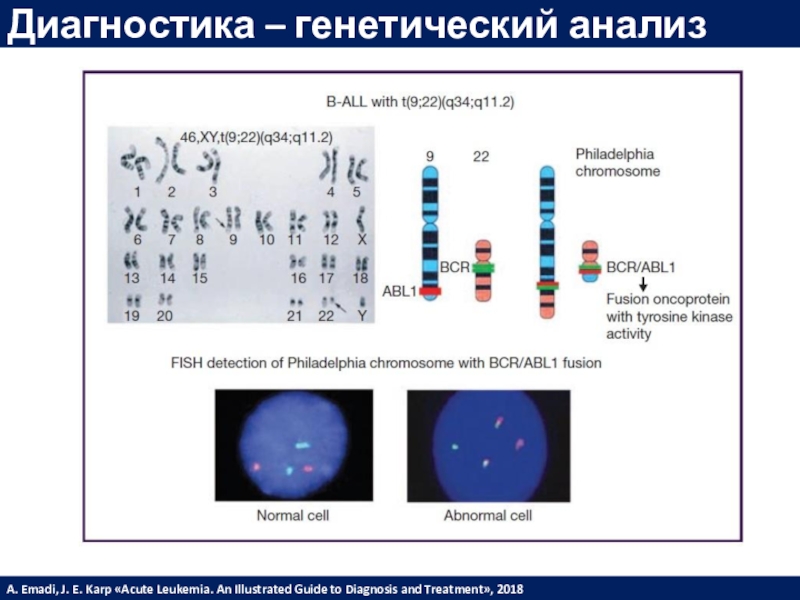
Слайд 28Диагностика – генетический анализ
A. Emadi, J. E. Karp «Acute
Leukemia. An Illustrated Guide to Diagnosis and Treatment», 2018
Слайд 29(1) Дети
(2) Взрослые
Bahoush G, Nojoomi M «Frequency of Cytogenetic Findings and its
Effect on the Outcome of Pediatric Acute Lymphoblastic Leukemia» Med Arch.
2019 Oct; 73(5): 311–315.(2) Jacob M. Rowe. Prognostic factors in adult acute lymphoblastic leukaemia. British Journal of Haematology, 2010
HeH – high hyperdiploidy;
Ho/Tr – hypodiploidy/near-triploidy.
Слайд 30Диагностика
Проведение СМ-пункции
В результате анализа ликвора возможны следующие варианты:
• CNS1
– пункция не травматичная (
– пункция не травматична, <10 лейкоцитов/мкл, возможно наличие лейкемических клеток• CNS3 – пункция не травматична, ≥10 лейкоцитов/мкл, наличие лейкемических клеток после цитоцентрифугирования
• TLP+ – травматичная пункция с примесью лейкемических клеток
• TLP− – травматичная пункция, отсутствие примеси лейкемических клеток.
(1) НАЦИОНАЛЬНОЕ ГЕМАТОЛОГИЧЕСКОЕ ОБЩЕСТВО, «КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ДИАГНОСТИКЕ И ЛЕЧЕНИЮ ОСТРЫХ ЛИМФОБЛАСТНЫХ ЛЕЙКОЗОВ ВЗРОСЛЫХ» , 2018
Слайд 31Диагностика
• Клинический анализ крови
• Биохимический анализ крови
• Коагулограмма
•
HLA типирование + Определение группы крови (АВ0, определение антигена D
системы Резус (резус-фактор), определение фенотипа по антигенам С, с, E, e, Cw, K, k и определение антиэритроцитарных антител с целью проведения заместительной терапии компонентами крови)НАЦИОНАЛЬНОЕ ГЕМАТОЛОГИЧЕСКОЕ ОБЩЕСТВО, «КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ДИАГНОСТИКЕ И ЛЕЧЕНИЮ ОСТРЫХ ЛИМФОБЛАСТНЫХ ЛЕЙКОЗОВ ВЗРОСЛЫХ» , 2018
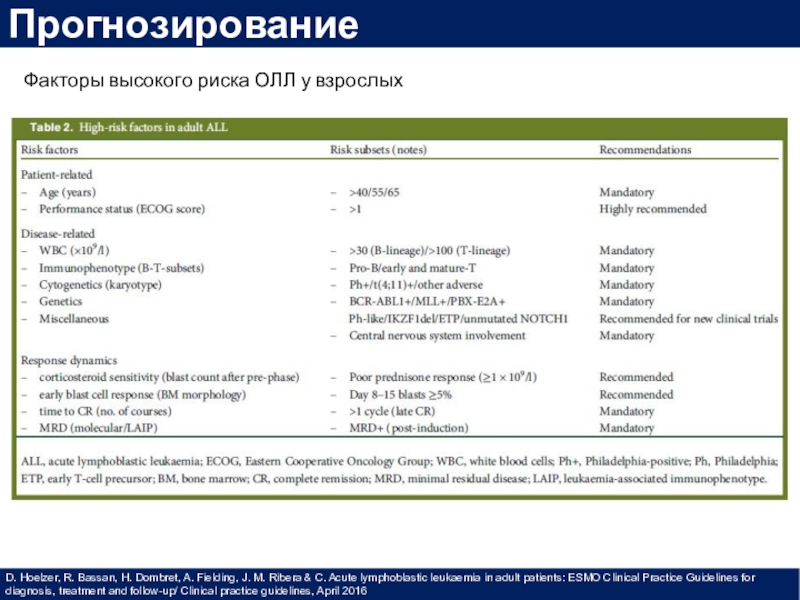
Слайд 32Прогнозирование
D. Hoelzer, R. Bassan, H. Dombret, A. Fielding, J.
M. Ribera & C. Acute lymphoblastic leukaemia in adult patients:
ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up/ Clinical practice guidelines, April 2016Факторы высокого риска ОЛЛ у взрослых
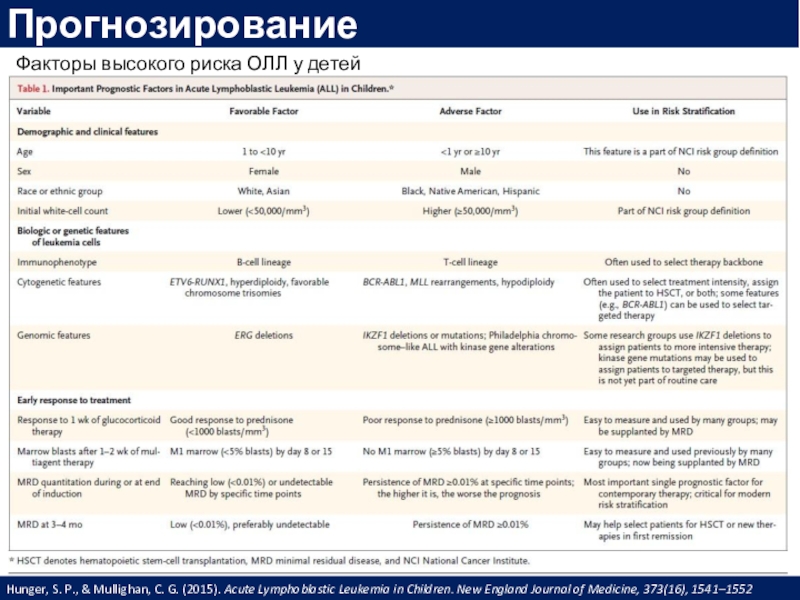
Слайд 33Факторы высокого риска ОЛЛ у детей
Hunger, S. P., & Mullighan,
C. G. (2015). Acute Lymphoblastic Leukemia in Children. New England Journal
of Medicine, 373(16), 1541–1552Прогнозирование
Слайд 34Лечение
Цели лечения:
• Эрадикация лейкемического клона
• Восстановление нормального кроветворения
• Достижение длительной
бессобытийной выживаемости
Взрослые
o AALL0232, Borowitz с соавт., 2015
o GRAALL,
Beldjord K с соавт., 2014 o PETHEMA ALL-AR-03, Ribera с соавт., 2014
o ALL-REZ BFM 2002, Eckert с соавт., 2013
o GMALL, Gokbuget с соавт., 2012
o o NILG-ALL09/00, Bassan с соавт., 2009
o AIEOP-BFM-ALL Basso с соавт., 2009
Детские
o группы Москва–Берлин (ALL-MB-2008 или ALL-MB-2015)
o группы BFM (ALL-BFM-95 или ALL-BFM-2000)
Протоколы :
Слайд 35Критерии ответа на терапию у пациентов с ОЛЛ
Лечение
Полная ремиссия
•
Отсутствие экстрамедуллярных очагов ОЛЛ
• Трехростковое кроветворение
•
кровь, костный мозг)Резистентность
• Отсутствие достижения полной ремиссии в конце индукции
Прогрессирование
• Повышение как минимум на 25% бластов в периферической крови и костном мозге или появление экстрамедуллярных проявлений ОЛЛ
Рецидив
• Появление бластов в периферической крови костном мозге (>5%) или появление экстрамедуллярных проявлений ОЛЛ после полной ремиссии
НАЦИОНАЛЬНОЕ ГЕМАТОЛОГИЧЕСКОЕ ОБЩЕСТВО, «КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ДИАГНОСТИКЕ И ЛЕЧЕНИЮ ОСТРЫХ ЛИМФОБЛАСТНЫХ ЛЕЙКОЗОВ ВЗРОСЛЫХ» , 2018
Слайд 36Минимальная остаточная болезнь (МОБ; minimal residual disease – MRD) –
наличие остаточных лейкемических клеток у пациента в ремиссии, не выявляемых
рутинными морфологическими методами, но определяемых при помощи высокочувствительных лабораторных технологий (ПЦР в реальном времени и/или многоцветной проточной цитометрией)Лечение
Сохранение МОБ после цитостатического воздействия является самым мощным прогностическим фактором у пациентов с ОЛЛ, свидетельствующим о необходимости изменения терапевтической тактики
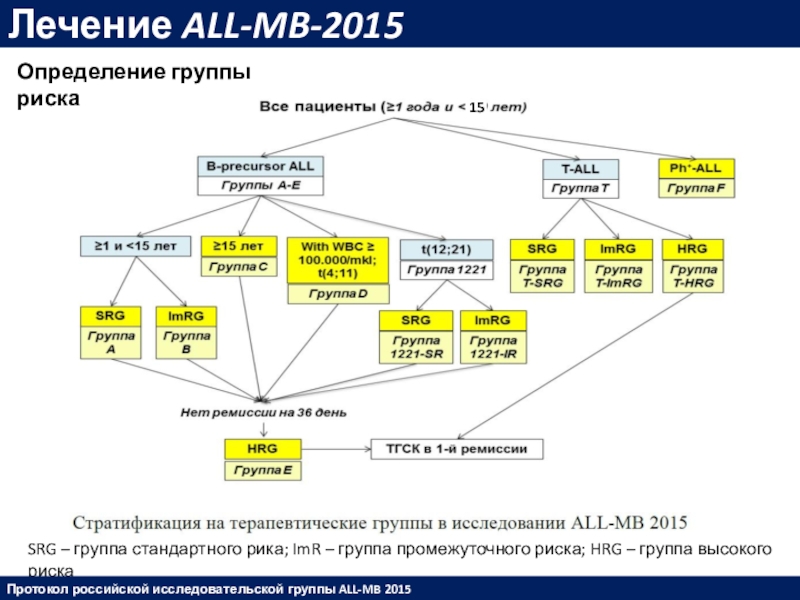
Слайд 38Лечение ALL-MB-2015
SRG – группа стандартного рика; ImR – группа промежуточного
риска; HRG – группа высокого риска
15
Определение группы риска
Протокол
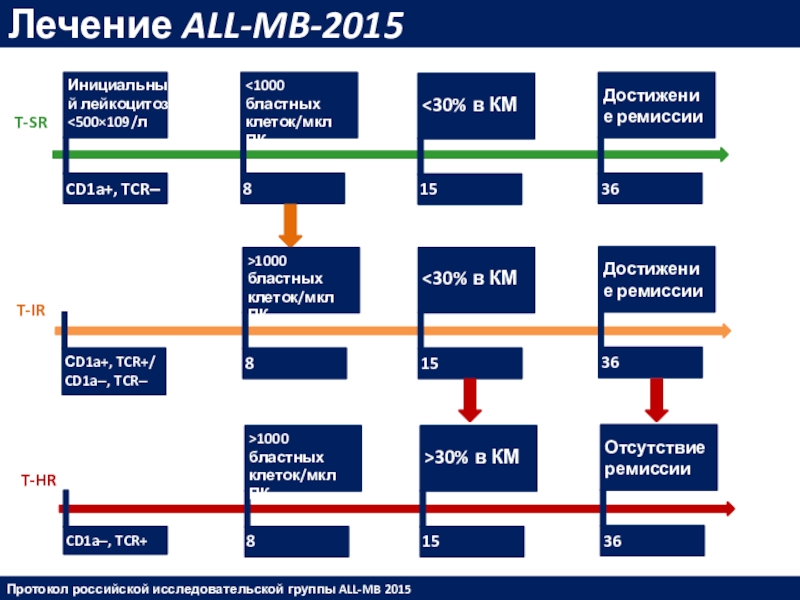
российской исследовательской группы ALL-MB 2015Слайд 39Лечение ALL-MB-2015
T-SR
T-IR
T-HR
CD1a+, TCR‒
Инициальный лейкоцитоз
в КМ
36 сутки
Достижение ремиссии
СD1a+, TCR+/ CD1a‒, TCR‒
8 сутки
>1000 бластных клеток/мкл
ПК15 сутки
<30% в КМ
36 сутки
Достижение ремиссии
15 сутки
>30% в КМ
36 сутки
Отсутствие ремиссии
CD1a‒, TCR+
8 сутки
>1000 бластных клеток/мкл ПК
Протокол российской исследовательской группы ALL-MB 2015
Слайд 40Лечение ALL-MB-2015
Этапы лечения острого лейкоза
1. Индукция ремиссии - это период
начального лечения, целью которого является максимально быстрое и существенное сокращение
опухолевой массы и достижение полной ремиссии (длительность 4-6 недель)2. Консолидация ремиссии - направлена на закрепление достигнутого противоопухолевого эффекта. Задачей этого периода является по возможности еще большее уменьшение числа остающихся после индукции лейкемических клеток (длительность 4-6 месяцев)
3. Поддерживающая терапия - это длительная цитостатическая терапия в небольших дозах, направленная на уничтожение возможного остаточного опухолевого клона (длительность 2-3 года)
НАЦИОНАЛЬНОЕ ГЕМАТОЛОГИЧЕСКОЕ ОБЩЕСТВО, «КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ДИАГНОСТИКЕ И ЛЕЧЕНИЮ ОСТРЫХ ЛИМФОБЛАСТНЫХ ЛЕЙКОЗОВ ВЗРОСЛЫХ» , 2018
Слайд 4129
3
8
15
22
1
36
Дэкс
ПЭГ-АСП
ВКР
ДРЦ
ТРИПЛЕТ
ИТБ*
Дэкс – дексаметазон; ПЭГ-АСП – пэгаспаргиназа; ВКР – винкристин; ДРЦ
- даунорубицин
Триплет – интратекальный метотрексат + цитарабин + преднизолон ; ИТБ – иматиниб*Для Ph+ОЛЛ
Лечение ALL-MB-2015
Протокол российской исследовательской группы ALL-MB 2015
Индукция
Сутки
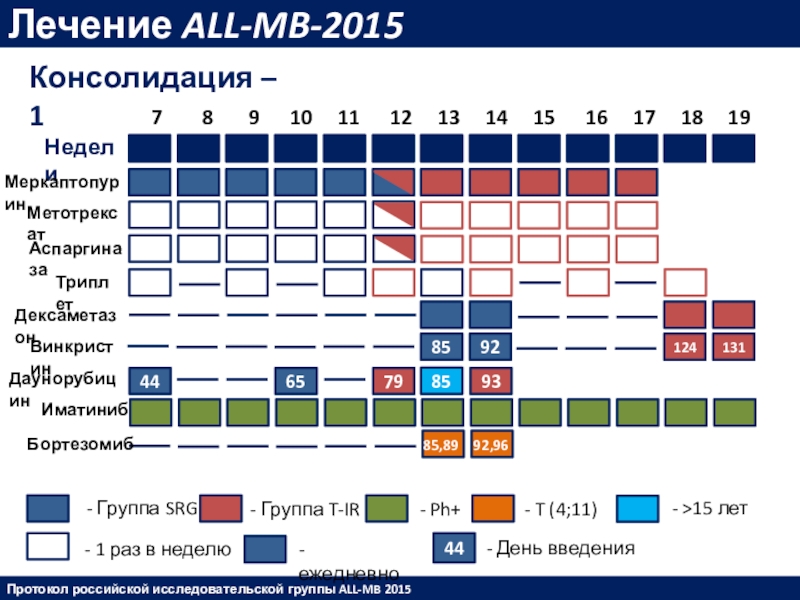
Слайд 42Лечение ALL-MB-2015
Консолидация – 1
7 8
9 10 11
12 13 14 15 16 17 18 1985
92
124
131
44
65
79
93
Протокол российской исследовательской группы ALL-MB 2015
Недели
Меркаптопурин
Метотрексат
Аспаргиназа
Триплет
Дексаметазон
Винкристин
Даунорубицин
Иматиниб
Бортезомиб
- Группа SRG
- Группа T-IR
- Ph+
- T (4;11)
85,89
92,96
85
- >15 лет
- 1 раз в неделю
- ежедневно
44
- День введения
Слайд 43Лечение ALL-MB-2015
Вторая фаза индукции (для группы T-IR)
Сутки
37
43
71
45 46 47
48
52 53 54 55
59 60 61 62
66
67 68 69 ЦФМ
Месна
МКП
Триплет
Цитарабин
ЦФМ – циклофосфамид; МКП - меркаптопурин
Протокол российской исследовательской группы ALL-MB 2015
Слайд 44Лечение ALL-MB-2015
Терапия пациентов высокого риска
Блок HR-1
Протокол российской исследовательской группы
ALL-MB 2015
Метилпреднизолон
Винкристин
Метотрексат
Фолинат кальция
Циклофосфамид
Месна
Цитарабин
ПЭГ-аспаргиназа
Триплет
Сутки
1
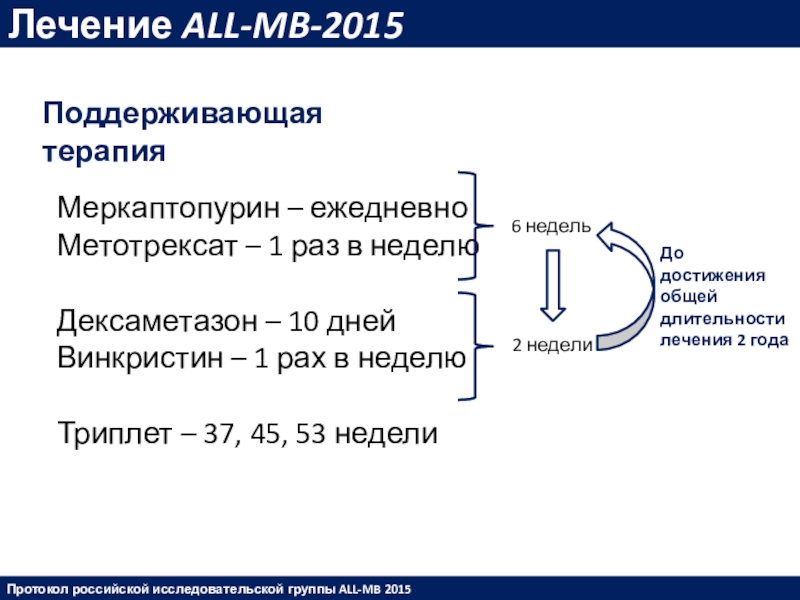
2 3 4 5 6Слайд 45Лечение ALL-MB-2015
Меркаптопурин – ежедневно
Метотрексат – 1 раз в неделю
Дексаметазон – 10 дней
Винкристин – 1 рах в неделю
Триплет – 37, 45, 53 недели
Протокол российской исследовательской группы ALL-MB 2015
Поддерживающая терапия
6 недель
2 недели
До достижения
общей длительности
лечения 2 года
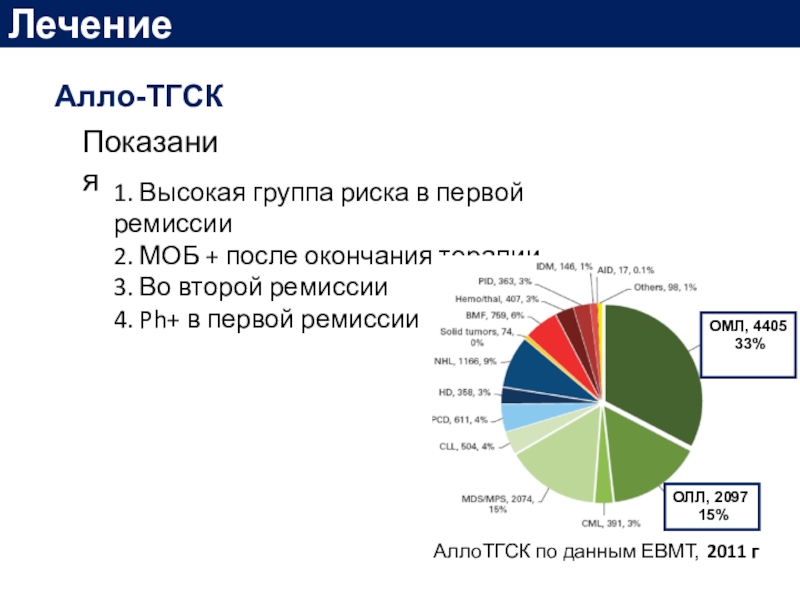
Слайд 46Лечение
Алло-ТГСК
1. Высокая группа риска в первой ремиссии
2. МОБ +
после окончания терапии
3. Во второй ремиссии
4. Ph+ в
первой ремиссииПоказания
ОМЛ, 4405
33%
ОЛЛ, 2097
15%
АллоТГСК по данным EBMT, 2011 г
Слайд 47Лечение
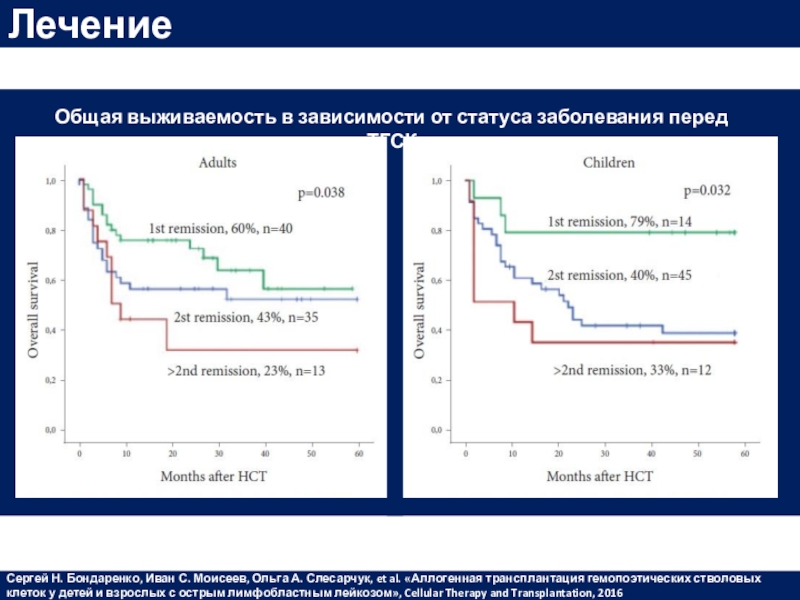
Сергей Н. Бондаренко, Иван С. Моисеев, Ольга А. Слесарчук, et al. «Аллогенная трансплантация
гемопоэтических стволовых клеток у детей и взрослых с острым лимфобластным
лейкозом», Cellular Therapy and Transplantation, 2016Общая выживаемость в зависимости от статуса заболевания перед ТГСК
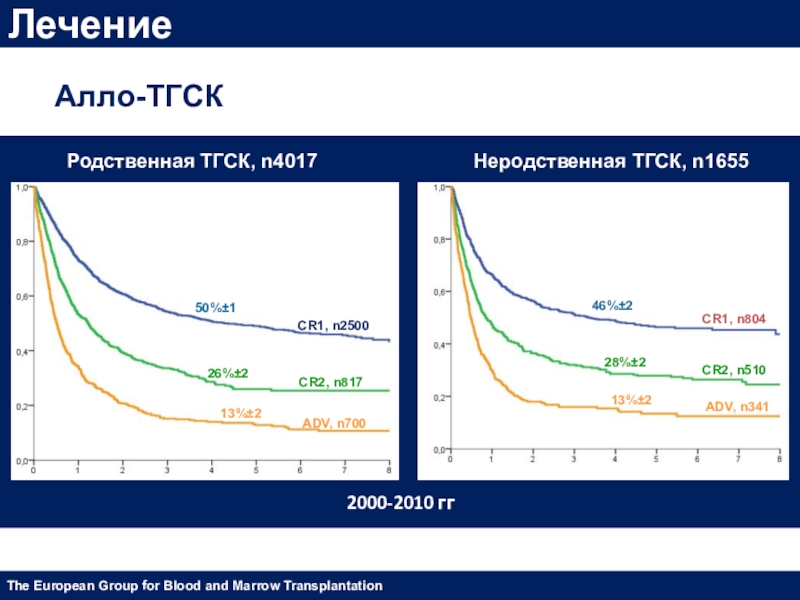
Слайд 48Лечение
CR1, n2500
CR1, n804
CR2, n817
CR2, n510
ADV, n700
ADV, n341
Неродственная ТГСК, n1655
Родственная ТГСК, n4017
50%±1
26%±2
13%±2
13%±2
28%±2
46%±2
Алло-ТГСК
The European Group for
Blood and Marrow Transplantation 2000-2010 гг
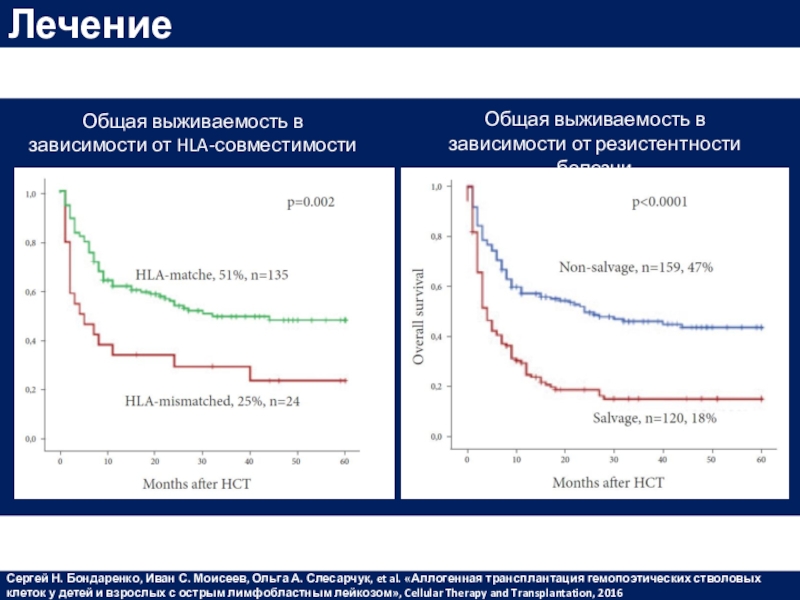
Слайд 49Лечение
Сергей Н. Бондаренко, Иван С. Моисеев, Ольга А. Слесарчук, et al. «Аллогенная трансплантация
гемопоэтических стволовых клеток у детей и взрослых с острым лимфобластным
лейкозом», Cellular Therapy and Transplantation, 2016Общая выживаемость в зависимости от HLA-совместимости
Общая выживаемость в зависимости от резистентности болезни
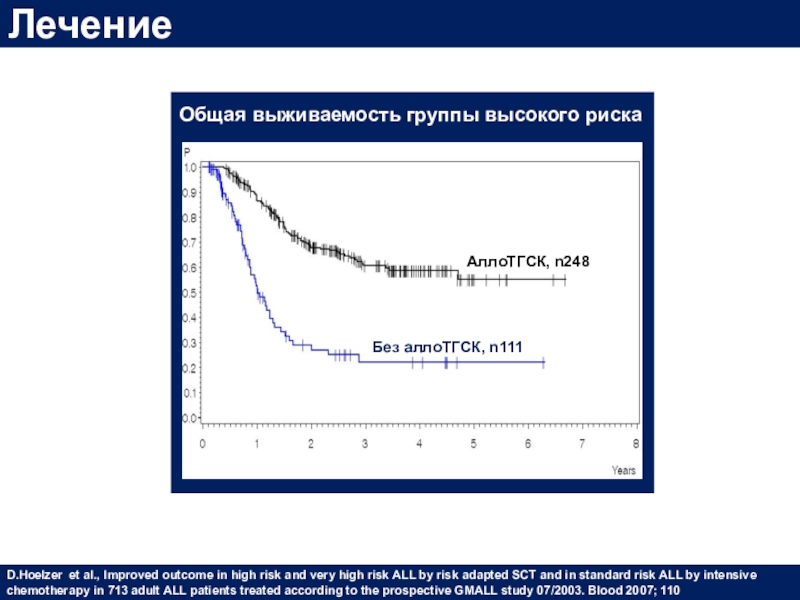
Слайд 50Общая выживаемость группы высокого риска
АллоТГСК, n248
Без аллоТГСК, n111
Лечение
D.Hoelzer et
al., Improved outcome in high risk and very high risk
ALL by risk adapted SCT and in standard risk ALL by intensive chemotherapy in 713 adult ALL patients treated according to the prospective GMALL study 07/2003. Blood 2007; 110Слайд 51ОЛЛ стандартного риска
Возраст 15-55 лет
МОБ+ на 16 неделе терапии
(после консолидации I)
Без аллоТГСК, n59, 23%
АллоТГСК, n27, 58%
Лечение
D.Hoelzer et al.,
Adult patients with acute lymphoblastic leukemia and molecular failure display a poor prognosis and are candidates for stem cell transplantatioфn and targeted therapies, Blood. 2012;120(9):1868-1876Слайд 52Лечение
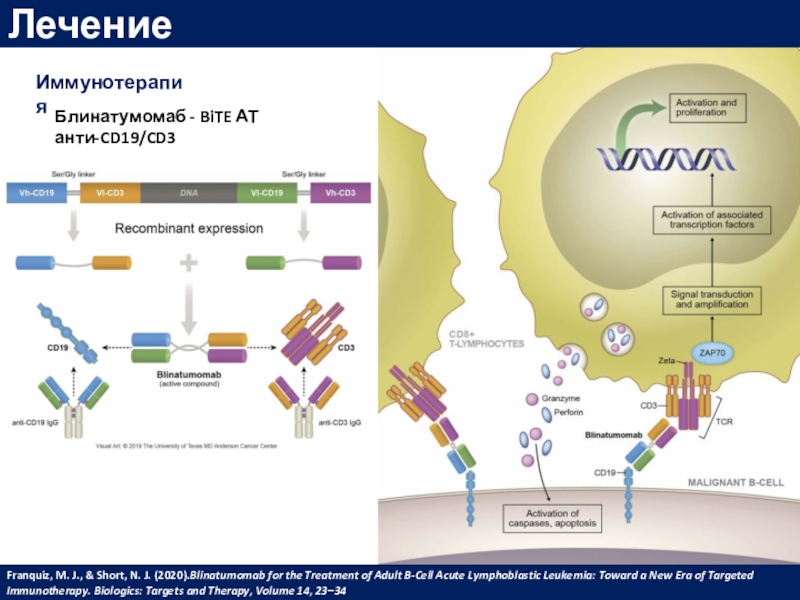
Иммунотерапия
Блинатумомаб - BiTE АТ анти-CD19/CD3
Franquiz, M. J., & Short,
N. J. (2020).Blinatumomab for the Treatment of Adult B-Cell Acute
Lymphoblastic Leukemia: Toward a New Era of Targeted Immunotherapy. Biologics: Targets and Therapy, Volume 14, 23–34Слайд 53Лечение
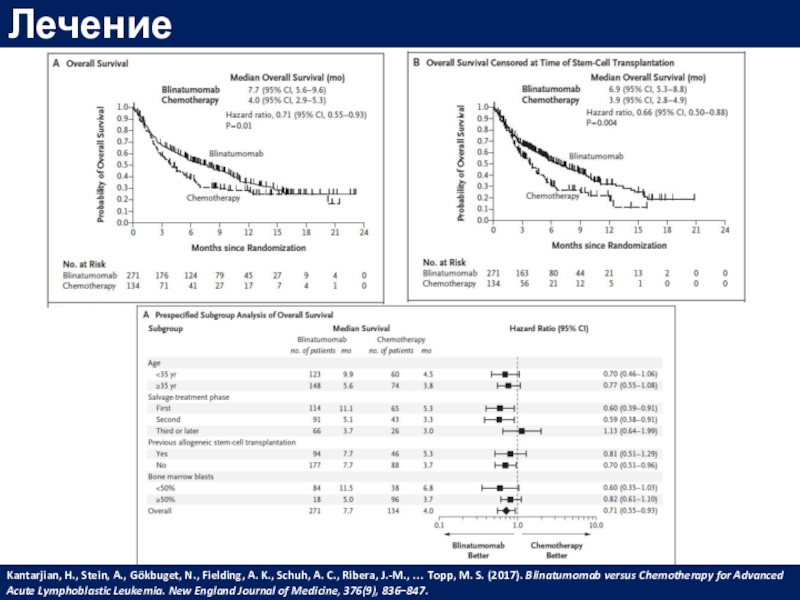
Kantarjian, H., Stein, A., Gökbuget, N., Fielding, A. K., Schuh,
A. C., Ribera, J.-M., … Topp, M. S. (2017). Blinatumomab versus
Chemotherapy for Advanced Acute Lymphoblastic Leukemia. New England Journal of Medicine, 376(9), 836–847.Слайд 54Лечение
Блинатумомаб в сравнении с историческим стандартным лечением минимальной
остаточной болезни
у взрослых с ОЛЛ из предшественников В-ОЛЛ
Gökbuget, N., Dombret, H.,
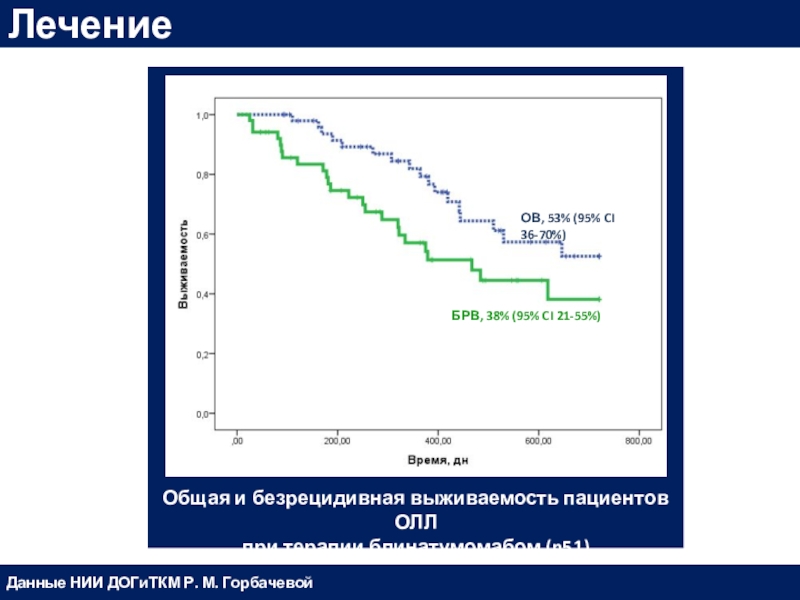
Giebel, S., Brüggemann, M., Doubek, M., Foa, R., … Bassan, R. (2019). Blinatumomab versus historic standard‐of‐care treatment for minimal residual disease in adults with B‐cell precursor acute lymphoblastic leukaemia. European Journal of Haematology.Слайд 55ОВ, 53% (95% CI 36-70%)
БРВ, 38% (95% CI 21-55%)
Общая и
безрецидивная выживаемость пациентов ОЛЛ
при терапии блинатумомабом (n51)
Лечение
Данные НИИ ДОГиТКМ
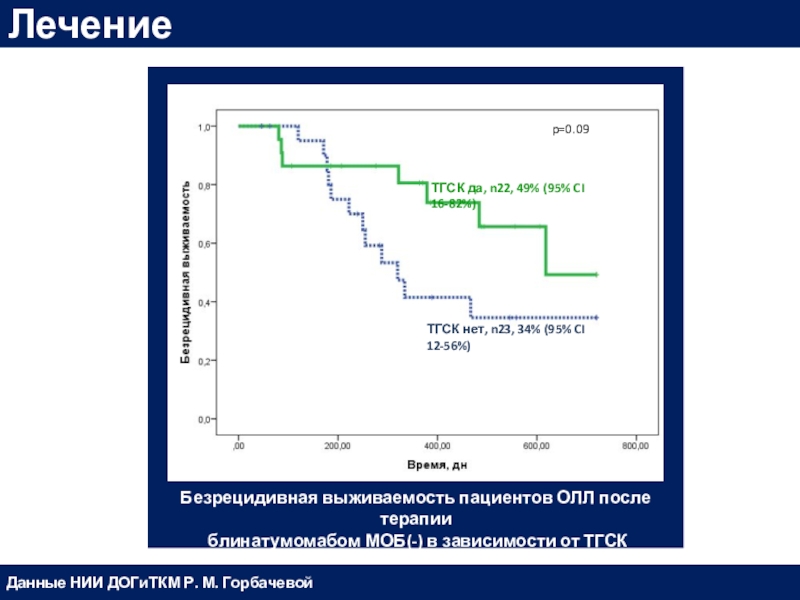
Р. М. ГорбачевойСлайд 56Безрецидивная выживаемость пациентов ОЛЛ после терапии
блинатумомабом МОБ(-) в зависимости
от ТГСК
Лечение
Данные НИИ ДОГиТКМ Р. М. Горбачевой
p=0.09
ТГСК нет, n23, 34%
(95% CI 12-56%)ТГСК да, n22, 49% (95% CI 16-82%)
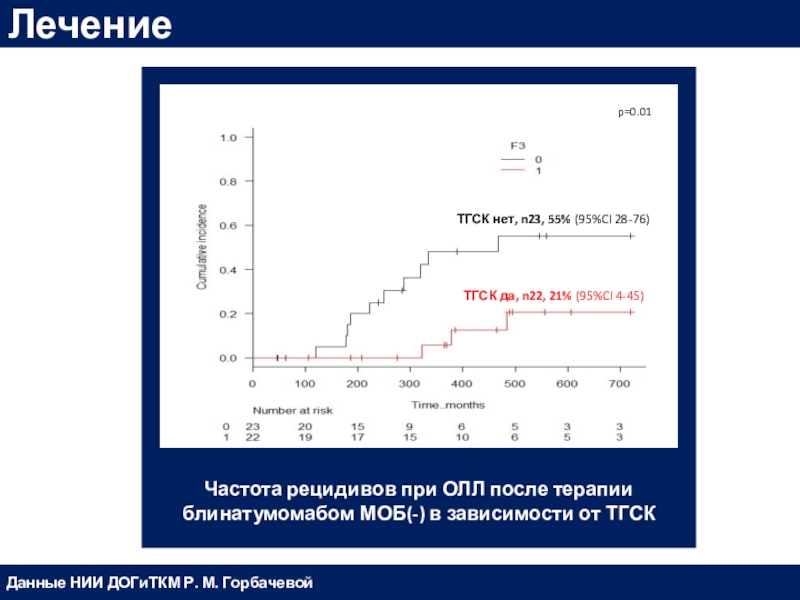
Слайд 57
Частота рецидивов при ОЛЛ после терапии блинатумомабом МОБ(-) в зависимости
от ТГСК
Лечение
Данные НИИ ДОГиТКМ Р. М. Горбачевой
ТГСК нет, n23, 55%
(95%CI 28-76)ТГСК да, n22, 21% (95%CI 4-45)
p=0.01
Слайд 59Лечение
Kantarjian, H. M., DeAngelo, D. J., Stelljes, M., Martinelli, G.,
Liedtke, M., Stock, W., … Advani, A. S. (2016). Inotuzumab Ozogamicin
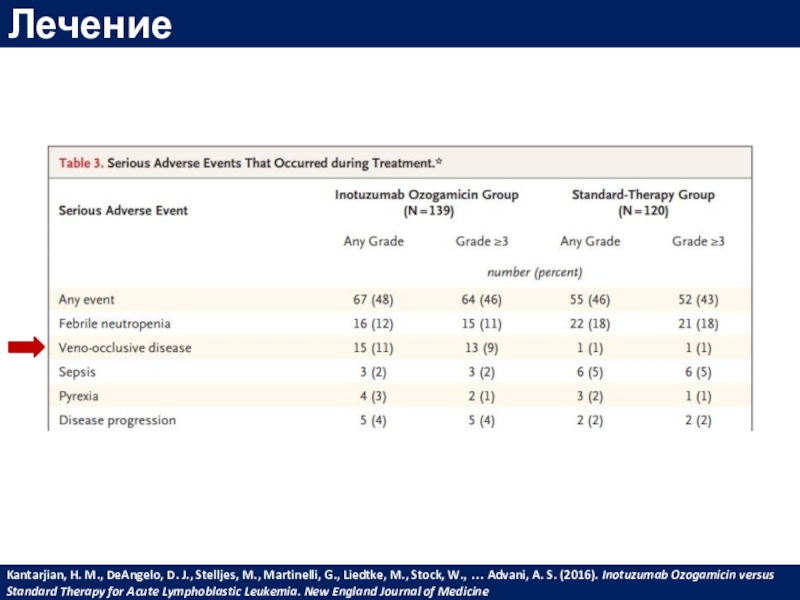
versus Standard Therapy for Acute Lymphoblastic Leukemia. New England Journal of MedicineСлайд 60Лечение
Kantarjian, H. M., DeAngelo, D. J., Stelljes, M., Martinelli, G.,
Liedtke, M., Stock, W., … Advani, A. S. (2016). Inotuzumab Ozogamicin
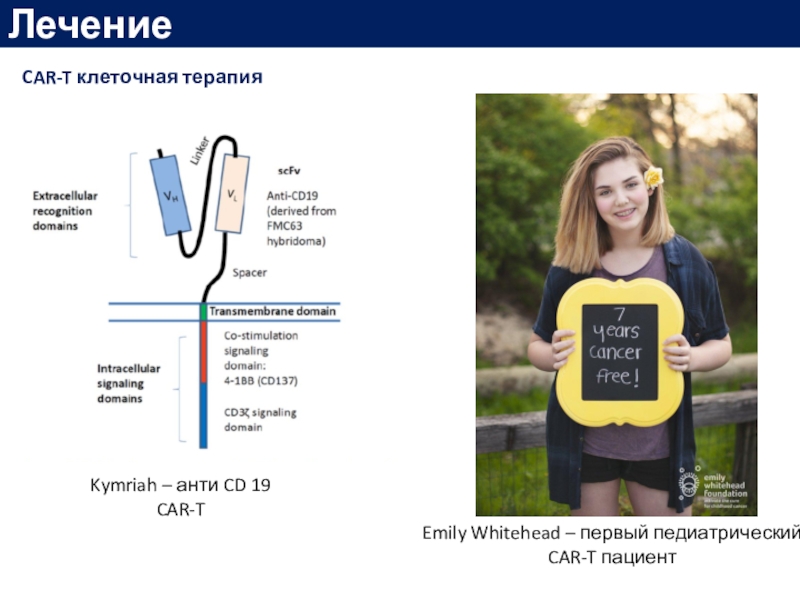
versus Standard Therapy for Acute Lymphoblastic Leukemia. New England Journal of MedicineСлайд 61Лечение
CAR-T клеточная терапия
Kymriah – анти CD 19 CAR-T
Emily Whitehead
– первый педиатрический CAR-T пациент
Слайд 63Лечение
«На данный момент мы находимся на стадии обсуждения плана, как
внедрить эту технологию наиболее эффективно», руководитель отдела вывода биомедицинских клеточных
продуктов (БМКП) на рынок в регионе «Европа» Этьен ЖоусемЖУРНАЛ VADEMECUM
Слайд 64Лечение
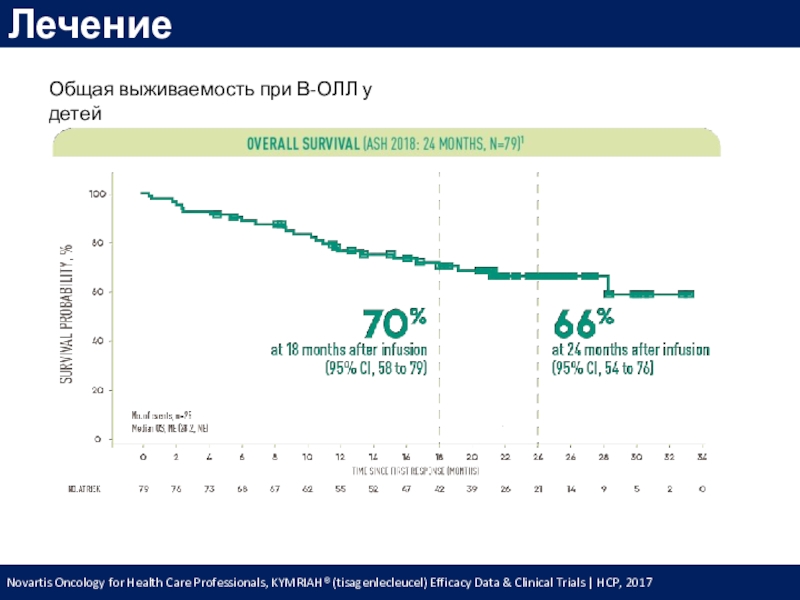
Novartis Oncology for Health Care Professionals, KYMRIAH® (tisagenlecleucel) Efficacy Data
& Clinical Trials | HCP, 2017
Общая выживаемость при В-ОЛЛ у
детейСлайд 65Лечение
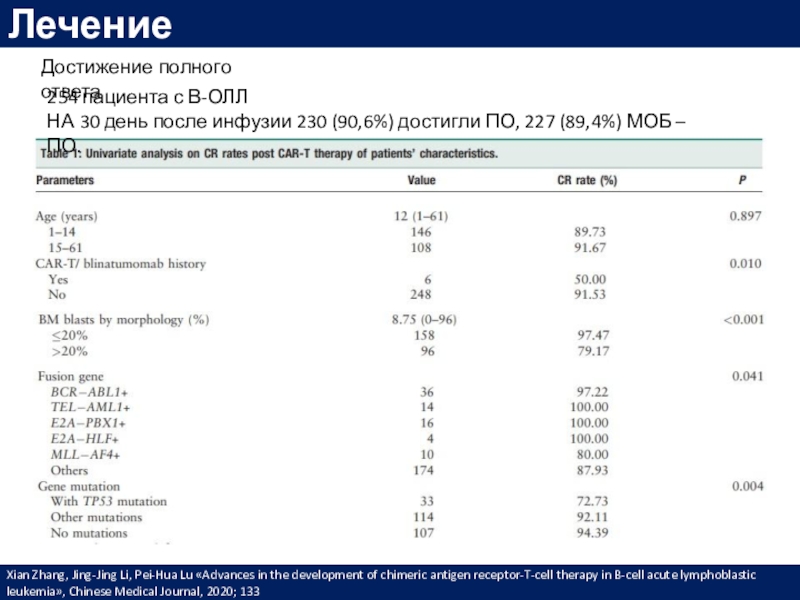
Xian Zhang, Jing-Jing Li, Pei-Hua Lu «Advances in the development
of chimeric antigen receptor-T-cell therapy in B-cell acute lymphoblastic leukemia»,
Chinese Medical Journal, 2020; 133Достижение полного ответа
254 пациента с В-ОЛЛ
НА 30 день после инфузии 230 (90,6%) достигли ПО, 227 (89,4%) МОБ – ПО.
Слайд 66Лечение
Побочные эффекты :
• Синдром выброса цитокинов
• Нейротоксичность
• В-клеточная
аплазия
Xian Zhang, Jing-Jing Li, Pei-Hua Lu «Advances in the
development of chimeric antigen receptor-T-cell therapy in B-cell acute lymphoblastic leukemia», Chinese Medical Journal, 2020; 133Слайд 67Проблема : высокодозная химиотерапия повреждает лимфоциты пациента, снижая качество произведенных
CAR-T
Решение : использование «универсальных» клеток CAR-T (UCAR) –
готовый продукт,
полученный из аллогенных здоровых донорских Т-клеток Проблема 2 : уничтожение чужих CAR-T иммунной системой реципиента
Решение : Генное модифицирование CAR-T?
Лечение
Слайд 68Лечение
CAR T – анти CD 19 (CD 52-, TCR αβ-)
+ Использование Алемтузумаба
(анти CD 52) в режиме кондиционирования
Слайд 69Лечение
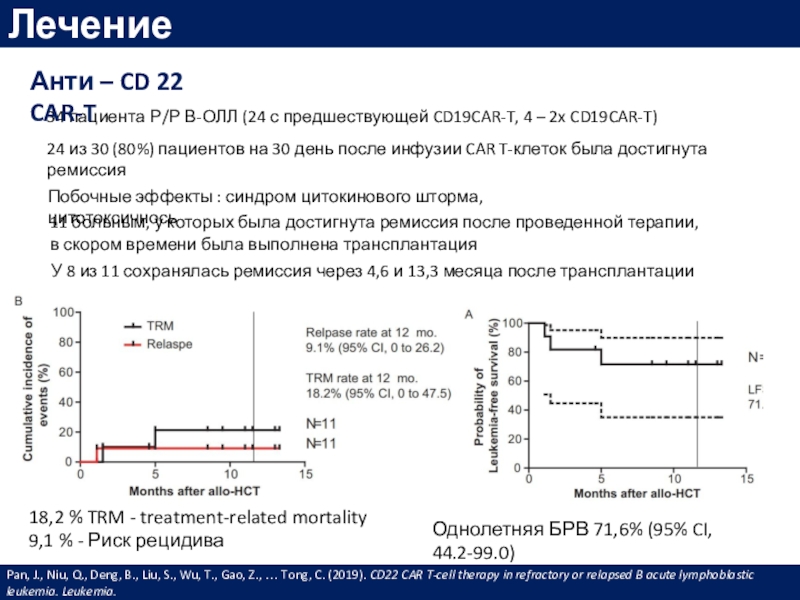
34 пациента Р/Р В-ОЛЛ (24 с предшествующей CD19CAR-T, 4 –
2x CD19CAR-T)
Анти – CD 22 CAR-T
Pan, J., Niu, Q., Deng,
B., Liu, S., Wu, T., Gao, Z., … Tong, C. (2019). CD22 CAR T-cell therapy in refractory or relapsed B acute lymphoblastic leukemia. Leukemia.24 из 30 (80%) пациентов на 30 день после инфузии CAR T-клеток была достигнута ремиссия
11 больным, у которых была достигнута ремиссия после проведенной терапии, в скором времени была выполнена трансплантация
У 8 из 11 сохранялась ремиссия через 4,6 и 13,3 месяца после трансплантации
Однолетняя БРВ 71,6% (95% CI, 44.2-99.0)
Побочные эффекты : синдром цитокинового шторма, цитотоксичнось
18,2 % TRM - treatment-related mortality
9,1 % - Риск рецидива
Слайд 70Динамика общей выживаемости детей с ОЛЛ в период с 1968
по 2009 год
Hunger, S. P., & Mullighan, C. G. (2015). Acute
Lymphoblastic Leukemia in Children. New England Journal of Medicine, 373(16), 1541–1552СПАСИБО ЗА ВНИМАНИЕ