Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
От простых правил
Содержание
- 1. От простых правил
- 2. Где начинается химия?..NaOHMgSO4Al(OH)3O2H2SO4KCl
- 3. Что нам потребуется?Структура молекулТаблица МенделееваОсновы геометрииУмение считать не более, чем до 18
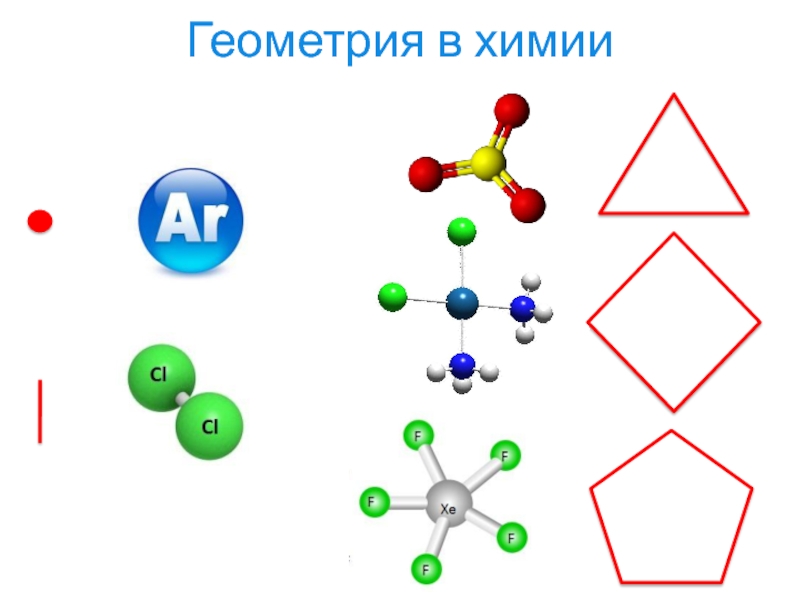
- 4. Геометрия в химии
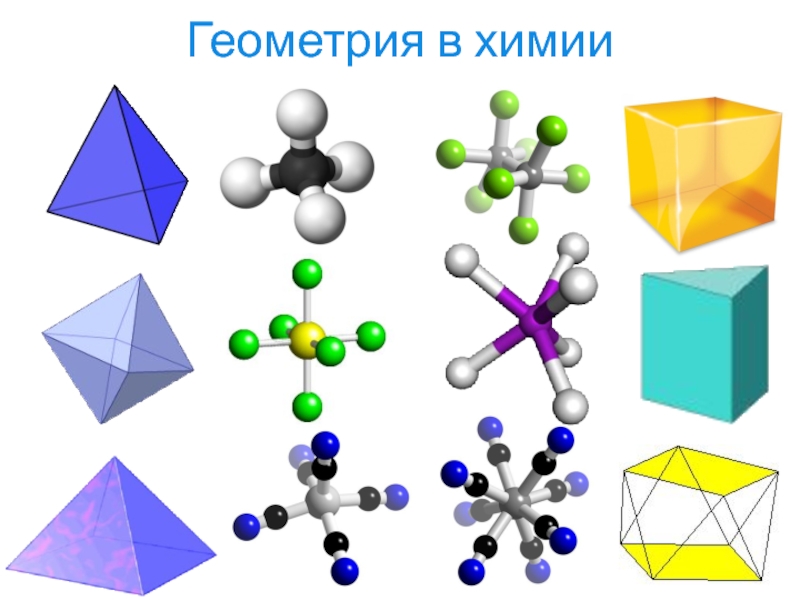
- 5. Геометрия в химии
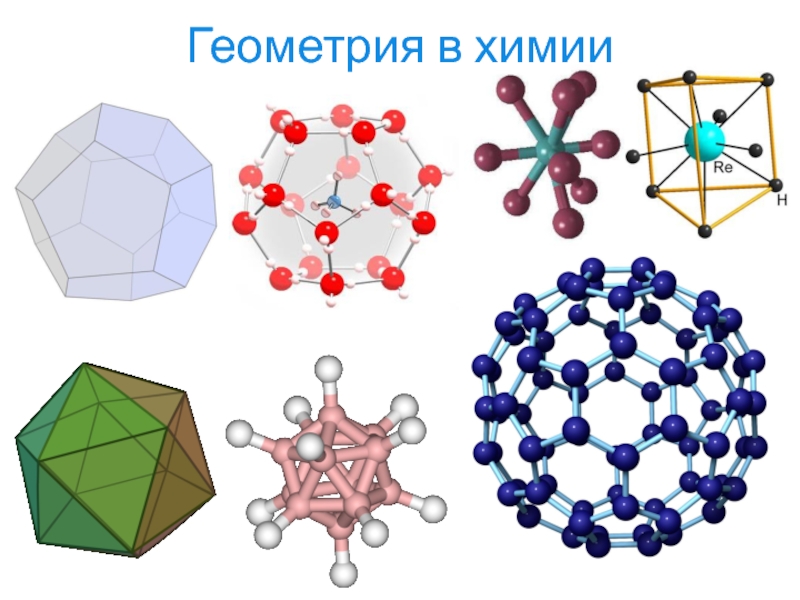
- 6. Геометрия в химии
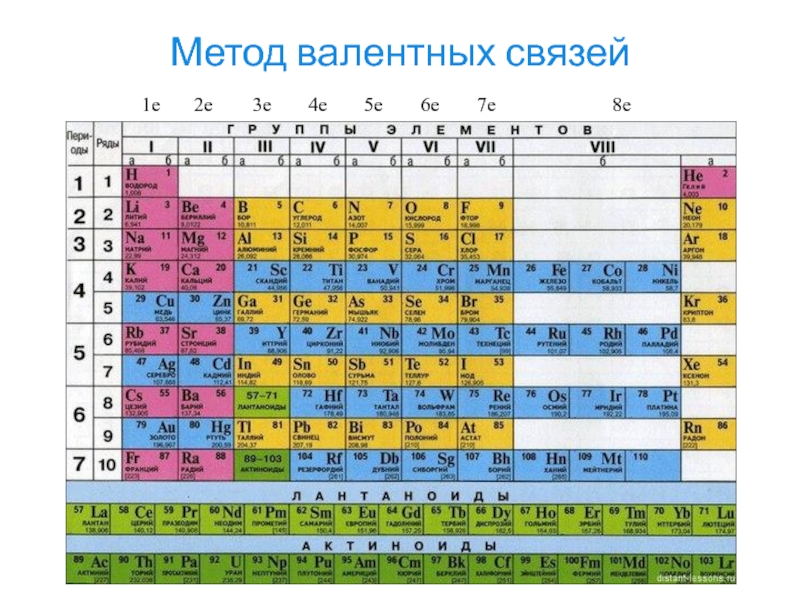
- 7. Метод валентных связей1e2e3e4e5e6e7e8e
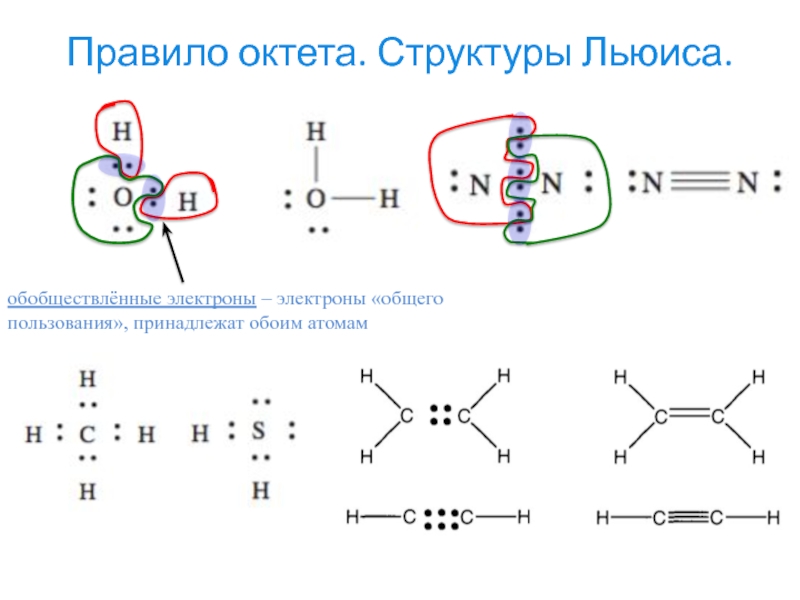
- 8. Правило октета. Структуры Льюиса.обобществлённые электроны – электроны «общего пользования», принадлежат обоим атомам
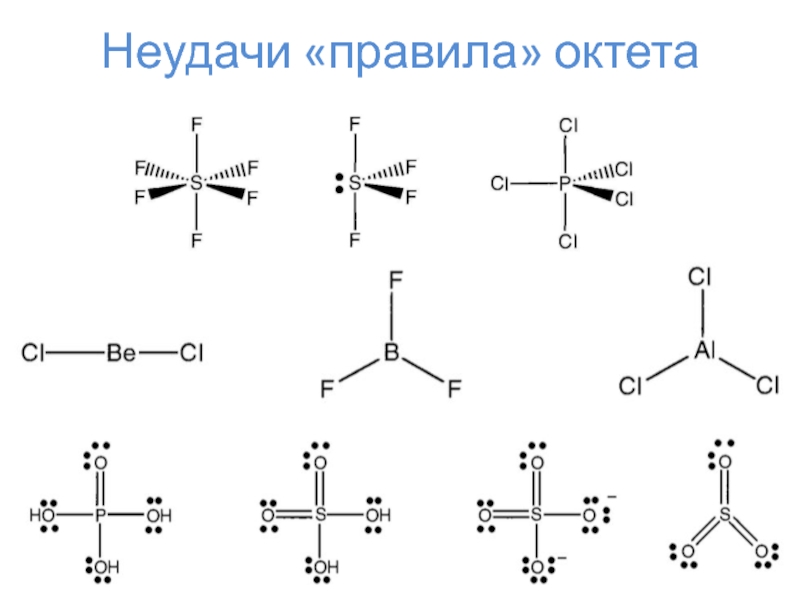
- 9. Неудачи «правила» октета
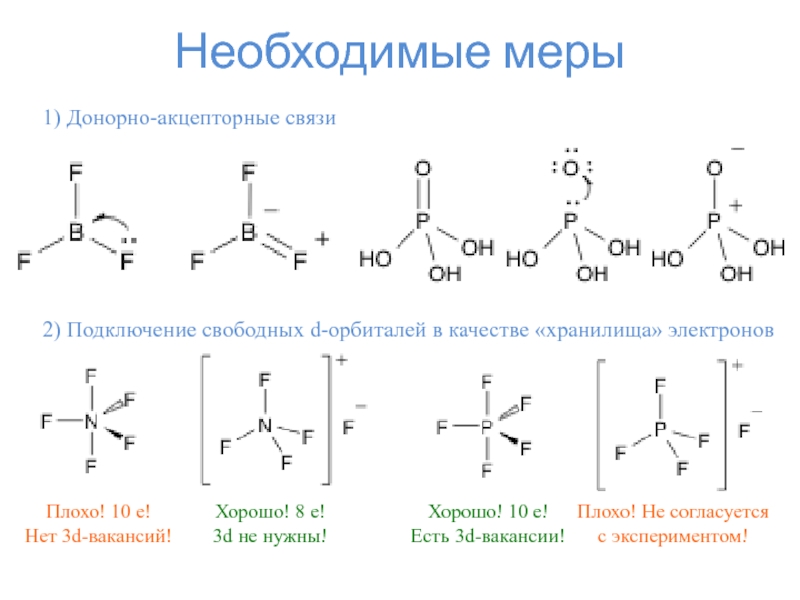
- 10. Необходимые меры1) Донорно-акцепторные связи2) Подключение свободных d-орбиталей
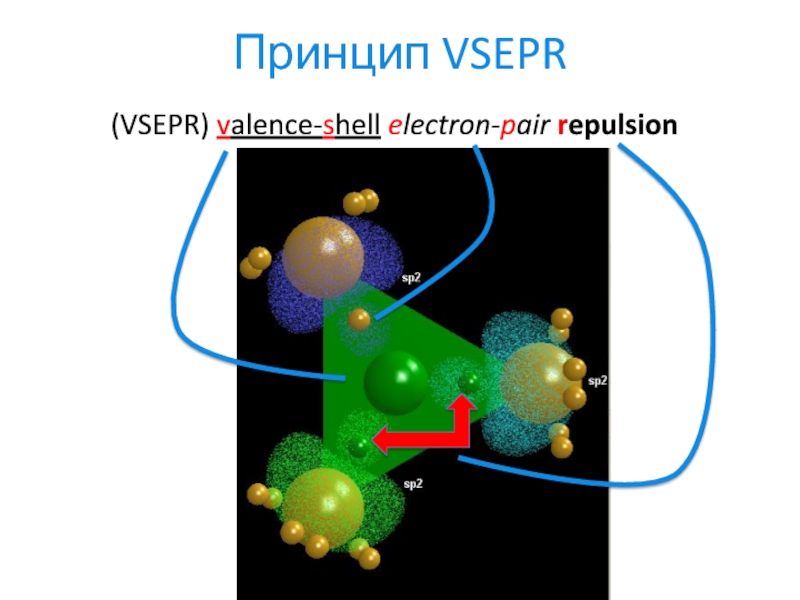
- 11. Принцип VSEPR(VSEPR) valence-shell electron-pair repulsion
- 12. Принцип VSEPR
- 13. Виды электронных парСвободные (несвязанные) пары электроновСвязанные пары электроновОбменные связиДонорно-акцепторные связи
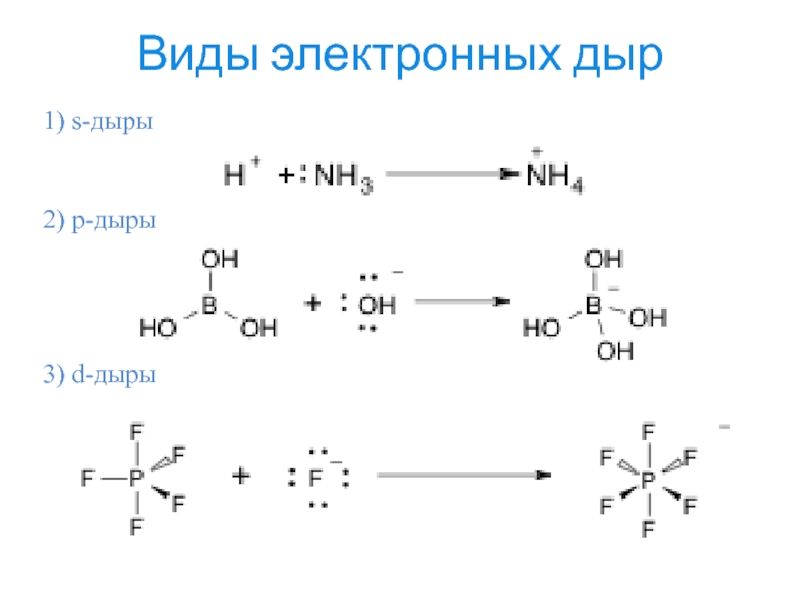
- 14. Виды электронных дыр1) s-дыры2) p-дыры3) d-дыры
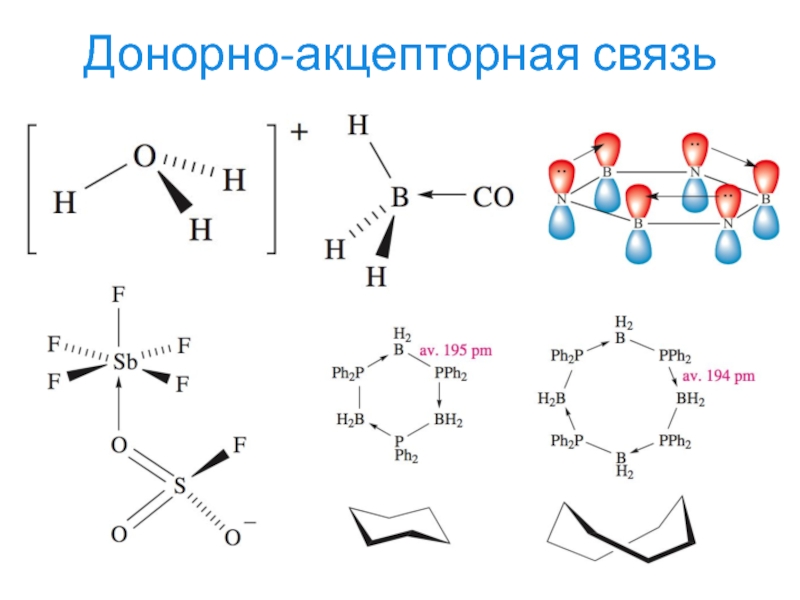
- 15. Донорно-акцепторная связь
- 16. Принцип VSEPR (правила Гиллеспи)Пары электронов внешней оболочки
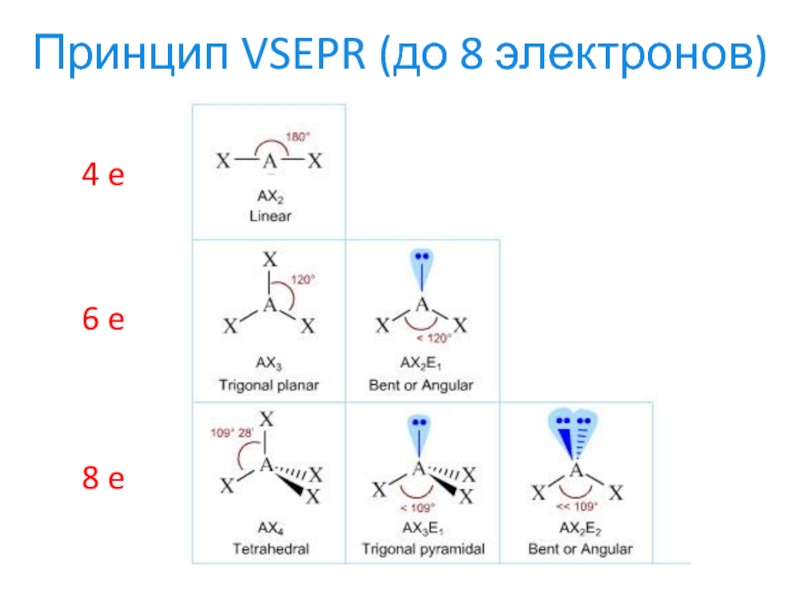
- 17. Принцип VSEPR (до 8 электронов)4 e6 e8 e
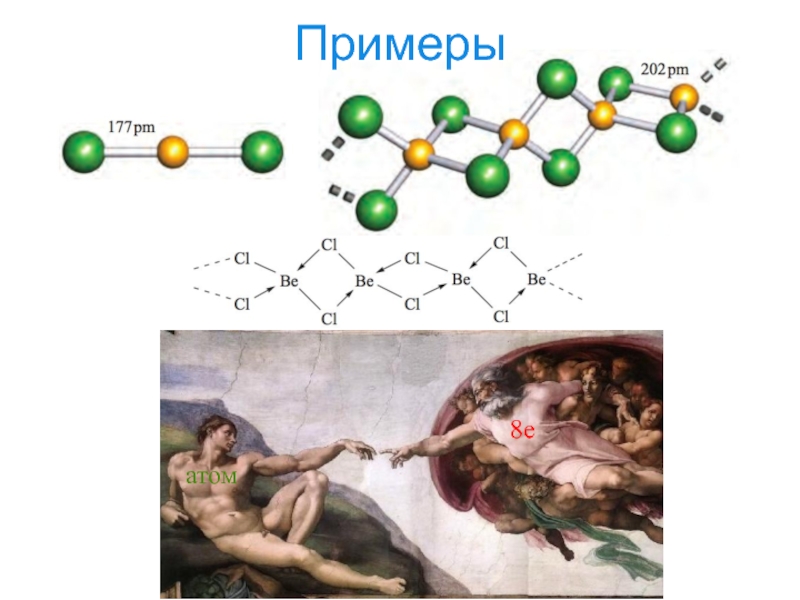
- 18. Примеры8eатом
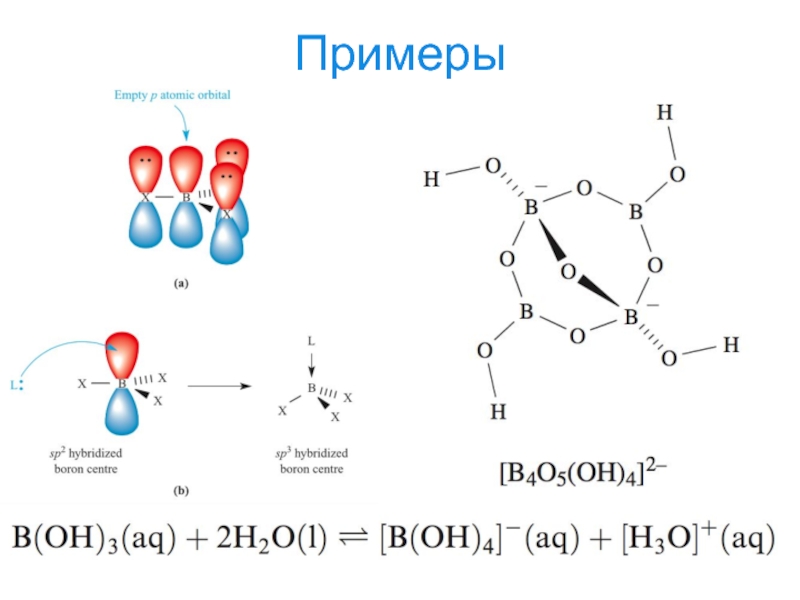
- 19. Примеры
- 20. Примеры[Be4(μ4-O)(μ-O2CMe)6]
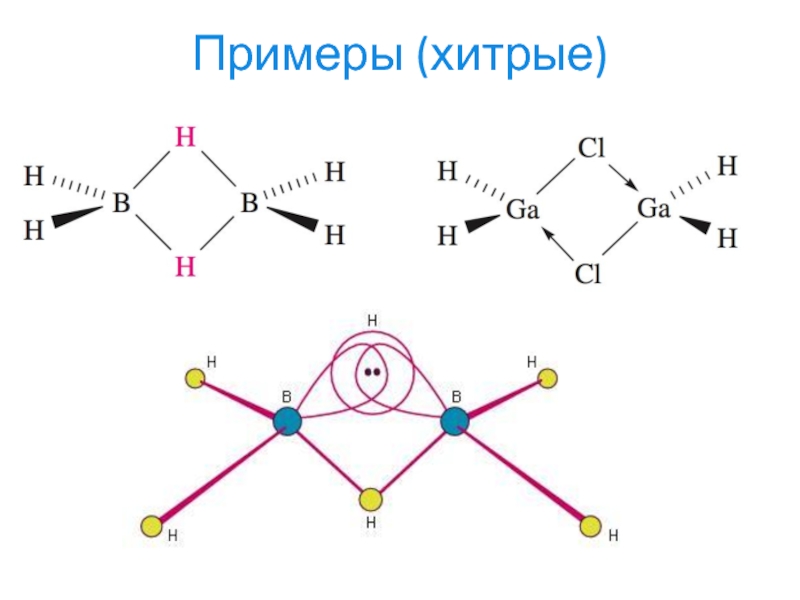
- 21. Примеры (хитрые)
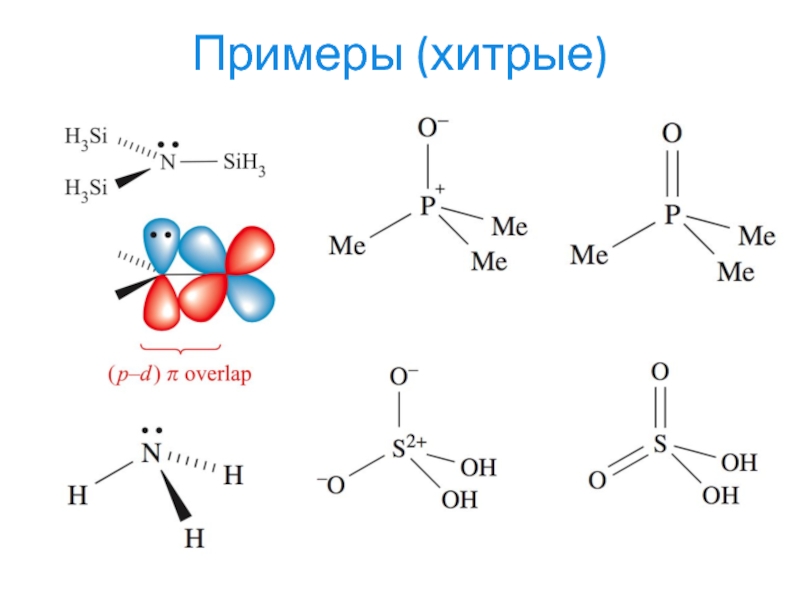
- 22. Примеры (хитрые)
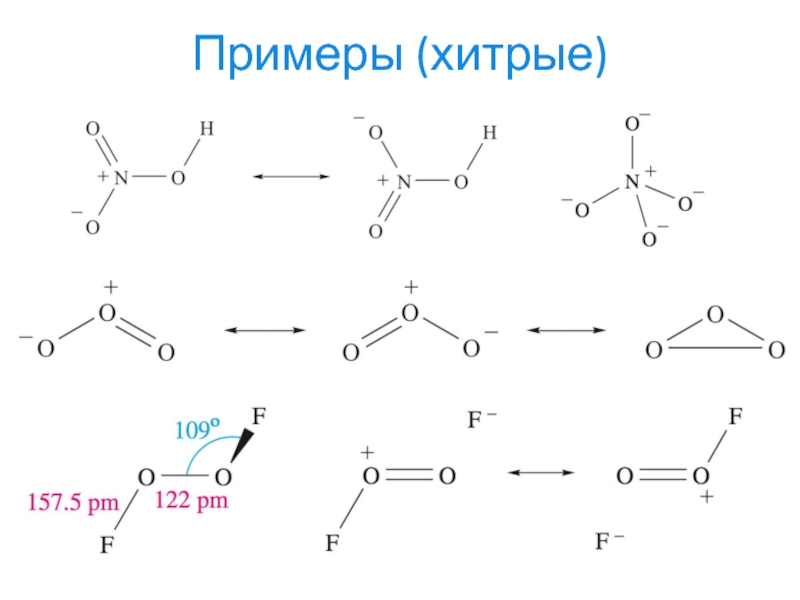
- 23. Примеры (хитрые)
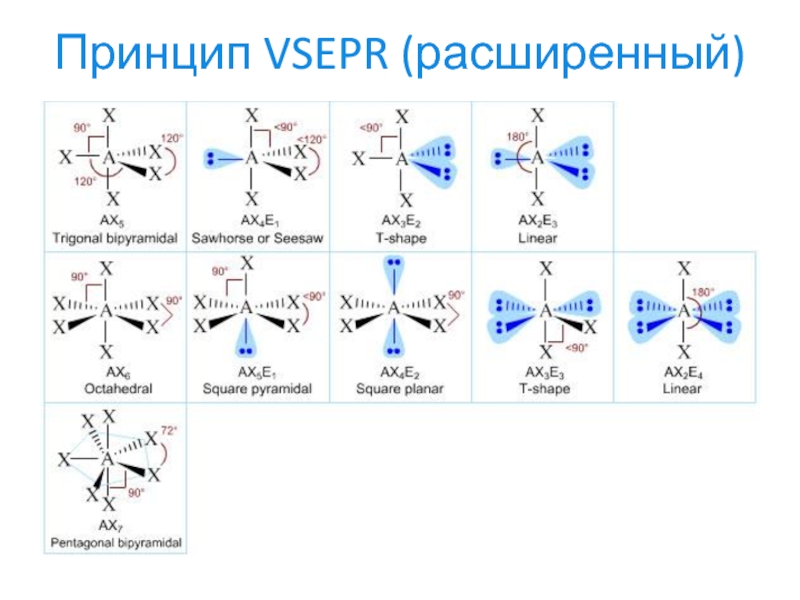
- 24. Принцип VSEPR (расширенный)
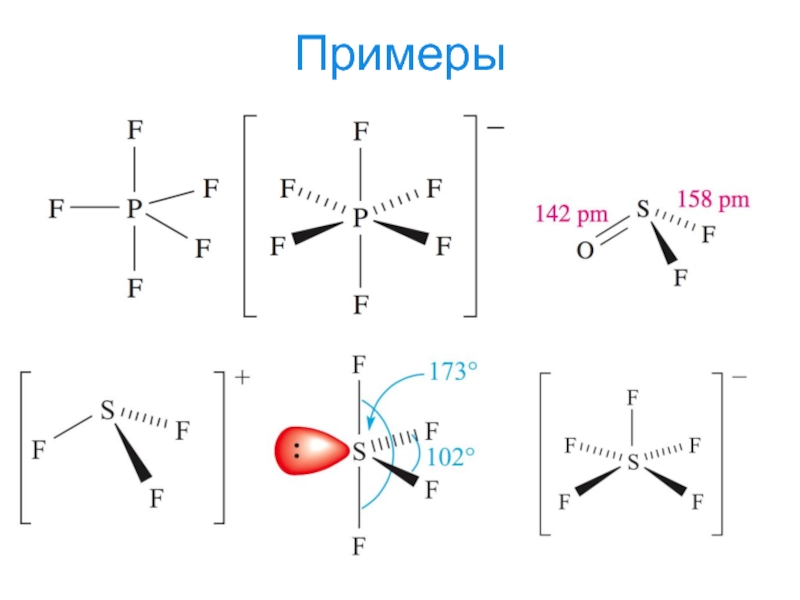
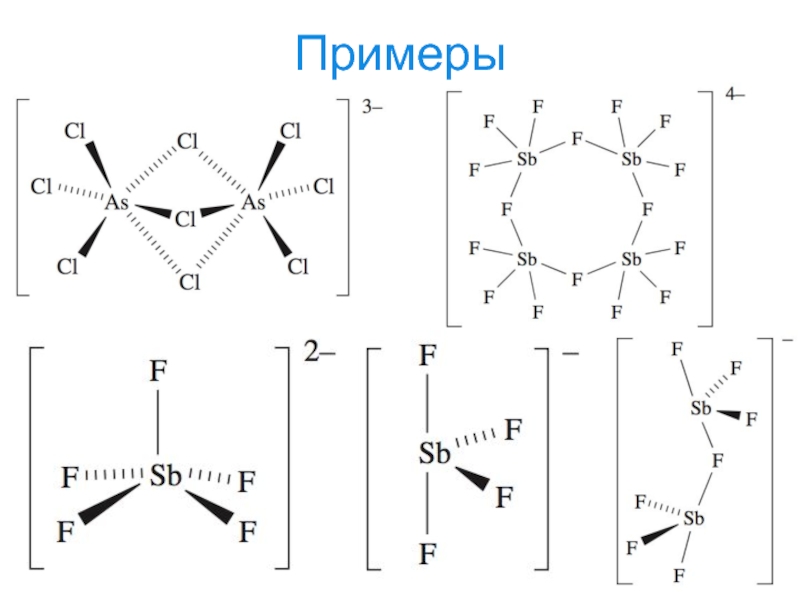
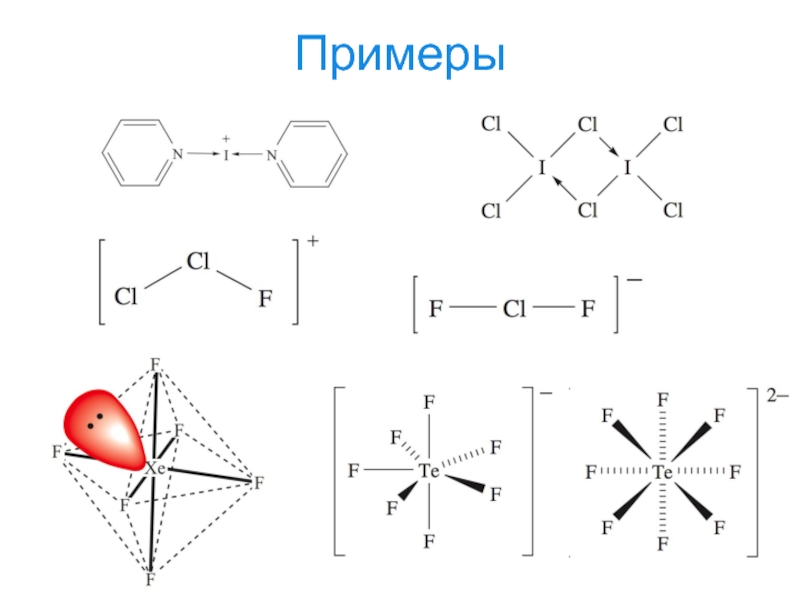
- 25. Примеры
- 26. Примеры
- 27. Примеры
- 28. Применим только для предсказания строения p-элементовНаблюдаются отклонения
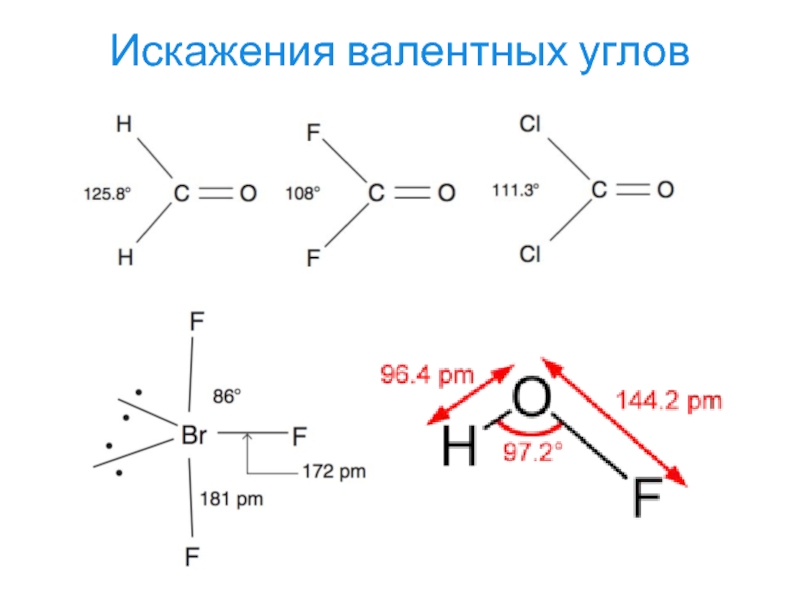
- 29. Искажения валентных углов
- 30. Конец
- 31. Скачать презентанцию
Где начинается химия?..NaOHMgSO4Al(OH)3O2H2SO4KCl
Слайды и текст этой презентации
Слайд 1От простых правил
Лекцию подготовил: Шлапаков Никита, студент 6 курса
Химического факультета МГУ.
Слайд 3Что нам потребуется?
Структура молекул
Таблица Менделеева
Основы геометрии
Умение считать не более, чем
до 18
Слайд 8Правило октета. Структуры Льюиса.
обобществлённые электроны – электроны «общего пользования», принадлежат
обоим атомам
Слайд 10Необходимые меры
1) Донорно-акцепторные связи
2) Подключение свободных d-орбиталей в качестве «хранилища»
электронов
Плохо! 10 e!
Нет 3d-вакансий!
Хорошо! 8 e!
3d не нужны!
Хорошо! 10 e!
Есть
3d-вакансии!Плохо! Не согласуется
с экспериментом!
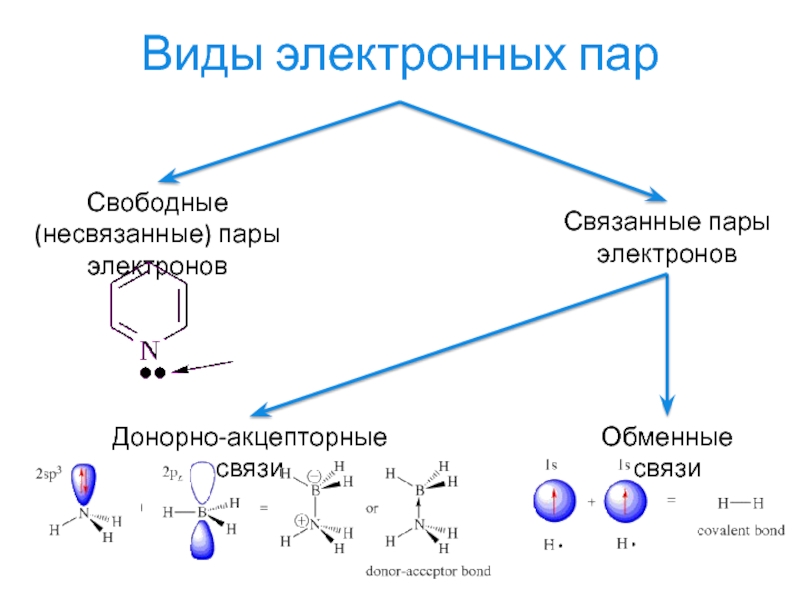
Слайд 13Виды электронных пар
Свободные (несвязанные) пары электронов
Связанные пары электронов
Обменные связи
Донорно-акцепторные связи
Слайд 16Принцип VSEPR (правила Гиллеспи)
Пары электронов внешней оболочки центрального атома испытывают
взаимное отталкивание;
Электронное отталкивание между парами ослабевает, если электронная плотность связи
уменьшается. Следствия:Отталкивание ослабевает при оттягивании электронной плотности от центрального атома за счёт электроотрицательности лигандов;
Отталкивание ослабевает при уменьшении порядка связи с лигандом;
Молекула стремится к такому расположению окружающих центральный атом лигандов, при котором отталкивание минимально.
Слайд 28Применим только для предсказания строения p-элементов
Наблюдаются отклонения от правила из-за
наличия стереохимически инертной s-пары у тяжёлых элементов с большим количеством
электроновНе учитывает отклонения от планарности ввиду стерических эффектов
Не учитывает специфические взаимодействия между лигандами
Ограничения использования VSEPR


![От простых правил Примеры[Be4(μ4-O)(μ-O2CMe)6] Примеры[Be4(μ4-O)(μ-O2CMe)6]](/img/thumbs/4ca4c6101317fd2d6fa61dcee8c7e2ca-800x.jpg)