Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Постаналитический этап лабораторной диагностики
Содержание
- 1. Постаналитический этап лабораторной диагностики
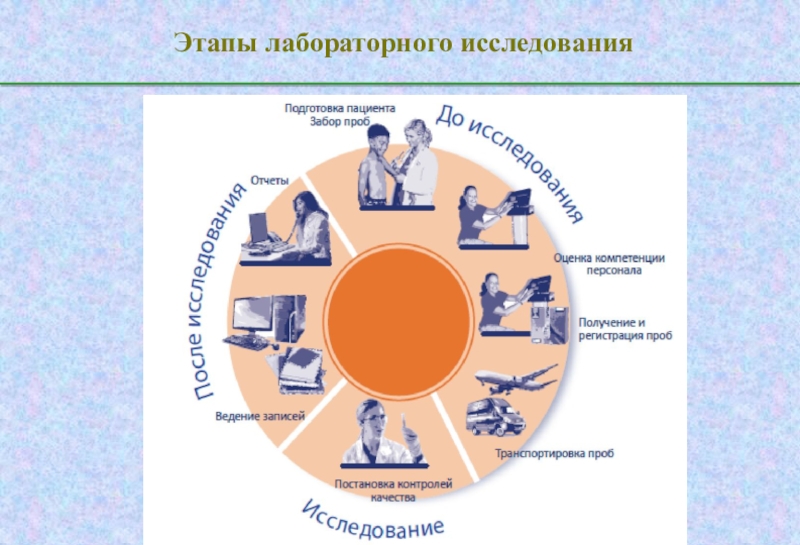
- 2. Этапы лабораторного исследования
- 3. Постаналитический этапПост-аналитический этапУчастие во внешней оценке качествавнелабораторные действия специалистаВыдача результатовОформлениерезультатовИнтерпретациярассмотрение результатов
- 4. Лабораторное исследование биоматериалаИнтерпретация полученного результатаПолучение результата исследованияУстановление
- 5. Постаналитический процессПо завершении аналитического процесса поступающие с
- 6. Референтные величиныПравильнее говорить не о «норме» лабораторного
- 7. Постаналитический процессПри необходимости специалист в области лабораторной
- 8. Постаналитический процессВ целях уточнения диагноза заболевания (состояния)
- 9. Постаналитический процессРезультат исследования направляется заказчику (лечащему врачу
- 10. Постаналитический процессКопия результата исследования может быть выдана
- 11. Сроки выполнения исследованийСроки выполнения клинических лабораторных исследований
- 12. Нормативное обеспечениеГОСТ Р ИСО 15189-2015 «Лаборатории медицинские.
- 13. Нормативное обеспечениеГОСТ Р 53079.2-2008 «Обеспечение качества клинических
- 14. Постаналитический этапПостаналитический этап можно разделить на:1. Внутрилабораторный
- 15. Обратите вниманиеВыдача результатов лабораторных исследований лечащему врачу
- 16. Индикаторы качества постаналитического этапаПредоставление отчетов о
- 17. Индикаторы качества постаналитического этапаИнтерпретация и оценка
- 18. Индикаторы качества постаналитического этапа3. Клиническое использование
- 19. Предотвращение ошибокСамый эффективный путь предотвращения ошибок на
- 20. Последствия лабораторных ошибокЛаборатории выдают результаты анализов, которые
- 21. Рекомендуемый перечень СОП-ов Для постаналитического этапа1 Правила
- 22. БЛАГОДАРЮ ЗА ВНИМАНИЕ (3822) 915-076
- 23. Скачать презентанцию
Этапы лабораторного исследования
Слайды и текст этой презентации
Слайд 1Томск - 25.09.2020
Постаналитический этап лабораторной диагностики
Пестерева С.В.
Зав. КДЛ ОГАУЗ «МСЧ
№ 2»
Слайд 3Постаналитический этап
Пост-аналитический
этап
Участие во внешней оценке качества
внелабораторные действия специалиста
Выдача
результатов
Оформление
результатов
Интерпретация
рассмотрение результатов
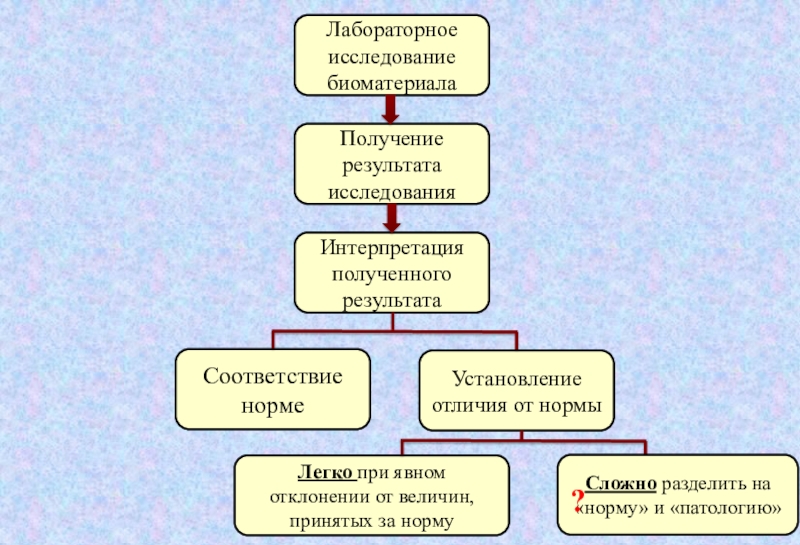
Слайд 4Лабораторное исследование биоматериала
Интерпретация полученного результата
Получение результата исследования
Установление отличия от нормы
Соответствие
норме
Легко при явном отклонении от величин, принятых за норму
Слайд 5Постаналитический процесс
По завершении аналитического процесса поступающие с анализаторов данные в
виде протокола сохраняются в ЛИС (МИС) или переносятся на бумажный
носитель, проверяются на соответствие референтным интервалам. В случае получения критических (угрожающих) значений либо эпидемиологически значимой информации сотрудник лаборатории передает информацию о результате исследования заказчику (лечащему врачу) в соответствии с установленным в организации порядке.Слайд 6Референтные величины
Правильнее говорить не о «норме» лабораторного показателя, а о
диапазоне, в котором располагаются нормальные (референтные) величины.
В настоящее время
ставший уже привычным в оценке результатов лабораторного исследования термин «норма» используется реже, вместо него говорят о референтных (референсных) значениях и результаты, полученные для конкретного пациента, сравнивают с так называемым референтным интервалом (диапазоном). Слайд 7Постаналитический процесс
При необходимости специалист в области лабораторной медицины может получать
разъяснения у врачей-специалистов, принимающих участие в обследовании и лечении пациента.
Правила взаимодействия сотрудников клинических подразделений и клинико-диагностических лабораторий медицинских организаций регламентируют национальные стандарты. При необходимости специалист в области лабораторной медицины может получать разъяснения у врачей-специалистов, принимающих участие в обследовании и лечении пациента. Правила взаимодействия сотрудников клинических подразделений и клинико-диагностических лабораторий медицинских организаций регламентируют национальные стандартыСлайд 8Постаналитический процесс
В целях уточнения диагноза заболевания (состояния) с учётом требований
стандартов медицинской помощи и клинических рекомендаций (протоколов лечения) по вопросам
оказания медицинской помощи могут быть назначены дополнительные лабораторные исследования при условии согласования с лечащим врачом либо с иным уполномоченным лицом учреждения или страховой компании.Результат исследования должен быть точным, ясным и недвусмыс-ленным, При необходимости вводится дополнительный текст с уточнением интерпретации либо дальнейшими рекомендациями.
Слайд 9Постаналитический процесс
Результат исследования направляется заказчику (лечащему врачу или в медицинскую
организацию) на бланке организации в электронном виде либо на бумажном
носителе при соблюдении требований законодательства Российской Федерации по защите конфиденциальной информации и персональных данных.Слайд 10Постаналитический процесс
Копия результата исследования может быть выдана пациенту или его
законному представителю в соответствии с законодательством в порядке, установленном в
медицинской организации.Слайд 11Сроки выполнения исследований
Сроки выполнения клинических лабораторных исследований с момента доставки
материала в лабораторию с учётом требований стандартов медицинской помощи и
клинических рекомендаций (протоколов лечения) по вопросам оказания медицинской помощи подразделяются на:экстренные – до 60 минут;
плановые – свыше 3 часов.
Слайд 12Нормативное обеспечение
ГОСТ Р ИСО 15189-2015 «Лаборатории медицинские. Частные требования к
качеству и компетентности»
ГОСТ Р 53022.3-2008 Технологии лабораторные клинические. Требования
к качеству клинических лабораторных исследований. Часть 3. Правила оценки клинической информативности лабораторных тестов ГОСТ Р 53022.4-2008 Технологии лабораторные клинические. Требования к качеству клинических лабораторных исследований. Часть 4. Правила разработки требований к своевременности предоставления лабораторной информации
Слайд 13Нормативное обеспечение
ГОСТ Р 53079.2-2008 «Обеспечение качества клинических лабораторных исследований. Часть
3. Правила взаимодействия персонала клинических подразделений и клинико-диагностических лабораторий медицинских
организаций при выполнении клинических лабораторных исследований»Приказ МЗ СССР от 04.10.1980 г. N 1030 "Об утверждении форм первичной документации учреждений здравоохранения"
Слайд 14Постаналитический этап
Постаналитический этап можно разделить на:
1. Внутрилабораторный :
Оформление бланка с
результатами теста (может выполняться на самом анализаторе)
Оценка результата по интервалам
норм (валидация)Регистрация результатов анализа
2. Внелабораторный:
доставка результатов исследования врачу
Использование результатов в диагностическом процессе.
Интерпретация результатов, диагноз и лечение пациента.
Слайд 15Обратите внимание
Выдача результатов лабораторных исследований лечащему врачу или пациенту допускается
лишь при условии их утверждения ответственным лабораторным специалистом, что заверяется
его подписью.При получении в лаборатории результатов, отражающих угрозу жизни пациента, сведения о них лабораторный персонал должен немедленно довести до лечащего врача для принятия необходимых мер.
Слайд 16Индикаторы качества постаналитического этапа
Предоставление отчетов о результатах:
Своевременность предоставления отчетов
о критически важной информации
Отражение результатов исследований референтной выличины каждого исследуемого
параметраРасположение результатов исследования на бланке по патофизиологическому принципу
Исправленные отчеты вследствие выявленных ошибок
Соблюдение конфиденциальности результатов исследования
Слайд 17Индикаторы качества постаналитического этапа
Интерпретация и оценка результатов исследования
Сопоставление результатов
с референтными интервалами для соответствую-щего контингента
Сопоставление результатов данного исследования с
предшествующими аналогичными или параллельно проведенными сопряженными тестами у данного пациентаОценка возможной лекарственной интерференции
Выявление причин обнаруженных грубых отклонений результатов от ожидаемых
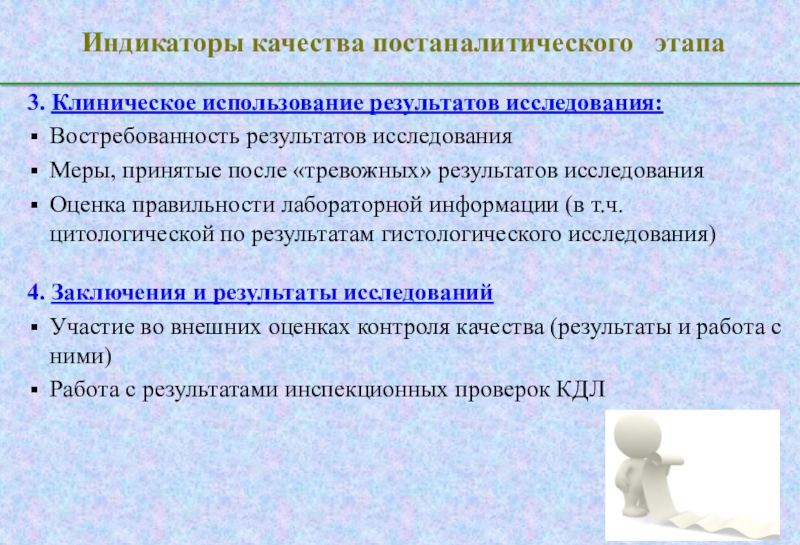
Слайд 18Индикаторы качества постаналитического этапа
3. Клиническое использование результатов исследования:
Востребованность результатов
исследования
Меры, принятые после «тревожных» результатов исследования
Оценка правильности лабораторной информации (в
т.ч. цитологической по результатам гистологического исследования) 4. Заключения и результаты исследований
Участие во внешних оценках контроля качества (результаты и работа с ними)
Работа с результатами инспекционных проверок КДЛ
Слайд 19Предотвращение ошибок
Самый эффективный путь предотвращения ошибок на любом этапе исследования
– это разработка стандартов (СОП-ов) для каждой его процедуры, разработка
критериев оценки качества каждой процедуры и квалифицированный персонал.Слайд 20Последствия лабораторных ошибок
Лаборатории выдают результаты анализов, которые широко используются в
клинических и санитарно-гигиенических учреждениях, и от правильности как самого анализа,
так и отчета о его результатах зависят конечные показатели индивидуального и общественного здоровья. Последствия выдачи неправильных результатов могут быть очень значительными:ненужное лечение,
осложнения в результате лечения,
отсутствие надлежащего лечения,
задержка в постановке правильного диагноза,
дополнительные и ненужные анализы.
Такие последствия приводят к увеличению затрат как времени, так и усилий сотрудников и часто к плохому результату лечения пациентов.
Слайд 21Рекомендуемый перечень СОП-ов
Для постаналитического этапа
1 Правила оформления, верификации и
утверждения данных протокола исследований
2 Правила выдачи информации пациенту или клиницисту
3
Правила пересылки информации по электронным средствам связи4 Правила информирования получателя обо всех значимых факторах проведения исследования (примеры: отсутствие информации о соблюдении/не соблюдении пациентом условий подготовки к сдаче биоматерила; различные не критичные данные по качеству биоматерила и т.п.)
5 Правила взаимодействия с клиницистами по интерпретации данных
6 Правила реагирования на претензии пользователей
СОПы 1 – 6 утверждает Главный врач учреждения здравоохранения.