Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Предмет изучения химии. Атомно-молекулярное учение
Содержание
- 1. Предмет изучения химии. Атомно-молекулярное учение
- 2. Слайд 2
- 3. Химия -наука о веществах, их строении, свойствах
- 4. «Если бы в результате какой-то мировой катастрофы
- 5. Атомистика - учение о прерывном строении материи
- 6. Демокрит (460-370 гг. до н.э.) впервые
- 7. Атомистика древних материалистоввсе состоит из атомоватомы физически
- 8. Механистическая атомистика Роберт Бойль
- 9. Закон Бойля–Мариотта 1662
- 10. Атомно-молекулярное учение М.В. Ломоносова «Элементы математической
- 11. Атомистическая теория Джона Дальтона «Новая система
- 12. Атомистическая теория Джона Дальтона «Новая система
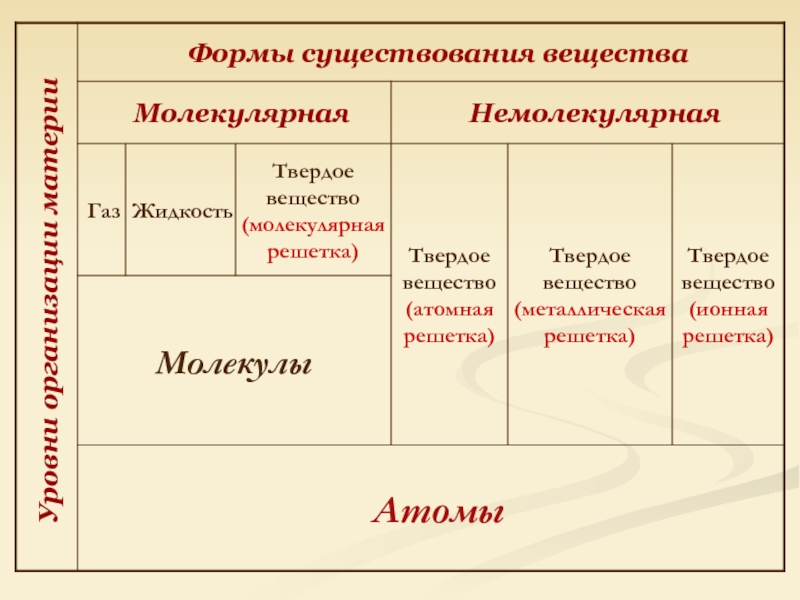
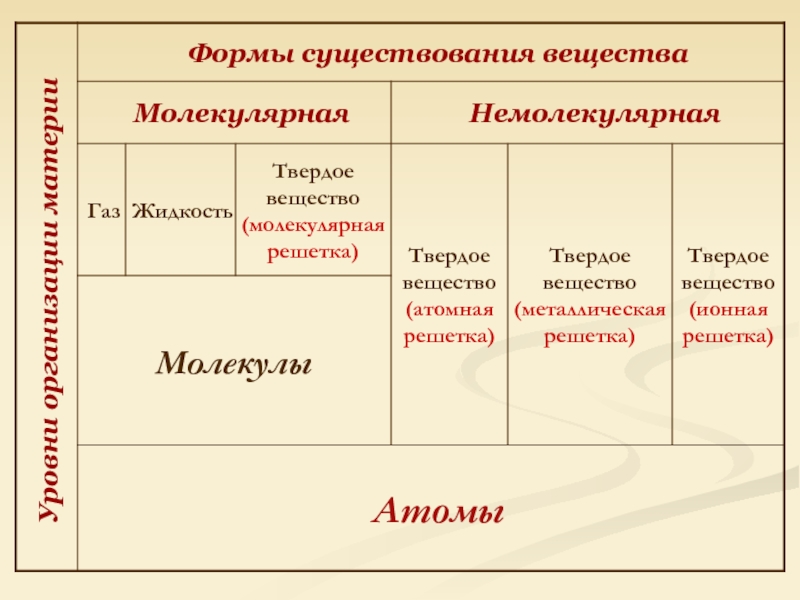
- 13. Уровни организации материи
- 14. Основные законы атомно-молекулярного ученияЗакон сохранения массыЗакон постоянства составаЗакон объёмных отношенийЗакон Авогадро
- 15. Основные законы атомно-молекулярного учения. Закон сохранения массы
- 16. Все перемены в натуре случающиеся, такого суть
- 17. Основные законы атомно-молекулярного учения. Закон сохранения массы
- 18. Основные законы атомно-молекулярного учения. Закон постоянства состава,
- 19. Уровни организации материи
- 20. Основные законы атомно-молекулярного учения. Закон объёмных отношений
- 21. Основные законы атомно-молекулярного учения. Закон Авогадро, 1811
- 22. Атомно-молекулярная теория I Всемирный химический конгресс,
- 23. Скачать презентанцию
Химия -наука о веществах, их строении, свойствах и взаимопревращениях.Веществосовокупность атомов и молекул, находящихся в определенном агрегатном состоянииформа материи, обладающая массой покоя
Слайды и текст этой презентации
Слайд 3Химия -
наука о веществах, их строении, свойствах и взаимопревращениях.
Вещество
совокупность атомов
и молекул, находящихся в определенном агрегатном состоянии
покояСлайд 4«Если бы в результате какой-то мировой катастрофы все накопленные научные
знания оказались бы уничтоженными и к грядущим поколениям живых существ
перешла бы только одна фраза, то какое утверждение, составленное из наименьшего количества слов, принесло бы наибольшую информацию? Я считаю, что это – атомная гипотеза … все тела состоят из атомов – маленьких телец, которые находятся в беспрерывном движении, притягиваются на небольшом расстоянии, но отталкиваются, если одно из них плотнее прижать к другому. В одной этой фразе … содержится невероятное количество информации о мире, стоит лишь приложить к ней немного воображения и чуть соображения ...»Ричард Фейнман
Слайд 5Атомистика - учение о прерывном строении материи
основные этапы
развития:
-атомистика древних материалистов - до XVII в.
-механистическая атомистика
– XVII-XVIII вв.-химическая атомистика - XIX в.
-современная физическая атомистика – XX в.
Слайд 6Демокрит (460-370 гг. до н.э.) впервые употребил понятие атом (от
греч. аtomos-неделимый)
Каждый атом непроницаем и неделим, потому что
не содержит пустот. Атомы могут лишь двигаться и сталкиваться друг с другом, иногда образуя соединения, когда им случается иметь пригодные к тому формы.Слайд 7Атомистика древних материалистов
все состоит из атомов
атомы физически неделимы
между атомами в
материи существует пустое пространство
атомы неразрушимы и существуют вечно
атомы всегда находятся
в движении существует бесконечное количество как самих атомов, так и их разновидностей – атомы различаются формой и размерами
Слайд 8Механистическая атомистика
Роберт Бойль (25.01.1627-30.12.1691) определил элементы как
«первоначальные и простые вполне не смешенные тела, которые не составлены
друг из друга, но представляют собой те составные части , из которых составлены все так называемые смешенные тела и на которые последние могут быть в конце концов разложены».Слайд 9Закон Бойля–Мариотта 1662
1676
При постоянной температуре объём газа обратно пропорционален его
давлениюP1V1 = P2V2
Слайд 10Атомно-молекулярное учение
М.В. Ломоносова
«Элементы математической химии», 1741 г.
Все вещества
состоят из молекул.
Молекулы состоят из атомов.
Молекулы простых веществ состоят из
одинаковых атомов, сложных – из различных.Молекулы и атомы находятся в непрерывном движении.
Слайд 11Атомистическая теория
Джона Дальтона
«Новая система химической философии», 1808 г.
Атомы представляют
собой мельчайшие частицы вещества, которые невозможно разделить на составные части,
превратить друг в друга или уничтожить.При химических реакциях атомы соединяются друг с другом в простых целочисленных отношениях.
При разложении соединения из него получаются исходные атомы в неизменном виде, которые могут затем образовывать тоже самое или другое соединение.
Слайд 12Атомистическая теория
Джона Дальтона
«Новая система химической философии», 1808 г.
Все атомы
одного элемента совершенно одинаковы и имеют одинаковый вес. Атомы различных
элементов имеют различные веса.Относительные веса элементов, которые соединяются друг с другом, непосредственно связаны с весами атомов. Так, если 1 г серы соединяется с 2 г меди, то это означает, что каждый атом меди весит вдвое больше атома серы.
Слайд 14Основные законы атомно-молекулярного учения
Закон сохранения массы
Закон постоянства состава
Закон объёмных отношений
Закон
Авогадро
Слайд 15Основные законы атомно-молекулярного учения.
Закон сохранения массы
(закон Ломоносова-Лавуазье)
Общая масса веществ, вступающих
в химическую реакцию, равна общей массе продуктов реакции.
Слайд 16Все перемены в натуре случающиеся, такого суть состояния, что сколько
чего у одного тела отнимается, столько же присовокупиться к другому.
Так, ежели где убудет несколько материи, то умножится в другом месте…Михайло Ломоносов, 1760 г.
Слайд 17Основные законы атомно-молекулярного учения.
Закон сохранения массы
(закон Ломоносова-Лавуазье)
Общая масса веществ, вступающих
в химическую реакцию, равна общей массе продуктов реакции.
Михаил Васильевич Ломоносов,
1748-1756Антуан Лоран Лавуазье, 1789
Альберт Эйнштейн, 1905
Слайд 18Основные законы атомно-молекулярного учения.
Закон постоянства состава, 1806 г.
Соединения содержат элементы
в строго определенных весовых пропорциях, независимо от способа получения.
Жозеф Луи
Пруст (1754-1826)
Слайд 20Основные законы атомно-молекулярного учения.
Закон объёмных отношений
(закон Гей-Люссака, 1808 г.)
При
неизменных температуре и давлении объёмы реагирующих газов относятся друг к
другу, а также к объёмам образующихся газообразных продуктов, как небольшие целые числа.Джозеф Луи Гей-Люссак
(1778-1850)
Слайд 21Основные законы атомно-молекулярного учения.
Закон Авогадро, 1811 г.
В равных объёмах различных
газов при одинаковых условиях (температуре и давлении) содержится одинаковое количество
молекул.Амедео Авогадро
(1776-1856)
Слайд 22Атомно-молекулярная теория
I Всемирный химический конгресс, 1860 г
Все вещества
состоят из молекул. Молекула – наименьшая частица вещества, обладающая его
химическими свойствами.Молекулы состоят из атомов. Атом – наименьшая частица элемента в химическом соединении. Различным элементам соответствуют различные атомы.
Молекулы и атомы находятся в непрерывном движении.
При химических реакциях молекулы одних веществ превращаются в молекулы других веществ. Атомы в химических реакциях не изменяются.
Станислао
Канниццаро
(1826-1910)