Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Пробиотики и пребиотики Всемирная Гастроэнтерологическая Организация
Содержание
- 1. Пробиотики и пребиотики Всемирная Гастроэнтерологическая Организация
- 2. ИсторияБолее века тому назад Илья Мечников (русский
- 3. Кишечная микробиота Кишечная микробиота (далее – микробиота)
- 4. Кишечная микробиотаСчитается, что бактерии начинают заселять кишечник
- 5. Кишечная микробиотаПо данным исследования американской Human Microbiome
- 6. Слайд 6
- 7. Слайд 7
- 8. Пробиотики и пребиотики - концепцияПробиотики – это
- 9. Молочнокислая бактерия (МКБ) - функциональная классификация непатогенной,
- 10. Пребиотики и синбиотикиКонцепция пребиотиков возникла значительно позже,
- 11. Пребиотики и синбиотикиЛактулоза – это синтетический дисахарид,
- 12. Типы, виды и штаммы, используемые как пробиотикиПробиотический
- 13. Типы, виды и штаммы, используемые как пробиотикиИспользование
- 14. Колонизация микробиотыФункции и пробиотиков и пребиотиков пересекаются
- 15. Колонизация микробиотыНормальным взаимодействием между кишечными бактериями и
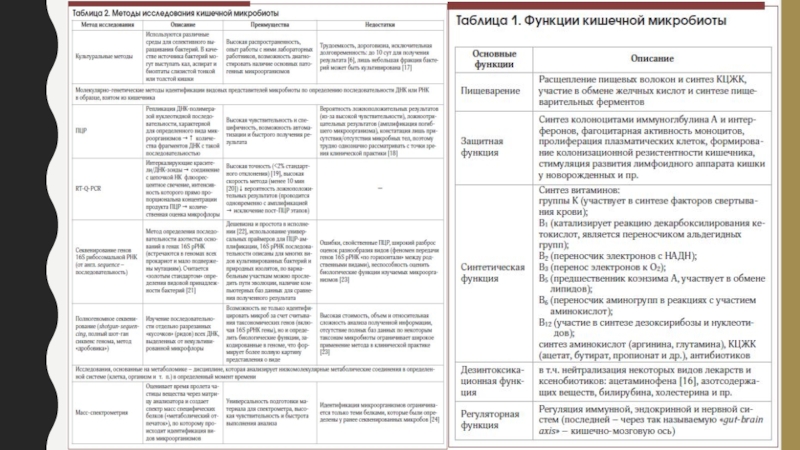
- 16. Таблица 3 Человеческая микробиота желудочно-кишечного тракта. Кишечная
- 17. Механизмы действия пробиотиковПребиотики влияют на бактерии ЖКТ
- 18. Таблица 4 Механизмы взаимодействия пробиотиков и пребиотиков
- 19. Клиническое применениеПрофилактика диареи, вызванной Clostridium difficile.В мета-анализе
- 20. Клиническое применениеПрофилактика и лечение печеночной энцефалопатии Такие
- 21. Клиническое применениеСиндром раздраженного кишечника (СРК)Уменьшение абдоминального метеоризма
- 22. Профилактика системных инфекцийВ настоящее время недостаточно доказательств,
- 23. Обзор доказательств эффективности пробиотиков и пребиотиков при
- 24. Таблица 9 Основанные на доказательствах показания для
- 25. Таблица 9 Основанные на доказательствах показания для
- 26. Таблица 9 Основанные на доказательствах показания для
- 27. Таблица 9 Основанные на доказательствах показания для
- 28. Таблица 9 Основанные на доказательствах показания для
- 29. Пробиотик первого поколения «Лактобактерин» создан на основе
- 30. Представитель первого поколения пробиотиков является «Бифидумбактерин». Форма
- 31. В состав симбиотика «Бифиформ» входят энтерококки и
- 32. Выпускается «Аципол» в капсулах, содержащих в себе
- 33. Многокомпонентный пробиотик «Энтерол» разработан французскими учеными. В
- 34. Действующим веществом препарата «Линекс» является либенин, содержащий
- 35. Форма выпуска «Пробифора» – капсулы или порошок
- 36. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Пробиотики и пребиотики
Всемирная Гастроэнтерологическая Организация
Практические рекомендации
Глобальные практические рекомендации
Всемирной Гастроэнтерологической Организации
Слайд 2История
Более века тому назад Илья Мечников (русский ученый, Нобелевский лауреат
и профессор Пастеровского института в Париже) постулировал, что молочнокислая бактерия
(МКБ) благотворно влияет на состояние здоровья и способствует долголетию. Он предположил, что «кишечная аутоинтоксикация», и вызываемое ею старение, может быть уменьшена модификацией кишечной микробиоты и замещением протеолитических микробов — которые продуцируют токсические вещества, включающие фенолы, индолы и аммиак при переваривании белков — полезными микробами. Мечников разработал диету с включением молока, ферментированного бактерией, которую он назвал «Болгарской бациллой».Появились и другие ранние разработки этой концепции. В попытке изменить или заместить кишечную микробиоту при лечении нарушений в пищеварительном тракте использовались живые непатогенные бактерии. В 1917 г., до того, как сэр Александр Флеминг открыл пенициллин, немецкий ученый Альфред Ниссле изолировал непатогенный штамм Escherichia coli, который не вызывал развития энтероколита во время серьезной вспышки шигеллеза, из фекалий солдата, воевавшего на Первой Мировой войне. Полученный штамм Escherichia coli Nissle 1917 – один из немногих примеров пробиотика, не связанного с МКБ.
Анри Тиссье (Пастеровский институт) впервые изолировал Bifidobacterium от новорожденного на грудном вскармливании для последующего ее введения детям, страдающим диареей. Он выдвинул гипотезу о возможности замещений этой бактерией протеолитических бактерий, вызывающих диарею. В Японии, д-р Минору Широта изолировал штамм Shirota Lactobacillus casei для борьбы со вспышками диареи. Пробиотический продукт с этим штаммом выпускается с 1935 г.
Слайд 3Кишечная микробиота
Кишечная микробиота (далее – микробиота) представляет собой множество
различных видов микроорганизмов, населяющих кишечник человека. Это более 50 родов
и более 500 видов бактерий, количество которых в ЖКТ человека превышает 1014, что на один порядок больше числа клеток человеческого организма. Данные некоторых молекулярно-филогенетических исследований свидетельствуют о наличии в человеческом кишечнике от 15 до 36 (!) тысяч видов бактерий. Тем не менее дискуссии о количестве микробов в организме человека не утихают до сих пор. В 2016 г. были опубликованы результаты исследования израильских и канадских ученых, согласно которым микроорганизмов в человеческом теле примерно столько же, сколько и клеток (3,9×1013 и 3,0×1013 соответственно).Численность микробиоты постепенно увеличивается по ходу кишечника, составляя в тонкой кишке 102–107 КОЕ/г и достигая максимального значения в толстой кишке – до 1011 КОЕ/г. Такая разница может объясняться наличием в верхних отделах кишечника более агрессивной среды из-за поступающего кислого содержимого желудка, действия пищеварительных ферментов, быстрого продвижения химуса. Преобладающих в тонкой кишке аэробов по мере движения вниз по ЖКТ сменяют факультативные, а затем облигатные анаэробы. Это связано со снижением парциального давления кислорода в дистальных отделах ЖКТ.
Микробиота включает облигатных представителей (постоянно присутствующих в организме хозяина) и транзиторных (поступающих из внешней среды и неспособных к длительному существованию в здоровом организме). Находиться микробы могут в просвете кишечника (полостная микрофлора) и в пристеночной слизи (пристеночная, мукозная микрофлора).
По типу метаболизма различают протеолитические бактерии, осуществляющие гидролиз белков (кишечная палочка, бактероиды, протей, клостридии), и сахаролитические (бифидобактерии, лактобактерии, энтерококки), получающие энергию из углеводов.
Слайд 4Кишечная микробиота
Считается, что бактерии начинают заселять кишечник человека сразу после
рождения. В основном это обитатели вагинального тракта матери. Тем не
менее имеются данные о возможности более раннего попадания микробов в ЖКТ человека: исследование М. Mshvildadze показало наличие бактериальной ДНК в меконии здоровых новорожденных. По мере развития ребенка увеличивается разнообразие и стабильность его микробиоты: если с первых дней жизни преобладают B. bifidum и Lactobacillus, то затем наблюдается относительное снижение представительства молочнокислой флоры, а среди Bifidobacterium начинают преобладать longum, breve, adolescentis. Ко второму году жизни ребенка его микробиота напоминает микробиоту взрослого организма.Рождение путем кесарева сечения негативно влияет на состав кишечной микробиоты у младенцев: ее разнообразие снижено, редуцировано представительство Bacteroidetes, а также ослаблен иммунный ответ, связанный с T-хелперами 1-го типа. Эти изменения сохраняются на протяжении первых двух лет жизни.
Слайд 5Кишечная микробиота
По данным исследования американской Human Microbiome Project (HMP) и
европейской Metagenomics of human intestinal tract (MetaHIT) популяции, у взрослых кишечная микрофлора
представлена двумя преобладающими типами бактерий: Bacteroidetes и Firmicutes. При этом был введен термин «энтеротипы» – это устойчивые кластеры на основе микробного состава в образцах из кишечника человека, которые определяются преобладанием тех или иных ключевых родов бактерий и не являются популяционно- и континент-специфичными. В энтеротипе-1 доминируют представители рода Bacteroides, в энтеротипе-2 – Prevotella, в энтеротипе-3 – Ruminococcus. Однако четкие критерии определения энтеротипов отсутствуют; кроме того, результаты ряда исследований указывают на незначительное преобладание в биотопах организма ключевых бактериальных родов, а не отдельных кластеров, в связи с чем требуется проведение дальнейших наблюдений, касающихся данного феномента. Наличие четко определенных энтеротипов не было доказано и при метагеномном исследовании кишечной микробиоты добровольцев из городской и сельской местности России: в основном в микробных сообществах не отмечалось доминирования Prevotella или Bacteroides, а в 50% случаев наблюдалось преобладание большого набора троек микроорганизмов (в основном Firmicutes, компанию которым составляли Bacteroidetes, Verrucomicrobia, Actinobacteria, Proteobacteria, Tenericutes и Archaea).Слайд 8Пробиотики и пребиотики - концепция
Пробиотики – это живые микроорганизмы, приносящие
пользу хозяину при введении в адекватных количествах. Как пробиотики чаще
всего используются виды Lactobacillus и Bifidobacterium, но также эту роль играют и дрожжи Saccharomyces boulardii и некоторые виды E. coli и Bacillus. Недавно, как новый пищевой продукт, в Европейском Союзе была зарегистрирована Clostridium butyricum. Молочнокислые бактерии, включая вид Lactobacillus, ферментация которых в течение тысяч лет использовалась для сохранения пищи, могут действовать и как средство для ферментации и, в дополнение к этому, потенциально способны оказывать благотворный эффект на состояние здоровья. Тем не менее, строго говоря, термин «пробиотик» должен резервироваться для живых микробов, которые показали положительные эффекты на состояние здоровья в контролируемых клинических исследованиях на человеке. Понятие «ферментация» во всем мире употребляется в отношении сохранения множества сырых сельскохозяйственных продуктов (круп, кореньев, клубней, овощей и фруктов, молока, мяса, рыбы и т.д.).Пребиотики - Селективно ферментированный ингредиент, который образуется при специфичных изменениях в составе и/или активности желудочнокишечной микробиоты, и, таким образом, оказывает положительный эффект(ы) на состояние здоровья хозяина
Синбиотики - Продукты, содержащие как пробиотики, так и пребиотики, оказывающие положительное влияние на состояние здоровья
Слайд 9Молочнокислая бактерия (МКБ) - функциональная классификация непатогенной, нетоксигенной, грамположительной, ферментативной
бактерии, которая связана с продукцией молочной кислоты из углеводов, что
делает их пригодными для ферментации пищи. В эту группу включаются виды Lactobacillus, Lactococcus и Streptococcus thermophilus. Многие пробиотики также входят в группу МКБ, но некоторые (такие как определенные штаммы E. coli, спорообразующие и дрожжи, используемые в качестве пробиотиков) в нее не входят.Ферментация - процесс, при котором микроорганизм трансформирует пищу в другие продукты, обычно посредством образования молочной кислоты, этанола и других конечных веществ метаболизма.
Слайд 10Пребиотики и синбиотики
Концепция пребиотиков возникла значительно позже, чем пробиотиков, и
впервые была предложена Gibson и Roberfroid в 1995 г. Ключевые
аспекты пребиотиков заключаются в том, что они не перевариваются в ЖКТ хозяина, и в том, что они оказывают благоприятное воздействие на состояние здоровья индивидуума посредством влияния на собственные полезные для хозяина микробы. Целью введения или использования пребиотиков или пробиотиков является оказание влияния на кишечную среду, заселенную миллиардами симбиотических микробов, для положительного влияния на здоровье человека. Как пробиотики, так и пребиотики показали свои положительные эффекты, выходящие за пределы желудочно-кишечного тракта, но данные рекомендации будут сфокусированы их на воздействии на кишечник.Пребиотики – это диетарные вещества (в основном состоящие из некрахмальных полисахаридов и олигосахаридов). Большинство пребиотиков используются как пищевые ингредиенты – например, в печенье, кашах, шоколаде, спредах и молочных продуктах. Самые известные пребиотики - это:
Олигофруктоза
Инулин
Галакто-олигосахариды
Лактулоза
Олигосахариды грудного молока
Слайд 11Пребиотики и синбиотики
Лактулоза – это синтетический дисахарид, применяемый как препарат
для лечения запоров и печеночной энцефалопатии. Естественная пребиотическая олигофруктоза обнаруживается
во многих пищевых продуктах, таких как пшеница, лук, бананы, мед, чеснок и лук-порей. Также олигофруктоза может быть выделена из корня цикория или энзиматически синтезирована из сукрозы. Ферментация олигофруктозы в толстой кишке приводит к большому количеству физиологических эффектов, включающих:Увеличение количества бифидобактерий в толстой кишке
Усиление всасывания кальция
Увеличение веса фекалий
Уменьшение времени транзита по желудочно-кишечному тракту
Возможное снижение уровня липидов в крови
Предполагается, что увеличение количества кишечных бифидобактерий оказывает положительный эффект на здоровье человека за счет выработки компонентов, ингибирующих потенциальные патогены, снижения уровня аммиака в крови и продукции витаминов и пищеварительных ферментов. Синбиотики представляют собой соответствующую комбинацию пребиотиков и пробиотиков. Синбиотический продукт обладает как пробиотическими, так и пребиотическими качествами.
Слайд 12Типы, виды и штаммы, используемые как пробиотики
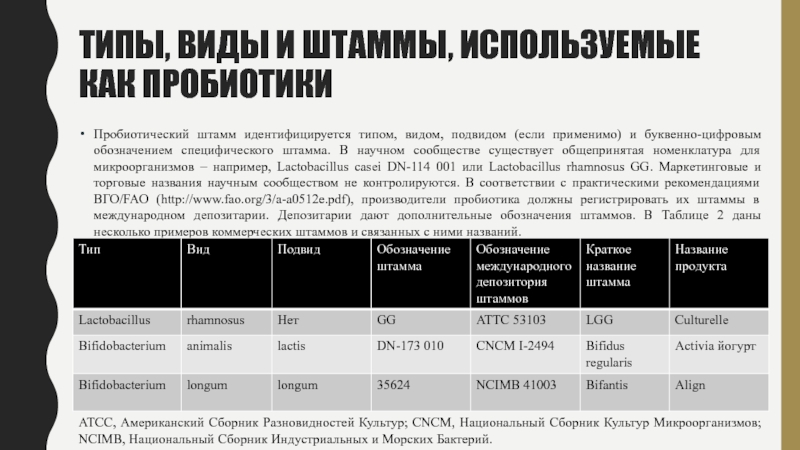
Пробиотический штамм идентифицируется типом,
видом, подвидом (если применимо) и буквенно-цифровым обозначением специфического штамма. В
научном сообществе существует общепринятая номенклатура для микроорганизмов – например, Lactobacillus casei DN-114 001 или Lactobacillus rhamnosus GG. Маркетинговые и торговые названия научным сообществом не контролируются. В соответствии с практическими рекомендациями ВГО/FAO (http://www.fao.org/3/a-a0512e.pdf), производители пробиотика должны регистрировать их штаммы в международном депозитарии. Депозитарии дают дополнительные обозначения штаммов. В Таблице 2 даны несколько примеров коммерческих штаммов и связанных с ними названий.ATCC, Американский Сборник Разновидностей Культур; CNCM, Национальный Сборник Культур Микроорганизмов; NCIMB, Национальный Сборник Индустриальных и Морских Бактерий.
Слайд 13Типы, виды и штаммы, используемые как пробиотики
Использование обозначений штаммов для
пробиотиков очень важно, так как самым надежным подходом к доказательству
эффективности пробиотика служит связь положительных влияний (например, в отношении желудочно-кишечного тракта, обсуждаемых в данных практических рекомендациях) со специфическими штаммами или комбинацией штаммов пробиотиков в эффективной дозировке. Рекомендации для применения пробиотиков, особенно в клинических условиях, должны связывать специфические штаммы с заявленными эффектами, основанными на исследованиях на человеке. У некоторых штаммов имеются уникальные качества, которые могут отвечать за определенные неврологические, иммунологические и антимикробные эффекты. Тем не менее, новой концепцией в сфере пробиотиков служит понимание того, что некоторые механизмы пробиотической активности, вероятно, являются общими для различных штаммов, видов и даже типов. Многие пробиотики могут действовать сходным образом в отношении способности к стимуляции резистентности к колонизации, регулирования желудочно-кишечного транзита, или нормализации нарушений в микробиоте. Например, способность к увеличению продукции короткоцепочечных жирных кислот или к снижению pH просвета толстой кишки могут быть главным эффектом, производимым многими различными штаммами пробиотиков. Следовательно, некоторые пробиотические эффекты могут быть оказаны многими штаммами определенных хорошо изученных видов Lactobacillus и Bifidobacterium. Если целью приема пробиотиков является поддержка здорового пищеварения, то, возможно, будет достаточным употребление многих разнообразных пробиотических смесей, содержащих адекватное количество хорошо изученных видов.Сейчас в сфере изучения пробиотиков общепринятым считается включать в системные обзоры и мета-анализы множественные штаммы. Такой подход возможен, если общие механизмы действия различных включенных штаммов позволяют считать их ответственными за полученный эффект.
Слайд 14Колонизация микробиоты
Функции и пробиотиков и пребиотиков пересекаются с микробами, колонизирующими
человеческий организм. Пребиотики служат источником питания для полезных членов симбиотического
микробного содружества и, следовательно, положительно влияют на состояние здоровья. Перекрестные действия между пробиотиками и клетками хозяина, или между пробиотиками и присутствующими микробами, представляют собой главные средства влияния на здоровье хозяина. Кишечник содержит огромной количество микробов, которые в основном населяют толстую кишку и представляют сотни видов (Таблица 3). По оценкам в толстой кишке взрослого человека существуют более 40 миллиардов бактериальных клеток (включая малую долю архей (архибактерий), менее 1%). Также присутствуют, с ничтожным вкладом в отношении количества клеток, грибки и протисты, в то время как количество вирусов/фагов может превышать количество бактерий. В целом, кишечные микробы добавляют в среднем 600,000 геном каждому человеческому организму. На уровне видов и штаммов, микробное расхождение между отдельными индивидуумами довольно значительно: каждый человек имеет свою четкую картину бактериальной композиции, частично обусловленную его генотипом, первичной колонизацией при рождении путем вертикальной передачи и диетическими привычками. У здоровых взрослых людей фекальная композиция стабильна на протяжении времени. В экосистеме человеческого кишечника доминируют две бактериальные группы —Bacteroidetes и Firmicutes—и представляют собой 90% всех микробов. Остающиеся 10% - это Actinobacteria, Proteobacteria, Verrucomicrobia и Fusobacteria.Слайд 15Колонизация микробиоты
Нормальным взаимодействием между кишечными бактериями и их хозяином являются
симбиотические отношения. Наличие важного влияние кишечных бактерий на иммунную функцию
можно предположить по присутствию большого количества организованных лимфоидных структур в слизистой оболочке тонкого кишечника (Пейеровы бляшки) и толстого кишечника (изолированные лимфоидные фолликулы). Эпителий над этими структурами специализирован на захвате и сэмплировании антигенов, и содержит лимфоидные герминальные центры для индукции адаптивных иммунных ответов. В толстой кишке микроорганизмы пролиферируют, ферментируя доступные вещества из пищи или эндогенной секреции, таким образом внося свой вклад в питание хозяина.Многие исследования показали, что у здоровых индивидуумов и людей с наличием заболевания или патологического состояния популяции колонизирующих микробов различаются. Тем не менее, исследователи все еще не способны четко очертить композицию здоровой микробиоты человека. Некоторые симбиотические бактерии (такие как Roseburia, Akkermansia, Bifidobacterium и Faecalibacterium prausnitzii) представляются более тесно связанными со здоровьем, но определение того, может ли добавление этих бактерий улучшить состояние здоровья и способствовать разрешению заболевания является в настоящее время активной областью исследований.
Слайд 16Таблица 3 Человеческая микробиота желудочно-кишечного тракта. Кишечная микробиота формирует разнообразную
и динамичную экосистему, включающую в себя бактерии, археи, эукариоты и
вирусы, которые адаптированы для жизни на поверхности слизистой оболочки или в просвете кишечникаОбозначения: 1, полость рта 2, глотка; 3, язык; 4, пищевод; 5, поджелудочная железа; 6, желудок; 7, печень; 8, поперечная ободочная кишка; 9, желчный пузырь; 10, нисходящая ободочная кишка; 11, двенадцатиперстная кишка; 12, тощая кишка; 13, восходящая ободочная кишка; 14, сигмовидная кишка; 15, подвздошная кишка; 16, прямая кишка; 17, анус.
Слайд 17Механизмы действия пробиотиков
Пребиотики влияют на бактерии ЖКТ путем увеличения количества
полезных анаэробных бактерий и снижения популяции потенциально патогенных микроорганизмов. Пробиотики
действуют на экосистему ЖКТ, влияя на иммунные механизмы в слизистой оболочке, взаимодействуя с симбиотическими или потенциально патогенными микробами, генерируя продукты метаболического обмена, такие как короткоцепочечные жирные кислоты и коммуницируя с клетками хозяина посредством химических сигналов (Рис. 2; Таблица 4). Эти механизмы могут приводить к антагонизму с потенциальными патогенами, улучшению среды ЖКТ, укреплению желудочно-кишечного барьера, отрицательной обратной связи с воспалением и обратной связи с иммунным ответом на антигенные вызовы. Предположительно эти феномены оказывают наиболее положительные эффекты, включающие снижение частоты и тяжести диареи, которая является одной из самых частых причин применения пробиотиков.Рис. 2 Механизмы взаимодействия между микробиотой и пробиотиками с хозяином. Нормальная микробиота и пробиотики взаимодействуют с хозяином в метаболических процессах и иммунной функции и предотвращают колонизацию оппортунистическими и патогенными микроорганизмами. Воспроизведено с разрешения Blackwell Publishing Ltd.
Слайд 18Таблица 4 Механизмы взаимодействия пробиотиков и пребиотиков с хозяином. Симбиоз
между микробиотой и хозяином может быть оптимизирован с помощью фармакологических
или нутрициональных вмешательств в микробную экосистему кишечника путем использования пробиотиков или пребиотиковСлайд 19Клиническое применение
Профилактика диареи, вызванной Clostridium difficile.
В мета-анализе 2016 г. было
сделано заключение, что пробиотики могут уменьшить риск развития C. difficile–ассоциированной
диареи у пациентов, получающих антибиотики. Тем не менее, авторы предупреждают, что необходимы дополнительные исследования для определения наилучшей дозы и штамма.Профилактика антибиотико-ассоциированной диареи
Существуют серьезные доказательства того, что пробиотики эффективны для профилактики диареи у взрослых и детей, получающих терапию антибиотиками.
Эрадикация Helicobacter pylori
В Консенсусном Сообщении 2016 г. Маастрихт V/Флоренция по ведению инфекции H. pylori сделано заключение, что пробиотики и пребиотики показали многообещающие результаты в уменьшении побочных эффектов лечения инфекции H. pylori. Тем не менее, качество доказательств и степень рекомендаций были низкими. В мета-анализе рандомизированных исследований 2014 г. было высказано предположение, что добавка определенных пробиотиков к антибиотическим режимам лечения инфекции H. pylori также может быть эффективной в отношении повышения скорости эрадикации, и может рассматриваться для назначения пациентам при неудаче эрадикационной терапии. Не существует доказательств, подтверждающих концепцию эффективности мононазначения пробиотика без сопутствующей антибиотикотерапии.
Слайд 20Клиническое применение
Профилактика и лечение печеночной энцефалопатии
Такие пробиотики как лактулоза
повсеместно используются для профилактики и лечения печеночной энцефалопатии. Доказательства для
средства с одним пробиотиком позволяют предположить, что оно может вызывать обратное развитие минимальной печеночной энцефалопатии.Иммунный ответ
Существуют предполагаемые доказательства того, что некоторые пробиотические штаммы и пребиотик олигофруктоза эффективны для улучшения иммунного ответа. Доказательства усиления иммунного ответа были получены в исследованиях, направленных на профилактику острой инфекционной болезни (внутрибольничная диарея у детей, эпизоды гриппа зимой) и в исследованиях, изучавших ответ антител на введение вакцин.
Воспалительная болезнь кишечника (ВБК)
Болезнь Крона
Исследования действия пробиотиков при болезни Крона показали, что нет доказательств, позволяющих предположить их эффективность в поддержании ремиссии при данном заболевании
Язвенный колит
Было показано, что определенные пробиотики безопасны и эффективны в качестве стандартной терапии для достижения более высоком степени ответа и уровня ремиссии при легкой степени и умеренной активности язвенного колита, как во взрослой, так и в педиатрической популяциях.
Слайд 21Клиническое применение
Синдром раздраженного кишечника (СРК)
Уменьшение абдоминального метеоризма и вздутия в
результате применения пробиотиков – это неизменный результат, указанный в опубликованных
исследованиях; некоторые штаммы могут уменьшать боль и обеспечивать общее улучшение самочувствия. Данные литературы позволяют предположить, что определенные пробиотики могут уменьшать симптоматику и улучшать качество жизни пациентов с функциональной абдоминальной больюКолика
Некоторые пробиотические штаммы доказали свою эффективность в уменьшении времени плача у новорожденных на грудном вскармливании при развитии колики.
Нарушение всасываемости лактозы
Streptococcus thermophilus и Lactobacillus delbrueckii подвид bulgaricus улучшают всасываемость лактозы и уменьшают симптомы, связанные с ее непереносимостью. Это было подтверждено во многих контролируемых исследованиях лиц, употреблявших йогурт с живой культурой.
Некротический энтероколит
Пробиотические добавки снижают риск развития некротического энтероколита у недоношенных новорожденных. Мета-анализы рандомизированных контролированных исследований также показали снижение риска смерти в группах, пролеченных пробиотиками, хотя не все исследуемые пробиотические средства оказались эффективными. Количество пациентов, которых необходимо пролечить пробиотиками для предотвращения одной смерти от всех причин составляет 20.
Слайд 22Профилактика системных инфекций
В настоящее время недостаточно доказательств, поддерживающих применение пробиотиков
и синбиотиков у взрослых пациентов в критических состояниях в отделениях
интенсивной терапии.Хотя это и выходит за рамки данных практических рекомендаций, читателю может быть интересно обратить внимание на то, что пробиотики и пребиотики показали свое влияние на некоторые клинические исходы заболеваний, не водящих в спектр гастроэнтерологических интересов. Появляющиеся доказательства позволяют предположить, что кишечная микробиота может влиять на несколько негастроэнтерологических состояний, таким образом устанавливая связь между этими состояниями и желудочно-кишечным трактом. Многочисленные исследования показали, что пробиотики могут уменьшать явления бактериального вагиноза, предотвращать развитие атопического дерматита у новорожденных, редуцировать количество оральных патогенов и уменьшать кариес зубов, снижать частоту и длительность распространенных инфекций верхних дыхательных путей. Выраженный эффект пробиотиков в профилактике аллергической болезни в перинатальном периоде привел к разработке рекомендаций Всемирной Аллергологической Организации по применению пробиотиков во время беременности, грудного вскармливания и отъема от груди в семьях с высоким риском развития аллергической болезни. Пробиотики и пребиотики также исследовались как средство профилактики некоторых проявлений метаболического синдрома, включая избыточный вес, диабет 2 типа и дислипидемию.
Слайд 23Обзор доказательств эффективности пробиотиков и пребиотиков при взрослых и педиатрических
состояниях — глобальная картина
* Уровень может быть снижен на
основании качества исследования, неточности, непрямолинейности — критерии PICO (исследуемая популяция, метод лечения, сравнение и исход) не соответствуют PICO вопроса; из-за несоответствия между исследованиями; или из-за того, что абсолютный показатель эффекта слишком мал. Уровень может быть повышен, если имеется больший или очень большой показатель эффекта. † Как всегда, системный обзор в основном лучше, чем индивидуальное исследование.Таблицы 8 и 9 обобщают желудочно-кишечные состояния, при которых имеются полученные минимум в одном клиническом исследовании с хорошим дизайном доказательства эффективности орального применения специфичного пробиотического штамма или пребиотика. Целью этих таблиц является информирование читателя о существовании исследований, подтверждающих эффективность и безопасность перечисленных продуктов, в то время как некоторые другие продукты, присутствующие на рынке, тестированы не были. Список может быть неполным, поскольку публикация новых исследований продолжается. Уровень доказательности между различными показаниями к применению может варьировать. Указанные дозы использовались в рандомизированных контролируемых исследованиях. Порядок расположения продуктов в списках случаен. Не существует доказательств, полученных в сравнительных исследованиях, позволяющих расположить продукты по уровню их эффективности. Таблицы не предоставляют степени рекомендаций, а только уровни доказательности в соответствии с критериями Оксфордского Центра Медицины, Основанной на Доказательствах (Таблица 7). Также представлены рекомендации медицинских ассоциаций.
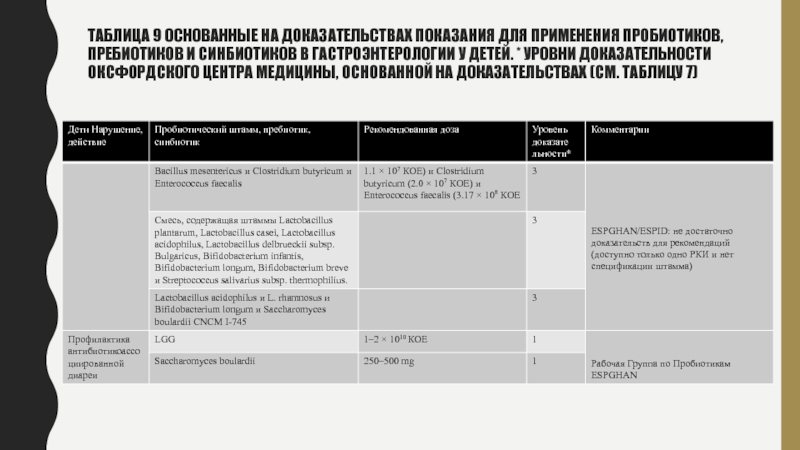
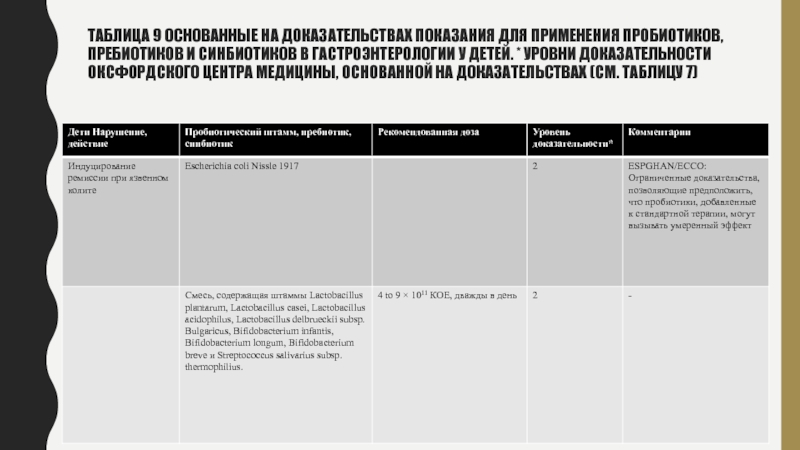
Слайд 24Таблица 9 Основанные на доказательствах показания для применения пробиотиков, пребиотиков
и синбиотиков в гастроэнтерологии у детей. * Уровни доказательности Оксфордского
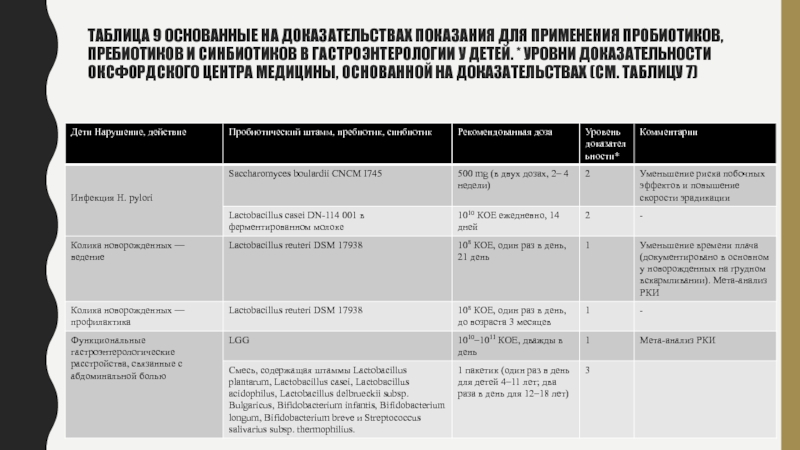
Центра Медицины, Основанной на Доказательствах (см. Таблицу 7)Слайд 25Таблица 9 Основанные на доказательствах показания для применения пробиотиков, пребиотиков
и синбиотиков в гастроэнтерологии у детей. * Уровни доказательности Оксфордского
Центра Медицины, Основанной на Доказательствах (см. Таблицу 7)Слайд 26Таблица 9 Основанные на доказательствах показания для применения пробиотиков, пребиотиков
и синбиотиков в гастроэнтерологии у детей. * Уровни доказательности Оксфордского
Центра Медицины, Основанной на Доказательствах (см. Таблицу 7)Слайд 27Таблица 9 Основанные на доказательствах показания для применения пробиотиков, пребиотиков
и синбиотиков в гастроэнтерологии у детей. * Уровни доказательности Оксфордского
Центра Медицины, Основанной на Доказательствах (см. Таблицу 7)Слайд 28Таблица 9 Основанные на доказательствах показания для применения пробиотиков, пребиотиков
и синбиотиков в гастроэнтерологии у детей. * Уровни доказательности Оксфордского
Центра Медицины, Основанной на Доказательствах (см. Таблицу 7)Слайд 29Пробиотик первого поколения «Лактобактерин» создан на основе одного компонента –
живых лактобактерий. После попадания в кишечник они вырабатывают молочную кислоту,
создавая благоприятные условия для образования полезных бактерий. Активный компонент борется со стафилококком, протеи и кишечными палочками. «Лактобактерин» разрешен малышам с первого дня жизни. Пробиотик практически не имеет противопоказаний и побочных действий, поэтому не способен навредить неокрепшему кишечнику новорожденных.Форма выпуска: в виде порошка, герметично упакованного во флаконы. В каждой пачке находится 10 таких флаконов. Применять средство можно не более 10 суток. Средство устойчиво к воздействию антибиотиков, поэтому возможно его применение одновременно с антибактериальными лекарствами.
Показания к применению:
кишечные инфекции и дисбактериоз;
диарея;
нарушенная работа кишечника у новорожденных.
Противопоказания:
вульвовагинит.
Слайд 30Представитель первого поколения пробиотиков является «Бифидумбактерин».
Форма выпуска; Однокомпонентный препарат
выпускается в виде таблеток, каплей, порошка и свечей. Средство улучшает
обменные процессы, повышает иммунитет и нормализует работу кишечника как у взрослых, так и у детей с 6 месяцев. Стоит отметить, что полугодовалым малышам можно принимать только «Бифидумбактерин» в порошке, остальные формы выпуска разрешены к использованию с 3 лет. Если грудные дети отказываются принимать препарат, то допускается приготовление раствора на основе грудного молока.Действующим веществом препарата являются бифидобактерии, которые активны в отношение штаммов кишечной палочки, дрожжеподобных грибков и стафилококка. Курс лечение не должен быть более 14 дней. Продлить период приема может только лечащий врач.
Показания к применению:
дисбактериоз;
кишечные инфекции;
колики.
Противопоказания:
индивидуальная непереносимость;
аллергия на пробиотик.
Слайд 31В состав симбиотика «Бифиформ» входят энтерококки и штаммы бифидобактерий. Активные
вещества нормализуют работу пищеварительной системы, поэтому пробиотик применяют для лечения
и профилактики дисбактериоза у детей и взрослых. Также средство эффективно борется с запором и диареей. Медикамент укрепляет иммунную систему и служит профилактикой инфекционных заболеваний.Для взрослых препарат реализуют в виде таблеток или капсул. Для детей Форма выпуска более разнообразна. «Бифиформ Малыш» представлен в виде порошка для приготовления раствора с апельсиново-малиновым вкусом. С таким же вкусом есть жевательные таблетки «Бифиформ Кидс». А для совсем маленьких пациентов выпускается масляной раствор «Бифиформ Бэби».
Показания к применению:
профилактика и лечение дисбактериоза;
запоры и диарея.
Противопоказания:
индивидуальная непереносимость.
Слайд 32Выпускается «Аципол» в капсулах, содержащих в себе кефирный грибок и
ацидофильные лактобациллы. Так как оболочка желатиновая, то перед приемом симбиотика
маленькими детьми, рекомендуется открыть капсулу и смешать содержимое в одной чайной ложке воды или молока. Пробиотик разрешен к употреблению малышам старше трех месяцев.Действие активных веществ препарата схожи с антибиотиками. Средство создает неблагоприятные условия для патогенных микробов, поэтому с легкостью нормализует баланс микрофлоры кишечника. Пробиотик применяют для профилактики и лечения дисбактериоза, образовавшегося в результате неправильного питания или приема антибиотиков. Он часто включен в курс комплексного лечения ЖКТ, например, при колитах и энтероколитах.
Показания к применению:
кишечные инфекции и дисбактериоз;
снижения интоксикации во время пищевых отравлений;
хронические энтероколиты и колиты.
Противопоказания:
чувствительность к компонентам.
Слайд 33Многокомпонентный пробиотик «Энтерол» разработан французскими учеными. В состав симбиотика входят
сахаромицеты буларди – это лиофилизированные живые бактерии, а в качестве
вспомогательного вещества выступает моногидрат лактозы. Выполнив свою основную функцию, дрожжевые грибы естественным способом выводятся из организма. Выпускается препарат в капсулах или пакетиках с порошком.Чаще всего «Энтерол» назначают после курса приема антибиотиков. Пробиотик борется с причинами диареи, который мог возникнуть из-за пищевого отравления или на фоне дисбактериоза. Средство нельзя принимать детям до 1 года без назначения лечащего врача.
Показания к применению:
диарея;
ротовирусная инфекция;
синдром раздраженной кишки.
Противопоказания:
аллергические реакции или высокая чувствительность к входящим в состав компонентам;
беременность и период лактации.
Слайд 34Действующим веществом препарата «Линекс» является либенин, содержащий штаммы живых лактобактерий,
бифидобактерий и энтерококки. Попав в кишечник, полезные микроорганизмы начинают не
только активно размножаться, но и синтезировать витамины В1, В2, В6, В12 и К. Молочнокислые бактерии увеличивают кислотность микрофлоры кишечника, что ведет к угнетению роста и развития патогенных микроорганизмов. Активные вещества не дают болезнетворным бактериям прикрепиться к стенке кишечника.Форма выпуска препарата – капсулы. «Линекс» безопасен для здоровья при правильном соблюдении дозировки. Средство назначают даже грудным детям, но предварительно рекомендуется аккуратно извлечь содержимое капсулы и смешать с грудным молоком или смесью.
Показания к применению:
лечение и профилактика дисбактериоза;
газообразование или изжога;
понос или запор.
Противопоказание:
сверхчувствительность к компонентам.
Слайд 35Форма выпуска «Пробифора» – капсулы или порошок в герметичных пакетиках.
Препарат не имеет возрастных ограничений, поэтому его могут принимать даже
новорожденные с первого дня жизни. Пробиотик состоит из живых бифидобактерий сорбированных на активированном угле, в качестве вспомогательного вещества выступает лактоза.Средство отлично борется с диареей, так как бифидобактерии не просто уничтожают патогенные микроорганизмы, а вырабатывают антибактериальные субстанции. Благодаря своему уникальному составу пробиотик в короткие сроки восстанавливает структуру слизистой кишечника, и без помощи антибиотиков борется с отравлениями и токсикацией. Препарат могут назначать в послеоперационный период или при подготовке к хирургическим вмешательствам, родам или кесаревому сечению. Часто применяется в комплексных курсах лечения ОРВИ или гриппа.
Показания к применению:
экзема и аллергические реакции;
синдром раздраженного кишечника;
хронический колит и панкреатит;
бактериальный вагиноз и кольпит (наружное применение).
Противопоказания:
непереносимость компонентов пробиотика.