Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Проект по теме Аддитивные технологии 2030
Содержание
- 1. Проект по теме Аддитивные технологии 2030
- 2. Слайд 2
- 3. I. Введение Гортань – это важный орган дыхательной
- 4. Серьезным заболеванием является рак, связанный с развитием злокачественного
- 5. Из-за малой осведомлённости пациентов и врачей чаще
- 6. Слайд 6
- 7. Цель проекта: создание гортани с помощью 3D-биопринтера.Задачи
- 8. II. Основная часть 1. Строение гортани Каркас гортани (хрящевой
- 9. 2. Преимущества создания гортани с помощью 3D-биопринтера Мы
- 10. 3. Каркас для создания гортани Для создания гортани
- 11. Для придания гидрогелю вязкости, необходимой для печати
- 12. 4. Использование стволовых клеток для нанесения на
- 13. 1) Преимущества получения стволовых клеток из жировой
- 14. 2) Процедура забора жировой ткани: Под местной
- 15. 3) Протокол выделения СВФЖТ: Процедура выделения стромальной сосудистой
- 16. Липоаспират может храниться при комнатной температуре до
- 17. 5. Создание сфероидов Сфероид - это крошечный (200–300
- 18. Простой вариант такой структуры можно получить путем
- 19. 6. Технологии биофабрикации в 3D-биопринтереВ качестве среды
- 20. FABION – первый отечественный 3D-биопринтер оригинальной конструкции
- 21. 1. Мультифункциональность. Биопринтер FABION позволяет использовать все
- 22. Данная модель 3D – биопринтера подойдёт для
- 23. 7. Помещение культуры клеток в биореактор Биореактор
- 24. Биореакторы для тканевой инженерии устроены гораздо сложнее,
- 25. Стандартные условия культивирования для хрящевой ткани:Температура 37°CОтносительная
- 26. 8. Соединение хрящей Соединение хрящей будет осуществляться при
- 27. III. Заключение Печать органов уже не фантастика, а
- 28. Список использованных источников1. Clarence T. Sasaki Обзор
- 29. 5. Гортань [Электронный ресурс]. Режим доступа: https://ru.wikipedia.org/wiki
- 30. Скачать презентанцию
I. Введение Гортань – это важный орган дыхательной системы, участвующий в проведении воздуха, голосообразовании и защите дыхательных путей от попадания пищи. Как и любой другой орган, она подвержена различным заболеваниям, опасность которых
Слайды и текст этой презентации
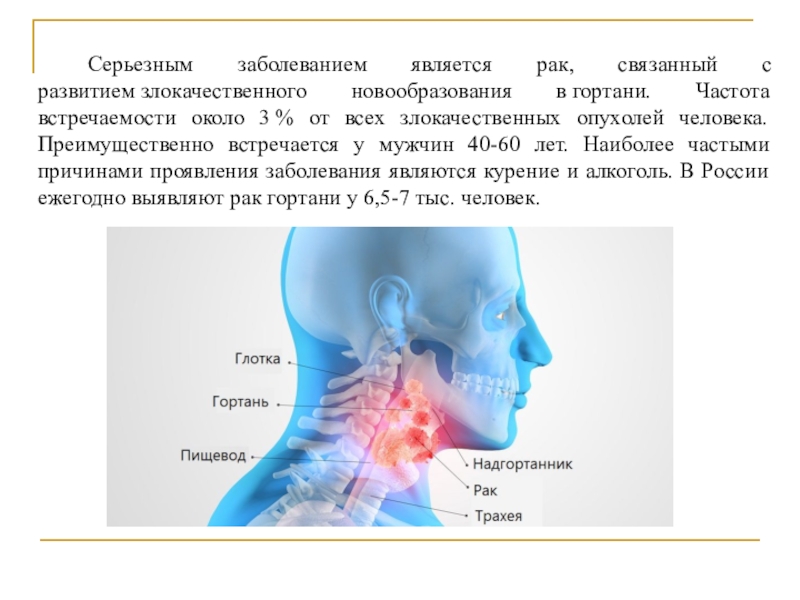
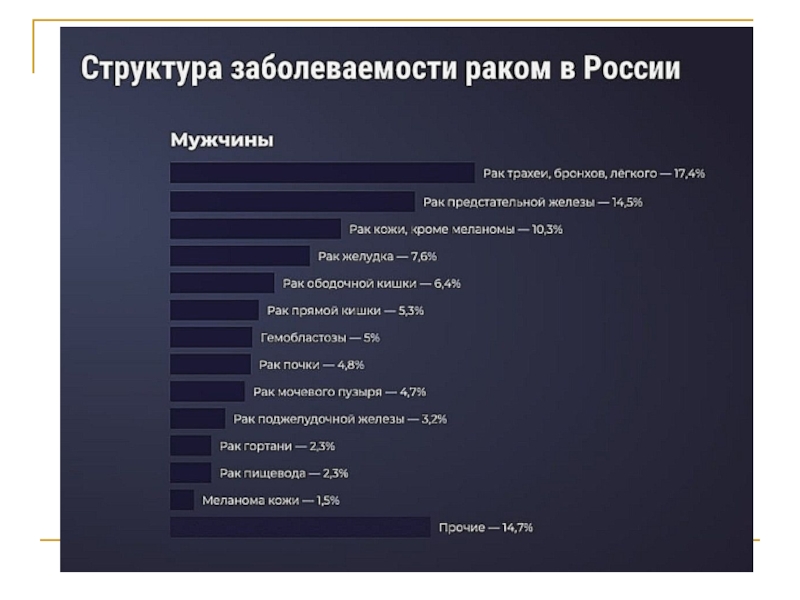
Слайд 4 Серьезным заболеванием является рак, связанный с развитием злокачественного новообразования в гортани. Частота
встречаемости около 3 % от всех злокачественных опухолей человека. Преимущественно встречается
у мужчин 40-60 лет. Наиболее частыми причинами проявления заболевания являются курение и алкоголь. В России ежегодно выявляют рак гортани у 6,5-7 тыс. человек.Слайд 5 Из-за малой осведомлённости пациентов и врачей чаще всего рак гортани
выявляют уже на последних стадиях. На III и IV стадиях
заболевания один из возможных вариантов лечения – это операция по удалению или проведение химиолучевой терапии.В связи с тем, что гортань является важным органом дыхательной системы, необходимым для жизни человека, его создание с помощью аддитивных технологий мы считаем наиболее актуальным.
Слайд 7Цель проекта: создание гортани с помощью 3D-биопринтера.
Задачи проекта:
1. Выявить
особенности строения гортани.
2. Оценить преимущества и риски создания гортани с
помощью 3D-биопринтера.3. Создать технологическую цепочку синтеза гортани.
4. Создать 3D модель гортани.
Цели и задачи
Слайд 8II. Основная часть
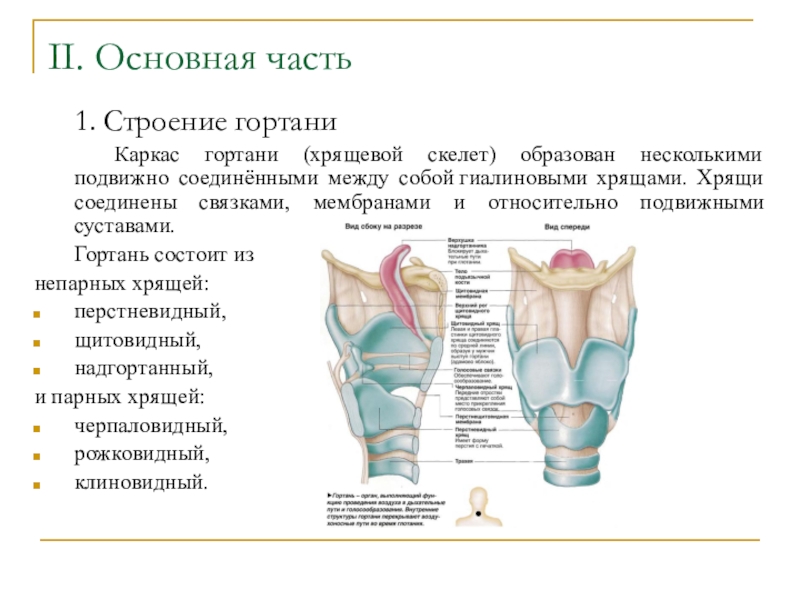
1. Строение гортани
Каркас гортани (хрящевой скелет) образован несколькими
подвижно соединёнными между собой гиалиновыми хрящами. Хрящи соединены связками, мембранами и
относительно подвижными суставами.Гортань состоит из
непарных хрящей:
перстневидный,
щитовидный,
надгортанный,
и парных хрящей:
черпаловидный,
рожковидный,
клиновидный.
Слайд 92. Преимущества создания гортани с помощью 3D-биопринтера
Мы предлагаем создание гортани
для дальнейшей пересадки пациенту с помощью 3D-биопринтера. Этот способ имеет
ряд преимуществ:1. Меньше шансов отторжения органа организмом.
2. Сокращение времени получения необходимого органа.
3. Экономически более выгодно, так как себестоимость биопечати будет снижаться по мере автоматизации процесса, развития методик и увеличении объёмов заказов.
4. Точность печати органов
Риски:
1. Отторжение после трансплан- тации.
Слайд 103. Каркас для создания гортани
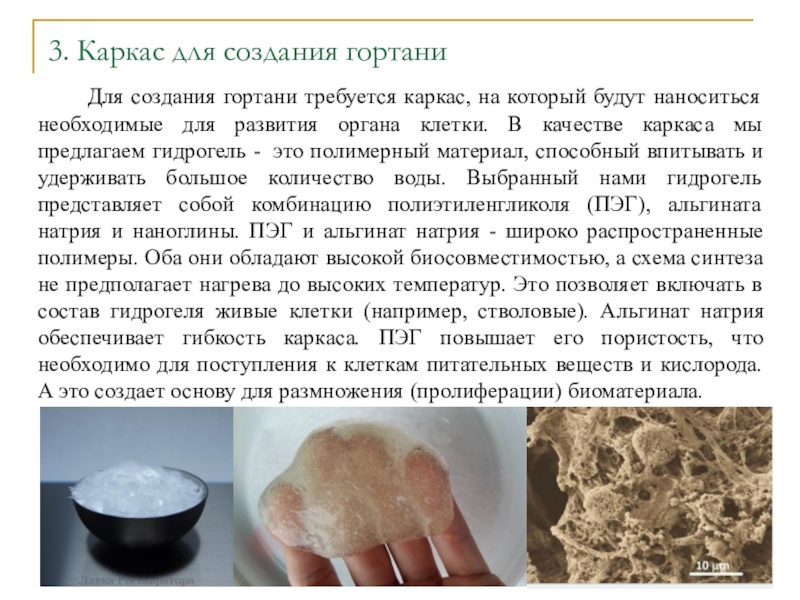
Для создания гортани требуется каркас, на
который будут наноситься необходимые для развития органа клетки. В качестве
каркаса мы предлагаем гидрогель - это полимерный материал, способный впитывать и удерживать большое количество воды. Выбранный нами гидрогель представляет собой комбинацию полиэтиленгликоля (ПЭГ), альгината натрия и наноглины. ПЭГ и альгинат натрия - широко распространенные полимеры. Оба они обладают высокой биосовместимостью, а схема синтеза не предполагает нагрева до высоких температур. Это позволяет включать в состав гидрогеля живые клетки (например, стволовые). Альгинат натрия обеспечивает гибкость каркаса. ПЭГ повышает его пористость, что необходимо для поступления к клеткам питательных веществ и кислорода. А это создает основу для размножения (пролиферации) биоматериала.Слайд 11Для придания гидрогелю вязкости, необходимой для печати на 3D-принтере, в
его составе будет использована "наноглина" — минеральное вещество, которое часто
используют как добавку к полимерным композитам. При сжатии фигурки из данного гидрогеля почти в 100 раз материал восстанавливает свою структуру, также он не рвётся при пятикратном растяжении.Этот материал хорошо подходит в качестве каркаса для выращивания новой ткани.
Слайд 124. Использование стволовых клеток для нанесения на каркас
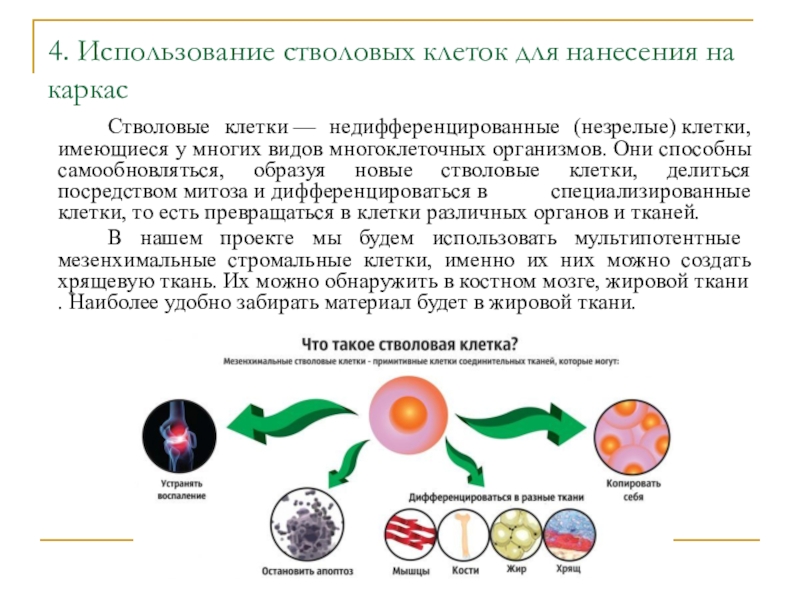
Стволовые клетки — недифференцированные
(незрелые) клетки, имеющиеся у многих видов многоклеточных организмов. Они способны самообновляться,
образуя новые стволовые клетки, делиться посредством митоза и дифференцироваться в специализированные клетки, то есть превращаться в клетки различных органов и тканей.В нашем проекте мы будем использовать мультипотентные мезенхимальные стромальные клетки, именно их них можно создать хрящевую ткань. Их можно обнаружить в костном мозге, жировой ткани . Наиболее удобно забирать материал будет в жировой ткани.
Слайд 131) Преимущества получения стволовых клеток из жировой ткани:
1. Быстрое, удобное
и эффективное получение клеток в сравнении с красным костным мозгом
или периферической кровью.2. Количество полученных клеток больше, чем из других источников стволовых клеток.
3. Клеткам свойствен высокий пролиферативный потенциал – это означает, что в условиях лаборатории эти клетки возможно размножить до количества необходимого для терапии.
4. Эти клетки секретируют цитокины, различные факторы роста, факторы роста внеклеточного ремодулирования матрикса, гиалуроновую кислоту, коллаген, эластин, гликозаминогликаны и другие факторы, которые способствуют регенерации тканей.
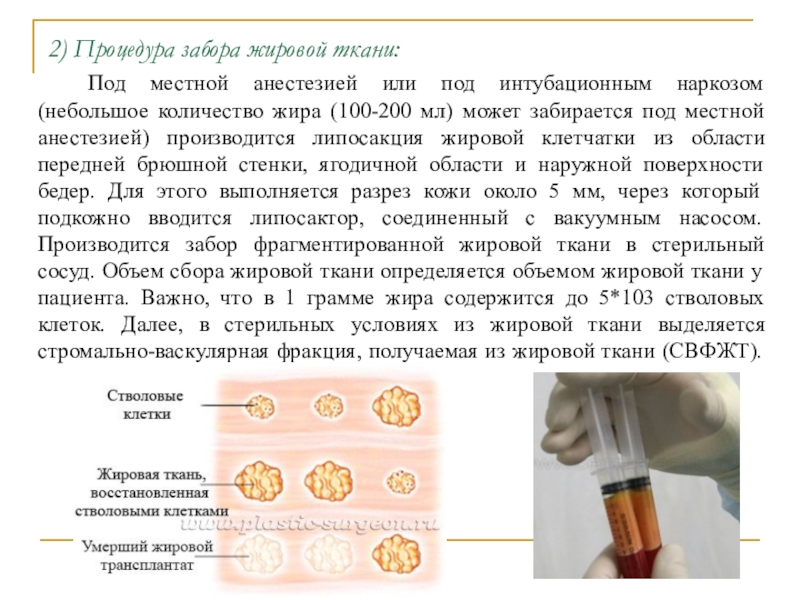
Слайд 142) Процедура забора жировой ткани:
Под местной анестезией или под
интубационным наркозом (небольшое количество жира (100-200 мл) может забирается под
местной анестезией) производится липосакция жировой клетчатки из области передней брюшной стенки, ягодичной области и наружной поверхности бедер. Для этого выполняется разрез кожи около 5 мм, через который подкожно вводится липосактор, соединенный с вакуумным насосом. Производится забор фрагментированной жировой ткани в стерильный сосуд. Объем сбора жировой ткани определяется объемом жировой ткани у пациента. Важно, что в 1 грамме жира содержится до 5*103 стволовых клеток. Далее, в стерильных условиях из жировой ткани выделяется стромально-васкулярная фракция, получаемая из жировой ткани (СВФЖТ).Слайд 153) Протокол выделения СВФЖТ:
Процедура выделения стромальной сосудистой фракции жировой ткани производится
в стерильных условиях, в ламинаре с использованием одноразовых расходных материалов:
Забранная
жировая ткань промывается в фосфатном буфере 3 раза по 5 минут.Производится аспирация буфера.
Жировая ткань растворяется в 0,1%-ном растворе коллагеназы в течение 40 минут в шейкере при температуре 37°С.
Зрелые адипоциты и соединительная ткань отделяются от стромально-васкулярной фракции путем центрифугирования (800 оборотов вминуту, 10 минут).
Для удаления эритроцитов полученные клетки ресуспендируются в лизирующем буфере (155 mM NH4CI, 10 mM KHCO3, 0.1 mM EDTA) в течение 5 минут при комнатной температуре.
Клетки промываются в фосфатном буфере и центрифугируются в режиме 800 об./мин., 10 минут.
Подсчет клеток производится в камере Горяева с использованием трипанового синего для определения количества жизнеспособных клеток.
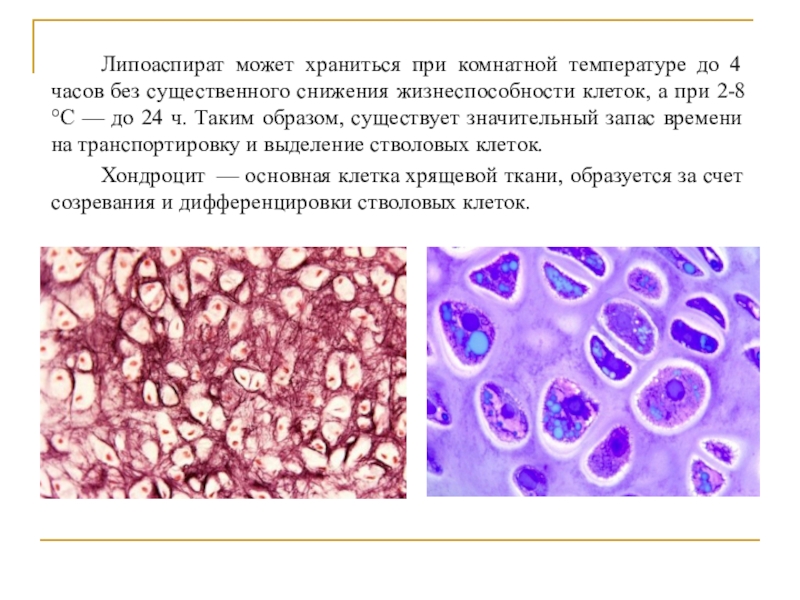
Слайд 16 Липоаспират может храниться при комнатной температуре до 4 часов без
существенного снижения жизнеспособности клеток, а при 2-8 °С — до
24 ч. Таким образом, существует значительный запас времени на транспортировку и выделение стволовых клеток.Хондроцит — основная клетка хрящевой ткани, образуется за счет созревания и дифференцировки стволовых клеток.
Слайд 175. Создание сфероидов
Сфероид - это крошечный (200–300 мкм диаметром) шарообразный
сгусток из живых клеток. Преимущество сфероидов перед отдельными клетками заключается
в том, что они образуют между собой межклеточные связи и матрикс, по сути, являясь готовыми микротканями для сборки полноценной ткани. Следовательно, выживаемость клеток в сфероиде больше.Слайд 18 Простой вариант такой структуры можно получить путем инкубации суспензий различных
клеток пациента в небольшом объеме культуральной среды, например, в формах
в виде мелких пчелиных сот. Удобным «сырьем» для биопечати являются стволовые клетки жировой ткани пациента, которые мы и будем использовать. Тканевые сфероиды, произведенные из этих стволовых клеток, могут сращиваться в кольцо или торус и сокращаться под действием специфических стимулов.Слайд 196. Технологии биофабрикации в 3D-биопринтере
В качестве среды для формирования сфероидов
будет использоваться неадгезивный гидрогель, благодаря чему клетки будут прилипать не
к поверхности культуральной посуды, а друг к другу, образуя шарообразную структуру. Автоматизированный вариант этой технологии, разработан в Медицинском университете Южной Каролины (США) группой В. А. Миронова. Он позволяет производить до 6 тыс. тканевых сфероидов в стандартных 96-луночных планшетах.Слайд 20 FABION – первый отечественный 3D-биопринтер оригинальной конструкции и дизайна, позволяющий
точно распределять тканевые сфероиды (биочернила) в последовательных слоях гидрогеля (биобумага)
согласно заданной цифровой модели. Уникальное техническое, дизайнерское и инженерное решение, разработанное в Лаборатории «3Д Биопринтинг Солюшенс», делают биопринтер универсальным. Предназначение этого аппаратно-программного комплекса – печать живого функционального трехмерного тканевого органного конструкта. Оригинальное тех- ническое и инженерное решение базиру- ется на особенностях собственной техно- логии 3D биопечати. FABION превосхо- дит по ряду параметров существующие в мире в настоящее время коммерческие биопринтеры.Слайд 21 1. Мультифункциональность. Биопринтер FABION позволяет использовать все известные методы и
способы трехмерной биопечати. 2. Уникальное устройство полимеризации гидрогелей (биобумаги) с использованием
УФ-излучения не контактирует со сфероидами и клетками, и соответственно не повреждает ДНК клетки, в отличие от существующих в мире инженерных решений систем полимеризации, воплощенных в существующих коммерческих биопринтерах. 3. Комбинаторность: возможность комбинировать между собой различные вариации методов биопечати, способов нанесения, материалов. Широкий перечень управляемых программным обеспечением параметров биопечати дополняет определение комбинаторности.4. Точность. Разрешающая способность печати биопринтера соответствует самым высоким требованиям стандартов ISO.
5. Система перемещения по осям Х-Y-Z выполнена с обратной связью, что позволяет размещать форсунки биопринтера с точностью 5 микрометров и тем самым точно воспроизводить заданную цифровую модель. 6. Компактность. Г-образный дизайн печатающей системы настоящего биопринтера обеспечивает достаточное пространство для размещения форсунок.
7. Контроль. Процессы трехмерной печати контролируются в режиме реального времени при помощи цифровой камеры, встроенной в биопринтер.
Основные преимущества и функциональные отличия биопринтера FABION:
Слайд 22 Данная модель 3D – биопринтера подойдёт для печати хрящей гортани.
Её большим преимуществом является то, что она умеет печатать сфероидами.
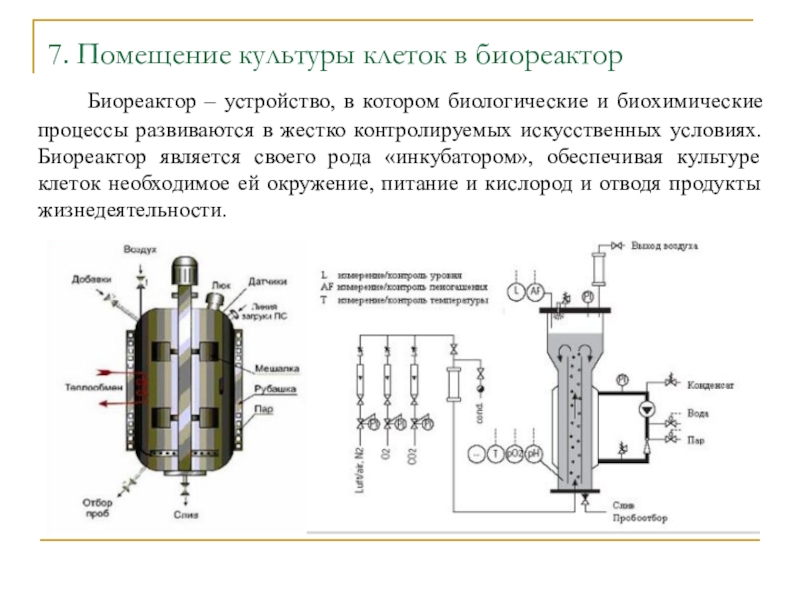
Также печать с помощью данного биопринтера будет обходиться дешевле, чем с помощью зарубежных.Слайд 237. Помещение культуры клеток в биореактор
Биореактор – устройство, в
котором биологические и биохимические процессы развиваются в жестко контролируемых искусственных
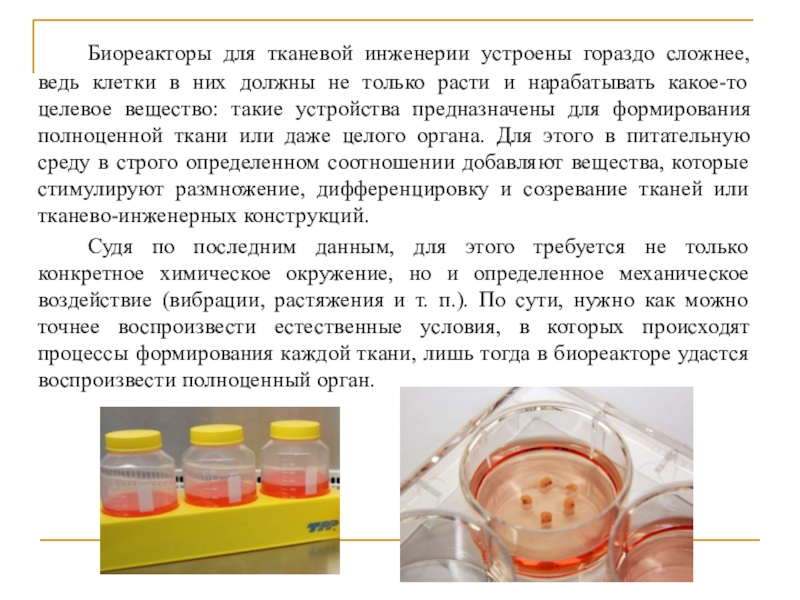
условиях. Биореактор является своего рода «инкубатором», обеспечивая культуре клеток необходимое ей окружение, питание и кислород и отводя продукты жизнедеятельности.Слайд 24 Биореакторы для тканевой инженерии устроены гораздо сложнее, ведь клетки в
них должны не только расти и нарабатывать какое-то целевое вещество:
такие устройства предназначены для формирования полноценной ткани или даже целого органа. Для этого в питательную среду в строго определенном соотношении добавляют вещества, которые стимулируют размножение, дифференцировку и созревание тканей или тканево-инженерных конструкций.Судя по последним данным, для этого требуется не только конкретное химическое окружение, но и определенное механическое воздействие (вибрации, растяжения и т. п.). По сути, нужно как можно точнее воспроизвести естественные условия, в которых происходят процессы формирования каждой ткани, лишь тогда в биореакторе удастся воспроизвести полноценный орган.
Слайд 25Стандартные условия культивирования для хрящевой ткани:
Температура 37°C
Относительная влажность воздуха 90-100%
Содержание
в газообразной смеси CO2 – 5% и O2 – 20%
Оптимальной комбинацией ростовых факторов для направленной хондрогенной дифференцировки стволовых клеток, полученных из жировой ткани, является BMP-2/TGF-P3 (bone morphogenetic protein-2/transforming growth factor-p3).
Слайд 268. Соединение хрящей
Соединение хрящей будет осуществляться при помощи поликапролактона. Поликапролактон
- это биоразлагаемый полиэфир с низкой температурой плавления (59-64 градусов). Он
является полимером ε-капролактона. В биомедицине поликапролактон применяется как шовный материал. Он одновременно и гибкий, и прочный. Биодеградация в теле человека происходит медленно, около 3 лет. Продуктами деградации являются капроновая кислота, вода, CO2 .Слайд 27III. Заключение
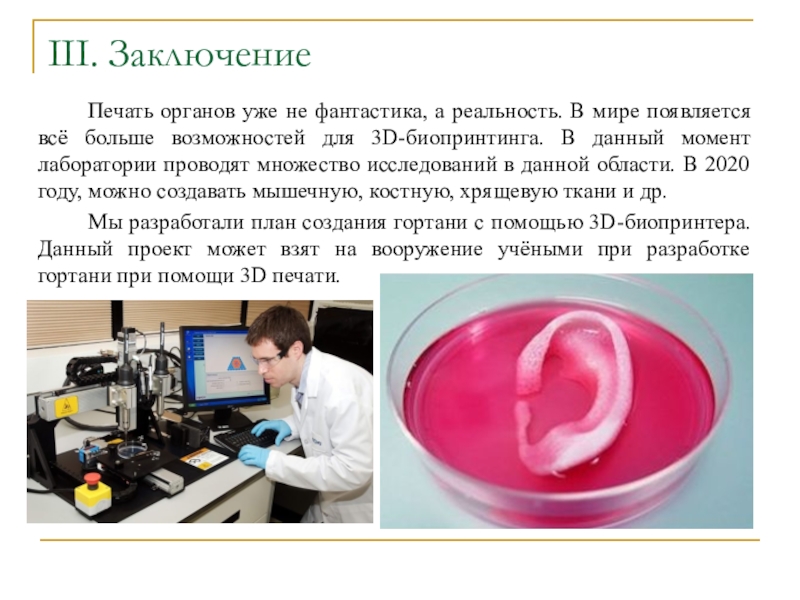
Печать органов уже не фантастика, а реальность. В мире
появляется всё больше возможностей для 3D-биопринтинга. В данный момент лаборатории
проводят множество исследований в данной области. В 2020 году, можно создавать мышечную, костную, хрящевую ткани и др.Мы разработали план создания гортани с помощью 3D-биопринтера. Данный проект может взят на вооружение учёными при разработке гортани при помощи 3D печати.
Слайд 28Список использованных источников
1. Clarence T. Sasaki Обзор заболеваний гортани [Электронный
ресурс]. Режим доступа: https://www.msdmanuals.com/ru/%D0%BF%D1%80%D0%BE%D1%84%D0%B5%D1%81%D1%81%D0%B8%D0%BE%D0%BD%D0%B0%D0%BB%D1%8C%D0%BD%D1%8B%D0%B9/%D0%B7%D0%B0%D0%B1%D0%BE%D0%BB%D0%B5%D0%B2%D0%B0%D0%BD%D0%B8%D1%8F-%D1%83%D1%85%D0%B0,-%D0%B3%D0%BE%D1%80%D0%BB%D0%B0-%D0%B8-%D0%BD%D0%BE%D1%81%D0%B0/%D0%B7%D0%B0%D0%B1%D0%BE%D0%BB%D0%B5%D0%B2%D0%B0%D0%BD%D0%B8%D1%8F-%D0%B3%D0%BE%D1%80%D1%82%D0%B0%D0%BD%D0%B8/%D0%BE%D0%B1%D0%B7%D0%BE%D1%80-%D0%B7%D0%B0%D0%B1%D0%BE%D0%BB%D0%B5%D0%B2%D0%B0%D0%BD%D0%B8%D0%B9-overview-of-laryngeal-disorders%D0%B3%D0%BE%D1%80%D1%82%D0%B0%D0%BD%D0%B8
2.Рак гортани [Электронный ресурс]. Режим доступа: https://ru.wikipedia.org/wiki/%D0%A0%D0%B0%D0%BA_%D0%B3%D0%BE%D1%80%D1%82%D0%B0%D0%BD%D0%B8
3.
Рак гортани: прогноз[Электронный ресурс]. Режим доступа: https://oncocenter-ichilov.com/lechenie-raka-gortani-v-izraile/prognoz-pri-rake-gortani/4. Рак гортани: как жить после потери голоса?[Электронный ресурс]. Режим доступа: https://takiedela.ru/news/2019/10/25/poterya-golosa/
Слайд 295. Гортань [Электронный ресурс]. Режим доступа: https://ru.wikipedia.org/wiki /%D0%93%D0%BE%D1%80%D1%82%D0%B0%D0%BD%D1%8C
6. Миронов В.А.
Вслед за Создателем. Технологии биопринтинга[Электронный ресурс]. Режим доступа: https://yandex.ru/turbo/s/scfh.ru/papers/vsled-za-sozdatelem-tekhnologii-bioprintinga/
7. Новый
гидрогель позволит печатать хрящи на 3D-принтере[Электронный ресурс]. Режим доступа: https://druid.ru/news/longborn/show/814.htm8. Стволовые клетки [Электронный ресурс]. Режим доступа: https://ru.wikipedia.org /wiki/%D0%A1%D1%82%D0%B2%D0%BE%D0%BB%D0%BE%D0%B2%D1%8B%D0%B5_%D0%BA%D0%BB%D0%B5%D1%82%D0%BA%D0%B8
9. Мезенхимальные стволовые клетки из жировой ткани[Электронный ресурс]. Режим доступа: https://ivfrigastemcells.lv/ru/poleznaja-informacija/ mezenkhimalnye-stvolovye-kletki-iz-zhirovoi-tkani/
10. Масгутов Р.Ф., Богов (Мл.) А.А., Ризванов А.А., Салафутдинов И.И., Ханнанова И.Г., Галлямов А.Р. Стволовые клетки из жировой ткани биологические свойства и перспективы клинического применения [Электронный ресурс]. Режим доступа: https://cyberleninka.ru /article /n/stvolovye-kletki-iz-zhirovoy-tkani-biologicheskie-svoystva-i-perspektivy-klinicheskogo-primeneniya
11. Биопринтер FABION [Электронный ресурс]. Режим доступа: https://bioprinting.ru /products-services/fabion/
12.https://vk.com/away.php?to=https%3A%2F%2Fjournal.transpl.ru%2Fvtio%2Farticle%2Fdownload%2F706%2F596&cc_key=















![Проект по теме Аддитивные технологии 2030 Список использованных источников1. Clarence T. Sasaki Обзор заболеваний гортани [Электронный ресурс]. Список использованных источников1. Clarence T. Sasaki Обзор заболеваний гортани [Электронный ресурс]. Режим доступа: https://www.msdmanuals.com/ru/%D0%BF%D1%80%D0%BE%D1%84%D0%B5%D1%81%D1%81%D0%B8%D0%BE%D0%BD%D0%B0%D0%BB%D1%8C%D0%BD%D1%8B%D0%B9/%D0%B7%D0%B0%D0%B1%D0%BE%D0%BB%D0%B5%D0%B2%D0%B0%D0%BD%D0%B8%D1%8F-%D1%83%D1%85%D0%B0,-%D0%B3%D0%BE%D1%80%D0%BB%D0%B0-%D0%B8-%D0%BD%D0%BE%D1%81%D0%B0/%D0%B7%D0%B0%D0%B1%D0%BE%D0%BB%D0%B5%D0%B2%D0%B0%D0%BD%D0%B8%D1%8F-%D0%B3%D0%BE%D1%80%D1%82%D0%B0%D0%BD%D0%B8/%D0%BE%D0%B1%D0%B7%D0%BE%D1%80-%D0%B7%D0%B0%D0%B1%D0%BE%D0%BB%D0%B5%D0%B2%D0%B0%D0%BD%D0%B8%D0%B9-overview-of-laryngeal-disorders%D0%B3%D0%BE%D1%80%D1%82%D0%B0%D0%BD%D0%B82.Рак гортани [Электронный ресурс].](/img/tmb/7/617501/80e1a493d2066e7151acb5cd00c126b7-800x.jpg)
![Проект по теме Аддитивные технологии 2030 5. Гортань [Электронный ресурс]. Режим доступа: https://ru.wikipedia.org/wiki /%D0%93%D0%BE%D1%80%D1%82%D0%B0%D0%BD%D1%8C6. Миронов В.А. Вслед 5. Гортань [Электронный ресурс]. Режим доступа: https://ru.wikipedia.org/wiki /%D0%93%D0%BE%D1%80%D1%82%D0%B0%D0%BD%D1%8C6. Миронов В.А. Вслед за Создателем. Технологии биопринтинга[Электронный ресурс]. Режим](/img/tmb/7/617501/a79b5d96e513bbbc7ea8d51f36393c24-800x.jpg)