Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Профилактика, скрининг и лечение рака молочной железы
Содержание
- 1. Профилактика, скрининг и лечение рака молочной железы
- 2. Рак молочной железы – злокачественная опухоль, развивающаяся
- 3. РаспространениеРак молочной железы является вторым (после рака
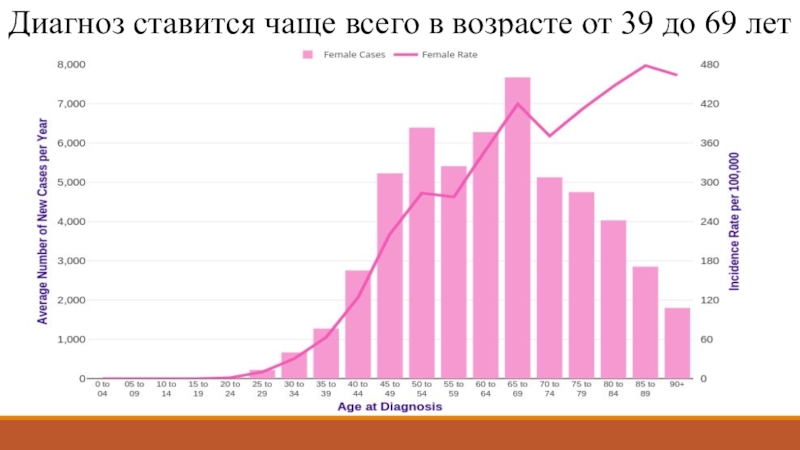
- 4. Диагноз ставится чаще всего в возрасте от 39 до 69 лет
- 5. Факторы рискаОбщие (неспецифичные для РМЖ) КурениеУпотребление алкоголяИзбыточные весМалоподвижный образ жизни
- 6. Специфические для РМЖ Нерожавшие женщины, впервые родившие
- 7. Регулярные физические нагрузки – не менее 150
- 8. Скрининг рака молочной железыСКРИНИНГ в медицине — методологический
- 9. Скрининг РМЖ среди общей популяцииРекомендуемый возраст начала
- 10. Генетическая предрасположенностьВысокая рентгенологическая плотность молочных железНаличие РМЖ
- 11. Методами молекулярной генетики идентифицирован и охарактеризован ряд
- 12. Вероятность того, что рак молочной железы (или
- 13. Скрининг при выявлении мутаций в генах BRCA1/2Для
- 14. Генетическая предрасположенностьВысокая рентгенологическая плотность молочных железНаличие РМЖ
- 15. Преобладание железисто-фиброзного компонента (до 75 %) по
- 16. Слайд 16
- 17. Скрининг при выявлении повышенной плотности молочных железДополнительная
- 18. Генетическая предрасположенностьВысокая рентгенологическая плотность молочных железНаличие РМЖ
- 19. В возрасте 30-34 года - маммография не
- 20. Генетическая предрасположенностьВысокая рентгенологическая плотность молочных железНаличие РМЖ
- 21. Рекомендуется МРТ – скрининг молочных желез у
- 22. Диагностика РМЖСкрининг/самообследованиеПодозрение на РМЖ (результат маммографии +
- 23. Морфологическое подтверждениеТонкоигольная пункционная биопсия (ТАБ) – достаточно
- 24. Core-биопсия ТАБ молочной железы
- 25. Остальные исследованияобщий анализ крови биохимический анализ крови
- 26. Лечение РМЖОперативное лечениеХимиотерапевтическое лечениеТаргетная терапияЛучевая терапияГормонотерапияИммунотерапия** Клинические исследования
- 27. Лечение РМЖ до IIIст (не местнораспространённый)Размер опухоли
- 28. Оперативное лечениеI.Радикальная мастэктомия с одномоментной или отсроченной
- 29. БСЛУ
- 30. Слайд 30
- 31. Уровни лимфодиссекцииПри выполнении радикальной мастэктомии и радикальной
- 32. Адъювантная терапияПоказания к проведению адъювантной терапии, а
- 33. На основании данных вышеперечисленных исследований определяется молекулярный
- 34. Сопоставляя данные патологоанатомического исследования операционного материала –
- 35. ПримерыЛюминальный А - только ГТ Назначение адъювантной
- 36. Особенности гормонотерапии РМЖТамоксифен 20 мг/сут – мин.
- 37. Неоадъювантная терапия при первично операбельном РМЖМожет быть
- 38. Алгоритм проведения неоадъювантной терапии
- 39. Местнораспространенный первично неоперабельный инвазивный рак молочной железыN
- 40. Адъювантная терапияАлгоритм назначения адъювантной лекарственной терапии аналогичен
- 41. Метастатический РМЖЕдиного стандарта лечения метастатического РМЖ не
- 42. Гормонотерапия метастатического рака молочной железыМетодом выбора терапии
- 43. Химиотерапия метастатического рака молочной железыХТ показана следующим
- 44. ХТ с использованием одной и той же комбинации может
- 45. Анти-HER2 терапия метастатического рака молочной железыБольные HER2‑положительным
- 46. МТС в костиКлинические проявления:Боли в костяхПатологические переломыКомпрессионные переломы тел позвонковКомпрессия спинного мозгаГиперкальциемия
- 47. Лечение больных с МТС в костиЭффективная лекарственная
- 48. Наблюдение после первичного лечения раннего и местно-распространённого
- 49. Женщины с неудаленной маткой, получающие адъювантно тамоксифен, должны
- 50. Спасибо за внимание
- 51. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Рак молочной железы – злокачественная опухоль, развивающаяся из железистой ткани
молочной железы, которая может встречаться как у женщин, так и
у мужчинСлайд 3Распространение
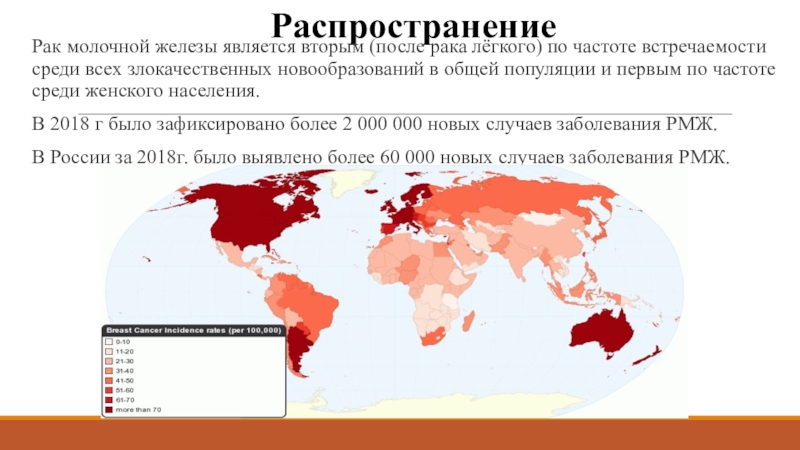
Рак молочной железы является вторым (после рака лёгкого) по частоте
встречаемости среди всех злокачественных новообразований в общей популяции и первым
по частоте среди женского населения.В 2018 г было зафиксировано более 2 000 000 новых случаев заболевания РМЖ.
В России за 2018г. было выявлено более 60 000 новых случаев заболевания РМЖ.
Слайд 5Факторы риска
Общие (неспецифичные для РМЖ)
Курение
Употребление алкоголя
Избыточные вес
Малоподвижный образ жизни
Слайд 6Специфические для РМЖ
Нерожавшие женщины, впервые родившие после 30 лет
Раннее
менархе (< 12 лет), поздняя менопауза (>55 лет)
Получение заместительной гормональной
терапииИспользование комбинированных оральных контрацептивов
Облучение грудной клетки в анамнезе до 30 лет!
Высокая рентгенологическая плотность молочных желез!
Носители мутаций в герминальных генах BRCA1 BRCA 2 CHEK 2 и др!
Наличие РМЖ у родственников 1-ой степени (мать, сестра, дочь)!
Факторы риска
Слайд 7
Регулярные физические нагрузки –
не менее 150 мин/неделя аэробных упражнений
Избежание
приёма алкоголя
Нормализация массы тела – ИМТ 18,5 – 22,9.
Коррекция факторов
рискаСлайд 8Скрининг рака молочной железы
СКРИНИНГ в медицине — методологический подход для массового
обследования населения (его отдельных контингентов) с целью выявления определенного заболевания
(группы заболеваний) или факторов, способствующих развитию этого заболевания (факторов риска)Слайд 9Скрининг РМЖ среди общей популяции
Рекомендуемый возраст начала - 40 лет
Вид
обследования – маммография молочных желез в прямой и косой проекциях
Интервал
между обследованиями – 2 годаДля менструирующих женщин - обследование проводится в первую фазу
Снимки оцениваются двумя специалистами
Слайд 10Генетическая предрасположенность
Высокая рентгенологическая плотность молочных желез
Наличие РМЖ у родственников 1-ой
степени
Облучение грудной клетки в анамнезе до 30 лет
Скрининг РМЖ среди
группы повышенного рискаСлайд 11Методами молекулярной генетики идентифицирован и охарактеризован ряд генов, мутации в
которых ассоциированы с повышенным риском возникновения рака молочной железы.
К
ним, в первую очередь, относятся гены BRCA (Breast Cancer Susceptibility gene)1,BRCA2.
Наличие клинически значимых мутаций в генах BRCA1
или BRCA2 вызывает потерю функции белков, кодируемых
этими генами, в результате чего нарушается основной
Механизм репарации двунитевых разрывов ДНК.
Слайд 12Вероятность того, что рак молочной железы (или яичников) связан с
мутацией BRCA1 или BRCA2 наиболее высока:
• в семьях с
более чем тремя случаями заболевания раком молочной железы или яичников у родственников первой линии родства (родители, сестры, братья, дети); • в семьях с более чем двумя случаями заболевания раком молочной железы, диагностированными в возрасте до 50 лет;
• при наличии в семейной истории случая рака молочной железы у мужчин;
• при наличии в семейной истории случаев двустороннего рака молочной железы
Требуется генетическое тестирование на наличие герминальных мутаций!
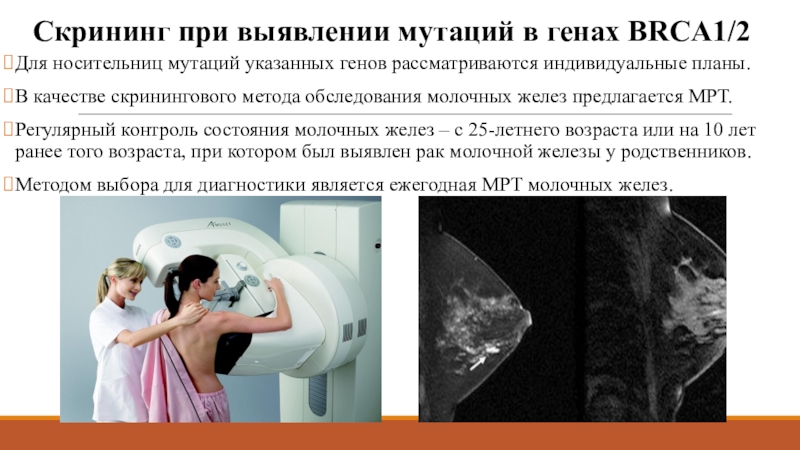
Слайд 13Скрининг при выявлении мутаций в генах BRCA1/2
Для носительниц мутаций указанных
генов рассматриваются индивидуальные планы.
В качестве скринингового метода обследования молочных
желез предлагается МРТ. Регулярный контроль состояния молочных желез – с 25-летнего возраста или на 10 лет ранее того возраста, при котором был выявлен рак молочной железы у родственников.
Методом выбора для диагностики является ежегодная МРТ молочных желез.
Слайд 14Генетическая предрасположенность
Высокая рентгенологическая плотность молочных желез
Наличие РМЖ у родственников 1-ой
степени
Облучение грудной клетки в анамнезе до 30 лет
Скрининг РМЖ среди
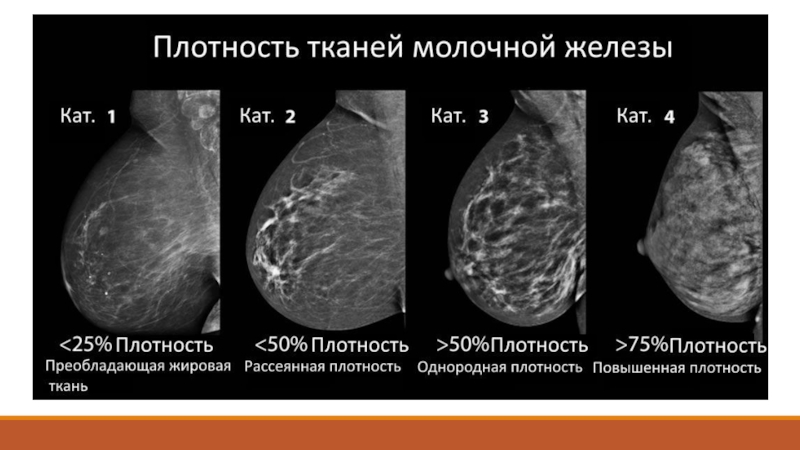
группы повышенного рискаСлайд 15Преобладание железисто-фиброзного компонента (до 75 %) по отношению к жировому
является фактором риска развития рака молочной железы
Относительный риск развития заболевания
у женщин с плотностью 75 % (и выше) в 4 раза выше, чем у женщин с плотностью 5 % (и ниже). При высокой плотности молочных желез значительно увеличивается риск потери опухоли, (особенно малых размеров) на снимке на фоне железисто-фиброзной ткани
Плотность ткани молочной железы представляет собой соотношение фиброзно-железистого и жирового компонентов в молочной железе
Слайд 17Скрининг при выявлении повышенной плотности молочных желез
Дополнительная ультразвуковая томография после
маммографии и в промежутке до следующего планового скринингового обследования
ИЛИ
МРТ
молочных желез в качестве скринингового методаСлайд 18Генетическая предрасположенность
Высокая рентгенологическая плотность молочных желез
Наличие РМЖ у родственников 1-ой
степени
Облучение грудной клетки в анамнезе до 30 лет
Скрининг РМЖ среди
группы повышенного рискаСлайд 19В возрасте 30-34 года - маммография не показана за исключением
случаев, когда рак молочной железы у одного из членов семьи
диагностирован в возрасте моложе 39 лет, в этом случае маммографию следует начинать в возрасте на 5 лет моложе возраста постановки диагнозаВ возрасте 35-49 лет - ежегодная маммография.
В возрасте 50 лет и старше -каждые 18 месяцев
Тщательный сбор анамнеза!
Слайд 20Генетическая предрасположенность
Высокая рентгенологическая плотность молочных желез
Наличие РМЖ у родственников 1-ой
степени
Облучение грудной клетки в анамнезе до 30 лет
Скрининг РМЖ среди
группы повышенного рискаСлайд 21Рекомендуется МРТ – скрининг молочных желез у женщин, получивших облучение
на область грудной клетки в возрасте 10-30 лет.
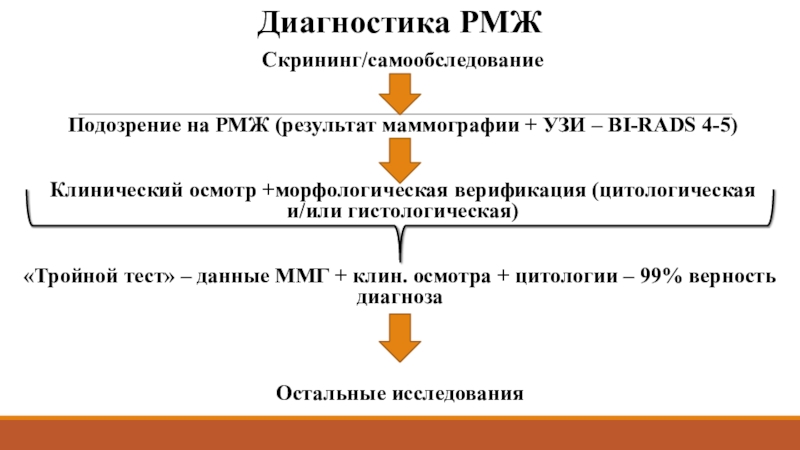
Слайд 22Диагностика РМЖ
Скрининг/самообследование
Подозрение на РМЖ (результат маммографии + УЗИ – BI-RADS
4-5)
Клинический осмотр +морфологическая верификация (цитологическая и/или гистологическая)
«Тройной тест» – данные
ММГ + клин. осмотра + цитологии – 99% верность диагнозаОстальные исследования
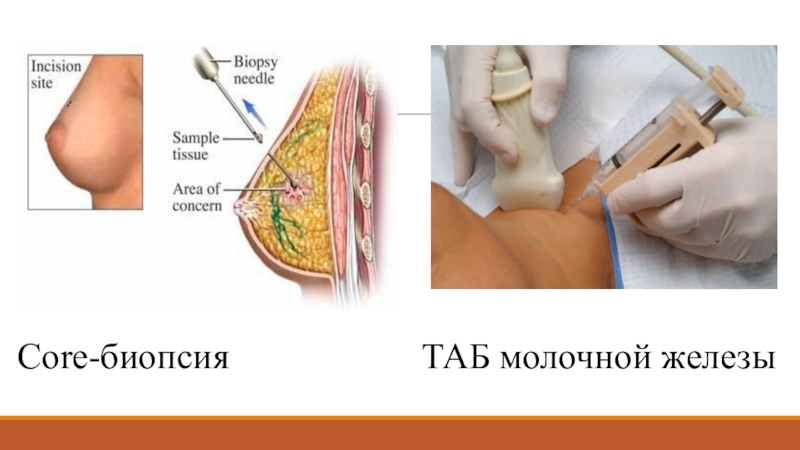
Слайд 23Морфологическое подтверждение
Тонкоигольная пункционная биопсия (ТАБ) – достаточно информативный метод для
постановки диагноза
Core-биопсия + иммуногистохимическое исследование (ИГХ) – считается более точным
методом, необходимым при планировании лечения в тех случаях, когда лечение начинается не с операции.В случае начала лечения с операции, Core-биопсия может не выполняться, при условии патологоанатомического исследования операционного материала*
* В условиях крупных центров, при финансовой возможности учреждения, Core-биопсия рекомендуется до начала любого вида лечения
Слайд 25Остальные исследования
общий анализ крови
биохимический анализ крови
МРТ молочных желез
— по показаниям (BRCA-ассоциированный РМЖ, наличие имплантов в молочной железе, дольковый
варианте, подозрение на мультицентричность / мультифокальность роста)R-графию органов грудной клетки
КТ / МРТ органов грудной клетки — по показаниям (подозрение в наличии МТС)
УЗИ органов брюшной полости и малого таза
радиоизотопное исследование скелета + рентгенографию и / или КТ / МРТ зон накопления РФП — по показаниям;
оценку функции яичников
консультацию медицинского генетика (при отягощённом семейном анамнезе – пациенткам моложе 40 лет, пациенткам моложе 50 лет с тройным негативным фенотипом РМЖ)
Слайд 26Лечение РМЖ
Оперативное лечение
Химиотерапевтическое лечение
Таргетная терапия
Лучевая терапия
Гормонотерапия
Иммунотерапия*
* Клинические исследования
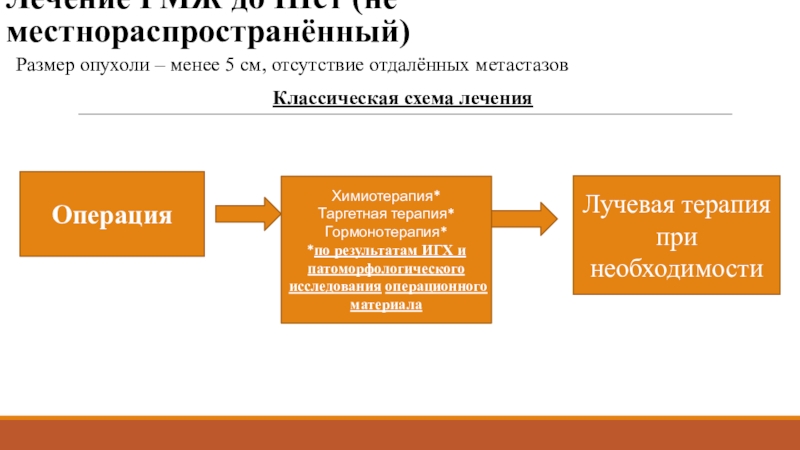
Слайд 27Лечение РМЖ до IIIст (не местнораспространённый)
Размер опухоли – менее 5
см, отсутствие отдалённых метастазов
Классическая схема лечения
Операция
Химиотерапия*
Таргетная терапия*
Гормонотерапия*
*по результатам ИГХ
и патоморфологического исследования операционного материалаЛучевая терапия при необходимости
Слайд 28Оперативное лечение
I.Радикальная мастэктомия с одномоментной или отсроченной реконструкцией или без
неё
Большой размер опухоли относительно молочной железы
Околососковое, центральное расположение опухоли
«Дорожка» инфильтрации
к соску, видимая на ММГМультицентрическое расположение опухоли
Отсутствие возможность провести облучение молочной железы в послеоперационном периоде
II.Радикальная резекция
Отсутствие вышеперечисленных факторов
III.Радикальная резекция с биопсией сторожевого лимфатического узла (БСЛУ)
Отсутствие клинически определяемого поражение регионарных л/у до момента операции при условии возможности органосохранной операции. Размер опухоли Т1-Т2
IV.Профилактическая мастэктомия с контралатеральной стороны - при наличие мутаций BRCA1/2 у лиц старше 50 лет
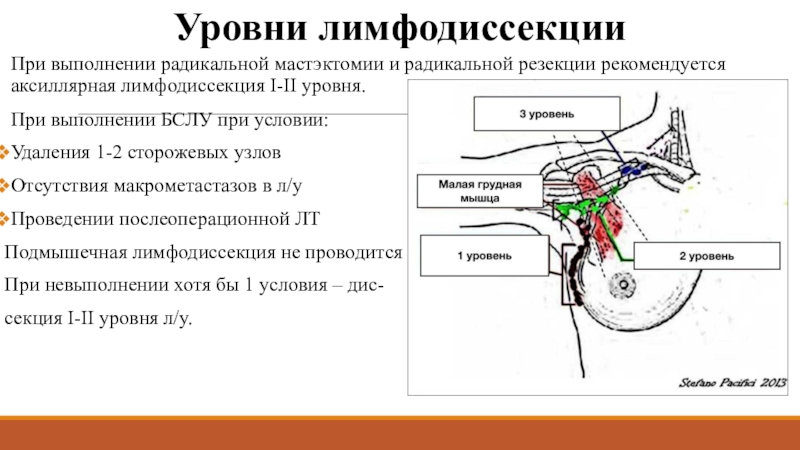
Слайд 31Уровни лимфодиссекции
При выполнении радикальной мастэктомии и радикальной резекции рекомендуется аксиллярная
лимфодиссекция I-II уровня.
При выполнении БСЛУ при условии:
Удаления 1-2 сторожевых узлов
Отсутствия
макрометастазов в л/уПроведении послеоперационной ЛТ
Подмышечная лимфодиссекция не проводится
При невыполнении хотя бы 1 условия – дис-
секция I-II уровня л/у.
Слайд 32Адъювантная терапия
Показания к проведению адъювантной терапии, а так же её
схема определяются результатами:
Патологоанатомического исследования операционного материала (размер опухоли, количество пораженных
л/у, инвазия в лимфатические сосуды, степень злокачественности)ИГХ – исследования (гормональный статус, уровень экспреcсии HER2/neu, Ki-67%)
FISH (флюоресцентная иммуногибридизация in situ) – при необходимости уточнения HER2/neu статуса
А так же возрастом, коморбидностью и наличием/отсутствием герминальный мутаций
Слайд 33На основании данных вышеперечисленных исследований определяется молекулярный подтип опухоли.
На данный
момент клиническое значение имеет следующая классификация:
Люминальный А подтип (РЭ+,РП+, Ki67
В HER2 положительный подтип (РЭ+,РП-любой, Ki67>20%, HER2- гиперэкспрессияЛюминальный В HER2 отрицательный подтип (РЭ+,РП-любой, Ki67>20%, HER2- отрицательный)
HER2 – обогащённый подтип (HER2 – гиперэкспрессия, РП -,РЭ - )
Тройной негативный подтип (РЭ-, РП-, HER2 – отрицательный)
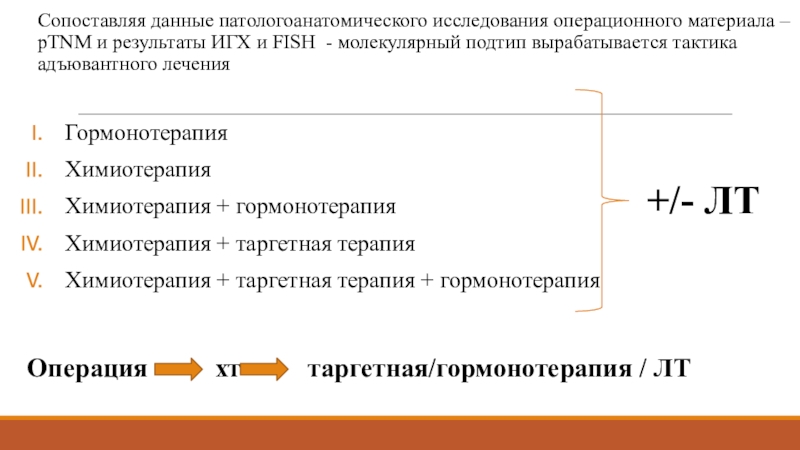
Слайд 34Сопоставляя данные патологоанатомического исследования операционного материала – pTNM и результаты
ИГХ и FISH - молекулярный подтип вырабатывается тактика адъювантного лечения
Гормонотерапия
Химиотерапия
Химиотерапия
+ гормонотерапияХимиотерапия + таргетная терапия
Химиотерапия + таргетная терапия + гормонотерапия
+/- ЛТ
Операция хт таргетная/гормонотерапия / ЛТ
Слайд 35Примеры
Люминальный А - только ГТ
Назначение адъювантной ХТ (в дополнение к адъювантной
ГТ) должно быть рассмотрено при наличии одного из следующих факторов:
• большая степень распространения болезни: – ≥4 поражённых метастазами регионарных лимфатических узлов; – ≥Т3;
• степень злокачественности - G3
В качестве ХТ рекомендуются режимы АС (4 курса) или DC
Люминальный В (HER2 положительный) - ХТ + анти-HER2 терапия + ГТ
При T1a (≤5 мм) и N0: только адъювантная ГТ; ХТ и анти-HER2 терапия не показаны.
При T1b, с (>5 мм, но ≤20 мм) и N0: возможна ХТ паклитакселом (без антрациклинов) в сочетании с трастузумабом (с последующей ГТ) (табл. 5, 7)
При Т2‑Т4 или N+: антрациклины → таксаны + анти-HER2 терапия (с последующей ГТ)
Слайд 36Особенности гормонотерапии РМЖ
Тамоксифен 20 мг/сут – мин. 5 лет (10
лет – при наличии факторов риска)
Выключение функции яичников:
Необходимая адъювантная системная
терапия не будет проведенаВ сочетании с ингибиторами ароматазы (противопоказания к приёму тамоксифена)
Возраст младше 40 лет
Больные с сохранной функцией яичников
Больные в менопаузе
Ингибиторы ароматазы + препараты кальция и витамин D - 5 лет
Режимы «переключения» – тамоксифен/ингибиторы ароматазы в общей сложность 5 лет
Продление терапии до 10 лет - при наличии МТС в л/у
Тамоксифен 20 мг/сут – 5 лет
Слайд 37Неоадъювантная терапия при первично операбельном РМЖ
Может быть назначена при:
HER2‑положительном
тройном
негативном фенотипе
Позволяет:
выполнить органосохраняющую операцию и / или улучшить косметический эффект
выявить больных с более
благоприятным прогнозом (в случае достижения полного патоморфологического ответа)оценить эффект лекарственной терапии и своевременно прекратить её в случае прогрессирования (с выполнением хирургического лечения).
Слайд 39Местнораспространенный первично неоперабельный инвазивный рак молочной железы
N 2-3 и/или Т4
+ отечные формы
Неоадъювантная терапия – как обязательный первый этап лечения,
а не возможная опцияЦель:
Уменьшение размеров опухоли и переведение в операбельное состояние
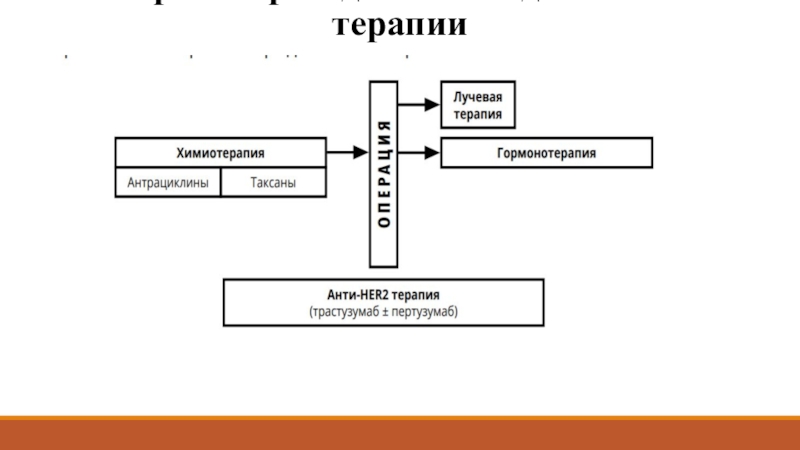
Слайд 40Адъювантная терапия
Алгоритм назначения адъювантной лекарственной терапии аналогичен таковому при первично
операбельном РМЖ:
• адъювантная ХТ, как правило, не назначается, если
все запланированные курсы проведены до операции • адъювантная гормонотерапия назначается всем больным с гормонозависимыми опухолями
• адъювантная анти-HER2 терапия назначается всем больным при HER2‑положительных опухолях: – больным, не получавшим неоадъювантную терапию, при N≥2 и отсутствии в опухоли РЭ и РП в качестве оптимального объёма лечения может быть рекомендована двойная анти-HER2 блокада трастузумабом и пертузумабом в течение 12 мес.
Слайд 41Метастатический РМЖ
Единого стандарта лечения метастатического РМЖ не существует
Выбор варианта лекарственной
терапии осуществляется с учётом:
биологических маркёров (РЭ и РП, HER2, Ki67)
клинико-анамнестических
особенностей больного включает химио- и / или гормонотерапию
анти-HER2 терапией по показаниям
Слайд 42Гормонотерапия метастатического рака молочной железы
Методом выбора терапии гормонозависимого (люминального) РМЖ
является ГТ даже при наличии висцеральных метастазов.
Исключение составляют:
•
быстропрогрессирующие варианты РМЖ, сопровождающиеся висцеральным кризом, в том числе развившимся в процессе предшествующих линий ГТ; • иные клинические ситуации, требующие максимально быстрого достижения противоопухолевого эффекта;
• гормонорезистентные случаи (неэффективность 3-х линий гормонотерапии)
Больным с сохранной функцией яичников рекомендуется выполнить овариальную супрессию любым доступным способом и назначить ГТ, рекомендованную больным в менопаузе.
Слайд 43Химиотерапия метастатического рака молочной железы
ХТ показана следующим категориям больных:
•
РМЖ с отрицательными РЭ и РП
• люминальный РМЖ, резистентный к ГТ
•
люминальный РМЖ с признаками висцерального кризаРекомендуется последовательное назначение химиопрепаратов в монотерапии. В качестве комбинированной терапии могут использоваться антрациклин-содержащие режимы, а также режимы, включающие платиновые производные.
Слайд 44ХТ с использованием одной и той же комбинации может продолжаться до прогрессирования
болезни, доказанного клинически и / или с помощью методов инструментальной диагностики, или неприемлемой / дозолимитирующей
токсичностиНе существует стандартных подходов к проведению второй и последующих линий ХТ, равно как и каких‑либо данных, свидетельствующих о преимуществах того или иного препарата или режима. Продолжение ХТ после третьей линии может обсуждаться для больных в удовлетворительном общем состоянии, ответивших на предшествующие линии ХТ.
Слайд 45Анти-HER2 терапия метастатического рака молочной железы
Больные HER2‑положительным РМЖ должны получать
анти-HER2‑терапию в сочетании с ХТ или ГТ.
При первом эпизоде прогрессирования на
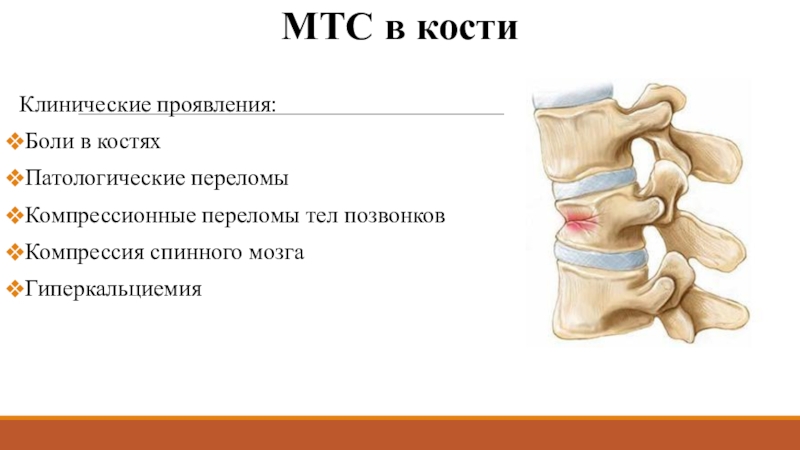
фоне терапии трастузумабом возможно продолжение лечения этим же препаратом со сменой химио- / гормонотерапевтического компонента. Слайд 46МТС в кости
Клинические проявления:
Боли в костях
Патологические переломы
Компрессионные переломы тел позвонков
Компрессия
спинного мозга
Гиперкальциемия
Слайд 47Лечение больных с МТС в кости
Эффективная лекарственная терапия основного заболевания
Применение
ОМА (бисфосфанаты, ингибиторы RANK- лигандов)
Применение лучевой терапии
Применение хирургических методов лечения
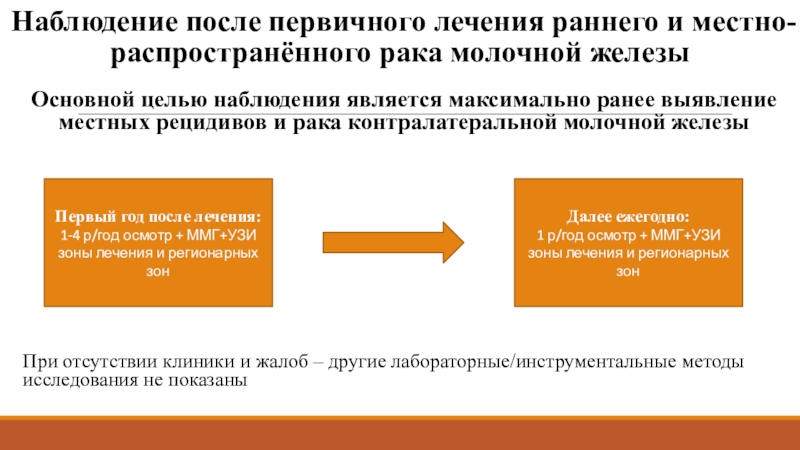
Слайд 48Наблюдение после первичного лечения раннего и местно-распространённого рака молочной железы
Основной
целью наблюдения является максимально ранее выявление местных рецидивов и рака контралатеральной
молочной железыПри отсутствии клиники и жалоб – другие лабораторные/инструментальные методы исследования не показаны
Первый год после лечения:
1-4 р/год осмотр + ММГ+УЗИ зоны лечения и регионарных зон
Далее ежегодно:
1 р/год осмотр + ММГ+УЗИ зоны лечения и регионарных зон
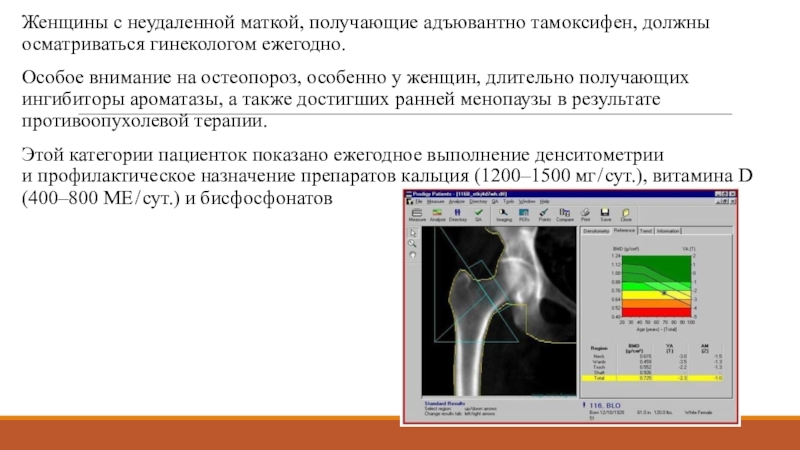
Слайд 49Женщины с неудаленной маткой, получающие адъювантно тамоксифен, должны осматриваться гинекологом ежегодно.
Особое внимание на остеопороз, особенно у женщин, длительно получающих ингибиторы ароматазы,
а также достигших ранней менопаузы в результате противоопухолевой терапии. Этой категории пациенток показано ежегодное выполнение денситометрии и профилактическое назначение препаратов кальция (1200–1500 мг / сут.), витамина D (400–800 МЕ / сут.) и бисфосфонатов