четырех стабильных изотопов:
32S , 33S , 34S , 36S
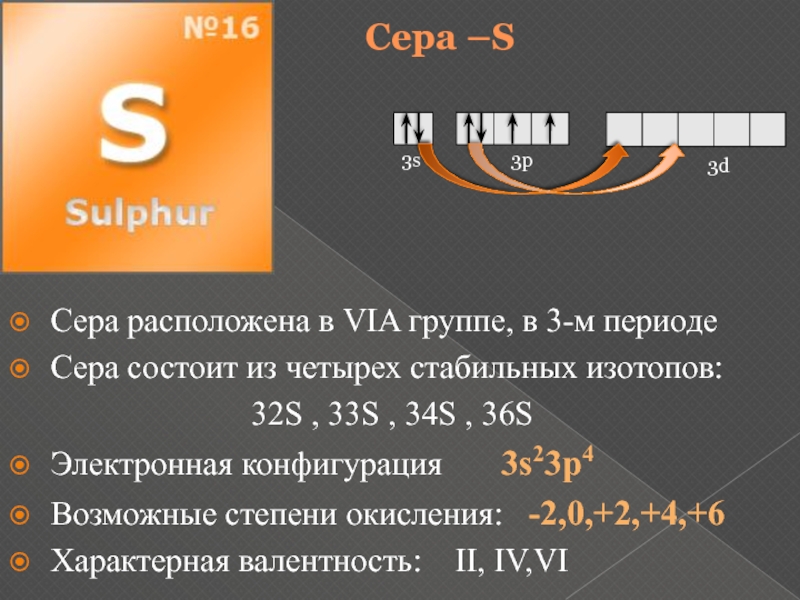
Электронная конфигурация 3s23p4
Возможные степени окисления: -2,0,+2,+4,+6
Характерная валентность: II, IV,VI
3s
3d
3p
Сера –S