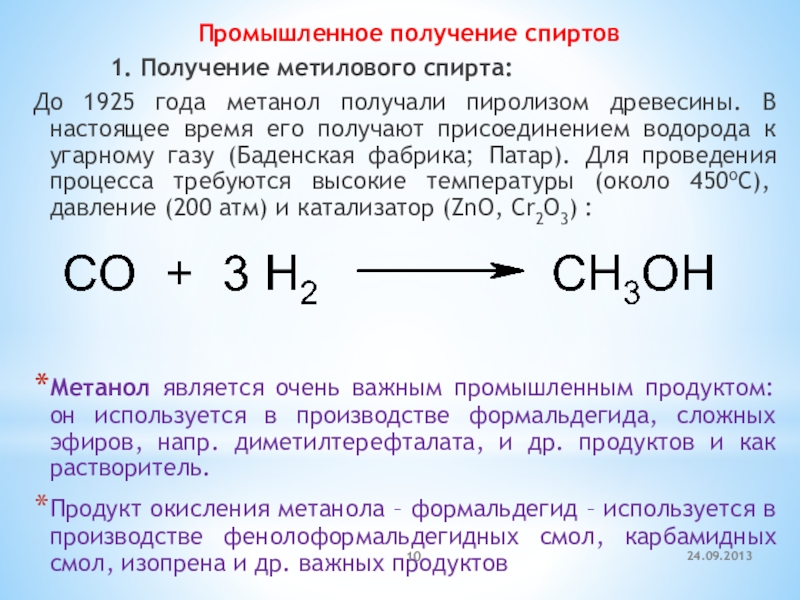
получали пиролизом древесины. В настоящее время его получают присоединением водорода
к угарному газу (Баденская фабрика; Патар). Для проведения процесса требуются высокие температуры (около 450оС), давление (200 атм) и катализатор (ZnO, Cr2O3) :Метанол является очень важным промышленным продуктом: он используется в производстве формальдегида, сложных эфиров, напр. диметилтерефталата, и др. продуктов и как растворитель.
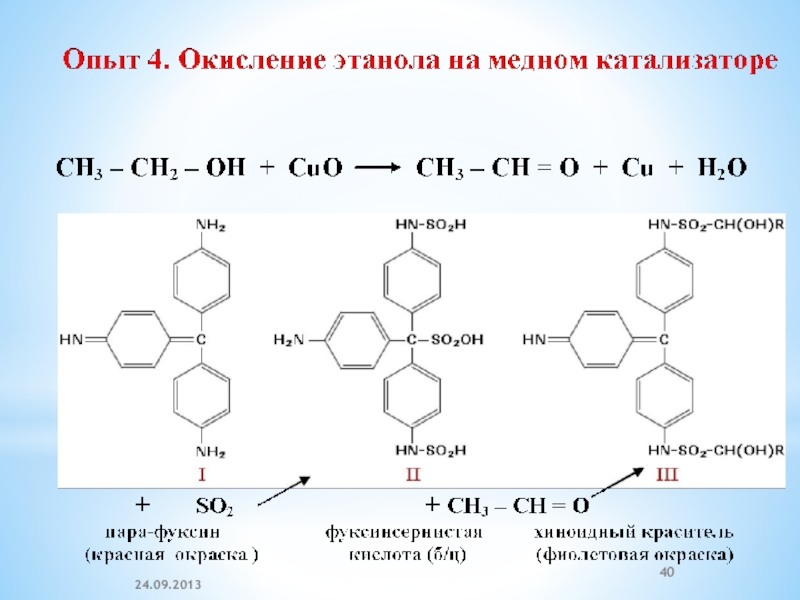
Продукт окисления метанола – формальдегид – используется в производстве фенолоформальдегидных смол, карбамидных смол, изопрена и др. важных продуктов