Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Тема: Принцип промышленного изготовления и биологического контроля биопрепаратов
Содержание
- 1. Тема: Принцип промышленного изготовления и биологического контроля биопрепаратов
- 2. Вакцины (лат. vaccinus коровий) -
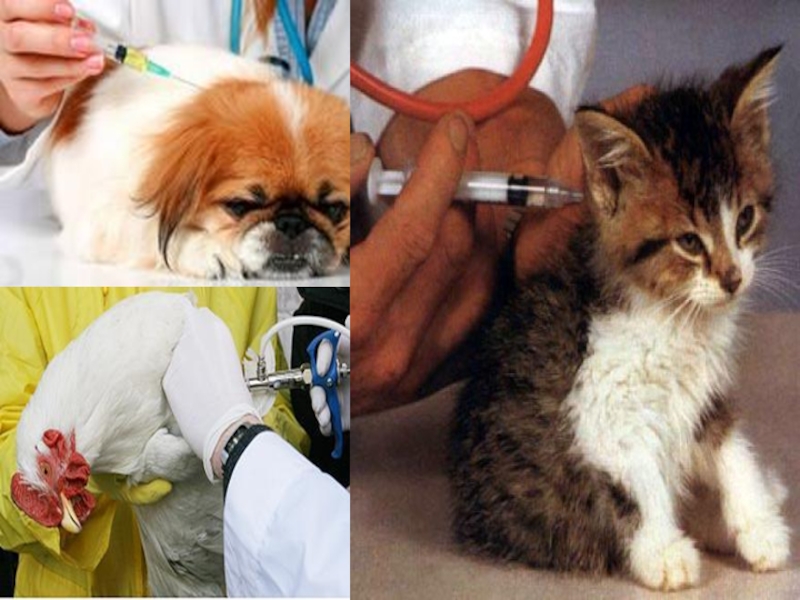
- 3. Вакцинопрофилактика занимает значительное место в борьбе с
- 4. Слайд 4
- 5. История появления вакцин Историю создания средств специфической
- 6. Первый период ознаменовался открытием живых вакцин Э.Дженнером
- 7. В 1884 году Л.С. Ценковский в России,
- 8. Второй период характеризуется изготовлением вакцин из убитых
- 9. В третий период (с 1930 года) в
- 10. Согласно современным международным требованиям штаммы, применяемые для
- 11. Классификация вакцин Различают следующие виды вакцин:Вакцина адсорбированная
- 12. Вакцина живая (v. vivum) - вакцина содержащая
- 13. Вакцина формалинизированная (v. formalinatum; син. формолвакцина) -
- 14. Слайд 14
- 15. Вакцины состоят из:действующего начала - специфического антигена;консерванта
- 16. В качестве антигенов при конструировании вакцин используют:живые
- 17. Слайд 17
- 18. В соответствии с природой специфического антигена вакцины
- 19. Неживые (убитые) вакцины подразделяют на молекулярные (химические)
- 20. Свойства вакцинОсновным свойством вакцин является создание активного
- 21. Эффективность применения вакцины определяется иммунологической реактивностью, зависящей
- 22. Получение вакцин Технология живых вакцин сводится к
- 23. Вирусные и риккетсиозные живые вакцины получают выращиванием
- 24. Инактивированные корпускулярные бактериальные вакцины или цельновирионные инактивированные
- 25. Производство молекулярных вакцин - сложный технологический процесс,
- 26. Слайд 26
- 27. Контроль вакцин Вакцины всех типов после приготовления
- 28. 3. В некоторых случаях об иммуногенности препарата
- 29. Слайд 29
- 30. Например, сухую живую вакцину против рожи свиней
- 31. Биологическая реакция на вакцину. Причины: Неполная аттенуация
- 32. Во время вакцинации животное инфицировано или инкубирует
- 33. ПРОРЫВ ВАКЦИННОГО ИММУНИТЕТА Явный прорыв иммунитета случается
- 34. Скачать презентанцию
Вакцины (лат. vaccinus коровий) - препараты, получаемые из микроорганизмов или продуктов их жизнедеятельности; применяются для активной иммунизации людей и животных с профилактической и лечебной целями.
Слайды и текст этой презентации
Слайд 1Тема: Принцип промышленного изготовления и биологического контроля биопрепаратов
Технология изготовления и
контроля
Слайд 2 Вакцины (лат. vaccinus коровий) - препараты, получаемые из
микроорганизмов или продуктов их жизнедеятельности; применяются для активной иммунизации людей
и животных с профилактической и лечебной целями.Слайд 3Вакцинопрофилактика занимает значительное место в борьбе с инфекционными болезнями: ликвидирована
оспа, сведена к минимуму заболеваемость полиомиелитом, дифтерией, резко снижена заболеваемость
корью, коклюшем, сибирской язвой, туляремией и другими инфекционными болезнями.Успехи вакцинопрофилактики зависят от качества вакцин и своевременного охвата угрожаемых контингентов. Большие задачи стоят по совершенствованию вакцины против гриппа, бешенства, кишечных инфекций, по разработке вакцин против сапа, мелиоидоза.
Современные иммунология и вакцинопрофилактика подвели теоретическую базу и наметили пути совершенствования вакцин в направлении создания очищенных поливалентных адъювантных синтетических вакцин и получения новых безвредных эффективных живых рекомбинантных вакцин.
Слайд 5История появления вакцин
Историю создания средств специфической профилактики можно разделить на
три периода:
1. Бессознательные попытки на заре научной медицины искусственно заражать
здоровых людей и животных выделениями от больных с легкой формой заболевания.2. Создание большого количества вакцин из убитых бактерий.
3. Создание и применение живых, убитых, субъединичных вакцин.
Слайд 6Первый период ознаменовался открытием живых вакцин Э.Дженнером (1796) и Л.
Пастером (1880). Главным было искусственное заражение с последующим переболеванием.
Вакцина
Дженнера против оспы, вакцины Пастера против холеры кур (1880), сибирской язвы (1880-1883), рожи свиней (1882-1883), бешенства (1-S81-1886) содержали живых возбудителей болезни, ослабленных различными методами:возбудитель холеры кур - длительным хранением культур в бульоне,
воздействием на возбудителя сибирской язвы повышенной температурой (42,5 °С),
пассажем возбудителя рожи через организм голубей и кроликов, пассированием вируса бешенства через организм кроликов.
Слайд 7В 1884 году Л.С. Ценковский в России, используя принцип аттенуации
(ослабления) по Пастеру, приготовил свои вакцины против сибирской язвы.
В
1908 году Велл и Лекланше получили вакцину против эмкара из культур возбудителя, выращенных при 43-44° С, или культуры, выращенные в средах со специфической сывороткой. Подобные живые вакцины были получены против холеры людей (Хавкин В., 1890-1896; Николь, 1912).
В 1897 году Р. Кох в практику профилактических прививок против чумы крупного рогатого скота предложил живой вирус из желчи убитых, больных или павших от чумы животных. Эти прививки давали отход до 30%.
Вскоре Ненцкий, Забер и Выжникевич заменили их «симультанными» прививками, то есть одновременным введением с живым вирусом специфической сыворотки.
Слайд 8Второй период характеризуется изготовлением вакцин из убитых бактерий и открытием
большого количества возбудителей заболеваний. 1898 год дал богатые плоды для
медицины и ветеринарии в создании корпускулярных вакцин.В разработке живых вакцин этот период сыграл печальную роль. Он задержал их развитие более чем на 20 лет. Но в то же время в этот период бытовало мнение о недостаточной эффективности убитых вакцин. Ученые не оставляли поисков все новых и новых живых вакцин, как наиболее эффективных и экономичных профилактических препаратов.
Слайд 9В третий период (с 1930 года) в равной мере получили
развитие живые, убитые и так называемые химические вакцины из очищенных
антигенов, третий период характеризуется развитием обоих направлений.Способы улучшения убитых вакцин были связаны с применением различных физических и химических агентов для обезвреживания микробов, подбором штаммов с полноценными антигенами, введение «щадящих» режимов инактивации культур микробов, использованием очищенных, так называемых протективных, антигенов (химических вакцин). Уделялось немало работ вопросам «депонирования» убитых и химических вакцин, методам их аппликации, кратностям, интервалам, дозам введения, проблеме ревакцинаций.
Слайд 10Согласно современным международным требованиям штаммы, применяемые для изготовления живых вакцин,
должны иметь генетические маркеры, позволяющие отличить их от полевых штаммов.
Они должны обладать постоянством (константность) своих биологических свойств, слабой остаточной вирулентностью и обеспечивать невосприимчивость к инфекции большинства животных при однократном применении вакцины.В технологическом процессе вакцинного производства важны все звенья: от подбора производственных штаммов и питательной среды до конечных этапов - стандартизации и расфасовки биопрепаратов.
Слайд 11Классификация вакцин
Различают следующие виды вакцин:
Вакцина адсорбированная (v. adsorptum) - вакцины,
антигены которой сорбированы на веществах, усиливающих и пролонгирующих антигенное раздражение.
Вакцина
антирабическая (v. antirabicum; анти- + лат. rabies бешенство) - вакцина, изготовленная из штамма фиксированного вируса бешенства в суспензии тканей головного мозга животных или в культуре клеток и предназначенная для предупреждения заболевания у лиц, укушенных животными, больными бешенством (подозреваемыми на заболевание).Вакцина ассоциированная (v. associatum) - препарат, состоящий из нескольких вакцин различного типа, предназначенный для одновременной иммунизации против нескольких инфекционных болезней.
Слайд 12Вакцина живая (v. vivum) - вакцина содержащая жизнеспособные штаммы патогенного
микроорганизма, ослабленные до степени, исключающей возникновение заболевания, но полностью сохранившие
антигенные свойства, обусловливающие формирование специфического иммунитета у привитого.Вакцина поливалентная (v. polyvalens; греч. poly - много + лат. valens, valentis сильный) - вакцина, изготовленная на основе нескольких серологических вариантов возбудителя одной инфекционной болезни.
Вакцина убитая (v. inactivatum) - вакцина, изготовленная из микроорганизмов инактивированных (убитых) воздействием физических или химических факторов.
Вакцина фенолизированная (v. phenolatum) - убитая вакцина, изготовленная из микроорганизмов, инактивированных фенолом.
Слайд 13Вакцина формалинизированная (v. formalinatum; син. формолвакцина) - убитая вакцина, изготовленная
из микроорганизмов, инактивированных формалином.
Вакцина химическая (v. chemicum) - вакцина, состоящая
из специфических антигенов, извлеченных из микроорганизмов, и очищенная от балластных веществ.Вакцина эмбриональная (v. embryonale) - вакцина, изготовленная из вирусов или риккетсий, выращенных на эмбрионах птиц (кур, перепелок).
Вакцина этеризованная (v. aetherisatum) - убитая вакцина, изготовленная из микроорганизмов, инактивированных эфиром.
Слайд 15Вакцины состоят из:
действующего начала - специфического антигена;
консерванта для сохранения стерильности
(в неживых вакцинах); стабилизатора, или протектора, для повышения сроков сохраняемости
антигена;неспецифического активатора (адъюванта), или полимерного носителя, для повышения иммуногенности антигена (в химических, молекулярных вакцинах).
Специфические антигены, содержащиеся в вакцине, в ответ на введение в организм вызывают развитие иммунологических реакций, обеспечивающих устойчивость организма к патогенным микроорганизмам.
Слайд 16В качестве антигенов при конструировании вакцин используют:
живые ослабленные (аттенуированные) микроорганизмы;
неживые
(инактивированные, убитые) цельные микробные клетки или вирусные частицы;
извлеченные из
микроорганизмов сложные антигенные структуры (протективные антигены); продукты жизнедеятельности микроорганизмов - вторичные метаболиты (например, токсины, молекулярные протективные антигены);
антигены, полученные путем химического синтеза или биосинтеза с применением методов генетической инженерии.
Слайд 18В соответствии с природой специфического антигена вакцины делят на живые,
неживые и комбинированные
Живые вакцин получают из дивергентных (естественных) штаммов микроорганизмов,
обладающих ослабленной вирулентностью, но содержащих полноценный набор антигенов, и из искусственных (аттенуированных) штаммов микроорганизмов.К живым вакцинам отнесят также векторные вакцины, полученные генно-инженерным способом и представляющие собой вакцинный штамм, несущий ген чужеродного антигена.
Слайд 19Неживые (убитые) вакцины подразделяют на молекулярные (химические) и корпускулярные.
Молекулярные
вакцины конструируют на основе специфических протективных антигенов, находящихся в молекулярном
виде и полученных путем биосинтеза или химического синтеза. К ним относят анатоксины-обезвреженные формалином молекулы токсинов, образуемых микробной клеткой (столбнячный, ботулинический и др.).Корпускулярные вакцины получают из цельных микроорганизмов, инактивированных физическими (тепло, ультрафиолетовое и др. излучения) или химическими (фенол, спирт) методами (корпускулярные, вирусные и бактериальные вакцины), или из субклеточных надмолекулярных антигенных структур, извлеченных из микроорганизмов (субвирионные вакцины, сплит-вакцины, вакцины из сложных антигенных комплексов).
Слайд 20Свойства вакцин
Основным свойством вакцин является создание активного поствакцинального иммунитета, который
по своему характеру и конечному эффекту соответствует постинфекционному иммунитету, иногда
отличаясь от него лишь количественно.Вакцинальный процесс при введении живых вакцин сводится к размножению и генерализации аттенуированного штамма в организме.
Вакцины при введении в организм вызывают ответную иммунную реакцию, которая в зависимости от природы иммунитета и свойств антигена может носить выраженный гуморальный, клеточный или клеточно-гуморальный характер.
Слайд 21Эффективность применения вакцины определяется иммунологической реактивностью, зависящей от генетических и
фенотипических особенностей организма, от качества антигена, дозы, кратности и интервала
между прививками. Поэтому для каждой вакцины разрабатывают схему вакцинации.Живые вакцины обычно используют однократно, неживые - чаще двукратно.
В зависимости от способа применения вакцины делят на инъекционные, пероральные и ингаляционные.
В соответствии с этим им придается соответствующая лекарственная форма: для инъекций применяют исходные жидкие или регидратированные из сухого состояния вакцины; пероральные - в виде таблеток, драже или капсул; для ингаляций используют сухие (пылевые или регидратированные) вакцины.
Слайд 22Получение вакцин
Технология живых вакцин сводится к выращиванию аттенуированного вакцинного
штамма с соблюдением условий, обеспечивающих получение чистых культур штамма, исключение
возможностей загрязнения другими микроорганизмами (микоплазы, аденовирусы) с последующей стабилизацией и стандартизацией конечного препарата.Вакцинные штаммы бактерий выращивают на жидких питательных средах (гидролизаты казеина или другие белково-углеводные среды) в аппаратах - ферментаторах емкостью от 0,1 м3 до 1-2 м3.
Полученная чистая культура вакцинного штамма подвергается лиофильному высушиванию с добавлением протекторов.
Слайд 23Вирусные и риккетсиозные живые вакцины получают выращиванием вакцинного штамма в
эмбрионах кур или перепелов, свободных от вирусов лейкоза, либо в
культурах клеток, лишенных микоплазм.Используют или первично-трипсинизированные клетки животных или перевиваемые диплоидные клетки человека.
Живые аттенуированные штаммы бактерий и вирусов, применяемые для приготовления живых вакцин, получены, из природных штаммов путем их селекции или пассажей через биологические системы (организм животных, эмбрионы кур, культуры клеток, питательные среды).
Слайд 24Инактивированные корпускулярные бактериальные вакцины или цельновирионные инактивированные вакцины получают соответственно
из культур бактерий и вирусов, выращенных на тех же средах
накопления, что и в случаях получения живых вакцин, и затем подвергнутых инактивации:нагреванием (гретые вакцины),
формалином (формолвакцины),
ультрафиолетовым излучением (УФ-вакцины),
ионизирующим излучением (радиовакцины),
спиртом (спиртовые вакцины).
Инактивированные вакцины имеют свойство недостаточно высокой иммуногенности и повышенной реактогенности.
Слайд 25Производство молекулярных вакцин - сложный технологический процесс, требует извлечения из
выращенной микробной массы протективных антигенов или антигенных комплексов, очистки и
концентрирования антигенов, введения в препараты адъювантов. Выделение и очистка антигенов с помощью традиционных методов (экстракции трихлоруксусной кислотой, кислотного или щелочного гидролиза, ферментативного гидролиза, высаливания нейтральными солями, осаждения спиртом или ацетоном) сочетаются с применением современных методов (скоростного ультрацентрифугирования, мембранной ультрафильтрации, хроматографического разделения, аффинной хроматографии, в т.ч. на моноклональных антителах). С помощью этих приемов удается получать антигены высокой степени очистки и концентрирования.Слайд 27Контроль вакцин
Вакцины всех типов после приготовления проверяют по следующим
параметрам.
Стерильность (инактивированные) или чистоту роста (живые) контролируют посевом на питательные
среды.Безвредность проверяют введением вакцины лабораторным животным. Вакцина не должна вызывать заболевание и гибель животных.
Активность (иммуногенность) контролируют следующим образом: вакцину вводят группе лабораторных животных, и через промежуток времени, достаточный для выработки активного иммунитета (15...20сут), эту группу вместе с контрольной группой непривитых животных заражают заведомо летальной дозой возбудителя. Контрольные животные должны погибнуть, 80 % и более вакцинированных должны выжить.
Слайд 283. В некоторых случаях об иммуногенности препарата судят по косвенным
показателям: количеству агглютининов у привитых животных (лептоспирозная вакцина), антитоксинов в
РН (вакцина против ботулизма).4. Реактогенность, т.е. побочные местные и общие реакции на введение вакцины, оценивают на животных и при прививках людей.
5. Пирогенность - это способность вещества вызывать повышение температуры тела.
Слайд 30Например, сухую живую вакцину против рожи свиней ВГНКИ из штамма
ВР-2 контролируют следующим образом.
Для контроля чистоты сухую (лиофилизированную) вакцину разводят
стерильным физиологическим раствором в соотношении 1: 10. Из суспензии бактерий готовят мазки, красят по Граму, микроскопируют. В препарате должны быть типичные мелкие грамположительные палочковидные клетки при отсутствии посторонних микроорганизмов. Одновременно проводят высевы на МПА, МПБ, среду Китта—Тароцци и агар Сабуро. Посевы выдерживают при 37...38°С 10 сут, посевы на грибы —при 20...25°С 15сут. Рост посторонней микрофлоры в указанные сроки на всех питательных средах должен отсутствовать при наличии типичного роста на МПА и в МПБ культуры возбудителя рожи.С целью контроля вакцины на безвредность и активность 20 белым мышам массой 17... 18 г вводят подкожно 0,2 мл препарата. Вакцину считают безвредной, если погибает не более 5 мышей. Через 14 дней всех оставшихся в живых вакцинированных и пять контрольных мышей заражают культурой вирулентного штамма возбудителя рожи свиней в заведомо летальной дозе. Вакцину признают активной, если погибают в течение трех-четырех суток контрольные и выживает не менее 75 % вакцинированных мышей.
Слайд 31Биологическая реакция на вакцину.
Причины:
Неполная аттенуация вирусного или
бактериального компонента. Встречается редко, но это известное явление, о котором
необходимо сообщить производителю вакцины.Встречаются животные, особо восприимчивые к инфекции аттенуированным патогеном. Например, живая вакцина введена очень маленькому щенку или котенку или иммуносупрессивной особи, которая недавно перенесла иммуноподавляющее заболевание (лейкемия кошек, чума собак и т.д.).
Вакцина введена неправильным путем. Живая вакцина "кошачьего гриппа", аттенуированная для подкожного введения, часто вызывает инфекцию при интраназальном введении (кошка лижет место инъекции или нечаянно вдохнула жидкость из полного шприца).
Слайд 32Во время вакцинации животное инфицировано или инкубирует инфекцию.
Животное является
носителем клинически скрытой инфекции. Стресс вакцинации может вызвать выделение патогена
и развитие клинических симптомов, например, кошка с латентной инфекцией герпесвирусом-1.Обычно живые вакцины могут провоцировать легкие клинические симптомы. Подкожное введение живой вакцины часто дает начало легким системным клиническим симптомам, таким как депрессия, летаргия и отсутствие аппетита, которые продолжаются около суток. Интраназальная вакцина часто вызывает легкие симптомы респираторного заболевания — чихание и иногда незначительные выделения из глаз и носа.
Слайд 33ПРОРЫВ ВАКЦИННОГО ИММУНИТЕТА
Явный прорыв иммунитета случается через несколько недель
или более после вакцинации, но в период предполагаемого иммунитета. Возможные
причины:Испорченная вакцина. Неправильное хранение вакцины. Не использовать вакцины после истечения срока хранения и хранить в соответствии с инструкциями производителя.
Неправильное назначение вакцины. Чаще всего это бывает результатом инъекции неправильной дозы вакцины. Введение вакцины неправильным путем (например, интраназальная вакцина вводится подкожно или убитая системная вакина дается ороназально) также неээфективно при развитии иммунитета.
Животное уже инфицировано. Вакцинация носителя вируса (например, калицивируса кошек или полевого герпесвируса-1) может вызвать персистирующую инфекцию, но не дает элиминации вируса, а животное может впоследствие выделять вирус и даже развить клиническое заболевание.