Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Температурная зависимость скорости химической реакции 1. Правило Вант-Гоффа
Содержание
- 1. Температурная зависимость скорости химической реакции 1. Правило Вант-Гоффа
- 2. Некоторая аналогия с распределением Больцмана – итоги сессии за разные семестрыУравнение Аррениуса: k = Be-Ea/RT
- 3. Температурная зависимость скорости химической реакции1. Правило Вант-Гоффа
- 4. Теория активных столкновенийВ теории активных столкновений считается,
- 5. Теория активированного комплекса (АК) или теория переходного
- 6. Слайд 6
- 7. Поверхность потенциальной энергии для взаимодействия H2 +
- 8. Поверхность потенциальной энергии для взаимодействия H2 + F = HF + H (2D – модель) rH-HrH-F
- 9. Для простейших случаев (для мономолекулярной реакции)(3) Смысл
- 10. Энергетическая диаграмма реакции A + B =
- 11. Реакции, происходящие на границе раздела фаз, называются
- 12. В общем случае адсорбцией называется повышение концентрации
- 13. Адсорбция может быть физической или химической. Химическую
- 14. P.S.: Давайте различать:Абсорбция (лат. absorptio - поглощение,
- 15. Некоторые отличия цепных и каталитических реакций: 1.
- 16. Скачать презентанцию
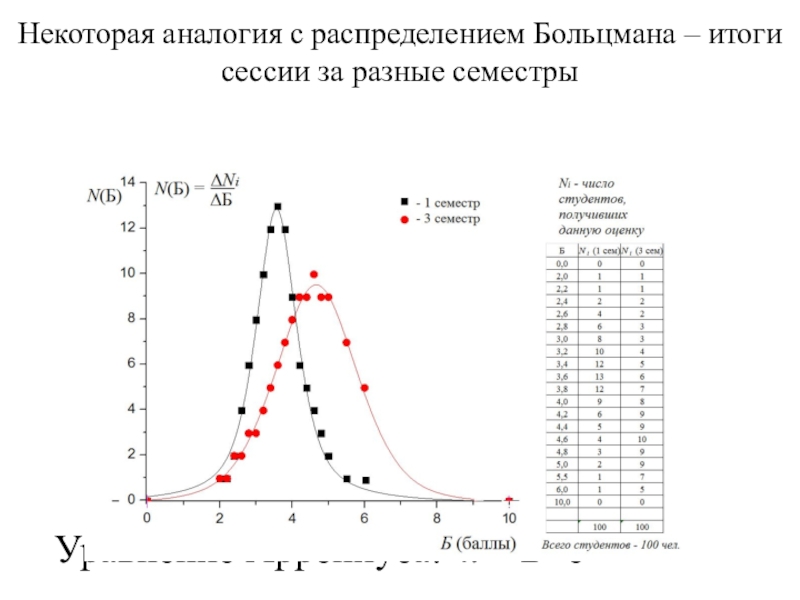
Некоторая аналогия с распределением Больцмана – итоги сессии за разные семестрыУравнение Аррениуса: k = Be-Ea/RT
Слайды и текст этой презентации
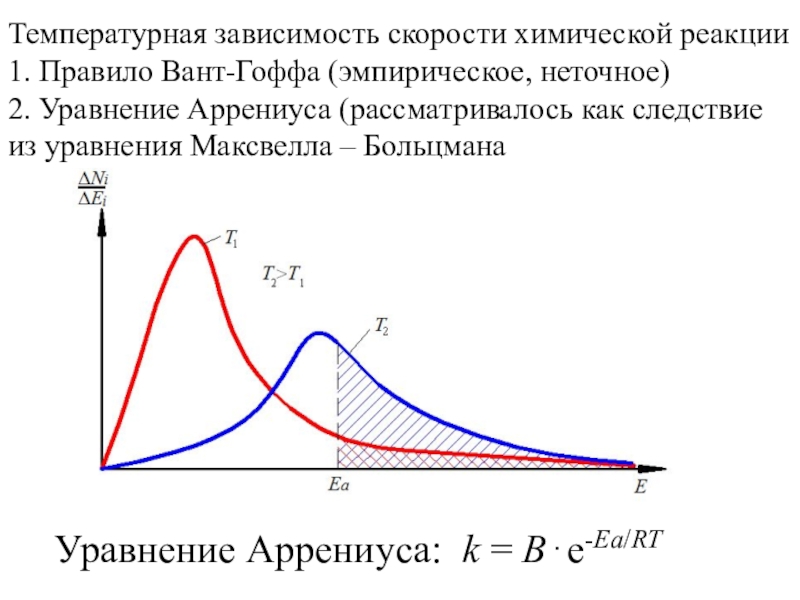
Слайд 1Температурная зависимость скорости химической реакции
1. Правило Вант-Гоффа (эмпирическое, неточное)
2. Уравнение
Аррениуса (рассматривалось как следствие из уравнения Максвелла – Больцмана
k = Be-Ea/RTСлайд 2Некоторая аналогия с распределением Больцмана – итоги сессии за разные
семестры
Уравнение Аррениуса: k = Be-Ea/RT
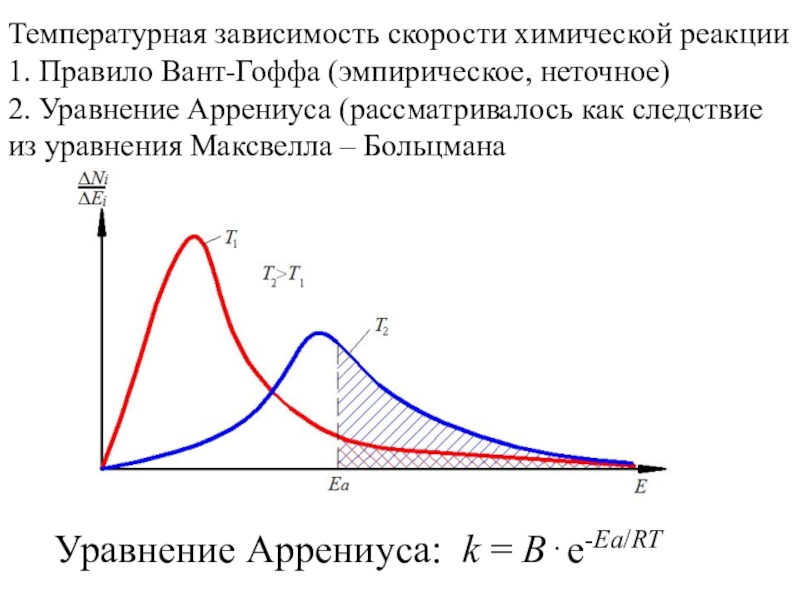
Слайд 3Температурная зависимость скорости химической реакции
1. Правило Вант-Гоффа (эмпирическое, неточное)
2. Уравнение
Аррениуса (рассматривалось как следствие из уравнения Максвелла – Больцмана
Уравнение Аррениуса:
k = Be-Ea/RTСлайд 4Теория активных столкновений
В теории активных столкновений считается, что акт превращения
начальных веществ в конечные продукты совершается в момент столкновения активных
молекул и протекает мгновенно. При этом молекулы рассматриваются как бесструктурные частицы.(1) (2)
Слайд 5Теория активированного комплекса (АК) или теория переходного состояния. Основные положения.
1.
Превращение проходит через образование АК – неустойчивую молекулу, отличающуюся по
своему строению от конечных и исходных веществ, и существующую на некотором интервале пространства. Образование АК связано с преодолением энергетического барьера, т.е. АК находится на вершине этого барьера и имеет энергию, равную активации.2. Активированный комплекс находится в равновесии с исходными веществами: A + B ↔ AB#
3. Каждый активированный комплекс переходит в продукты с равными вероятностями перехода АК в прямом и обратном направлениях. Полагают, что половина квазимолекул АК движется в направлении продуктов и половина – в сторону реагентов.
4. Скорость реакции равна скорости распада комплекса, концентрация которого мала. Теория позволяет рассчитывать константу скорости отдельной стадии, а не всего процесса, т.к. АК может быть несколько.
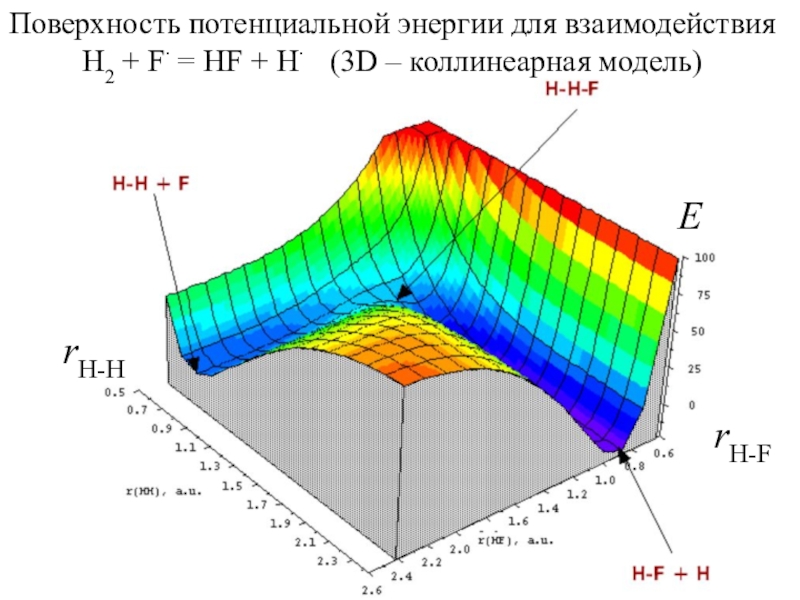
Слайд 7Поверхность потенциальной энергии для взаимодействия H2 + F = HF
+ H (3D – коллинеарная модель)
rH-H
rH-F
E
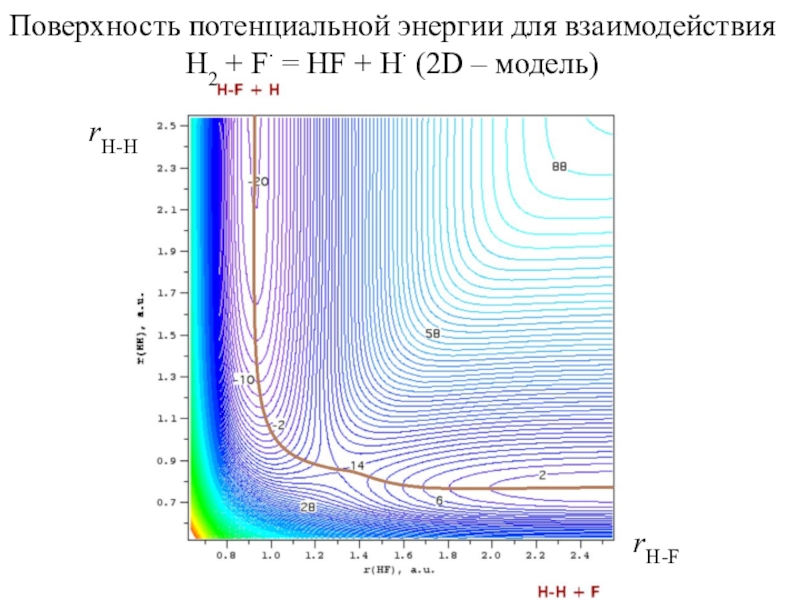
Слайд 8Поверхность потенциальной энергии для взаимодействия H2 + F = HF
+ H (2D – модель)
rH-H
rH-F
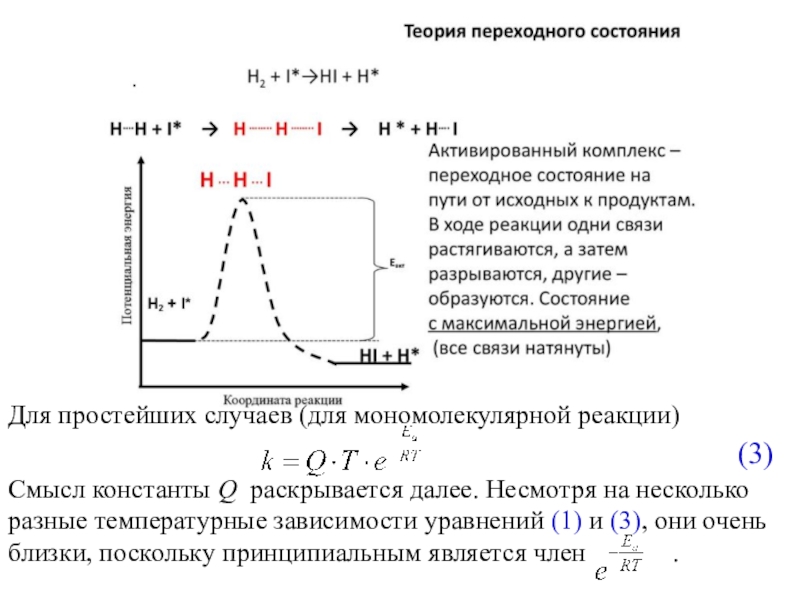
Слайд 9Для простейших случаев (для мономолекулярной реакции)
(3)
Смысл константы Q раскрывается
далее. Несмотря на несколько разные температурные зависимости уравнений (1) и
(3), они очень близки, поскольку принципиальным является член .Слайд 10Энергетическая диаграмма реакции
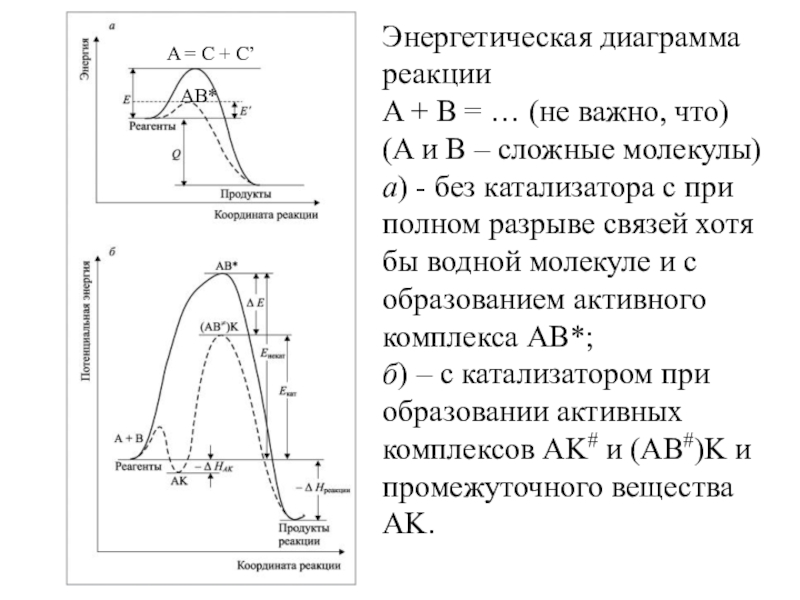
A + B = … (не важно,
что)
(A и B – сложные молекулы)
а) - без катализатора с
при полном разрыве связей хотя бы водной молекуле и с образованием активного комплекса AB*;б) – с катализатором при образовании активных комплексов AK# и (AB#)K и промежуточного вещества AK.
AB*
A = C + C’
Слайд 11Реакции, происходящие на границе раздела фаз, называются гетерогенными
В гетерогенной
реакции всегда есть следующие стадии:
доставка вещества к границе раздела фаз
(диффузия);адсорбция (хемосорбция);
реакция;
десорбция;
удаление продуктов от границы реакции (диффузия продуктов).
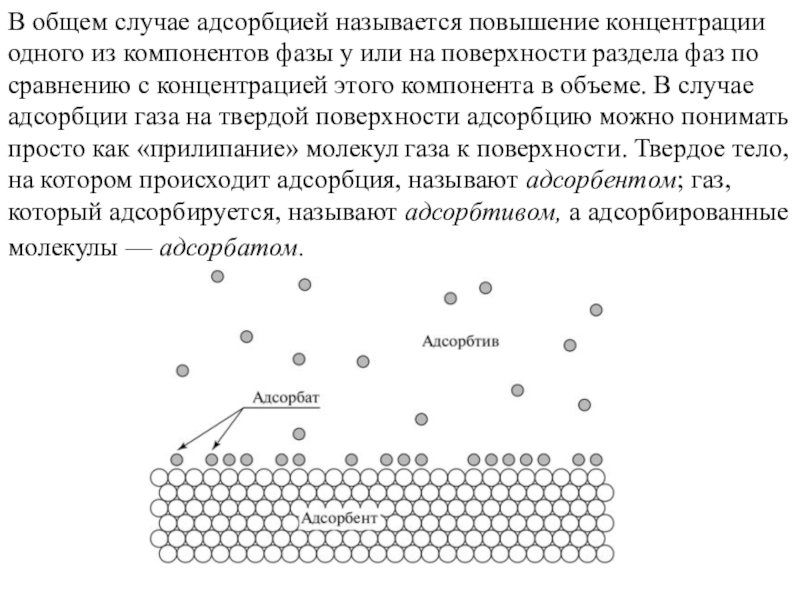
Слайд 12В общем случае адсорбцией называется повышение концентрации одного из компонентов
фазы у или на поверхности раздела фаз по сравнению с
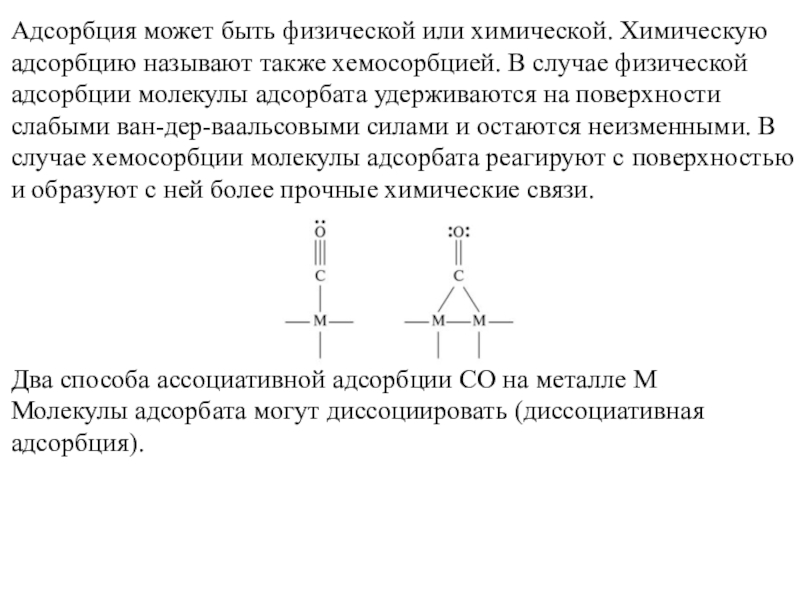
концентрацией этого компонента в объеме. В случае адсорбции газа на твердой поверхности адсорбцию можно понимать просто как «прилипание» молекул газа к поверхности. Твердое тело, на котором происходит адсорбция, называют адсорбентом; газ, который адсорбируется, называют адсорбтивом, а адсорбированные молекулы — адсорбатом.Слайд 13Адсорбция может быть физической или химической. Химическую адсорбцию называют также
хемосорбцией. В случае физической адсорбции молекулы адсорбата удерживаются на поверхности
слабыми ван-дер-ваальсовыми силами и остаются неизменными. В случае хемосорбции молекулы адсорбата реагируют с поверхностью и образуют с ней более прочные химические связи.Два способа ассоциативной адсорбции СО на металле М
Молекулы адсорбата могут диссоциировать (диссоциативная адсорбция).
Слайд 14P.S.: Давайте различать:
Абсорбция (лат. absorptio - поглощение, от absorbeo -
поглощаю), поглощение веществ из газовой смеси жидкостями.
Адсорбция (от лат. ad
- на, при и sorbeo - поглощаю), поглощение вещества из газообразной среды или раствора поверхностным слоем жидкости или твёрдого тела.Слайд 15Некоторые отличия цепных и каталитических реакций:
1. Измененная компонентность системы,
в продукты компонент «К» не входит (кроме автокатализа).
2. Нет стадии
зарождения цепи.3. В катализе обрыв цепи обычно не происходит.
4. В катализе реакционный путь не требует полного разрыва связей.
4. Скорость реакции цепной реакции всегда меньше скорости образования радикалов.
5. Катализ – это разбиение реакции на последовательность реакций, каждая из которых имеет меньший тепловой эффект, чем суммарная реакция (Н.И.Кобозев).
Некоторые аналогии: - циклический характер, наличие активных частиц.