Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Трансплантация гемопоэтических стволовых клеток (ГСКК ) при
Содержание
- 1. Трансплантация гемопоэтических стволовых клеток (ГСКК ) при
- 2. 1949г: Якобсон и коллеги обнаруживают, что интрапеританиальное
- 3. 1955г: данные о котрансплантации костного мозга и
- 4. 1968г – первая удачная трансплантация у
- 5. 50.000- трансплантаций ежегодно в мире 1.000.000 зарегистрировано в 2014 году
- 6. Слайд 6
- 7. Трансплантация гемопоэтических стволовых клеток - этап лечения
- 8. TBI
- 9. Виды трансплантации в зависимости от источника
- 10. Основные свойства гемопоэтической ткани«Хоуминг», или способность кроветворных
- 11. Преимущества и недостаткиАутологичная ТКМОтсутствие иммунологических осложненийУвеличение частоты
- 12. Получение стволовых клеток периферической кровиГ-КСФ 10 мкг/кг/сут
- 13. Основные принципы выполнения трансплантации аллогенных гемопоэтических клетокПолная
- 14. Возраст и соматический статус пациента Адекватность химиотерапии
- 15. Схема аллогенной ТКМКостный мозг реципиентахимиотерапияЦитопенияСмешанныйхимеризм Полный донорский химеризмКостный мозг донора
- 16. Клеточность костного мозга в процессе лечения Нормальныйкостный мозгОпухольАплазияХимиотерапияВосстановление
- 17. Эффективность аллогенной ТКМЦиторедуктивное воздействие (ТОТ + циклофосфан,
- 18. Проблемы трансплантации аллогенных гемопоэтических клетокТоксичность режимов
- 19. Острая РТПХ
- 20. Факторы риска РТПХСо стороны донора- HLA- различияРасхождение
- 21. Слайд 21
- 22. Острая РТПХКишечникПеченьКожа
- 23. Слайд 23
- 24. Слайд 24
- 25. Эксфузия костного мозга
- 26. Слайд 26
- 27. Слайд 27
- 28. Вопросы ?
- 29. Основные показания к трансплантации аутологичных
- 30. Показания к трансплантации аллогенного костного мозга при
- 31. Показания к трансплантации аллогенного костного мозгаОЛЛ –
- 32. Показания к трансплантации аллогенного костного мозгаХМЛ 1.
- 33. Острыемиелоидные лейкозы – основное показаниеАллогенная ТСКК в Европев 2011 году
- 34. Российский Межрегиональный регистр 2003-2012: Аллогенные трансплантацииМенделеева Л.П.
- 35. Трансплантация аллогенных гемопоэтических клеток при ОЛ
- 36. Трансплантация костного мозга при острых миелоидных
- 37. Классификация РИСКОВ (клинико-лабораторные параметры, химиочувствительность, молекулярно-генетические
- 38. Эффективность лечения ОМЛ в зависимости от
- 39. Общая выживаемость больных ОМЛ по итогам 4-х
- 40. Общая и безрецидивная выживаемость в зависимости от возраста ( 40 лет)16-40 лет16-40 лет40-60 лет40-60 летОМЛ 01-10
- 41. HSCT in 46%HSCT in 22%Gunnar Juliusson et
- 42. 2002-2013 = 58,8%1989-2001 = 29,5%р
- 43. Межрегиональный трансплантационный регистр РФ (данные за 2011
- 44. Показания к трансплантации аллогенного костного мозга при
- 45. Значение аллогенной трансплантации у взрослых пациентов
- 46. Годы после ТГСКОбщая выживаемость для пациентов ОЛЛ
- 47. Выживаемость пациентов ОЛЛ после алло-ТКМ2002-2013 = 79,5%1989-2001 = 57,1%месГНЦ МЗ РФ
- 48. Трансплантация аутологичных гемопоэтических клеток при ОЛЛ
- 49. Значение аутологичной ТГСК при ОЛЛ у взрослыхEORTCB.
- 50. D.Hoelzer et al Blood (ASH) 2009 114:
- 51. T-клеточный ОЛЛ – аутологичная ТГСК (кондиционирование
- 52. RALL study group protocolClinicalTrials.gov NCT01193933Аллогенная ТГСК -
- 53. Характеристика больных при диагностике заболевания (группа ауто-ТГСК)Всего
- 54. АУТО-ТГСКВремя от достижения ремиссии до ауто -ТГСК
- 55. Длительность агранулоцитоза медиана
- 56. Результаты АУТО- TГСК Начало поддерживающей
- 57. Выживаемость без признаков прогрессии: ауто-ТГСК vs ПХТАуто-ТГСКПХТ
- 58. Вероятность рецидива ОЛЛ: ауто-ТГСК vs ПХТПХТАуто-ТГСК
- 59. Трансплантация гемопоэтических клеток- этап терапии многих онкогематологических
- 60. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Трансплантация гемопоэтических стволовых клеток (ГСКК) при онкогематологических заболеваниях у взрослых
Кузьмина
Л.А.
Слайд 21949г: Якобсон и коллеги обнаруживают, что интрапеританиальное введение клеток селезенки
может спасти мышей при летальном облучении
1940г
1960г
1954г: Барнс выполняет мышам сингенную
трансплантацию, продолжительность жизни более 100 дней. Мыши, получившие аллогенный костный мозг выживают в течение 30 дней, но умирают от «вторичной болезни».Слайд 31955г: данные о котрансплантации костного мозга и кожного лоскута у
мышей - впервые вводится слово «толерантность»
1956г: Barnes публикует результаты опытов
по трансплантации у мышей больных лейкозомВ это же время D. Тhomas проводит 6 терминальным пациентам трансплантацию от здоровых доноров после TBI – лишь у одного получено временное приживление
1959 год – D. Тhomas получает приживление костного мозга у пациента после сингенной трансплантации с резистентным лейкозом после облучения 800 рад
Аутологичные трансплантации при лимфомах
1979год - первая трансплантация аллогенного костного мозга с тотальным облучением в 1000 рад в нашей клинике….
1950г
1960г
Слайд 41968г – первая удачная трансплантация у ребенка с иммунодефицитом
( Университет Миннесоты)
1969г – Эдвард Доннел Томас получает грант на
исследование1990г - Нобелевская премия за открытия, касающиеся “органной и клеточной трансплантации”
Слайд 7Трансплантация гемопоэтических стволовых клеток - этап лечения онкогематологических заболеваний
Режимы
кондиционирования
Миелоаблативные
Пониженной интенсивности
Гемопоэтические стволовые клетки
Костный мозг 3х108/кг
Стволовые клетки крови
2 - 5х106/кг CD 34+
Пуповинные клетки 2,5х107/кг
1.2х105/кг CD 34+
Слайд 9 Виды трансплантации в зависимости от источника стволовых клеток
Ауто-ТГСК
-костный мозг
-СКК
Алло-TГСК (неродственная, родственная, в т.ч. сингенная)
-костный мозг
-стволовые клетки крови (СКК)
-стимулированный
костный мозг - пуповинные клетки (преимущественно у детей)
Слайд 10Основные свойства гемопоэтической ткани
«Хоуминг», или способность кроветворных клеток узнавать клетки
стромы и распределяться среди клеток микроокружения, обусловлен молекулами клеточной адгезии,
интегринами, непосредственными клеточными контактами.При трансплантации 85% введенных внутривенно гемопоэтических клеток попадает в костный мозг (15% - в печень, легкие, селезенку и др. органы)
Слайд 11Преимущества и недостатки
Аутологичная ТКМ
Отсутствие иммунологических осложнений
Увеличение частоты рецидивов
Аллогенная ТКМ
Иммунологические
осложнения (РТПХ)
Необходимость длительной иммуносупрессивной профилактики/терапии
Снижение частоты рецидивов (реакция трансплантат против
лейкоза)
Слайд 12Получение стволовых клеток периферической крови
Г-КСФ 10 мкг/кг/сут п/к 1-5 дни
Лейкаферезы
(1-2) на 4-5 дни в зависимости от лейкоцитоза и числа
стволовых гемопоэтических клетокНа реципиента должно быть заготовлено не менее 2,0*106/кг CD34+
Слайд 13Основные принципы выполнения трансплантации аллогенных гемопоэтических клеток
Полная или частичная совместимость
по антигенам основного комплекса гистосовместимости (HLA)
Высокодозное циторедуктивное воздействие (кондиционирование)
Иммуносупрессия с
целью профилактики реакции «трансплантат против хозяина»Слайд 14Возраст и соматический статус пациента
Адекватность химиотерапии до ТКМ
Развитие рецидива
до выполнения трансплантации
Наличие совместимого донора
Вопросы селекции
Слайд 15Схема аллогенной ТКМ
Костный мозг
реципиента
химиотерапия
Цитопения
Смешанный
химеризм
Полный донорский химеризм
Костный мозг донора
Слайд 16Клеточность костного мозга в процессе лечения
Нормальный
костный мозг
Опухоль
Аплазия
Химиотерапия
Восстановление
Слайд 17Эффективность аллогенной ТКМ
Циторедуктивное воздействие (ТОТ + циклофосфан, бусульфан+циклофосфан), позволяющее уменьшить
опухолевый клон до минимального объема
Феномен «трансплантат против лейкоза»
Слайд 18 Проблемы трансплантации аллогенных гемопоэтических клеток
Токсичность режимов кондиционирования
Реакция трансплантат против
хозяина
Отсроченное восстановление иммунной системы
Инфекционные осложнения
Несостоятельность трансплантата
Рецидивы
Слайд 20Факторы риска РТПХ
Со стороны донора
- HLA- различия
Расхождение по полу (Ж-
М)
Возраст >35
Аллоиммунизация
Источник СК (ГСКК>КМ>ПК)
Аллореактивность NK-клеток
Со стороны реципиента
Возраст >35
Режим кондиционирования
ЦМВ, инфекции
НЕРОДСТВЕННЫЙ
ДОНОРСлайд 29 Основные показания к трансплантации
аутологичных стволовых клеток
Множественная миелома
Первичный
амилоидоз
Диффузная В-крупноклеточная лимфома
Лимфома из клеток мантийной зоны
Фолликулярная лимфома (II ремиссия)
Лимфогранулематоз
(рецидив, отвечающий на ПХТ, CR2 ) Т-ОЛЛ (протокол ОЛЛ-2009)
Слайд 30Показания к трансплантации аллогенного костного мозга при острых миелоидных лейкозах
ОМЛ
– взрослые (кроме М3)
1. Группа высокого риска
2. «Вторичный» лейкоз
3. Неудача
в индукции ( ремиссия после 2-го и далее курса ПХТ)4. CR1 группа промежуточного или плохого прогноза (цитогенетика, молекулярное исследование)
5. CR2 и более…(в. т.ч. при ОПЛ (М3))
Слайд 31Показания к трансплантации аллогенного
костного мозга
ОЛЛ – взрослые:
1. CR1 высокий
риск
2.BCR-ABL t(9;22)
3. MLL (11q23)
4. Гиперлейкоцитоз (>30,000 для B клеточного ,
>100,000 для T-клеточного лейкоза)5. Неудача в индукции
6. CR2 и далее
МДС
INT-1, INT-2, или высокий риск по IPSS
Слайд 32Показания к трансплантации аллогенного костного мозга
ХМЛ
1. Неудача лечения ингибиторами
тирозинкиназ особенно у пациентов из группы высокого риска
2.Резистентность (мутация
T315I)3.Фаза акселерации
4. II хроническая фаза
Первичный миелофиброз
Хронический лимфолейкоз
Апластическая анемия
ПНГ (при наличии HLA-идентичного сиблинга)
Слайд 36Трансплантация костного мозга
при острых миелоидных лейкозах
ОМЛ – взрослые (кроме
М3)
1. Группа высокого риска
2. «Вторичный» лейкоз
3. Неудача в индукции (
ремиссия после 2-го и далее курса ПХТ)4. CR1 группа промежуточного или плохого прогноза (цитогенетика, молекулярное исследование)
5. CR2 и более…( в. т.ч. при ОПЛ (М3))
Слайд 37 Классификация РИСКОВ
(клинико-лабораторные параметры, химиочувствительность, молекулярно-генетические маркеры)
The European LeukemiaNet AML
Working Party consensus statement on allogeneic HSCT for patients with
AML in remission:an integrated-risk adapted approach
Cornelissen et al., Nat Rev Clin Oncol. 2012 Oct;9(10):579-90.
Цитогенетические Молекулярные маркеры Клинические факторы
Благоприятные прогностические факторы
Неблагоприятные прогностические факторы
МРБ негативность
Старший возраст
Лейкоцитоз
Экстрамедуллярные очаги
Нет ПР после 1 курса
Персистенция МРБ
СД34+ бластные клетки
Вторичный ОМЛ
Слайд 38
Эффективность лечения ОМЛ в зависимости от цитогенетических аномалий
GRIMWADE et al
BLOOD, 22 JULY 2010 VOLUME 116, NUMBER 3
Слайд 39Общая выживаемость больных ОМЛ по итогам 4-х многоцентровых исследований (реализация
ТКМ ~2%)
20%
25,5%
24,3%
23%
ОМЛ-92
ОМЛ-95
ОМЛ-01
ОМЛ-06
Паровичникова Е.Н.тер.архив 2010, 7, с 5-11.
Слайд 40Общая и безрецидивная выживаемость в зависимости от возраста ( 40
лет)
16-40 лет
16-40 лет
40-60 лет
40-60 лет
ОМЛ 01-10
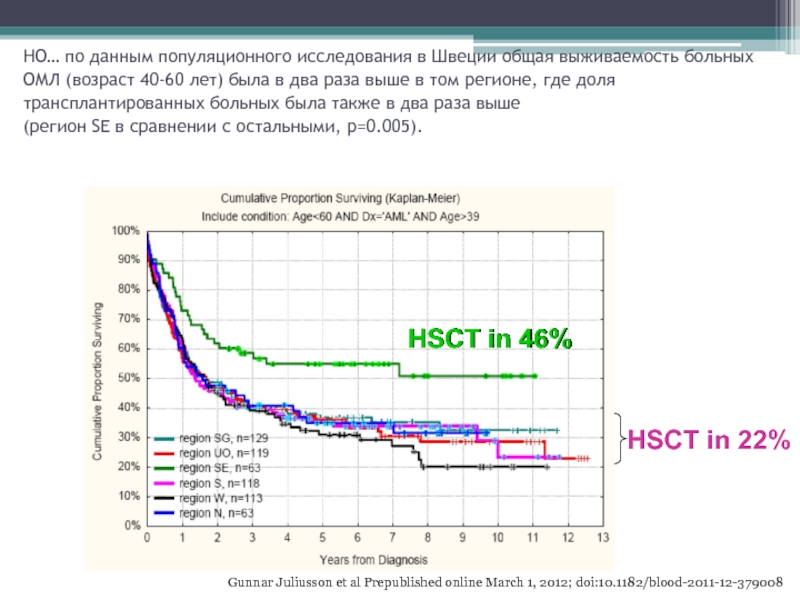
Слайд 41HSCT in 46%
HSCT in 22%
Gunnar Juliusson et al Prepublished online
March 1, 2012; doi:10.1182/blood-2011-12-379008
НО… по данным популяционного исследования в Швеции
общая выживаемость больных ОМЛ (возраст 40-60 лет) была в два раза выше в том регионе, где доля трансплантированных больных была также в два раза выше
(регион SE в сравнении с остальными, p=0.005).Слайд 43Межрегиональный трансплантационный регистр РФ
(данные за 2011 год)
Трансплантация Всего ОМЛ
Аллогенная
166
48 (28,9%)Аутологичная 234 46 (19,6%)
При заболеваемости в России - 1500 новых случаев в год - аллогенная ТКМ выполнена 48 больным (~3%)
должно быть минимум ~ 500!!!
Слайд 44Показания к трансплантации аллогенного костного мозга при острых лимфобластных лейкозах
ОЛЛ
– взрослые:
1. CR1 высокий риск
2.BCR-ABL t(9;22)
3. MLL (11q23)
4. Гиперлейкоцитоз (>30,000
для B- клеточного , >100,000 для T-клеточного лейкоза)5. Неудача в индукции
6. CR2 и далее
Слайд 45 Значение аллогенной трансплантации у взрослых пациентов с ОЛЛ
Миелоаблативный режим
кондиционирования (TBI+Bu; Bu+Cy)
Отсутствие поддерживающей терапии
76% -ауто ТСКК
18%- неродственный донор
Dutch-Belgian HOVON
Cooperative GroupJ.Corenllissen et al Blood,
2009; 113, 1375-82
42%
Слайд 46Годы после ТГСК
Общая выживаемость для пациентов ОЛЛ после аллогенной ТГСК
А
- Ph- негативные ОЛЛ
B – Ph+ ОЛЛ
Значение аллогенной трансплантации после
кондиционирования в режиме пониженной интенсивности при ОЛЛ (группа высокого риска)Слайд 49Значение аутологичной ТГСК при ОЛЛ у взрослых
EORTC
B. Labar et al
[haematologica] 2004;89:809-817
PETHEMA
J.Ribera et al Haematologica 2005; 90:1346-1356
36%
54%
UKALL XII/ECOG 2993
A.Goldestone et
al Blood, 2008 ; 111, 1827-33
auto
32%
GOELAMS
M. Hunault et al BLOOD,
2004; 104;3028
32%
Слайд 50D.Hoelzer et al Blood (ASH) 2009 114: Abstract 324
GMALL:
Значение аутологичной ТГСК для Т-ОЛЛ
Аутологичная ТГСК
20% пациентов
Общая выживаемость – 35%
Аллогенная
ТГСК Родственная
Общая выживаемость - 65%
Ранний Т-ОЛЛ - 60%,
Тимический – 73%,
Зрелый – 69%
Неродственная
Общая выживаемость - 55%
Ранний Т-ОЛЛ - 45%, Тимический – 73%,
Зрелый – 69%)
Слайд 51T-клеточный ОЛЛ – аутологичная ТГСК (кондиционирование пониженной интенсивности BEAM)
для всех пациентов (при отсутствии HLA - идентичного сиблинга
Длительное поддерживающее
лечение после ауто -ТГСКRALL study group protocol
ClinicalTrials.gov NCT01193933
Январь 2009 года
Ph-негативный ОЛЛ, 15-55 лет
Протокол ОЛЛ-2009
ГНЦ МЗ РФ
Слайд 52RALL study group protocol
ClinicalTrials.gov NCT01193933
Аллогенная ТГСК - 6 пациентов Т-ОЛЛ
T1/T2 – 4, TIII/TIV- 2
Доноры: HLA
- идентичные сиблинги - 4 неродственные HLA -идентичные доноры - 2
Рецидив – 1 пациент
Живы в ПР - 5
Аутологичная ТГСК – 28 пациентов T-ОЛЛ
Слайд 53Характеристика больных при диагностике заболевания (группа ауто-ТГСК)
Всего - 28 пациентов
(13 м/15ж)
Возраст 17 – 43 (медиана 26 л)
Иммунологический вариант Т-ОЛЛ
ранний - 12 (43%)тимический – 13 ( 46%)
зрелый – 3 (11%)
Индукционная терапия в ГНЦ - 18 больных
Высокая группа риска - 20 (72%)
Массивное поражение средостения -16 (57%)
Слайд 54АУТО-ТГСК
Время от достижения ремиссии до ауто -ТГСК – 6,2 мес
(2,2 - 10)
Время от заготовки трансплантата до ауто - ТГСК
- 2 месНеэффективная мобилизация – 4 пациента (15%)
Источник трансплантата СКК – 24
СКК + костный мозг - 2
костный мозг - 2
Оптимальное время мобилизации СКК после проведения консолидации III
Слайд 55Длительность агранулоцитоза медиана
11 дней (5-21)
Восстановление показателей
Лейкоциты (>1*109/l) +11 день (8-17)
Тромбоциты (>30*109/l) +12 день (8-22) (>100*109/l) +20 день (9-280)
Инфекционные осложнения - 24 пациента
85%
Грам+/Грам- сепсис - 6 больных - 21,4%
АУТО- TГСК
Слайд 56
Результаты АУТО- TГСК
Начало поддерживающей терапии
после ауто-ТГСК
- 1,5 мес (1 - 2)
Медиана наблюдения после ауто-ТГСК 20,5 мес (1,5 - 64)
28 (100%) пациентов живы в полной ремиссии заболевания
Слайд 59Трансплантация гемопоэтических клеток- этап терапии многих онкогематологических заболеваний
Трансплантация аутологичного и
аллогенного костного мозга является эффективным методом терапии ОЛ
При выборе тактики
лечения и отборе пациента на ТКМ необходимо учитывать факторы прогноза заболевания Благодарю за внимание















































![Трансплантация гемопоэтических стволовых клеток (ГСКК ) при Значение аутологичной ТГСК при ОЛЛ у взрослыхEORTCB. Labar et al [haematologica] Значение аутологичной ТГСК при ОЛЛ у взрослыхEORTCB. Labar et al [haematologica] 2004;89:809-817PETHEMAJ.Ribera et al Haematologica 2005; 90:1346-135636%54%UKALL](/img/thumbs/627a631029dd3330c0276b6af6ea2462-800x.jpg)





























