Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Учение о растворах. Коллигативные свойства растворов. Осмос, его роль в биосистемах
Содержание
- 1. Учение о растворах. Коллигативные свойства растворов. Осмос, его роль в биосистемах
- 2. Раствор — фаза переменного состава. «Фаза» указывает
- 3. Дмитрий Иванович Менделеев (1834 − 1907)Профессор Петербургского
- 4. Слайд 4
- 5. Термодинамическая классификация растворовКомпоненты взаимодействуют между собой и
- 6. Коллигативные свойства − …… свойства растворов, которые
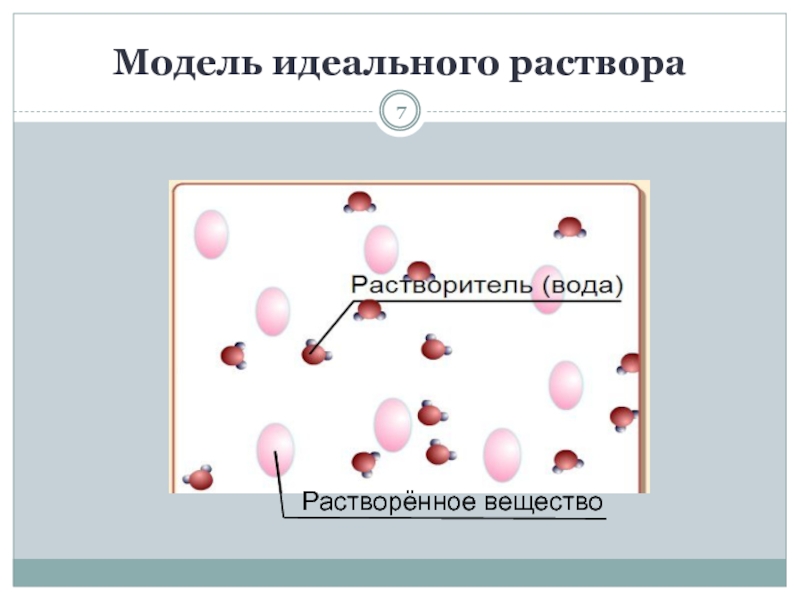
- 7. Модель идеального раствора
- 8. Физикохимик, профессор университета в Гренобле. Термин «криоскопия»
- 9. Закон РауляПри постоянной температуре относительное понижение давления
- 10. Повышение Ткипения и понижение Тзамерзания растворовПовышение Ткип.
- 11. Борьба с гололёдом
- 12. Криоскопияg – масса вещества, растворенного в G
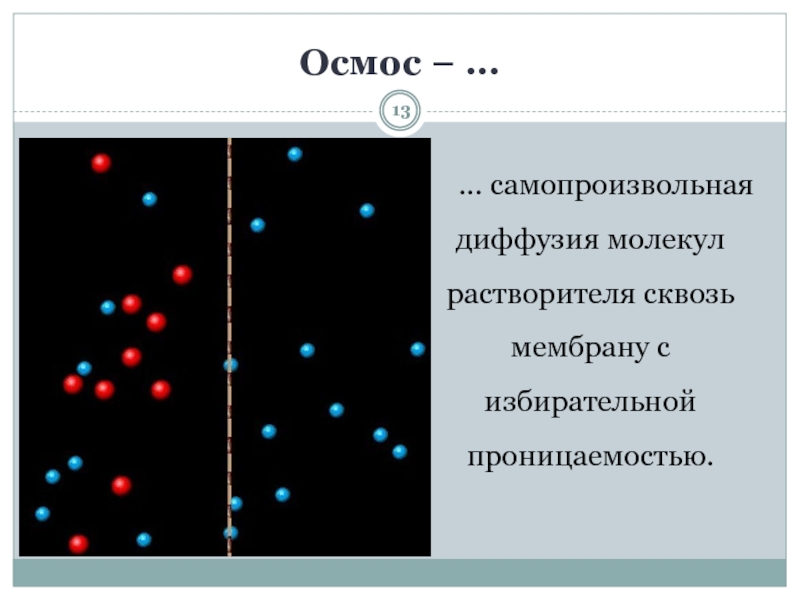
- 13. Осмос − …… самопроизвольная диффузия молекул растворителя сквозь мембрану с избирательной проницаемостью.
- 14. π = сRТОсмотическое давление раствора равно тому
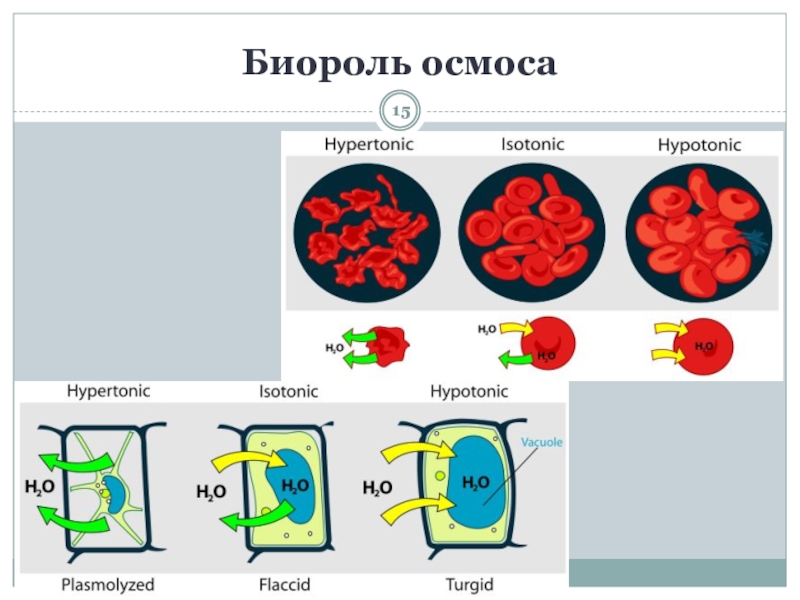
- 15. Биороль осмоса
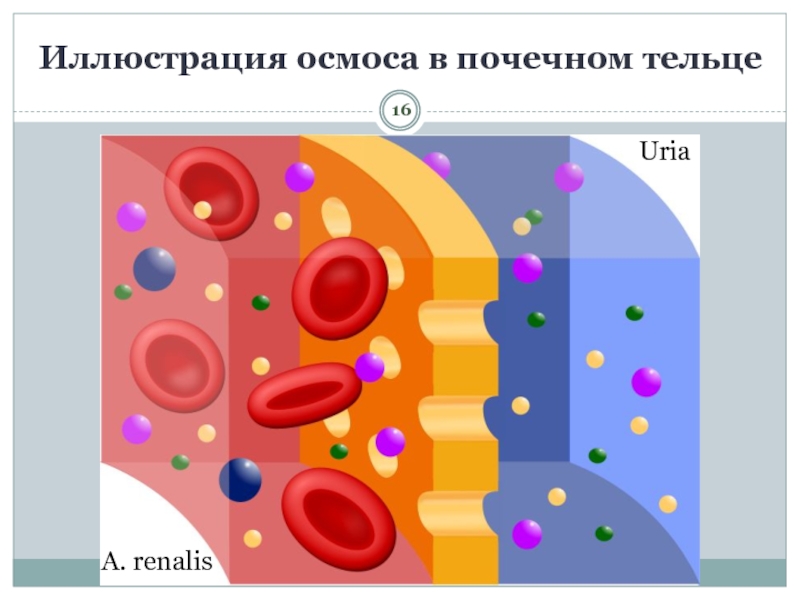
- 16. Иллюстрация осмоса в почечном тельцеA. renalisUria
- 17. Нормальное зрениеГлаукомаГлаукома − повышение внутриглазного давления
- 18. Изотонический коэффициентДля реальных растворов математические выражения, характеризующие
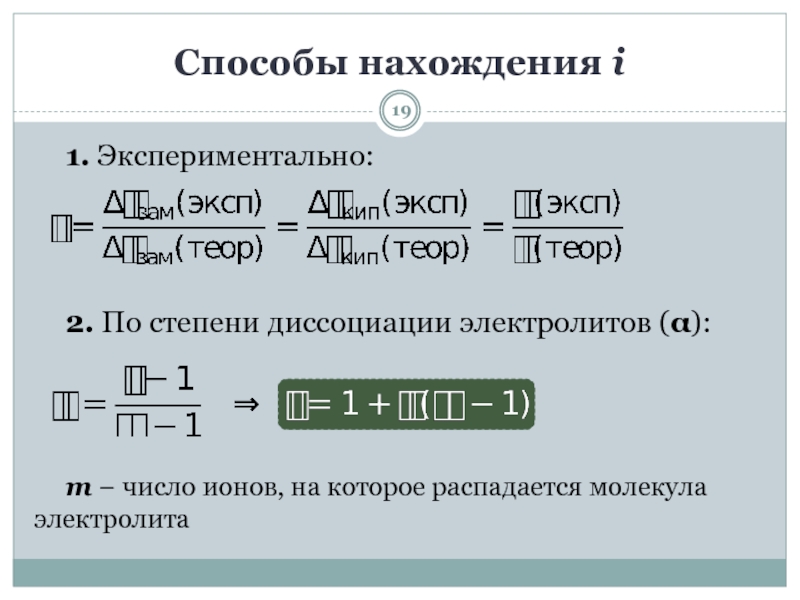
- 19. 1. Экспериментально:2. По степени диссоциации электролитов (α):m
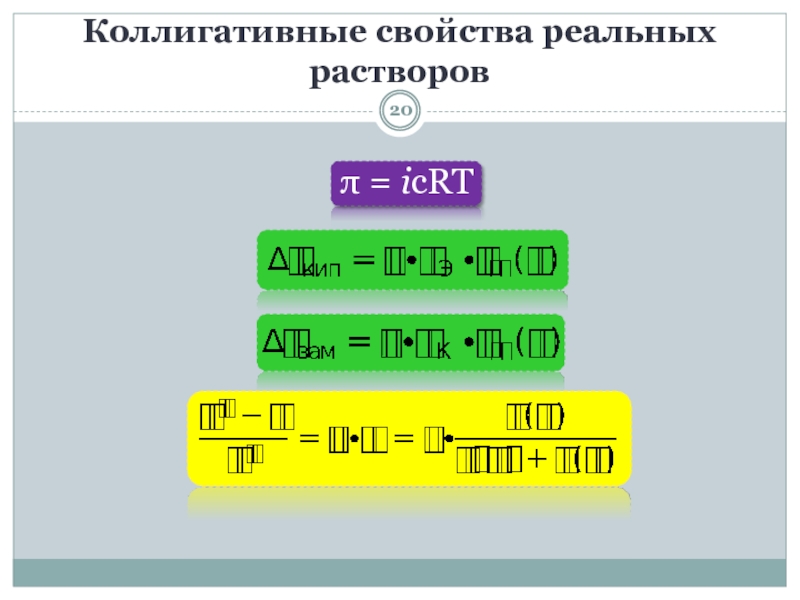
- 20. Коллигативные свойства реальных растворовπ = iсRТ
- 21. СПАСИБОЗА ВНИМАНИЕ!
- 22. Скачать презентанцию
Раствор — фаза переменного состава. «Фаза» указывает на однородность раствора, «переменный состав» на существование различных концентраций одного и того же раствора.
Слайды и текст этой презентации
Слайд 1Лекция №7 курса
«Общая химия»
Лектор: проф. Иванова Надежда Семёновна
Учение о растворах.
Коллигативные свойства растворов. Осмос, его роль в биосистемах
Слайд 2Раствор — фаза переменного состава. «Фаза» указывает на однородность раствора,
«переменный состав» на существование различных концентраций одного и того же
раствора.Слайд 3Дмитрий Иванович Менделеев
(1834 − 1907)
Профессор Петербургского университета. Основоположник сольватной теории
растворения, создатель Периодичесокй системы химических элементов.
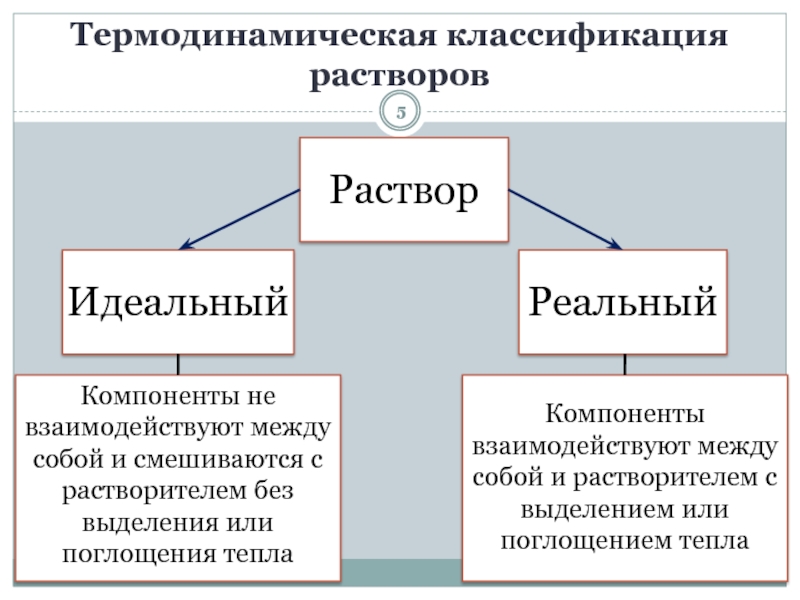
Слайд 5Термодинамическая классификация растворов
Компоненты взаимодействуют между собой и растворителем с выделением
или поглощением тепла
Компоненты не взаимодействуют между собой и смешиваются с
растворителем без выделения или поглощения теплаСлайд 6Коллигативные свойства − …
… свойства растворов, которые пропорциональны концентрации растворённого
вещества и не зависит от его химической природы.
Наличие коллигативных свойств
указывает на следующие факты:1. вещество не реагирует с растворителем, ведёт себя подобно газу;
2. его молекулы не подвергаются ни ассоциации, ни диссоциации, следовательно, тепловых эффектов не наблюдается.
Слайд 8Физикохимик, профессор университета в Гренобле. Термин «криоскопия» был введён им
в 1885г. в связи с открытием им закона, названного его
именем.Сейчас методом криоскопии пользуются для определения молекулярной массы низкомолекулярных веществ.
Франсуа Мари Рауль
(1830−1901)
Слайд 9
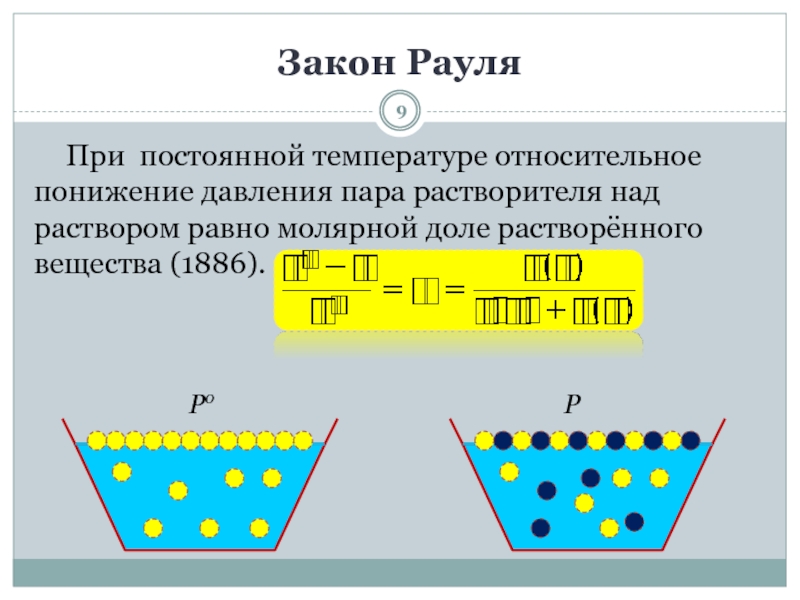
Закон Рауля
При постоянной температуре относительное понижение давления пара растворителя над
раствором равно молярной доле растворённого вещества (1886).
Ро
Р
Слайд 10
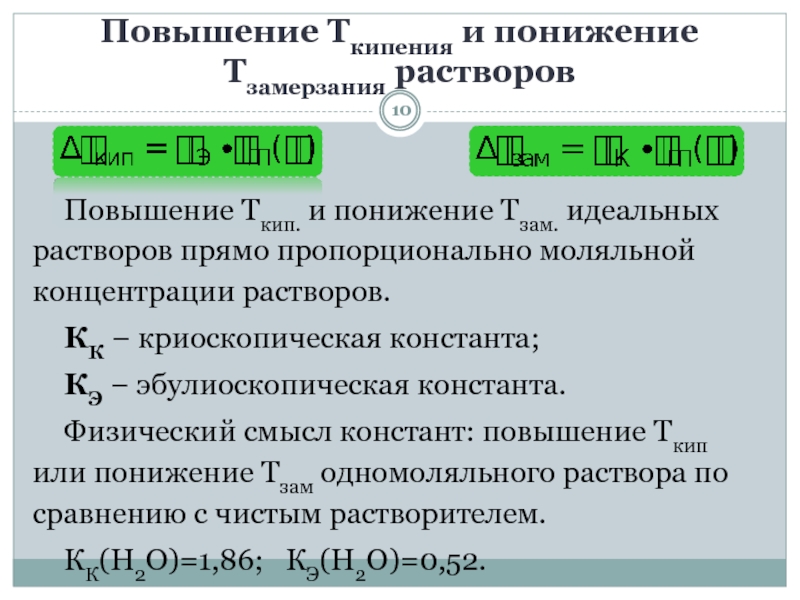
Повышение Ткипения и понижение Тзамерзания растворов
Повышение Ткип. и понижение Тзам.
идеальных растворов прямо пропорционально моляльной концентрации растворов.
КК − криоскопическая константа;
КЭ
− эбулиоскопическая константа.Физический смысл констант: повышение Ткип или понижение Тзам одномоляльного раствора по сравнению с чистым растворителем.
КК(Н2О)=1,86; КЭ(Н2О)=0,52.
Слайд 12
Криоскопия
g – масса вещества, растворенного в G граммах растворителя;
M –
молекулярная масса растворенного вещества;
KК – криоскопическая константа растворителя.
Слайд 13Осмос − …
… самопроизвольная диффузия молекул растворителя сквозь мембрану с
избирательной проницаемостью.
Слайд 14
π = сRТ
Осмотическое давление раствора равно тому давлению, которое производило
бы растворённое вещество, если бы оно при той же Т
находилось в газообразном состоянии и занимало V, равный Vраствора.Закон Вант-Гоффа (1887)
Якоб Хендрик Вант-Гофф
(1852-1911)