Слайд 2
Распространенность умственной отсталости оценить весьма трудно, поскольку цифры сильно
варьируют в зависимости от определения отдельных случаев умственной отсталости.
Если
принять условной границей нижней нормы уровень IQ = 70, то тогда частота умственной отсталости составит 2-3%.
Подавляющее большинство случаев умственной отсталости (примерно 85%) относится к легким (дебильность, IQ - от 50 до 69 единиц).
Среди детей с умственной отсталостью преобладают мальчики (встречаются в 1,5-2 раза чаще).
Частота умственной отсталости повышается после 6-7-летнего возраста, т.е. после поступления в школу. В этот период выявляются случаи легкой умственной отсталости и задержки умственного развития, поскольку дети испытывают трудности в обучении.
Слайд 3
Под умственной отсталостью понимается стойкое необратимое нарушение интеллекта.
Клинически
выделяют две основных формы умственной отсталости - олигофрению и деменцию.
Олигофрения включает несколько групп стойких нарушений интеллекта вследствие недоразвития мозга в раннем возрасте.
Под деменцией понимается распад уже сформированных интеллектуальных функций в результате различных заболеваний мозга.
Задержкой умственного развития считаются более легкие формы интеллектуального недоразвития, часто сопровождающиеся лишь парциальным (частичным) нарушением высших психических функций.
Слайд 4
Фенилкетонурия является рецессивным аутосомным моногенным заболеванием, связанным с нарушением
обмена аминокислоты фенилаланина. Дети, родившиеся с таким диагнозом, еще некоторое
время назад были обречены на тяжелую умственную отсталость, поскольку поступающий с пищей фенилаланин не подвергался необходимым превращениям. В результате страдали функции мозга. Сейчас можно избежать столь тяжелых последствий, если сразу же после рождения больного ребенка исключить из пищи продукты, содержащие фенилаланин. Такие диеты разработаны и применяются.
Диагностика фенилкетонурии у новорожденных не представляет трудностей, поэтому при всеобщем скрининге новорожденных и применении диетотерапии частота умственной отсталости вследствие фенилкетонурии может быть снижена.
Слайд 5
Ген фенилкетонурии локализован на 12 хромосоме. В последнее время
установлено, что причиной фенилкетонурии могут быть более 100 разнообразных мутаций
этого гена, которые могут вызывать разные степени умственной отсталости. Кроме фенилкетонурии на уровень умственного развития могут влиять и другие наследственные нарушения обмена веществ.
Причиной умственной отсталости в таких случаях, как правило, является плейотропный (множественный) эффект действия генов, поскольку нарушения метаболизма приводят к системным нарушениям развития, затрагивающим в том числе и мозг.
Изучение генетики тяжелой умственной отсталости показало значительную гетерогенность этой группы заболеваний.
Часть из них имеют экзогенную природу. Остальные связаны с хромосомными нарушениями и различными наследственными заболеваниями.
Слайд 6
Умственная отсталость может обусловливаться как эндогенными, так и экзогенными
причинами.
Считается, что примерно 75% случаев умственной отсталости имеют наследственную
природу. Среди них 15% составляют хромосомные аномалии. Хромосомные аномалии связаны с изменением числа хромосом или перестройкой их структуры.
Аномалии могут затрагивать как аутосомы, так и половые хромосомы. Нарушение числа и структуры аутосом приводит к более серьезным последствиям и сопровождается, кроме умственной отсталости, множественными пороками развития, затрагивающими различные органы и ткани.
Изменение числа половых хромосом вызывает менее выраженную умственную отсталость.
Среди хромосомных аномалий, связанных с умственной отсталостью, чаще других встречается синдром Дауна (1:700).
Синдром Дауна является следствием нерасхождения хромосом.
В кариотипе больных отмечается лишняя 21 хромосома. Коэффициент интеллекта лиц с синдромом Дауна колеблется в пределах 20-60 единиц. Большинство больных не способны жить самостоятельно.
Тяжелая умственная отсталость может возникать и в результате наследственных заболеваний, связанных с нарушениями метаболизма, например, фенилкетонурия

Слайд 7
В последнее время внимание генетиков привлечено к изучению Х-сцепленной
умственной отсталости (синдром ломкой, или фрагильной Х-хромосомы, синдром Мартина -
Белла).
Название синдрома объясняется особой формой строения Х-хромосомы, которая имеет хорошо заметную перетяжку на конце длинного плеча.
Слайд 8
После выявления этой наследственной формы умственной отсталости стала понятной
большая частота встречаемости интеллектуального недоразвития у мальчиков. Это рецессивное заболевание
передается с Х-хромосомой через мать, поскольку мальчики получают свою единственную Х-хромосому от матери. У мальчиков, в отличие от девочек, только одна Х-хромосома, поэтому рецессивные Х-сцепленные заболевания у них наблюдаются гораздо чаще. Оказалось, что синдром ломкой Х-хромосомы является одним из наиболее распространенных наследственных заболеваний, сопоставимым по частоте с болезнью Дауна (примерно 1 на 2000 мужчин). Кроме ломкой Х-хромосомы для больных характерны некоторые морфологические признаки, которые не всегда отчетливо проявляются (высокий выпуклый лоб, крупные уши и челюсти, крупные кисти рук, увеличенные яички).
Умственное развитие колеблется между значениями IQ от 30 до 65 (иногда в границах нормы). Речь изобилует повторами, часто встречается своеобразное заикание. Для детей характерна двигательная расторможенность и некоторые симптомы аутизма (ребенок избегает глазного контакта, производит стереотипные движения руками, испытывает страхи). Даже при легкой степени интеллектуальной недостаточности дети с трудом овладевают навыками счета и письма. Дети с ломкой Х-хромосомой имеют своеобразную электроэнцефалограмму. В связи с тем, что симптомы заболевания разнообразны, часто ставится ошибочный диагноз (шизофрения, ранний детский аутизм, эпилепсия, синдром дефицита внимания и гиперактивности). В результате дети не получают соответствующего лечения, а семья остается в неведении относительно истинных причин нарушения развития.

Слайд 9
Генетический механизм заболевания связан с экспансией тринуклеотидных повторов (CGG
- цитозин-гуанин-гуанин) в соответствующем перетяжке участке Х-хромосомы. В норме число
повторов не должно превышать 50. Количество повторов от 50 до 200 считается премутацией, выраженная картина болезни наблюдается при наличии более 200 повторов.
Для данного заболевания характерно явление антиципации, т.е. усиление тяжести заболевания от поколения к поколению. Это связано с нарастанием числа тринуклеотидных повторов в мутировавшем участке хромосомы.
Поскольку заболевание является широко распространенным, ранняя его диагностика важна для своевременной организации лечебно-коррекционных мероприятий и медико-генетического консультирования семьи, чтобы предупредить риск рождения детей с таким же диагнозом
Слайд 10
Легкие формы умственной отсталости представляют качественно иную группу с
точки зрения наследственности, чем ее тяжелые формы: меньше представлена экзогенная
патология, хотя неблагоприятные факторы среды играют несомненную роль.
Легкая умственная отсталость обычно не сопровождается заметными изменениями в физическом облике или в поведенческих реакциях.
Слайд 11
Особую группу когнитивных нарушений составляет специфическая неспособность к обучению
(СНО).
В англоязычной литературе эти расстройства носят общее название learning
disabilities. В отечественной литературе пока нет общепринятого термина для обозначения этой группы нарушений развития. Часто их отождествляют с понятием задержки психического развития (ЗПР). Иногда можно встретить такие обозначения, как "трудности школьного обучения" или "школьные трудности". Понятно, что неуспех в школе может объясняться различными причинами - низкой мотивацией, педагогической запущенностью, истинной умственной отсталостью, заболеваниями, не связанными с психической сферой и т.д.
Не следует смешивать школьную неуспеваемость с СНО.
Неспособность к обучению
Слайд 12
Нейродегенеративные заболевания
Нейродегенеративные заболевания (греч. νέυρο-, нейро-, «нервы-» и лат.
dēgenerāre, «вырождаться») — группа в основном медленно прогрессирующих, наследственных или приобретённых
заболеваний нервной системы.
Общим для этих заболеваний является прогрессирующая гибель нервных клеток (нейродегенерация), ведущая к различным неврологическим симптомам - прежде всего, к деменции и нарушению движений. Заболевания могут наступить в различном возрасте, протекают диффузно или генерализированно, гистологически определяется специфический тип изменений.
Слайд 13
Нейродегенеративные заболевания (НДЗ) приводят к постепенному нарастанию психической и
физической несостоятельности. Прогрессирующая патология головного мозга как центра регуляции приводит
к когнитивным и двигательным расстройствам.
При этом на начальных этапах сохраняется критика, что влечёт тяжелые переживания больного от осознания собственной ущербности.
Комплекс прогрессирующих нарушений при НДЗ включает:
поведенческие расстройства;
двигательные нарушения;
утрату памяти, мышления;
угасание способности к восприятию и осмыслению;
нарушения речи;
дисбаланс в эмоционально-волевой сфере.
Нейродегенеративные заболевания
Слайд 14
Нейродегенеративным заболеваниям свойственно прогрессирование, приводящее к дегенерации личности, полной
утрате трудоспособности и дееспособности. Как правило, смерть пациентов наступает по
истечении нескольких (иногда десятков) лет от присоединившихся заболеваний, что отчасти можно связать с возрастающими трудностями в уходе и обслуживании таких больных.
Нейродегенеративные заболевания
Слайд 15
На начальных этапах различные НДЗ могут иметь схожую клиническую
картину.
Диагностика должна основываться не только на сборе анамнестических данных
и динамическом наблюдении, а также затрагивать генетические аспекты. Дифференцировать конкретный диагноз помогают специальные тесты. Для исключения опухолевого, травматического, сосудистого генеза начавшихся нарушений применяются инструментальные методы диагностики.
Наиболее показательны следующие методики обследования при подозрении на НДЗ:
МРТ, КТ головного мозга;
ПЭТ;
однофотонная КТ;
исследование уровня нейромедиаторов;
ангиография;
УЗДГ сосудов головного мозга и шейного отдела;
ЭЭГ.
Диагностика и клиническая картина
при нейродегенеративных заболеваниях
Слайд 16
Болезнь Альцгеймера
Лобно-височная деменция (Болезнь Пика)
Хорея Гентингтона
Деменция с
тельцами Леви
5. Подкорковая сосудистая деменция
Нейродегенеративные заболевания
Слайд 17
Механизмы развития нейродегенеративных заболеваний
Патофизиологические механизмы нейродегенеративных заболеваний включают в
себя синтез и агрегацию белков с патологической конформацией, что, в
свою очередь, запускает каскад иммунных и метаболических нарушений, накопление металлов в центральной нервной системе, нарушение энергетического обмена клеток, дефицит ферментов и т.д.
Большая роль в развитии нейродегенеративного процесса принадлежит генетическим факторам. Выделяют как моногенные нейродегенеративные заболевания (например, болезнь Гентингтона, спинальные амиотрофии, ряд вариантов спиноцеребеллярных атаксий, болезнь Вильсона, моногенные варианты болезни Паркинсона, спастические параплегии, пароксизмальные дискинезии и пр.), так и болезни, развивающиеся вследствие нарушений функционирования целых ансамблей генов в сочетании с действием неблагоприятных факторов внешней среды (идиопатическая болезнь Паркинсона, атипичный паркинсонизм, болезнь Альцгеймера, боковой амиотрофический склероз, лобно-височная деменция и пр.).
При этом, важно помнить, что отсутствие отягощённого семейного анамнеза по нейродегенеративному заболеванию не исключает наличие генетической предрасположенности к его развитию.

Слайд 18
Клинические проявления нейродегенеративных заболеваний зависят от стадии и определённого
вида патологии. Чаще всего симптомокомплекс включает двигательные нарушения (изменение походки,
тремор, акинезию и ригидность). Часто по мере прогрессирования болезни развивается постуральная неустойчивость. Возможны гиперкинезы, самопроизвольные или насильственные движения.
В уровне интеллекта имеет место деменция, ослабление памяти, мыслительной деятельности, нарушаются контакты с окружающими. Как следствие – больной человек постепенно самоизолируется.
Для постановки диагноза часто показательным является факт первичности нарушений двигательной активности или интеллекта.
Сохранной остаётся мышечная активность на начальных стадиях болезни Альцгеймера, при сосудистой деменции, болезни Пика. Тогда как болезнь Паркинсона, Хорея Гентингтона изначально проявляются изменениями в походке, тремором, гиперкинезами.
Слайд 19
Неуклонное прогрессирование заболеваний, связанных с нейродегенерацией, приводит таких больных
к инвалидности. Они подвержены не только расстройствам интеллекта, памяти и
мышления, но и беззащитны перед нарастающими двигательными нарушениями. Утрата здоровой координации движений нередко приводит к травмам.
Вегетативная нервная система под «руководством» больного мозга начинает неправильно функцтонировать, приводя к расстройствам пищеварения, сухости кожи, запорам, нарушению мочеиспускания.
Дееспособность больных нейродегенеративными заболеваниями также всегда является спорным вопросом. Многие из них способны на асоциальные поступки и представляют угрозу для самих себя и окружающих.
Лечение НДЗ всегда неспецифическое и направлено на оказание симптоматической помощи, осуществление должного ухода за больным, сохранение как можно более длительно способности пациента взаимодействовать с теми, кто берёт его под свою опеку.
На более тяжёлых стадиях основные задачи – кормление, гигиена, профилактика инфекций и травм, а также пролежней и иных осложнений.
Течение болезни и уход за больными НДЗ

Слайд 20
40 млн.
людей в мире
страдают нейродегенеративными заболеваниями
Старше 70 лет -
5%
Старше 80 лет - 1 0-15%
67 СЛУЧАЕВ ИЗ 1000 -
Болезнь Альцгеймера
9,5 СЛУЧАЕВ ИЗ 1000 - Болезнь Паркинсона
1:1500 - распространённость нейродегенеративных
заболеваний
Слайд 21
Болезнь Альцгеймера (старческое слабоумие, деменция альцгеймеровского типа)
Болезнь Альцгеймера впервые
описана в 1906 году немецким психиатром Алоисом Альцгеймером (1864 -1915)
как прогрессирующее заболевание центральной нервной системы, сопровождающееся потерей кратковременной памяти, утерей навыков, замедленностью мышления. Болезнь развивается у людей в возрасте старше 50 лет.
Общемировая заболеваемость на 2006 г. оценивалась в 26,6 млн. человек, а к 2050 году число больных может вырасти вчетверо [Brookmeyer R., Johnson E., Ziegler-Graham K.,. Arrighi M H., 2007].
Слайд 22
В настоящее время основными патоморфологическими признаками болезни Альцгеймера считаются
следующие:
Сенильные бляшки
2. Амилоидоз сосудов мозга, поражающий сосуды малого и
среднего калибра мозговых оболочек.
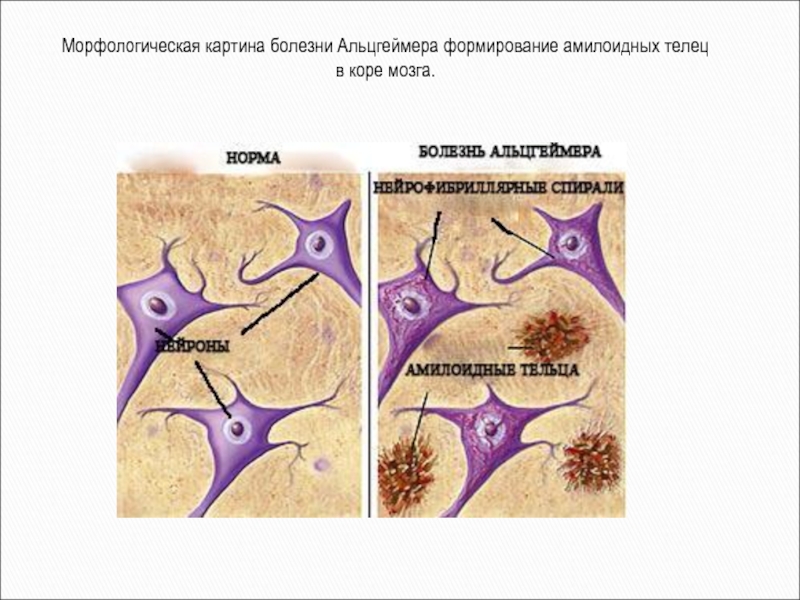
3. Внутринейрональные отложения фибрилл (альцгеймеровские нейрофибрилы или нейрофибриллярные клубки).
Альцгеймеровские нейрофибриллы структурно отличаются от отложений бета- амилоида. Данные нейрофибриллы сформированы из закрученных фибрилл фосфорилированного белка (tau) тау. В норме функция этого белка состоит в стабилизации микротрубочек. При патологии гиперфосфорилирование тау приводит к разрыву его связи с микротрубочками, что в конечном итоге ведет к дегенеративным процессам в нейрон. Данный факт послужил основой для возникновения так называемой tau-гипотезы патогенеза болезни Альцгеймера.
Факторами риска являются – возраст, семейный анамнез, выраженные сосудистые заболевания. Это тотальное слабоумие в пожилом и старческом возрасте
Слайд 23
Морфологическая картина болезни Альцгеймера формирование амилоидных телец
в коре
мозга.
Слайд 24
Болезнь имеет тенденцию прогрессировать. Нарастают раздражительность, нетерпимость, теряются гигиенические
навыки, возникают проблемы с речью. Прогрессирующий характер болезни является результатом
интенсивной гибели клеток в некоторых областях мозга. Что является толчком к развитию болезни, пока неясно.
Болезнью Альцгеймера страдают примерно 3-5% людей старше 65 лет и 20% - старше 80 лет. Гораздо реже болезнь начинается относительно рано - на 40-х-50-х годах жизни.
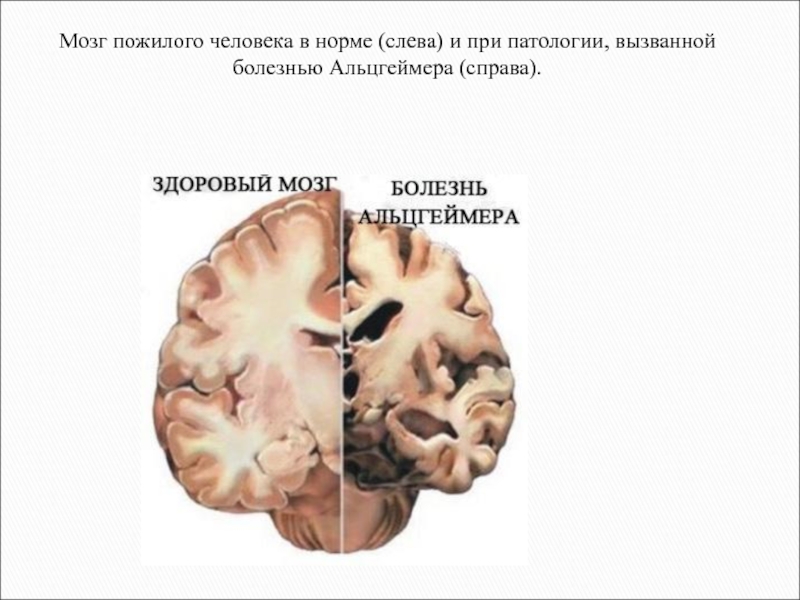
Болезнь характеризуется потерей нейронов и синаптических связей в коре головного мозга и определённых субкортикальных областях. Гибель клеток приводит к выраженной атрофии поражённых участков, в том числе к дегенерации височных и теменной долей, участков фронтальной корыи поясной извилины [Wenk G.L., 2003].
Слайд 25
Мозг пожилого человека в норме (слева) и при патологии,
вызванной болезнью Альцгеймера (справа).
Слайд 26
В настоящее время не достигнуто полного понимания причин и
хода болезни Альцгеймера.
Объяснение возможных причин заболевания предложено в трёх
основных конкурирующих гипотезах:
холинергическая гипотеза;
амилоидная гипотеза;
тау-гипотеза
Слайд 27
Согласно первой теории ведущая роль в патогенезе болезни Альцгеймера
придается изменениям со стороны нейротрансмиттерных систем, особенно центральному ацетилхолинергическому дефициту.
Сходные процессы, хотя и не столь значительно выраженные, затрагивают норадренергическую и серотонинергическую системы, с патологией которых связывают возникновение некогнитивных симптомов - экстрапирамидных расстройств, депрессии, агрессивного поведения. Роль ГАМК-ергической, глутаматергической и пептидергических (соматостатин, кортикотропин-релизинг фактор) нейротрансмиттерных систем в патогенезе этого заболевания активно изучается.
Таким образом, в основе возникновения и прогрессирования когнитивных нарушений при болезни Альцгеймера, как считается, лежит нарушение ацетилхолинергической передачи. Это открывает определенные возможности для терапии – использование предшественников ацетилхолина и центральных ингибиторов ацетилхолинэстеразы [Stahl S.M., 2000; Raina P., Santaguida P., Ismaila A. et al., 2008].
Слайд 28
Амилоидная гипотеза, предполагает, что продукция и деградация бета-амилоида являются
основными в патогенезе не только менделевской формы заболевания, но и
болезни мультифакториальной, развившейся в общей популяции.
Слайд 29
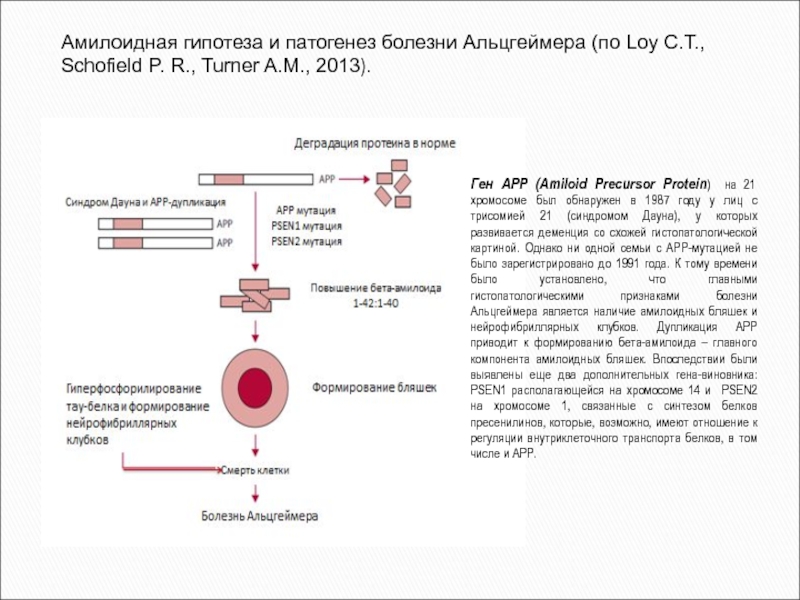
Амилоидная гипотеза и патогенез болезни Альцгеймера (по Loy C.T.,
Schofield P. R., Turner A.M., 2013).
Ген APP (Amiloid Precursor Protein)
на 21 хромосоме был обнаружен в 1987 году у лиц с трисомией 21 (синдромом Дауна), у которых развивается деменция со схожей гистопатологической картиной. Однако ни одной семьи с АРР-мутацией не было зарегистрировано до 1991 года. К тому времени было установлено, что главными гистопатологическими признаками болезни Альцгеймера является наличие амилоидных бляшек и нейрофибриллярных клубков. Дупликация АРР приводит к формированию бета-амилоида – главного компонента амилоидных бляшек. Впоследствии были выявлены еще два дополнительных гена-виновника: PSEN1 располагающейся на хромосоме 14 и PSEN2 на хромосоме 1, связанные с синтезом белков пресенилинов, которые, возможно, имеют отношение к регуляции внутриклеточного транспорта белков, в том числе и АРР.
Слайд 30
Согласно третий из основных теорий патогенеза болезни Альцгеймера её
относят к таупатиям, болезням, связанным с ненормальной агрегацией тау-белка.
Каждый нейрон
содержит цитоскелет, отчасти составленный из микротрубочек, которые действуют подобно рельсам, направляя питательные вещества и другие молекулы из центра на периферию клетки, к окончанию аксона, и обратно. Тау-белок, наряду с несколькими другими белками, асоциирован с микротрубочками, в частности, после фосфорилирования он их стабилизирует.
При болезни Альцгеймера тау-белок подвергается избыточному фосфорилированию, из-за чего нити белка начинают связываться друг с другом, слипаться в нейрофибриллярные клубки и разрушать транспортную систему нейрона [Hernández F., Avila A. J., 2007].
Слайд 31
Клинически, типичная форма болезни Альцгеймера характеризуется градуальным началом и
быстрым прогрессированием в виде расстройств памяти и когнитивной дисфункции (по
критериям 1984г. Тhe National Institute of Neurological and Communicative Disorders and Stroke–Alzheimer’s Disease and Related Disorders Association [NINCDS-ADRDA]). Эти диагностические критерии были пересмотрены с целью выявления форм болезни без нарушений памяти (с языковыми, зрительно-пространственными дисфункциями) и определения роли биомаркеров в диагностике (критерии 2011г. Тhe National Institute on Aging–Alzheimer’s Association [NIA-AA]).
Слайд 32
Постепенно прогрессирует упадок интеллектуальных функций, нарушается понимание окружающего мира
и самостоятельные действия в нем. Первыми страдают память и внимание,
ориентация во времени, изменяется характер. При прогрессировании нарастают нарушения ориентации во времени, месте нахождения, себе самом. Больные не узнают родственников, теряют профессиональные и бытовые навыки, у них нарушается речь – словарный запас уменьшается, появляются ложные воспоминания, бессмысленные выражения, утрачивается способность читать, считать. Возможны бред и галлюцинации.
В тяжелых случаях больные полностью становятся зависимыми от постороннего ухода и не могут существовать самостоятельно. Происходит полный распад личности. Остаются стереотипные бессмысленные крики и движения в пределах постели. При МРТ – атрофия вещества мозга.
Слайд 33
Подкорковая сосудистая деменция
Характеризуется замедлением информационных процессов, расстройством памяти и
внимания, нарушением процессов запоминания и удерживания новой информации, нарушением абстрагирования,
речевыми дисфункциями, расстройствами программирования и переключения, апатией, депрессией, нарушением ходьбы лобного типа (ходьба замедляется, шаг укорачивается, трудно начать ходьбу, неустойчивость при поворотах, увеличивается площадь опоры). В тяжелых случаях - слабоумие, полная беспомощность, нарушение тазовых функций. Это болезнь Бинсвангера. Синонимы – субкортикальная атеросклеротическая энцефалопатия, гипертоническая энцефалопатия бинсвангеровского типа, атеросклеротическая энцефалопатия, прогрессирующая сосудистая лейкоэнцефалопатия. При МРТ обнаруживаются множественные двусторонние очаги в белом веществе размерами более 2 см и отсутствие корковых поражений.
Слайд 34
Болезнь Пика
Болезнь Пика представляет собой редкий вид лобно-вислчной
деменции с характерным началом в возрасте 50-60 лет и преимущественной
атрофией коры височных и лобных долей мозга.
Названа в честь описавшего ее в 1892 г. Арнольда Пика.
Сам Пик считал описанную им патологию лишь отдельным клиническим вариантом старческой деменции. Однако позже, после выявления подтвержденных паталогоанатомическими исследованиями отличительных морфологических признаков, болезнь Пика была выделена как самостоятельная нозология.
Слайд 35
Болезнь Пика – редкое, хроническое прогрессирующее заболевание центральной нервной
системы, проявляющееся атрофией и разрушением коры головного мозга в лобной
и височной долях. Течение заболевания более злокачественно по сравнению с болезнью Альцгеймера. Более быстро нарастают симптомы тотального слабоумия, распада речевых функций, мышления и восприятия, афазии, амнезии, апатии и экстрапирамидные нарушения и быстро происходит «распад» личности.
Дифференциальный диагноз деменций проводится между болезнью Альцгеймера, Пика, Кройцфельда – Якоба, сосудистой деменцией и вторичными деменциями, связанными с соматическими заболеваниями и интоксикациями.
Слайд 36
Лечение и прогноз болезни Пика
Специфическая терапия не разработана. В
схему лечение, как правило, включают антихолинэстеразные фармпрепараты (холина альфосцерат, галантамин,
ривастигмин, донепезил), ноотропы (пирацетам, фонтурацетам, гамма-аминомасляная кислота), мемантин.
При наличии агрессивного поведения назначают нейролептики:
алимемазин,
хлорпротиксен.
В начальных стадиях рекомендована психотерапия, участие в когнитивных тренингах, консультирование психолога; в более поздних — сенсорная комната, арт-терапия, симуляция присутствия.
Слайд 37
Все вышеуказанные методы направлены на замедление прогрессирования симптомов.
Однако
их эффективность при деменции Пика существенно ниже, чем при болезни
Альцгеймера.
Несмотря на проводимую терапию, состояние глубокой деменции наступает в среднем через 5-6 лет после дебюта болезни.
Продолжительность жизни от начала заболевания не превышает 10 лет.
Слайд 38
Болезнь Гентингтона - генетическое заболевание нервной системы, характеризующееся постепенным
началом обычно в возрасте 35-50 лет и сочетанием прогрессирующего хореического
гиперкинеза и психических расстройств.
Наследуется по аутосомно-доминантному типу с высокой пенетрантностью (80-85%); мужчины болеют чаще, чем женщины.
Как показали современные генетические исследования, детерминирующий его ген локализуется на коротком плече 4-й хромосомы. Хорея (chorea; от греческого слова "choreia" - пляска) - форма гиперкинеза, характеризуется непроизвольными, быстрыми, нерегулируемыми движениями, возникающими в различных мышечных группах.
Психические расстройства при данном заболевании чаще всего представлены деменцией, апатией, депрессией с нередкими суицидальными попытками, нарушениями эмоционального контроля с частыми вспышками раздражения и агрессии, отчужденностью.
В некоторых случаях развиваются бред и навязчивые состояния.
Слайд 39
Патоморфология и патофизиология Болезнь Хантингтона поражает специфические области мозга.Наиболее
заметные ранние изменения затрагивают область базальных ганглиев называемую полосатым телом,
которое состоит из хвостатого ядра и скорлупы. Другие повреждаемые области включают чёрную субстанцию, 3, 5 и 6 слои коры головного мозга, гиппокамп, клетки Пуркинье в мозжечке, боковые туберальные ядра гипоталамуса и часть таламуса. Базальные ганглии — часть головного мозга, наиболее заметно повреждающиеся при болезни Хантингтона — играют ключевую роль в контроле движений и поведения. Их функция полностью не ясна, но современные теории предполагают, что они являются частью когнитивной исполнительной системы и двигательного контура. Базальные ганглии в норме ингибируют большое число контуров (circuit), генерирующих специфические движения. Для инициации специфических движений кора посылает сигналы базальным ганглиям для снятия ингибирования. Повреждение базальных ганглиев может привести к снятию ингибирования или его постоянным неконтролируемым изменениям, что служит причиной затруднения начала движения или к их непроизвольной инициации, или движение может быть прервано до или после достижения желаемого результата. Накапливающиеся повреждения в этой области приводят к беспорядочным движениям, характерным для болезни Хантингтона.

Слайд 40
Болезнь Крейтцфельдта-Якоба — редко встречающееся дегенеративное заболевание головного мозга,
связанное с накоплением в нейронах патологического белка приона. Клинически болезнь
Крейтцфельдта-Якоба проявляется слабоумием, пирамидными и экстрапирамидными нарушениями, миоклониями, симптомами поражения мозжечка и нарушением зрения. Диагноз болезни Крейтцфельдта-Якоба основывается на совокупности клинических симптомов, данных ЭЭГ, анализа цереброспинальной жидкости, МРТ и ПЭТ головного мозга, а также морфологического исследования образца тканей мозга, полученного в результате биопсии или посмертно. Эффективное лечение болезни Крейтцфельдта-Якоба пока не найдено. Заболевание имеет 100% летальный исход.
Слайд 41
Болезнь Крейтцфельдта-Якоба очень редкое заболевание. Ранее в литературе указывалось,
что частота его встречаемости примерно 1 случай на 1 млн.
человек населения. Однако в 90-х годах прошлого века начали отмечаться случаи так называемого нового варианта болезни Крейтцфельдта-Якоба, связанного с заражением от крупного рогатого скота и названного «коровьим бешенством». Только в Англии за 5 лет от этого заболевания умерло 86 человек. Наиболее распространена болезнь Крейтцфельдта-Якоба среди людей в возрасте 65-70 лет и старше. Однако в новом варианте болезнь Крейтцфельдта-Якоба зачастую поражает лиц молодого возраста.
Относительно высокий уровень заболеваемости отмечается в Англии, Израиле, Чили и Словакии
Слайд 42
Установлено, что болезнь Крейтцфельдта-Якоба имеет инфекционный характер. Заражение может
произойти при пересадке зараженных прионами тканей, через нейрохирургический инструмент и
препараты крови, при введении некоторых гормональных препаратов (человеческого гонадотропина для лечения бесплодия и соматотропина для терапии гипопитуаризма). Болезнь Крейтцфельдта-Якоба новой формы может развиваться после употребления в пищу мяса заболевших животных (коровы) или носителей инфекции (овец и коз).
В результате ряда исследований стало известно, что болезнь Крейтцфельдта-Якоба связана с проникновением в организм инфекционного белка — приона. В норме в клетках головного мозга человека содержится здоровый прион, имеющий несколько другое строение. Инфекционный прион, попадая в организм человека не разрушается, а с током крови поступает в головной мозг и откладывается на поверхности нейронов. Его взаимодействие с нормальными прионами мозговой клетки приводит к тому, что они изменяют свою структуру, постепенно трансформируясь в патогенную, подобную инфекционному приону, форму. Патогенные прионы образуют бляшки и приводят к гибели нейрона.
Болезнь Крейтцфельдта-Якоба имеет достаточно длительный инкубационный период, связанный с временем, необходимым для проникновения инфекционных прионов в мозговую ткань и патогенной трансформации здоровых прионов. Длительность инкубационного периода напрямую зависит от способа заражения. При инфицировании тканей головного мозга зараженным хирургическим инструментом болезнь Крейтцфельдта-Якоба развивается через 15-20 месяцев. При инфицировании через имплантированные в околомозговые структуры ткани (например, твердую мозговую оболочку, роговицу глаза) инкубационный период может длиться до 5,5 лет. При внутримышечном введении инфицированных лекарственных препаратов (например, гонадотропина, соматотропина, содержащих бычий тромбин гемостатиков) болезнь Крейтцфельдта-Якоба начинает проявляться спустя 12,5 лет.
Отмечаются также наследственные формы болезни Крейтцфельдта-Якоба, связанные с генетическими нарушениями, приводящими к образованию патологических прионов.

Слайд 43
Классификация болезни Крейтцфельдта-Якоба
Практическая неврология классифицирует болезнь Крейтцфельдта-Якоба с
учетом ее клинической формы. В соответствии с этим выделяют:
подострую спонгиоформную энцефалопатию, отличающуюся быстрым течением и диффузным поражением мозговой коры;
классическую (дискинетическую) форму, представляющую собой сочетание пирамидных и экстрапирамидных симптомов со слабоумием (деменцией);
промежуточную форму болезни Крейтцфельдта — Якоба, характеризующуюся преобладанием мозжечковых и подкорковых расстройств; амиотрофическую форму, двигательные и речевые расстройства при которой напоминают клинику бокового амитрофического склероза.
Слайд 44
Симптомы болезни Крейтцфельдта-Якоба
В большинстве случаев болезнь Крейтцфельдта-Якоба характеризуется постепенным
развитием, однако возможно подострое или острое начало. Примерно в 30%
случаев болезнь Крейтцфельдта-Якоба начинается с продромальных симптомов: раздражительности, рассеянности, головных болей, нарушения сна, головокружения, ухудшения памяти, снижения зрения, безынициативности, снижения либидо, изменения поведенческих реакций. Возможно эпизодическое возникновение эйфории и/или беспричинного страха, отрывистые бредовые или галлюцинаторные переживания. Из неврологических нарушений в продромальном периоде наблюдаются: шаткость во время ходьбы, парестезии, расстройство высших функций коры головного мозга (алексия, акалькулияи пр.). Описаны несколько случаев, когда болезнь Крейтцфельдта-Якоба дебютировала с появления корковой слепоты.
В стадии развернутых клинических проявлений болезнь Крейтцфельдта-Якоба характеризуется прогрессирующим спастическим параличем (параплегией или гемиплегией), атаксией,э пилептическими припадками. Возникают экстрапирамидные нарушения: мышечная ригидность, атетоз, тремор. Практически у всех больных наблюдаются миоклонии — быстрые неритмичные сокращения отдельных мышц. Чаще всего отмечается миоклонус губы и века. Наблюдаются вторично генерализованные миоклонические приступы. Появляется и нарастает ярко выраженная деменция, сопровождающаяся нарушениями речи вплоть до ее полного распада. Новый вариант болезни Крейтцфельдта-Якоба отличается преобладанием психиатрической симптоматики и расстройств чувствительности. В 100% случаев он сопровождается мозжечковыми нарушениями, в то время как при спорадической болезни Крейтцфельдта-Якоба расстройства функции мозжечка наблюдаются лишь в 40% случаев.
В терминальной стадии болезнь Крейтцфельдта-Якоба характеризуется глубокой деменцией. Пациенты не контактны, находятся в состоянии прострации, утрачен контроль над функцией тазовых органов. Наблюдаются гиперкинезы, выраженные мышечные атрофии, нарушения глотания, пролежни. Возможна гипертермия и эпилептические приступы. Смерть наступает в коматозном состоянии на фоне децеребрационной ригидности и выраженной кахексии.