единой горсти – бесконечность
И небо - в чашечке цветка.
Уильям Блейк (1757-1827)“Отыщи всему начало и ты многое поймёшь”.
(Козьма Прутков.)
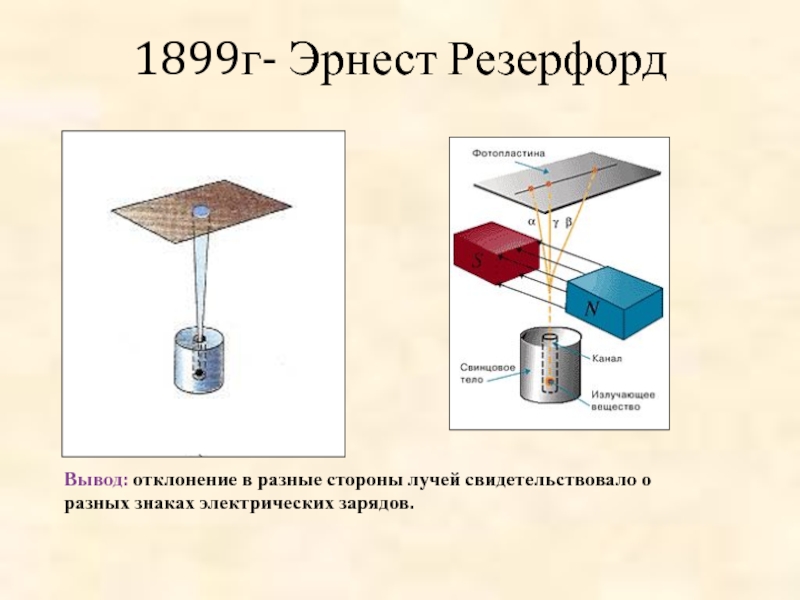
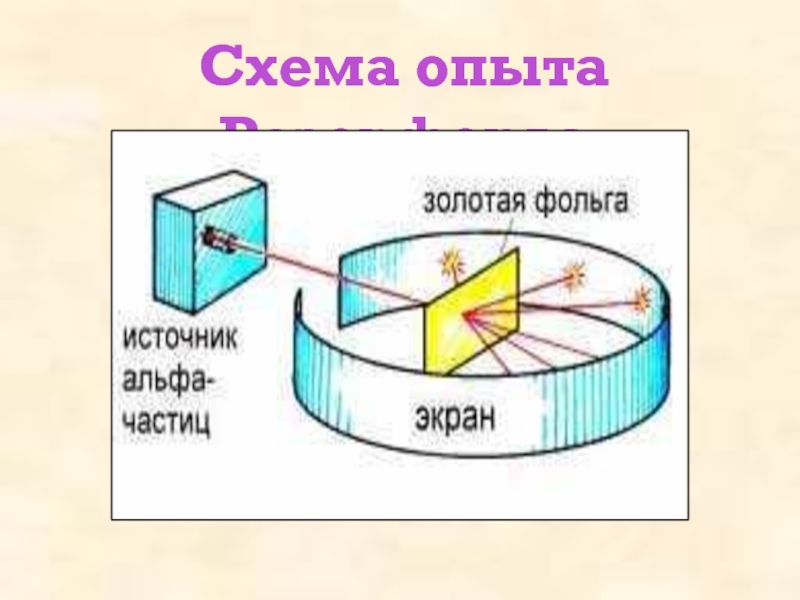
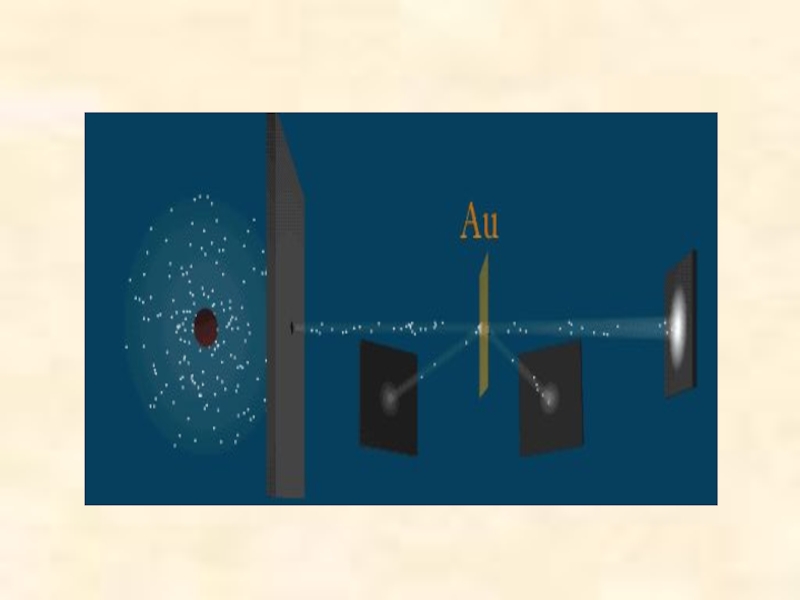
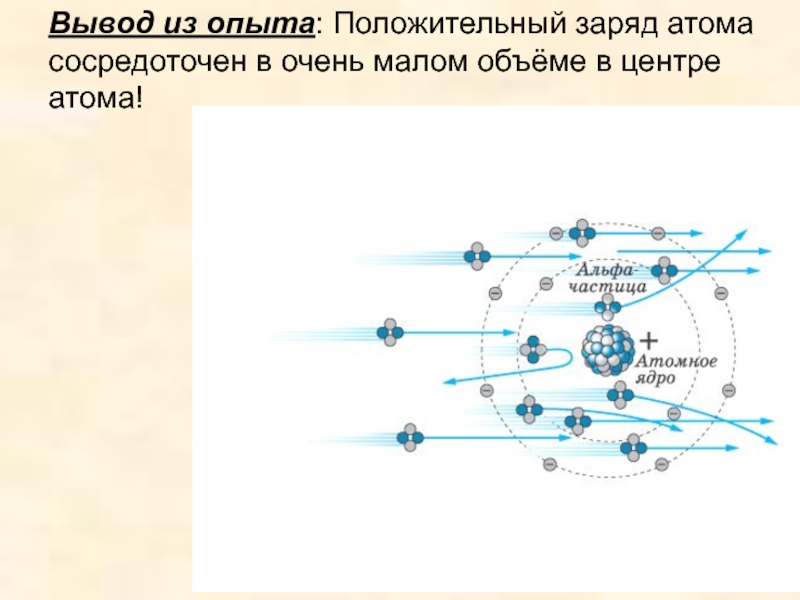
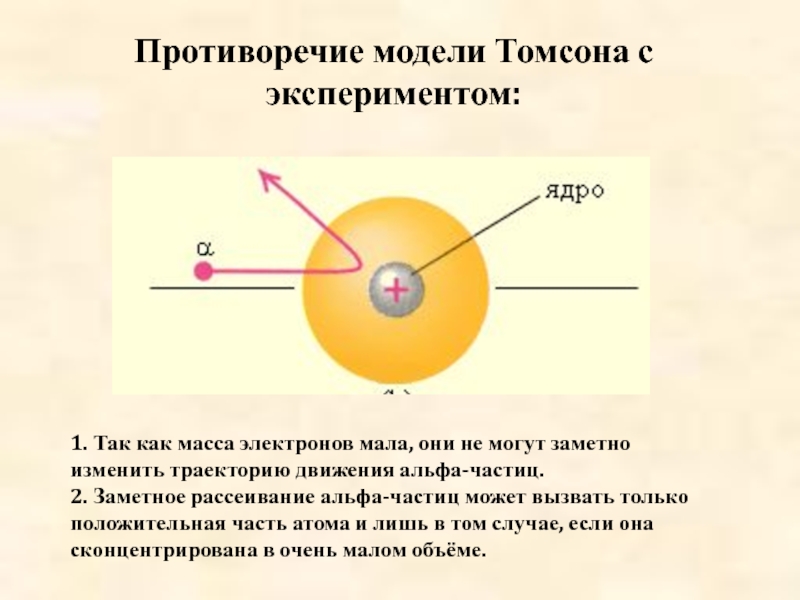
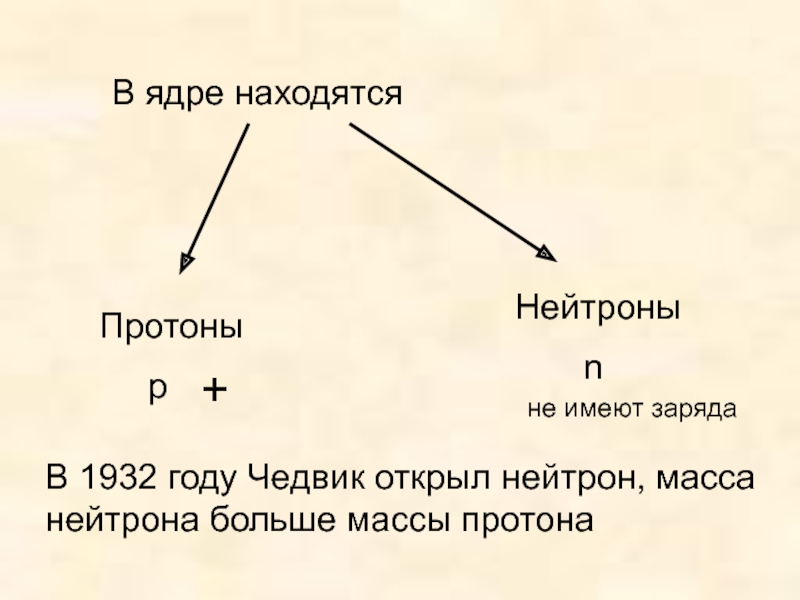
Тема урока: Опыт Резерфорда. Планетарная модель атома. Состав ядра.
Учитель физики сш № 31 пос. Жалагаш, Кызылординская область, Казахстан Иванченко Галина Николаевна.
2014 г