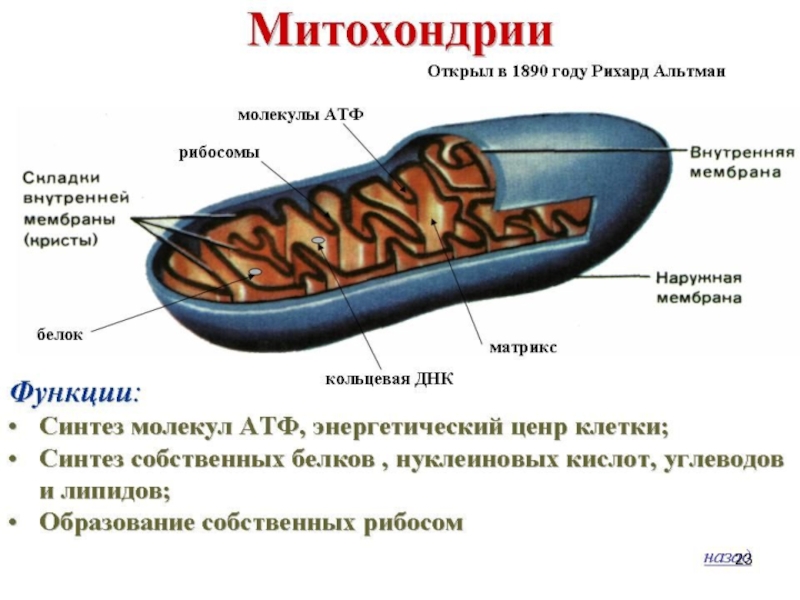
Слайд 1Введение в обмен веществ
Занятие 5
Слайд 2Обмен веществ и энергии — совокупность процессов превращения веществ и
энергии, происходящих в живых организмах, и обмен веществами и энергией
между организмом и окружающей средой.
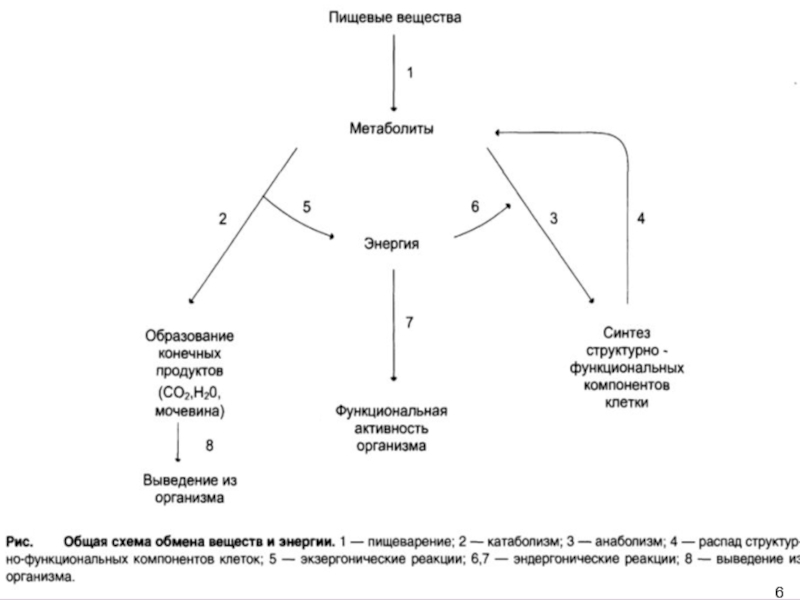
Обмен веществ и энергии является основой жизнедеятельности организмов и принадлежит к числу важнейших специфических признаков живой материи, отличающих живое от неживого. В обмене веществ, или метаболизме, обеспеченном сложнейшей регуляцией на разных уровнях, участвует множество ферментных систем.
В процессе обмена поступившие в организм вещества превращаются в собственные вещества тканей и в конечные продукты, выводящиеся из организма. При этих превращениях освобождается и поглощается энергия.
Слайд 3Метаболизм
Метаболические пути
Слайд 4Метаболизм — совокупность химических реакций, протекающих в клетках организма с
момента поступления пищевых веществ в организм до образования конечных продуктов
обмена.
Функции метаболизма:
▪cнабжение клеток химической энергией;
▪превращение молекул пищи в строительные блоки;
▪сборка из этих блоков компонентов клетки (белки, липиды, нуклеиновые кислоты);
▪синтез и разрушение специализированных биологических молекул (гем, холин).
Метаболический путь — последовательность химических превращений вещества. Метаболические пути многоэтапны, взаимосвязаны, регулируемы, скоординированы в пространстве. Они бывают линейными (распад и синтез гликогена, гликолиз и др.) и циклическими (цикл трикарбоновых кислот, орнитиновый цикл).
Метаболические пути делятся на:
1. катаболические, которые включают реакции расщепления биомолекул (гидролиза, окисления и др.);
2. анаболические, которые состоят из реакций синтеза сложных соединений (белков, полисахаридов, нуклеиновых кислот);
3. амфиболические; метаболиты этих процессов могут превращаться как в катаболических,так и в анаболических процессах. Примером является цикл трикарбоновых кислот.

Слайд 7Специфические и общие пути катаболизма
В катаболических процессах можно выделить
два звена:
- специфические пути катаболизма, разные для
различных классов соединений (белков, жиров, углеводов и др.)
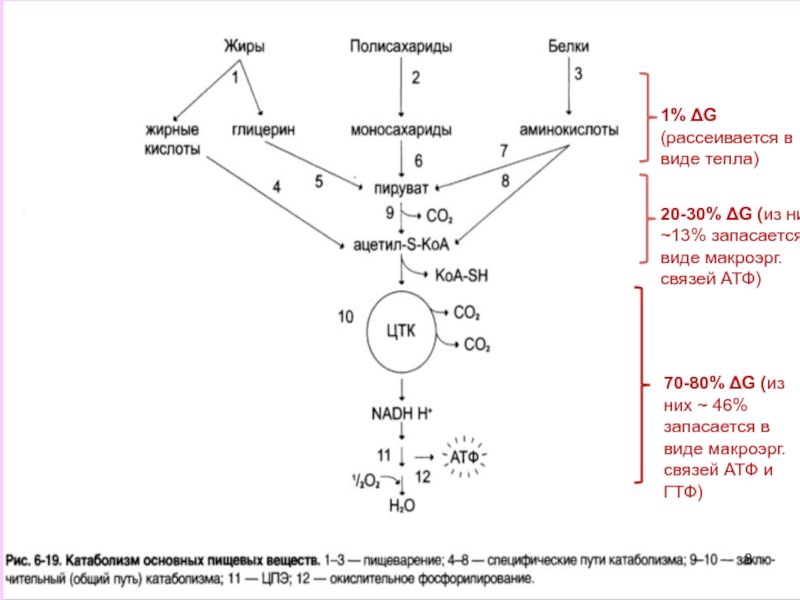
К специфическим путям катаболизма относятся реакции гидролиза белков, углеводов, липидов происходящие в ЖКТ или в тканях, реакции разрушения моносахаридов, аминокислот, жирных кислот, спиртов, происходящие в клетках и, в конце концов, завершающиеся образованием пировиноградной кислоты или ацетильным радикалом в форме ацетил-КоА.
- общие пути катаболизма - единые пути катаболизма для различных классов веществ, являющиеся продолжением специфических путей. С общими путями катаболизма, в основном, связаны главные биоэнергетические процессы, сопряженные с высвобождением и накоплением энергии в клетке.
Слайд 81% ΔG (рассеивается в виде тепла)
70-80% ΔG (из них ~
46% запасается в виде макроэрг. связей АТФ и ГТФ)
20-30% ΔG (из них ~13% запасается в виде макроэрг. связей АТФ)
Слайд 9Катаболизм и анаболизм происходят в клетках одновременно и неразрывно связаны
друг с другом. По существу, их следует рассматривать не как
два отдельных процесса, а как две стороны одного общего процесса — метаболизма, в котором превращения веществ теснейшим образом переплетены с превращениями энергии.
Процессы анаболизма и катаболизма находятся в организме в состоянии динамического равновесия.
Преобладание анаболических процессов над катаболическими приводит к росту, накоплению массы тканей, а преобладание катаболических процессов ведет к частичному разрушению тканевых структур.
Состояние равновесного или неравновесного соотношения анаболизма и катаболизма зависит от возраста (в детском возрасте преобладает анаболизм, у взрослых обычно наблюдается равновесие, в старческом возрасте преобладает катаболизм), состояния здоровья, выполняемой организмом физической или психоэмоциональной нагрузки.
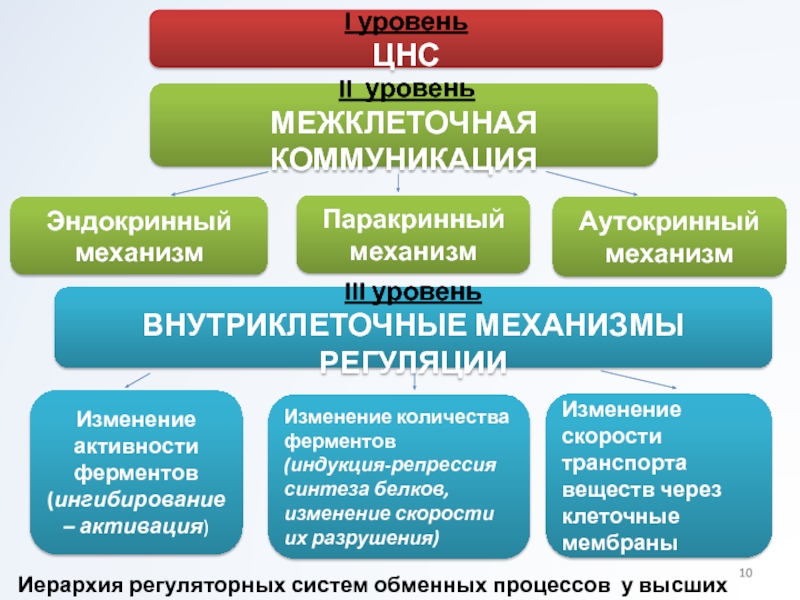
Слайд 10 II уровень
МЕЖКЛЕТОЧНАЯ КОММУНИКАЦИЯ
III уровень
ВНУТРИКЛЕТОЧНЫЕ МЕХАНИЗМЫ РЕГУЛЯЦИИ
I уровень
ЦНС
Эндокринный механизм
Паракринный механизм
Аутокринный
механизм
Изменение активности ферментов
(ингибирование – активация)
Изменение количества ферментов
(индукция-репрессия синтеза
белков, изменение скорости их разрушения)
Изменение скорости транспорта веществ через клеточные мембраны
Иерархия регуляторных систем обменных процессов у высших организмов
Слайд 12К энергетическим субстратам для клеток животного организма относятся углеводы, липиды
и аминокислоты. Удельная калорийность углеводов равна 4,1 ккал/г, липидов -
9,3 ккал/г и белков (аминокислот) - 4,1 ккал/г.
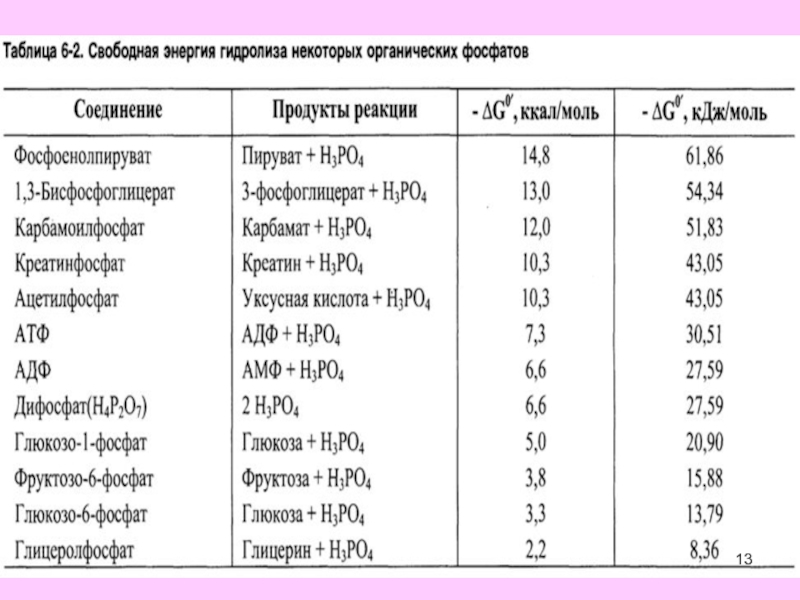
Высвобождение свободной энергии из основных энергетических субстратов идет в катаболических процессах. При этом свободная энергия может накапливаться в макроэргической связи некоторых фосфорорганических соединений, в маркоэргах.
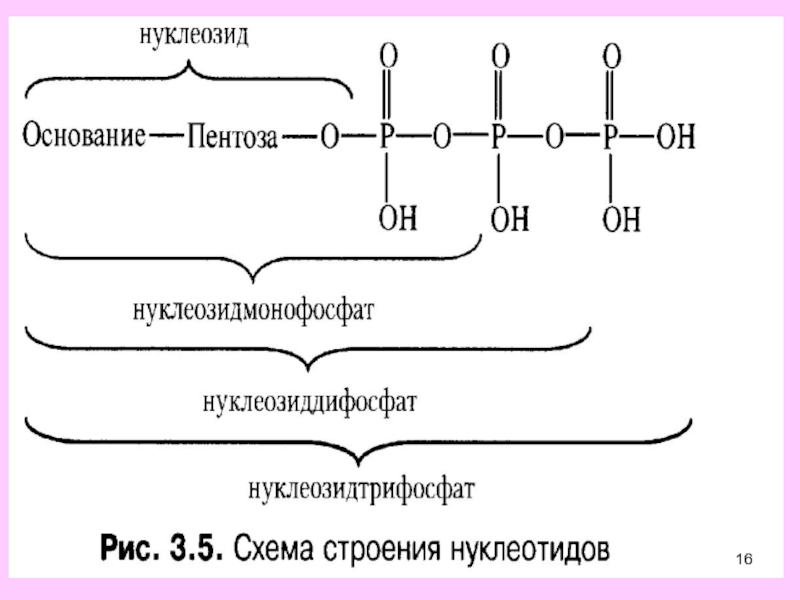
К макроэргическим соединениям относятся АТФ и другие нуклеотид-5`-трифосфаты (ГТФ, УТФ, ЦТФ), креатинфосфат, 1,3-дифосфоглицерат, фосфоенол-пируват.
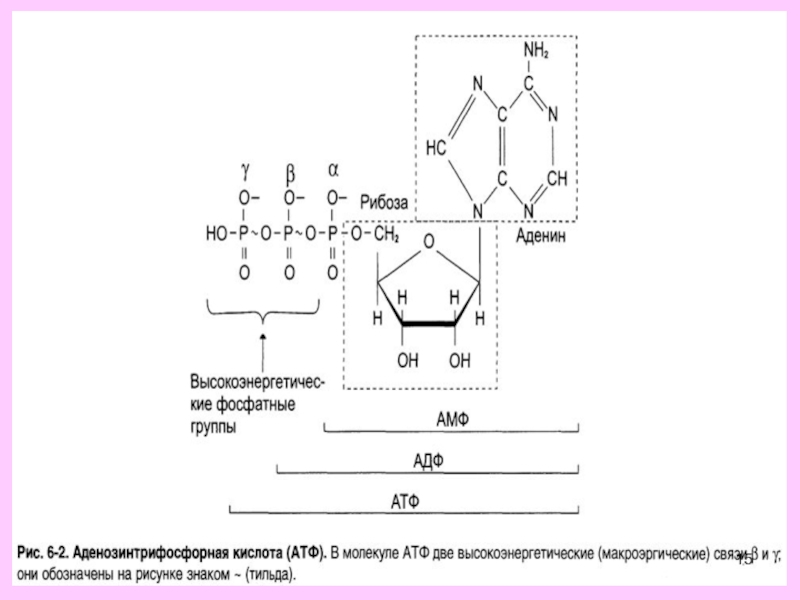
Слайд 14Из всех макроэргов АТФ - главный химический посредник клетки, связывающий
между собой процессы идущие с выделением и поглощением энергии (катаболизма
и анаболизма), служит общим промежуточным продуктом в реакциях переноса энергии с фосфатными группами.
Будучи макроэргическим соединением, АТФ выполняет функцию аккумулирования биологической энергии и ее последующего использования для выполнения клеточных функций.
«Макроэргичность» АТФ объясняется рядом особенностей его молекулы. Это прежде всего высокая плотность зарядов, сконцентрированная в «хвосте» молекулы, обеспечивающая легкость диссоциации терминального фосфата при водном гидролизе. Продукты этого гидролиза представляют собой АДФ и неорганический фосфат и далее – АМФ и неорганический фосфат. Это обеспечивает высокую величину свободной энергии гидролиза терминального фосфата АТФ в водной среде.
NB! В клетке молекула АТФ расходуется в течение одной минуты после её образования. У человека количество АТФ, равное массе тела, образуется и разрушается каждые 24 ч.
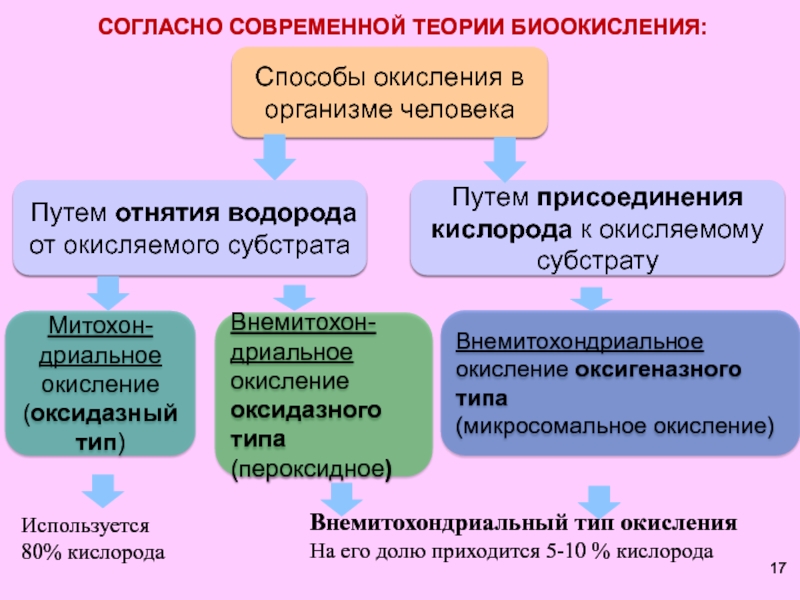
Слайд 17СОГЛАСНО СОВРЕМЕННОЙ ТЕОРИИ БИООКИСЛЕНИЯ:
Способы окисления в организме человека
Путем отнятия водорода
от окисляемого субстрата
Митохон-дриальное
окисление
(оксидазный тип)
Внемитохон-дриальное
окисление
оксидазного типа
(пероксидное)
Путем присоединения кислорода к окисляемому
субстрату
Внемитохондриальное
окисление оксигеназного
типа
(микросомальное
окисление)
Используется
80% кислорода
Внемитохондриальный тип окисления
На его долю приходится 5-10 % кислорода
Слайд 18НАДФН・Н+
S – ОН
Н+ ē
ФАД
ē
цит Р450
2 Н+
S – H
О2
Н20
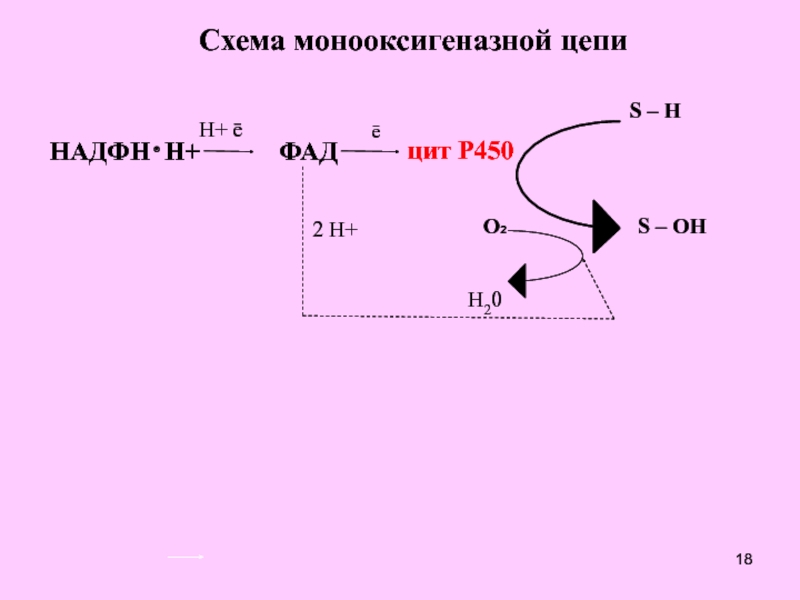
Схема монооксигеназной цепи
Слайд 19Тканевое дыхание
и
биологическое окисление
Слайд 20Тканевое дыхание, клеточное дыхание – процесс поглощения кислорода (О2) тканями
при окислении органического субстрата с выделением углекислого газа (СО2) и
воды (Н2О).
Тканевое дыхание – совокупность ферментативных процессов, протекающих при участии кислорода воздуха в клетках органов и тканей, в результате чего продукты расщепления углеводов, жиров, белков окисляются до углекислого газа и воды. При этом часть освобождающейся энергии запасается в форме макроэргических соединений. Многие ферменты, катализирующие эти реакции, находятся в особых клеточных органоидах — митохондриях.
[Тканевое дыхание отличают от внешнего дыхания — совокупности физиологических процессов, обеспечивающих поступление в организм кислорода и выведение из него углекислого газа.]
Биологическое окисление — это процесс окисления биологических веществ с выделением энергии.
Биологическое окисление — совокупность окислительно-восстановительных реакций катаболизма органических соединений, сопряженных с высвобождением свободной энергии, катализируемых локализованными в митохондриях ферментами класса оксидоредуктаз.

Слайд 21Аэробное окисление намного эффективнее анаэробного. В первом случае, где глюкоза
"сжигается" до CO2 и воды, из 1 молекулы глюкозы образуется
36 молекул АТФ, а во втором — 2. Это и объясняет широкое распространение и бурную эволюцию аэробных организмов.
При биологическом окислении от органической молекулы под действием соответствующего фермента отщепляются два атома водорода.
Дальнейшая судьба водорода может быть различной. При анаэробном окислении он переносится на некоторые органические молекулы. При аэробном окислении водород передаётся на кислород с образованием воды. Основная часть цепи переноса водорода расположена в мембранах митохондрий. При этом из АДФ и неорганического фосфата образуется АТФ.
Слайд 22Механизм биологического окисления
Основной функцией этого процесса является обеспечение организма энергией
в доступной для использования форме (прежде всего в форме АТФ).
Основным топливом при биологическом окислении является ВОДОРОД.
Известно, что реакция окисления водорода кислородом в газовой среде сопровождается выделением большого количества энергии, сопровождаемым взрывом и пламенем. Эволюция живых организмов привела к тому, что реакция окисления водорода до воды оказалась разделенной на отдельные этапы, что обеспечивает постепенное высвобождение энергии в процессе биологического окисления. При этом часть полученной энергии рассеивается в виде тепла (около 60%) а другая часть (около 40%) аккумулируется в молекулах АТФ.
Слайд 24Основной функцией биологического окисления является обеспечение организма энергией в доступной
для использования форме (прежде всего в форме АТФ).
В переносе
электронов от субстратов к молекулярному кислороду принимают участие:
1.Пиридинзависимые анаэробные дегидрогеназы, для которых коферментами служат либо НАД, либо НАДФ
2.Флавинзависимые аэробные дегидрогеназы, у которых коферментом является ФАД или ФМН;
3.Убихинон (коэнзим Q) и белки, содержащие негемовое железо
4.Цитохромы, содержащие в качестве коферментов используются железопорфирины
(гем и его производные).
Слайд 25Пиридинзависимые анаэробные дегидрогеназы
Эти ферменты катализируют реакции переноса атомов водорода (протоны
и электроны) на любой акцептор кроме кислорода
Представители:
Пируват
дегидрогеназа
Альфа-кетоглутаратдегидрогеназа
Изоцитрат дегидрогеназа
Малат дегидрогеназа
Коферментом этих ферментов являются НАД, НАДФ- производные витамина РР ( В5- никотиновая кислота)
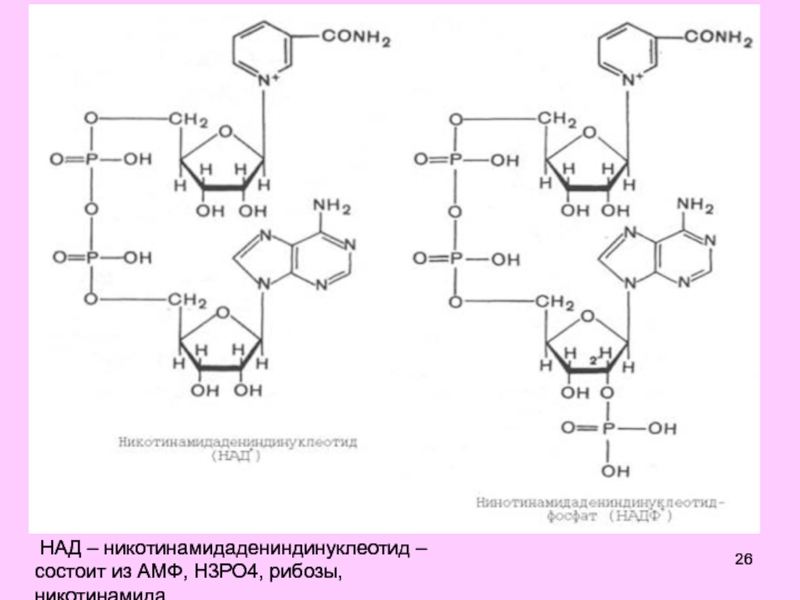
Слайд 26 НАД – никотинамидадениндинуклеотид – состоит из АМФ, Н3РО4, рибозы,
никотинамида
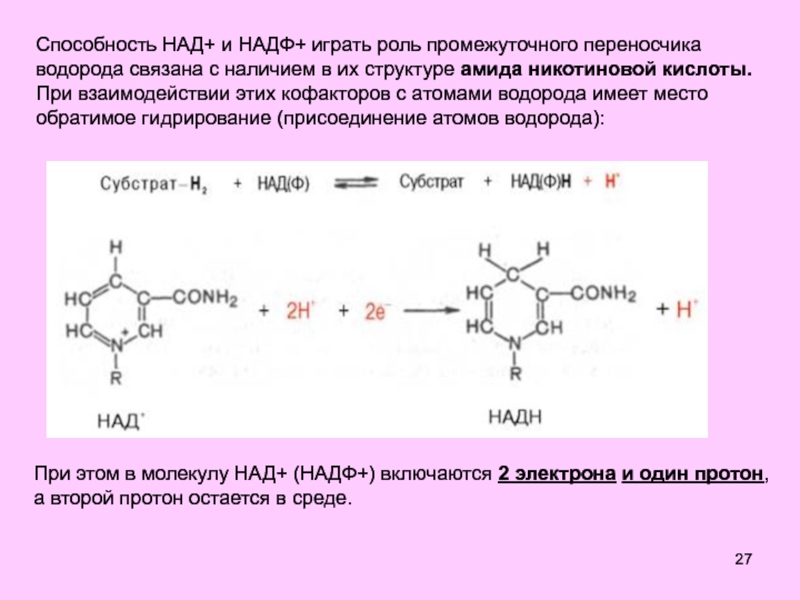
Слайд 27Способность НАД+ и НАДФ+ играть роль промежуточного переносчика водорода связана
с наличием в их структуре амида никотиновой кислоты. При взаимодействии
этих кофакторов с атомами водорода имеет место обратимое гидрирование (присоединение атомов водорода):
При этом в молекулу НАД+ (НАДФ+) включаются 2 электрона и один протон, а второй протон остается в среде.
Слайд 28АЭРОБНЫЕ ДЕГИДРОГЕНАЗЫ
Эти ферменты катализируют реакции переноса атомов водорода (протоны и
электроны) на любой акцептор, в том числе и на кислород
Представители:
сукцинатдегидродгеназа
глицерофосфатдегидрогеназа
ацил-КоА-дегидрогеназа
Коферментами этих ферментов являются ФАД, ФМН- производные витамина В2 ( рибофлавин)
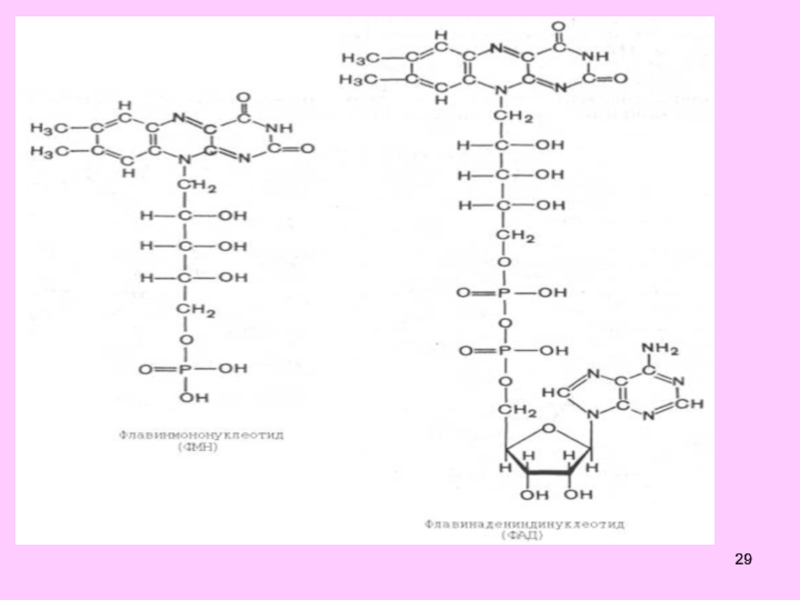
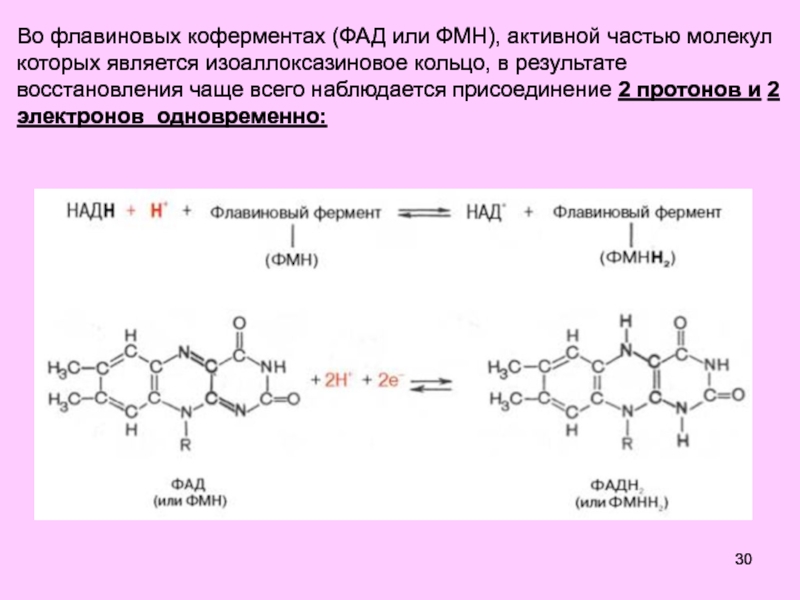
Слайд 30Во флавиновых коферментах (ФАД или ФМН), активной частью молекул которых
является изоаллоксазиновое кольцо, в результате восстановления чаще всего наблюдается присоединение
2 протонов и 2 электронов одновременно:
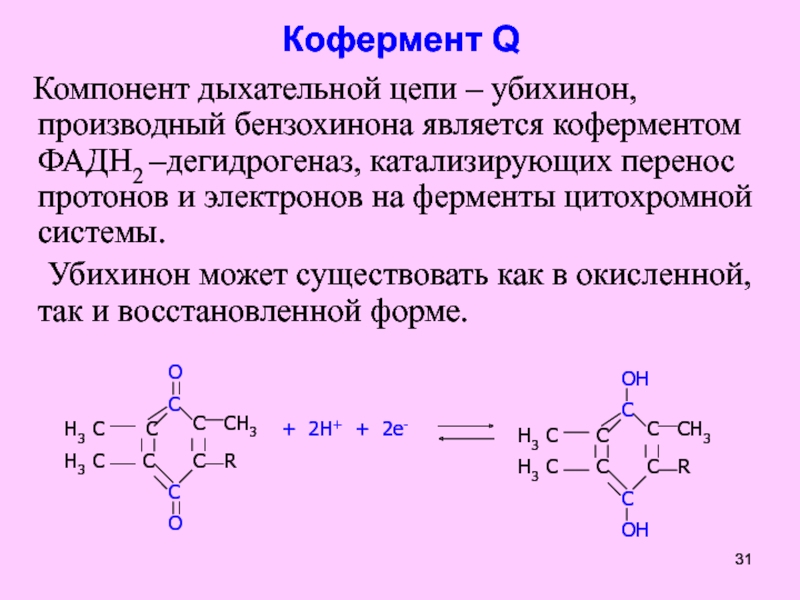
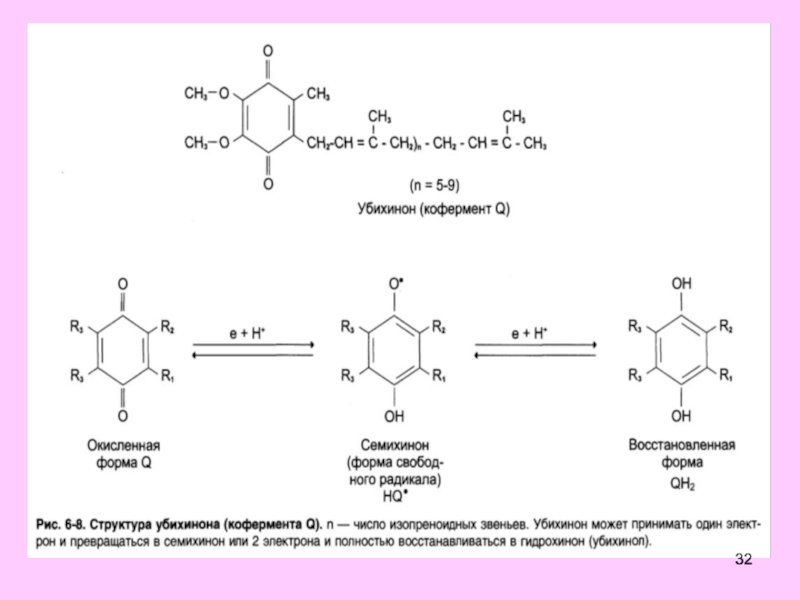
Слайд 31Кофермент Q
Компонент дыхательной цепи – убихинон, производный бензохинона
является коферментом ФАДН2 –дегидрогеназ, катализирующих перенос протонов и электронов на
ферменты цитохромной системы.
Убихинон может существовать как в окисленной, так и восстановленной форме.
С
С
С
С
С
С
О
O
H3
H3
С СН3
С R
С
С
С
С
С
С
ОH
OH
H3
H3
С СН3
С R
+ 2H+ + 2е-
Слайд 33ЦИТОХРОМЫ
Дальнейший перенос электронов от убихинона на кислород осуществляет система цитохромов:
b, c1, c, a- a3.
Все они имеют в качестве кофермента геминовую группу.
В ходе каталитического процесса валентность содержащегося в цитохромах железа обратимо изменяется:
Fe++ Fe+++
Величины окислительно-восстановительного потенциала у разных цитохромов неодинаковы. В цепи окисления они располагаются между убихиноном и кислородом :
b С1 С aa3
Цитохромы b, c1, c выполняют функцию промежуточных переносчиков электронов, а цитохром аа3 является терминальным дыхательным ферментом, непосредственно взаимодействующим с кислородом.
Представители цитохромов: аскорбат ДГ, адреналин ДГ, норадреналин ДГ.
Слайд 34СТРУКТУРА ДЫХАТЕЛЬНОЙ ЦЕПИ
Перенос электронов и протонов в митохондриальной дыхательной цепи
происходит по градиенту их окислительно-восстановительного потенциала (редокс-потенциал), который отражает величину
свободной энергии в соответствии с редокс-системой.
Каждый фермент дыхательной цепи имеет свою величину редокс-потенциала. Его величина возрастает от НАД (-0,32в) до О2(+0,82в) и общая разность редокс-потенциала между ними равна 1,14 Вольт.
Такое количество энергии, освобождаемой при окислении 1 молекулы субстрата НАДН2 –дегидрогеназами, достаточно для синтеза трех молекул АТФ.
В дыхательной цепи имеются 3 участка, в которых энергии разности редокс-потенциалов достаточно для фосфорилирования (присоединения фосфорной кислоты) 3-х молекул АДФ, с образованием 3 молекул АТФ
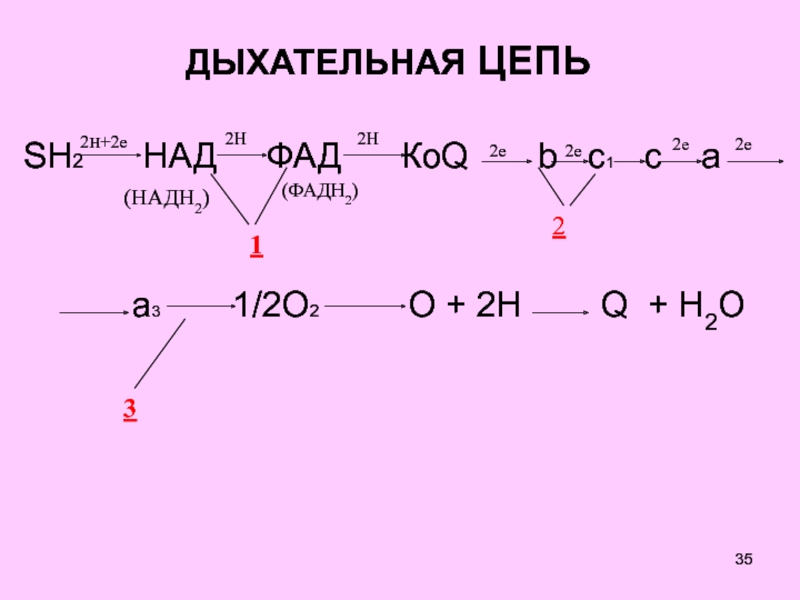
Слайд 35ДЫХАТЕЛЬНАЯ ЦЕПЬ
SH2 НАД ФАД
КоQ b c1 c
a
a3 1/2O2 O + 2H Q + H2O
2н+2е
(НАДН2)
(ФАДН2)
2е
2е
2е
2е
2Н
2Н
1
2
3
Слайд 36ДЫХАТЕЛЬНАЯ ЦЕПЬ И РЕДОКС ПОТЕНЦИАЛ
Слайд 37ПУНКТЫ ФОСФОРИЛИРОВАНИЯ
Первый пункт фосфорилирования находится между ферментами НАД и ФАД,
где разность их потенциала равна 0,246
АДФ + Н3РО4 АТФ
Второй пункт – между цитохромами В и С1, где разность их потенциала равна 0,19
АДФ + Н3РО4 АТФ
Третий пункт - между цитохромами аа3 и 1/2О2, где разность их потенциала равна 0,30 Вольт.
АДФ + Н3РО4 АТФ
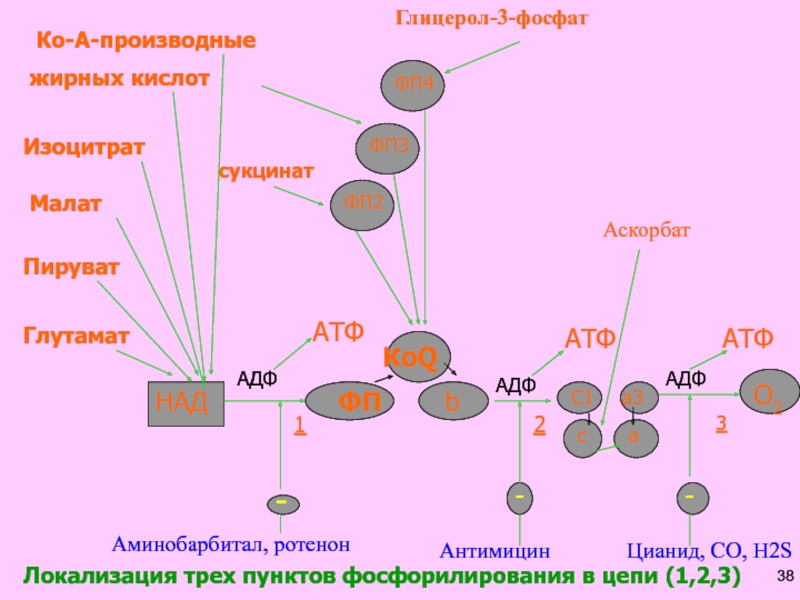
Слайд 38 Ко-А-производные
жирных кислот
Изоцитрат
Малат
Пируват
Глутамат
НАД
ФП
b
КоQ
АТФ
АДФ
-
Аминобарбитал, ротенон
ФП2
ФП3
ФП4
Глицерол-3-фосфат
сукцинат
АДФ
АТФ
C1
c
a3
a
Антимицин
-
Аскорбат
О2
-
Цианид, СО, Н2S
АДФ
АТФ
1
2
3
Локализация трех пунктов фосфорилирования в
цепи (1,2,3)
Слайд 39Окислительное фосфорилирование
При окислении одной молекулы субстрата на один атом поглощенного
митохондриями кислорода может использоваться от одной до трех молекул фосфорной
кислоты и синтезироваться при этом 1, 2 или 3 молекулы АТФ.
Это процесс - процесс синтеза АТФ в реакциях биологического окисления субстратов получил название - окислительное фосфорилирование.
Для его количественной оценки был введен показатель окислительного фосфорилирования - коэффициент Р/О .
Коэффициент Р/О (АДФ/О) - это есть отношение количества молекул фосфорной кислоты (АДФ) к количеству атомов кислорода, использованных митохондриями при окислении какого-либо субстрата.
Слайд 40
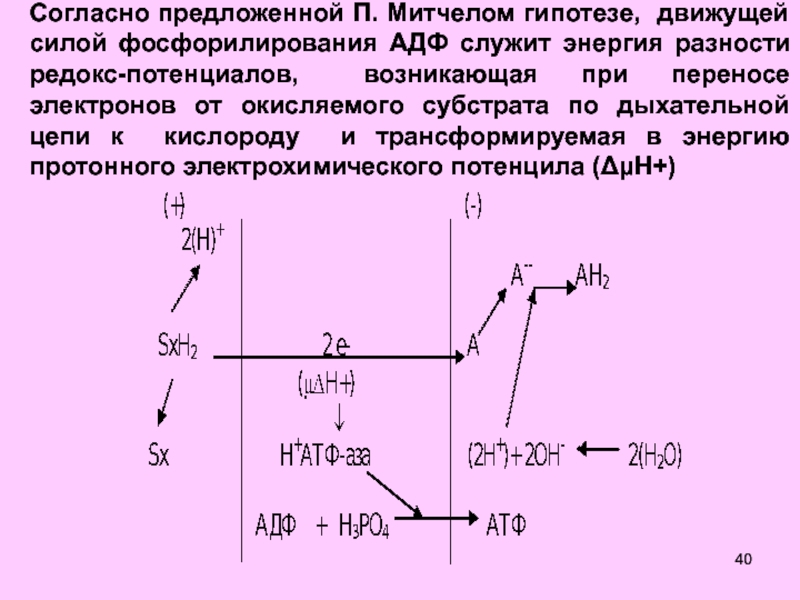
Согласно предложенной П. Митчелом гипотезе, движущей силой фосфорилирования АДФ служит
энергия разности редокс-потенциалов, возникающая при переносе электронов от
окисляемого субстрата по дыхательной цепи к кислороду и трансформируемая в энергию протонного электрохимического потенцила (H+)
Слайд 41Основные постулаты хемиоосмотической теории Митчелла (Нобелевская премия 1978 г.).
▪внутренняя митохондриальная
мембрана (ВММ) непроницаема для ионов, в частности для Н+ и
ОН-;
▪за счет энергии транспорта электронов через I, III и IV комплексы дыхательной цепи из матрикса выкачиваются протоны;
▪возникающий на мембране электрохимический потенциал (ЭХП) и есть промежуточная форма запасания энергии;
▪возвращение (транслокация) протонов в матрикс митохондрии через протонный канал протонной АТФ-синтазы за счет ЭХП является движущей силой синтеза АТФ.
Слайд 42Таким образом, тканевой дыхание «заряжает» митохондриальную мембрану, а окислительное фосфорилирование
«разряжает» ее.
Разность электрических потенциалов на митохондриальной мембране, создаваемая дыхательной цепью,
которая выступает в качестве молекулярного проводника электронов, является движущей силой образования АТФ и других видов полезной биологической энергии.
Слайд 43Протонный (трансмембранный ) электрохимический потенциал (H+)
Трансмембранный электрохимический потенциал, возникающий
на мембране за счет Н+-градиента, является универсальной формой энергии в
клетке и может быть использован:
- для синтеза АТФ
- для транспорта ионов Са и других ионов
- для транспорта фосфатов
- для транспорта АДФ и АТФ
- для теплообразования
- для сократительной и двигательной активности
Слайд 44Дыхательный контроль
Окислительное фосфорилировние контро-лирует скорость биологического окисления, осуществляя так называемый
дыхательный контроль.
Дыхательный контроль – это свойство неповрежденных митохондрий. При
наличии всех компонентов биологического окисления, но при отсутствии АДФ скорость биологического окисления замедляется. При большом количестве АДФ и малом содержании АТФ скорость биологического окисления увеличивается.
Слайд 45Дыхательный контроль
Дыхательный контроль – это прямое влияние электрохимического градиента на
скорость движения электронов по дыхательной цепи (т.е. на величину дыхания).
В свою очередь, величина градиента напрямую зависит от соотношения АТФ и АДФ, количественная сумма которых в клетке практически постоянна ([АТФ] + [АДФ] = const). Реакции катаболизма направлены на поддержание постоянно высокого уровня АТФ и низкого АДФ.
Возрастание протонного градиента возникает при снижении количества АДФ и накоплении АТФ (состояние покоя), т.е. когда АТФ-синтаза лишена своего субстрата и ионы Н+ не проникают в матрикс митохондрии. При этом ингибирующее влияние градиента усиливается и продвижение электронов по цепи замедляется. Ферментные комплексы остаются в восстановленном состоянии. Следствием является уменьшение окисления НАДН и ФАДН2 на I и II комплексах и замедление катаболизма в клетке.
Снижение протонного градиента возникает при исчерпании резервов АТФ и избытке АДФ , т.е. при работе клетки. В этом случае активно работает АТФ-синтаза и через канал Fо проходят в матрикс ионы Н+. При этом градиент, естественно, снижается, поток электронов возрастает, в результате повышается выкачивание ионов Н+ в межмембранное пространство и снова их быстрое "проваливание" через АТФ-синтазу внутрь митохондрий с синтезом АТФ. Ферментные комплексы I и II усиливают окисление НАДН и ФАДН2 (как источников электронов) и снимается ингибирующее влияние НАДН на цикл лимонной кислоты и пируватдегидрогеназный комплекс. Как итог – активируются реакции катаболизма углеводов и жиров.