Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Алюминий ?осылысы
Содержание
- 1. Алюминий ?осылысы
- 2. Білімділік – алюминийдің табиғатта кездесуі, негізгі қасиеттері,
- 3. Сабақтың типі: Жаңа білімді қалыптастыруСабақтың түрі:
- 4. Сабақтың барысы: І. Ұйымдастыру кезеңі:
- 5. 1.Кальцийдің табиғи қосылыстары СаSO4*2H2O –
- 6. “Қарлы кесек”(оқыта үйрету ойыны)АВС
- 7. «А» ТОБЫНЫҢ ЕСЕПТЕРІ СаСІ2 + Na3PO4
- 8. «В» ТОБЫНЫҢ ЕСЕПТЕРІ Ca + CI2 →
- 9. «С» ТОБЫНЫҢ ЕСЕПТЕРІ АІ2О3
- 10. Болмасам да айтарлықтай салмағым,Мен көбіңнен ардақтымынҰшақ болып
- 11. Алюминийдің тұрмыстағы маңызы...(ой қозғау)
- 12. ІІІ. Жаңа сабақ1. Периодтық жүйедегі орны2. Атом құрылысы3. Химиялық қасиеттері4. Физикалық қасиеттері5.Маңызды қосылыстары6.Қазақстанда таралу аймағы
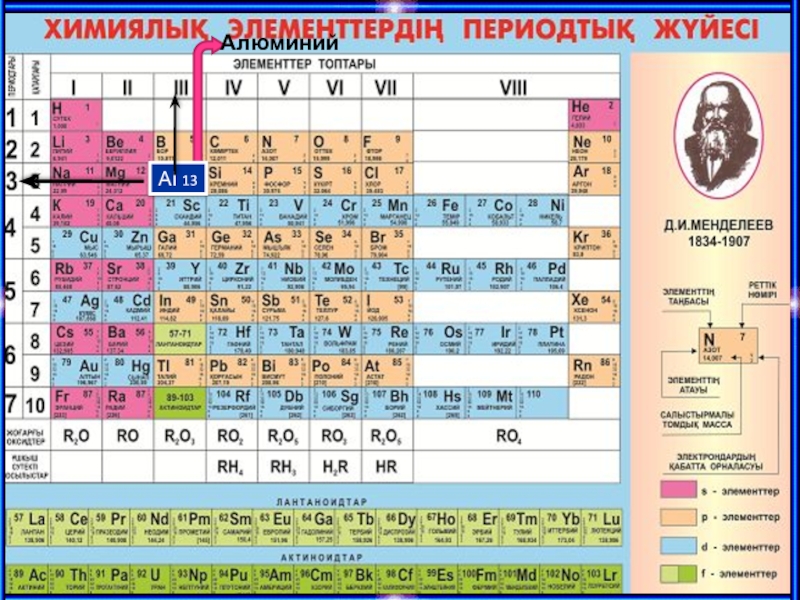
- 13. АІ 13 Алюминий
- 14. Алюминий Al 27+130283P = 13e = 13N
- 15. Химиялық қасиеттеріЖай заттармен әрекеттесуі: 2 A1 +
- 16. Алюминий күмістей ақэлектр өткізгіш құралдар жасауға кең
- 17. Al₂O₃- қиын балқитын, ақ түсті зат. Табиғатта
- 18. Al қолданылуы
- 19. Бұрын алу әдісі өте қиын болғандықтан, алюминий
- 20. МЕТАЛДАР ҚОСЫЛЫСТАРЫНЫҢ ҚАЗАҚСТАН АЙМАҒЫНДА ТАРАЛУЫ
- 21. Сергіту сәті3 – 15 арасында бір сан
- 22. Терең ой (Оқулықпен жұмыс)“В” тобы №2 есеп
- 23. Химиялық жәрмеңке(Жаңа сабақты меңгерту)
- 24. Каструл сұрағыАлюминийдің периодтық жүйедегі орнына сипаттама беріңіз
- 25. Александрит сақинаАлюминий бейметалдармен оның ішінде оттекпен
- 26. Ыдыс – аяқтар сұрағыАлюминий металын екідайлы металдар қатарына қосамыз неліктен?
- 27. Қызыл сафир сақина 18 ғасырда өмір
- 28. Сусын Алюминийдің оксиді қалай аталады?.
- 29. Құрылыс материалыАлюминий гидроксиді қандай зат?Формуласын жаз
- 30. Сафир сақинаАлюминийдің атомдық құрылысын жаз?
- 31. Мағынаны тануЖаңа сабақты бекіту Аты жөні:Туған жылы:Жасы: Мекен-жайы:Отбасы құрамы:Тегі:Сыртқы келбеті:Мінезі:Достары:Достарының аттары:Пайдасы:Туыстары:
- 32. Аты жөні: АлюминийТуған жылы: 1825
- 33. АлюминийКальцийБейне сурет сұрақтарҚай металдың минералдары
- 34. Бейне сурет сұрақтарАлюминийКальций«Венн диаграммасы»Қорытынды.Калций – адам ағза-сында
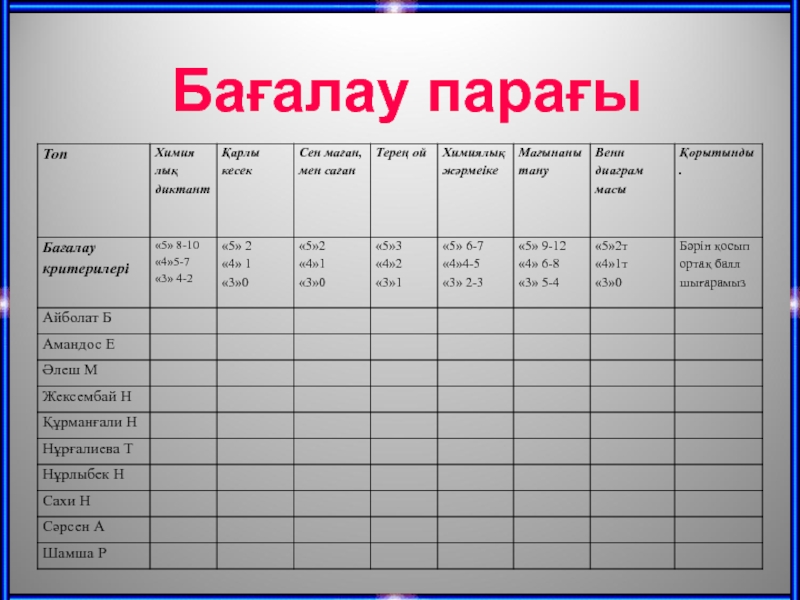
- 35. Бағалау: Кесте бойынша Үйге тапсырма: пар 38.39 “С” 2,3 есептері.
- 36. Бағалау парағы
- 37. Слайд 37
- 38. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1САБАҚТЫҢ ТАҚЫРЫБЫ:
Алюминий және оның маңызды қосылыстары және олардың Қазақстандағы таралу
аймағы.
Слайд 2Білімділік – алюминийдің табиғатта кездесуі, негізгі қасиеттері, алынуы, қолданылуы туралы
түсінік бере отырып, алюминий мен оның маңызды қосылыстарының мәнін ашу.
Дамытушылық
– оқушылардың зейінін,танымдық белсенділігін, өзіндік пікірін қалыптастыру, тұлғалық қасиеттерін дамыту.Тәрбиелік – сабақтың мазмұны бойынша алғырттыққа, өз бетінше жұмыс жүргізулеріне, ізденімпаздыққа және өзгенің пікірімен санасуға тәрбиелеу.
Сабақтың мақсаты :
Слайд 3 Сабақтың типі: Жаңа білімді қалыптастыру
Сабақтың түрі: Әңгімелесу, сұрақ –
жауап дәріс, ой дамыту
Сабақтың әдісі: ой қозғау, топтастыру,
Көрнекілігі: периодтық жүйе,
алюминий бұйымдары, интерактивті тақтаПән аралық байланыс: тарих, физика, география, технология.
Слайд 4Сабақтың барысы:
І. Ұйымдастыру кезеңі:
Сынып оқушыларымен
сәлемдесу, кезекші мәліметін тыңдау.
ІІ. Үй тапсырмасын сұрау.
1. Химиялық диктанты
2. “Қарлы
кесек” (оқыта үйрету ойын)3. “Сен маған, мен саған” (сұрақ – жауап)
Слайд 51.Кальцийдің табиғи қосылыстары СаSO4*2H2O –
доломит –
- Ca3(PO4)2, 2.Суға тұрақты кермектік беретін иондар иондар
3. Кальций оксиді – СаО – негіздік оксид.
4. Кальций қосылыстарында тотығу дәрежесін көрсетеді.
5. Суға кермектік қасиет беретін иондар тұздары.
6. Калций және магний суда ерігенде оған кермектік қасиет береді.
7. Судың кермектігі жалпы және болып бөлінеді.
8. Ғанышты сусыздандырғанда алебастр қалады
9. Кальцийдің биологиялық ролі – адам ағзасында, сүйек,
кеңінен кездеседі.
10. Уақытша кермектікті яғни иондарды жою үшін суды
( Химиялық диктант5
ғаныш
СаСО3*МgCO3
фосфорит
корбанатсыз
сөндірілмеген әк,
тұрақты +2
Са – Мg
тұздары
уақытша
тұрақты
қан ұюға
тіс ұлпаларында
корбанатты
қайнатады.
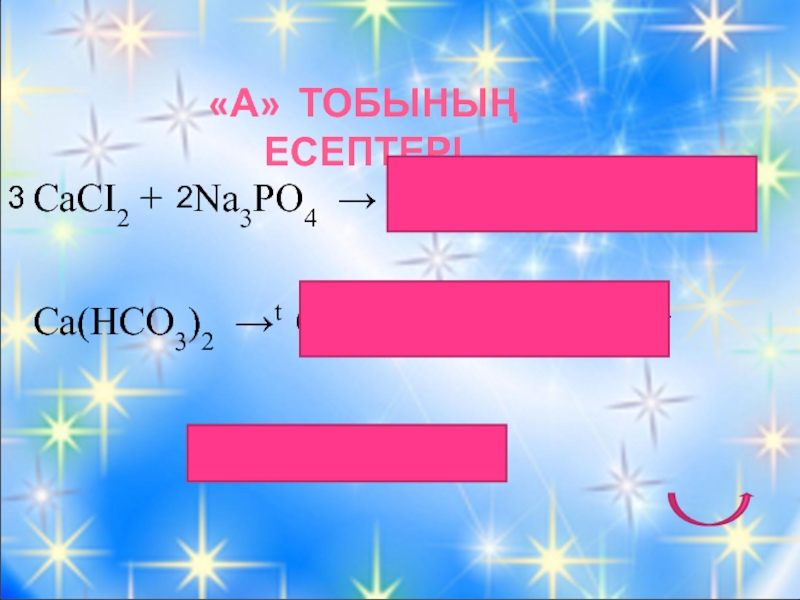
Слайд 7«А» ТОБЫНЫҢ ЕСЕПТЕРІ
СаСІ2 + Na3PO4 → Ca3(PO4)2↓ +
NaCI
Ca(HCO3)2 →t CaCO3↓ + CO2 + H2O↑
Судың кермектігі
3
6
2
3
Слайд 8«В» ТОБЫНЫҢ ЕСЕПТЕРІ
Ca + CI2 → CaCI2
Ca +
H2SO4 → CaSO4 + H2↑
Кальцийдің химиялық қасиеттері
Слайд 10
Болмасам да айтарлықтай салмағым,
Мен көбіңнен ардақтымын
Ұшақ болып аспанға ұшып қалықтап
Жердің
жүзін , көк аспанды шарладым.
Дуралюмин дейтін менің қоспамды,
Әспеттейді химияның
достары Тұрмыста үстел ыдыс-аяқ, кереует,
Бағандардың бұйдаларын қостым мен
Қағаз да мен кәмпит, шайды сәндеген
Тоққа балқып келіп тұрған ән де мен.
Қандай металл?
Алюминий
Слайд 12ІІІ. Жаңа сабақ
1. Периодтық жүйедегі орны
2. Атом құрылысы
3. Химиялық қасиеттері
4.
Физикалық қасиеттері
5.Маңызды қосылыстары
6.Қазақстанда таралу аймағы
Слайд 15Химиялық қасиеттері
Жай заттармен әрекеттесуі:
2 A1 + 3 C12 =
2A1 C13;
2 A1 + 3 S = A12
S3; 2 A1 + N2 = 2 A1 N;
4 A1 + 3 C = A14C3
Күрделі заттармен әрекеттесуі:
2A1 + 6H20 = 2A1(0H)3 + 3H2
2Al + 6HCl = 2AlCl3 + 3H2
2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2
2Al + 3 CuCl2= 2AlCl3+ 3Cu
Алюминий қосылыстары
Al2O3 + 2NaOH = 2NaAlO2 + H2O
Al(OH)3 + 6HCl = 2AlCl3 + 6H2O
Al(OH)3 + NaOН = NaAlO2 + 2H2O
Аl2O3 + 6HCl = 2AlCl3 + 3H2O
Al(OH)3 + 3HCl = Al Cl3 + 3H2O
Слайд 16
Алюминий
күмістей ақ
электр өткізгіш құралдар жасауға кең қолданылады
электр және жылу
өткізгіштігі жоғары
сым түрінде созылады
оңай фольга болып жайылады
Қатты, иілімді металл
Металдар арасында
қайнау температу-расы - 660°С.
Ол жеңіл (тығыздығы 2,7г/см3),
Физикалық қасиеті
Слайд 17Al₂O₃- қиын балқитын, ақ түсті зат. Табиғатта корунд деген атпен
кездеседі. Алюминий оксиді суда ерімейді, екідайлы қасиет көрсетеді: Al₂O₃+6HCl = 2AlCl₃+3H₂O Al₂O₃+2NaOH+3H₂O
= 2Na[Al(OH)₄] Алюминий гидроксидінің (Al(OH)₃) түрөзгерісі екі түрлі : кристалдық және аморфтық. Алюминий гидроксидін алюминий түздары ерітінділеріне сілтімен әсер ету арқылы алады: AlCl₃ + 3NaOH = Al(OH)₃ + 3NaCl Жаңа тұнған Al(OH) 3 ақ қоймалжың тұнба, суда мүлдем ерімейді және типтік екідайлы гидроксид болып табылады: Al(OH)₃+3HCl = AlCl₃+3H₂O Al(OH)₃+NaOH = Na[Al(OH)₄]Маңызды қосылыстары
Слайд 19Бұрын алу әдісі өте қиын болғандықтан, алюминий аса бағалы металдар
қатарында болған. Қазір алюминийді глинозем мен бокситтен элекролиздеп алады. Глинозем
мен бокситте алюминий оксид түрінде Al₂O3 болады. Оның балқу темпуратурасы ≈2050°С. Электролиз жақсы жүру үшін боксит пен криолит Na₃[AlF₆] қоспасына кальций фторидін CaF₂ қосып қыздырады. Сонда ғана қоспаның балқу температурасы ≈960°C-қа төмендейді.Боксит рудасынан электролиз әдісімен алынуы: (Қызылжарда) 2Al₂O₃ −−−−−> 4Al + 3O₂
Алюминий
Алюминий – табиғатта кең тараған элемент. Таралуы жағынан ол – металдар арасында бірінші, ал жалпы үшінші орындағы элемент. Алюминий белсенді элемент болғандықтан табиғатта тек қосылыс түрінде кездеседі. Оның маңызды кендеріне – Al₂O₃ (корунд, рубин, сапфир) KAlSi₃ O ₁₀ортоклаз, NaAlSi₃O₁₀ альбит, Ca(AlSiO₄)² aнортит, KNaAlSiO₄ нефелин, Na₃AlF₆ криолит, Al₂O₃*xH₂O боксит жатады. Алюминий кендері Хибин тауларында, Оралда, Сібірде, Қазақстанда Торғайда көптеп кездеседі.
Слайд 21Сергіту сәті
3 – 15 арасында бір сан ойла ....
2 көбейт!
5
қос!
Шыққан санды 5 көбейт!
Соңғы санды алып таста!
Қалған саннан 2
ал!Ойлаған санымыз шықты ма?
Ол қандай элемент?
Слайд 22Терең ой
(Оқулықпен жұмыс)
“В” тобы №2 есеп
Массасы 5,4г алюминийді
еріту үшін қанша 10% - дық тұз қышқылының ерітіндісі қажет
№3 есеп
Алюмотермия әдісімен темір алғанда массасы 20г темір (ІІІ) оксидімен массасы 50г алюминий әрекеттескенде қанша грамм темір шығады?
“С” тобы №1 есеп
Массасы 1т темір алу үшін қанша алюминий керек және осы кезде қанша жылу бөлінеді.
Слайд 25
Александрит сақина
Алюминий бейметалдармен оның ішінде оттекпен гологендермен әрекеттеседі, бір
ғажабы коррозияға ұшырамайтындығы түсініксіз жағдай.
Себебін түсіндір?
Слайд 27Қызыл сафир сақина
18 ғасырда өмір сүрген орыстың ұлы
ғалымы М. В. Ломоносов алюминийді басқа металл оксидтерінің құрамынан ығыстырып
шығаратынын дәлелдеді. Бұл қандай әдіс деп аталады?Слайд 31 Мағынаны тану
Жаңа сабақты бекіту
Аты жөні:
Туған жылы:
Жасы:
Мекен-жайы:
Отбасы құрамы:
Тегі:
Сыртқы
келбеті:
Мінезі:
Достары:
Достарының аттары:
Пайдасы:
Туыстары:
Слайд 32 Аты жөні: Алюминий
Туған жылы: 1825 жылы дат химигі
әрі физигі Эрстед “Мен балшықтан металл алдым”
1827 ж
Неміс химигі Веллер (AlCl3 +3K Al +3KCl)Жасы: №13 Ar27
Мекен-жайы: 3 кіші периодтың ІІІ негізгі топшасы
Отбасы құрамы: 13p,14n,13e
Тегі: Металл
Сыртқы келбеті: күміс түстес, ақ металл, мықты, кристалл торы орталықтанған куб, жеңіл, өте иілімді, жұмсақ, шағылу қабілеті жоғары, электр және жылу өткізгіш, жемірілуге тұрақты, ρ=2,7г/см3 , t=650°С
Мінезі: белсенді
Достары: бейметалдар
Достарының аттары: АІ оксиді, АІ хлориді, АІ сульфиді, АІ фосфиді, АІ карбиді
Пайдасы: бояу, электротехника, ыдыс –аяқ, конц азот қышқылын тасымалдаушы цестернада, авиацияда, электр сымдарында, жеңіл металл конструкцийларына, зергерлік
Туыстары: галий, индий, талий
Слайд 34Бейне сурет сұрақтар
Алюминий
Кальций
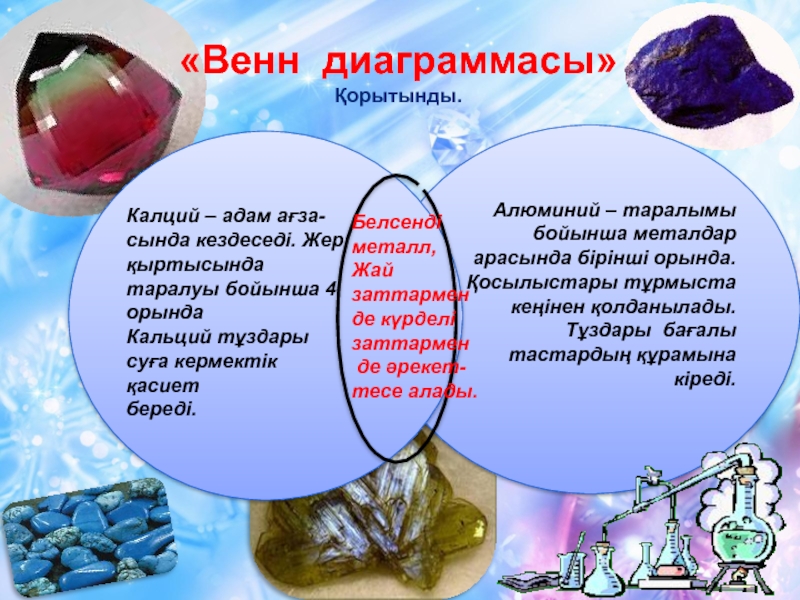
«Венн диаграммасы»
Қорытынды.
Калций – адам ағза-
сында кездеседі. Жер қыртысында
таралуы бойынша 4 орында
Кальций тұздары суға кермектік қасиет
береді.
Алюминий –
таралымы бойынша металдар арасында бірінші орында. Қосылыстары тұрмыста
кеңінен қолданылады.
Тұздары бағалы
тастардың құрамына
кіреді.
Белсенді металл,
Жай заттармен
де күрделі заттармен
де әрекет-тесе алады.