Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Металлы, свойства металлов
Содержание
- 1. Металлы, свойства металлов
- 2. Металлы – химические элементы , образующие в
- 3. Роль металлов в жизни человека и общества.В
- 4. Из серебра, золота и меди чеканили монеты.
- 5. Материал, из которого сооружена пирамида Хеопса, изготовлен из камня и меди.
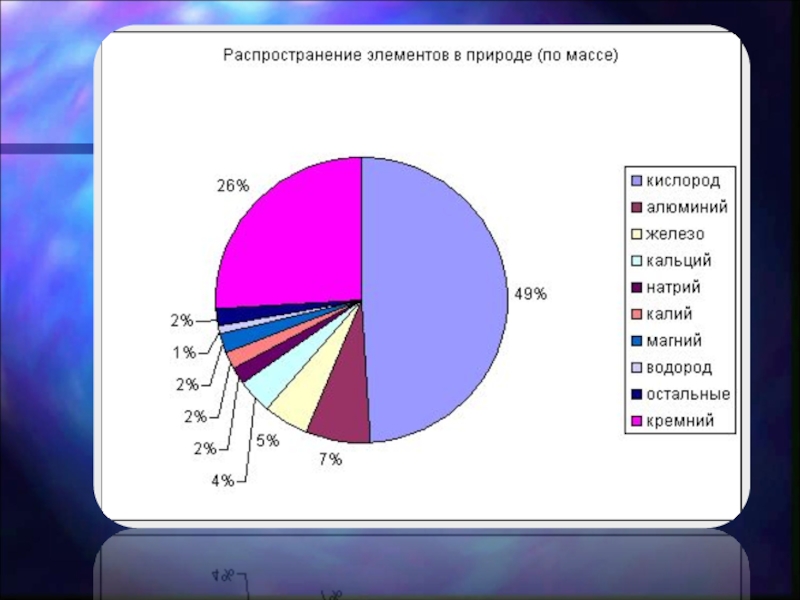
- 6. Слайд 6
- 7. Большинство Х Э - металлы.Граница между металлами и неметаллами-условная.
- 8. Металлы Переходный элемент
- 9. Закономерность изменения свойств металлов в группе.Заряд ядра
- 10. Закономерность изменения свойств металлов в периоде.Заряд ядра
- 11. Физические свойства металлов.Все металлы обладают общими физическими
- 12. Все металлы- твердые вещества, кроме ртути.
- 13. ПластичныеAu, Ag, Cu, Sn, Pb,Zn, Fe уменьшается
- 14. Температура плавленияЛегкоплавкие
- 15. Слайд 15
- 16. Обладают металлическим блеском
- 17. Щелочные металлы Переходные металлы Щелочно-земельные металлыПо химической активности
- 18. Химические свойства металловМеталлы в химических реакциях являются
- 19. Металлы вытесняются из их соединений другими металламиН.Н.
- 20. Взаимодействуют с простыми веществамиС элементами VII группы
- 21. Взаимодействие со сложными веществамиС растворами кислот (металлы,
- 22. Применение металловСтанко-строениемедицинаСельское хозяйство получение сплавовВ бытуМеталлургическая промыш-ленность
- 23. Получение металловПирометаллургический способ -восстановление углеродом,
- 24. СПАСИБО ЗА ВНИМАНИЕ
- 25. Скачать презентанцию
Металлы – химические элементы , образующие в свободном состоянии простые вещества с металлической связью. М.В. Ломоносов - металлы «светлое тело, которое ковать можно»Что такое металлы?Ba CrK Li
Слайды и текст этой презентации
Слайд 2Металлы – химические элементы , образующие в свободном состоянии простые
вещества с металлической связью.
М.В. Ломоносов - металлы «светлое тело,
которое ковать можно»Что такое металлы?
Ba
Cr
K
Li
Слайд 3Роль металлов в жизни человека и общества.
В древности человеку были
известны только 7металлов, которые соответствовали числу известных в то время
планет : Солнце (золото), Юпитер (олово), МЕСЯЦ (серебро), Марс (железо), Меркурий (ртуть), Сатурн (свинец), Венера (медь).Сначала человек познакомился с металлами, которые встречаются в самородном виде - это золото, серебро и медь.
Остальные металлы появились после того, как человек научился добывать их из руд с помощью огня.
Каменный век → Медный век → Бронзовый век → Железный век.
Слайд 4Из серебра, золота и меди чеканили монеты.
1. Серебряная монета
с изображением богини
Афины и совы.
2. Золотая монета с
изображением Александра
Македонского и бога Зевса.3. Медная монета в виде дельфина.
Из металлов и их сплавов из- готавливаються памятники и статуи.
Статуя Колосса Родосского (Бронза)
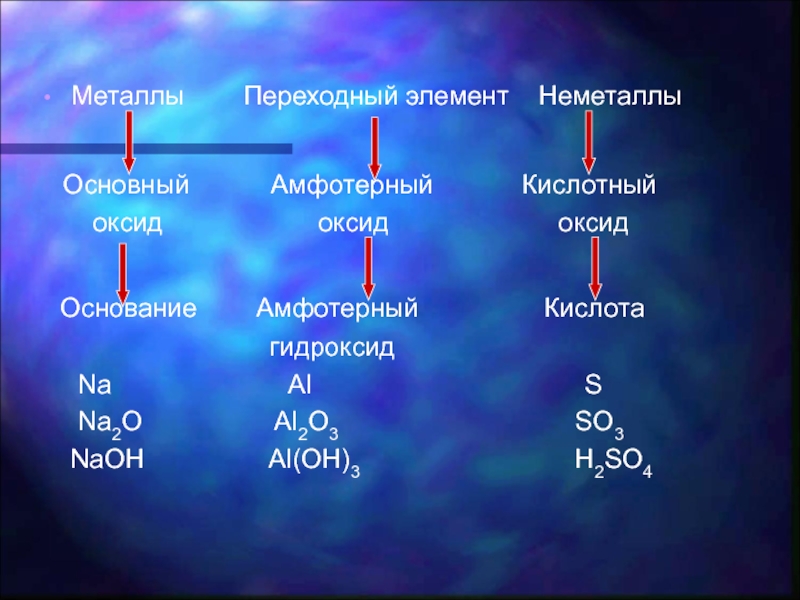
Слайд 8Металлы Переходный элемент Неметаллы
Основный Амфотерный
Кислотный оксид оксид оксид
Основание Амфотерный Кислота
гидроксид
Na Al S
Na2O Al2O3 SO3
NaOH Al(OH)3 H2SO4
Слайд 9Закономерность изменения свойств металлов в группе.
Заряд ядра увеличивается,так как увеличивается
порядковый номер.
R увеличивается,так как увеличивается количество энергетических уровней.
Число электронов на
последнем уровне постоянно.Способность к отдаче электронов увеличивается.
Восстановительные способности и металлические свойства увеличиваются.
Слайд 10Закономерность изменения свойств металлов в периоде.
Заряд ядра увеличивается,так как увеличивается
порядковый номер.
R уменьшается,так как заряд ядра больше, способность притягивать электроны
возрастает, за счет этого происходит стягивание электронных оболочек.Число электронов на внешнем уровне увеличивается,так как растёт номер группы.
Восстановительные способности и неметаллические свойства уменьшаются.
Слайд 11Физические свойства металлов.
Все металлы обладают общими физическими свойствами,так как во
всех металлах существует металлическая химическая связь и металлическая кристаллическая решётка.
Слайд 18Химические свойства металлов
Металлы в химических реакциях являются восстановителями, при этом
они окисляются
Mo – ne =Mn+Al, Be, Mg, Ca, Li, Na, K, Rb, Cs
Восстановительная способность возрастает
Слайд 19Металлы вытесняются из их соединений другими металлами
Н.Н. Бекетов – создал
«вытеснительный ряд» (прототип электрохимического ряда напряжения металлов)
Li, K, Ca,
Na, Mg, Al, Mn, Zn, Cr, Fe, Ni, Sn, Pb, (H), Cu, Hg, Ag, Pt, Au.Слайд 20Взаимодействуют с простыми веществами
С элементами VII группы (при обычных условиях)
2Na + Cl2
= 2 Na Cl- С элементами VI группы (труднее)
Mg + O2 = 2Mg O
C элементами V группы (в жестких условиях)
3Ca + 2P =Ca3P2
Слайд 21Взаимодействие со сложными веществами
С растворами кислот (металлы, стоящие в ряду
напряжений до «Н»)
Zn + H2SO4 = Zn S O4 + H2↑C растворами солей металлов, стоящих в ряду напряжений правее
Zn + Pb(NO3)2 = Zn(NO3)2 + Pb
C водой (активные)
2Na + 2H2O =2Na OH + H2↑
Реакция идет в том случае, если образуется растворимое основание.
Слайд 22 Применение металлов
Станко-
строение
медицина
Сельское хозяйство
получение сплавов
В быту
Металлургическая промыш-ленность
Слайд 23 Получение металлов
Пирометаллургический способ -восстановление углеродом, оксидом углерода (II),
водородом при высокой температуре.
Алюминотермический способ – восстановление металлов с помощью
алюминия.Гидрометаллургический способ – получение из руды более активным металлом или из растворов
Электролиз – с помощью электрического тока из расплавов или растворов